文章信息
- 宋金凤, 刘永, 崔晓阳.
- Song Jinfeng, Liu Yong, Cui Xiaoyang.
- 毛细管气相色谱法测定森林凋落物中的有机酸
- Determination of Organic Acids in Forest Litters by a Capillary Gas Chromatography
- 林业科学, 2004, 40(4): 185-188.
- Scientia Silvae Sinicae, 2004, 40(4): 185-188.
-
文章历史
- 收稿日期:2003-10-14
-
作者相关文章
2. 中国水产科学研究院黑龙江水产研究所 哈尔滨 150070
2. Heilongjiang Fishery Research Institute, Chinese Academy of Fishery Sciences Harbin 150070
有机酸在土壤养分活化、释放中的作用日益受到关注,已成为国内外植物营养和土壤学研究的热点(Fox et al., 1990b;1992;胡红青等,1997;陆文龙等,1998;McColl et al., 1999;Sollins et al., 1999)。土壤中的有机酸可来自有机质分解、微生物代谢或植物根分泌作用等不同途径(莫淑勋,1986;沈阿林等,1997)。对于森林土壤来说,森林凋落物的分解和淋溶过程无疑是有机酸的最主要来源。目前,已有越来越多的研究者注意到森林凋落物分解、淋溶过程中释放的有机酸并对此进行研究(Pohlman et al., 1988;Fox et al., 1990a;王晓水等,1997;吴俊民等,2000),这就要求有准确、快速、简便的分析检测方法。
森林凋落物中有机酸的分析尚无统一方法,研究者采用的主要有高效液相色谱法和气相色谱法2大类。用高效液相色谱法(紫外检测器)测定有机酸时,检测波长一般在羧基的最大吸收峰205 nm左右,易受夹杂成分的干扰,引起较大误差,且需要较为复杂的前处理(Fox et al., 1990a);另外在测定小分子有机酸时需要较低的pH值,易引起色谱柱的流失,而高级脂肪酸又以结合态(甘油三酯)存在,且存在形式不唯一,无法直接测定,使其游离而不破坏脂肪酸的特性需要复杂的处理过程。应用传统的气相色谱法测定有机酸时,前处理大多选用不同溶剂浸提,然后进行浓缩、酯化,这就不可避免地产生易挥发性有机酸在浓缩和酯化过程中的损失以及高温引起的不饱和脂肪酸的氧化,且由于处理方法的不同,通常仅能分析大分子有机酸,而对低分子有机酸的选择性较差(王晓水等,1997;吴俊民等,2000)。对于同一种凋落物而言,要想测定出其所含有的低分子量有机酸及高级脂肪酸,往往需用2种不同方法进行测定,从而导致2种不同方法之间可比性差,容易造成误差。因此,进行树种凋落物中各种有机酸的综合、一次性测定研究就显得尤为重要。
本文采用甲醇浸提的同时进行甲酯化处理,用毛细管气相色谱法进行检测,建立了一种准确且同时测定森林凋落物中低分子量有机酸和高级脂肪酸的毛细管气相色谱法。该方法操作简便,不需要额外的样品浓缩处理过程,能同时分析多种低分子量有机酸及高级脂肪酸。
1 试验材料选择东北林区主要造林树种水曲柳(Fraxinus mandshurica)和落叶松(Larix olgensis) 的新鲜凋落物为供试材料。于10月上旬在东北林业大学帽儿山实验林场(45°12′~45° 30′ N, 127°30′~127°48′E)收集当年新鲜凋落物(L层)。样品在实验室内通风阴干,粉碎,装瓶待测。
2 样品处理(浸提与甲酯化)准确称取凋落物样品0.500 0 g放入干净的50 mL反应瓶中,加入体积之比为7:100的H2SO4:CH3OH溶液10 mL(刘百战等,1999),密闭摇匀,置于60℃水浴锅中加热24 h浸提并直接进行甲酯化,然后用布氏漏斗将甲酯化后的样品抽滤,用甲醇冲洗反应瓶3次,抽滤后合并滤液,转移到盛有20 mL高纯水的分液漏斗中。用三氯甲烷萃取(5 mL,分3次),分层后下层萃取液经无水硫酸钠玻璃小柱(玻璃小柱中加入约5 mm厚无水硫酸钠,下端用玻璃纤维固定;无水硫酸钠及玻璃纤维在250℃下烘干4 h)干燥,用带刻度试管接取,直接取1 μL进样分析。
3 仪器设备与色谱条件美国Agilent-6890N气相色谱仪,氢火焰离子化检测器(FID)。色谱分析条件如下:色谱柱:30 m×0.25 mm×0.53 μm FFAP弹性石英毛细管柱;柱流速:2.5 mL·min-1;进样口温度:230 ℃;载气:氮气(N2),纯度≥99.999%;程序升温:120℃(保持2 min)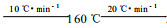
分别取一定浓度的草酸、丙二酸、丁二酸、反丁烯二酸、顺丁烯二酸、苹果酸、柠檬酸、棕榈酸、硬脂酸、油酸、亚油酸、亚麻酸和花生酸(均为色谱纯,Sigma产品)标样,在上述最佳色谱条件下,按样品处理方法进行甲酯化,得到标样色谱图,以确定各有机酸峰的位置及不同有机酸所对应的保留时间。在相同色谱条件下,将样品色谱图与有机酸标准样品色谱图进行对照,根据保留时间确定样品中各有机酸的色谱峰,进行定性分析;同时还在样品中加入有机酸标样,以进一步确定。图 1和图 2分别为水曲柳和落叶松凋落物样品的典型气相色谱图。

|
图 1 水曲柳凋落物中有机酸(甲酯)的典型气相色谱图 Fig. 1 A typical chromatogram of organic acids in F. mandshurica forest litter 1.草酸Oxalic;2.丙二酸Malonic;3.反丁烯二酸Fumaric;4.丁二酸Succinic;5.顺丁烯二酸Maleic; 6.苹果酸Malic;7.棕榈酸C16:0;8.柠檬酸Citric;9.硬脂酸C18:0;10.油酸C18:1;11.亚油酸C18:2;12.亚麻酸C18:3;13.花生酸C20:0.下同。The same below. |

|
图 2 落叶松凋落物中有机酸(甲酯)的典型气相色谱图 Fig. 2 A typical chromatogram of organic acids in L. olgensis forest litter |
从图 1和图 2可以看出,水曲柳和落叶松凋落物样品含有多种有机酸,包括草酸、丙二酸、反丁烯二酸、丁二酸、顺丁烯二酸、苹果酸、棕榈酸、柠檬酸、硬脂酸、油酸、亚油酸、亚麻酸、花生酸等,其中大部分峰都能得到较好的分离。另外还有部分含量较高的物质未能确认。
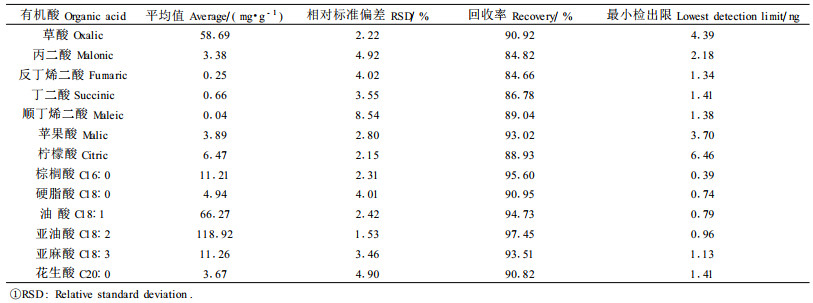
5 定量分析应用外标法进行定量分析,用峰面积计算出样品中各有机酸的含量。为测定该方法的精密度,同一凋落物样品重复称样6次,分别进行甲酯化处理和色谱分析,计算各有机酸含量的平均值和相对标准偏差。另外,采用标准加入法进行有机酸的回收率试验,并取一定浓度的有机酸标样进行最小检出限测定(S/N=3)。水曲柳凋落物中13种有机酸的定量测定结果及方法的相对标准偏差、回收率、最小检出限等参数列于表 1。
|
|
由表 1可以看出,所检测的13种有机酸中有12种相对标准偏差在1.53%~5.30%,只有顺丁烯二酸因为含量少,相对标准偏差达到8.54%,但也满足分析测定的要求;13种有机酸的加标回收率在84.66%~97.45%之间;各有机酸的最小检出限为0.89~6.46 ng。
6 结论与讨论本研究将密封样品的反应瓶置于60℃水浴锅中,采用甲醇浸提有机酸并直接甲酯化24 h,建立了一种准确测定森林凋落物中有机酸的毛细管气相色谱法。该方法不需要特殊设备及样品浓缩处理,不但能有效避免传统测定方法浓缩和酯化过程中易挥发有机酸的损失,以及高温引起的不饱和脂肪酸的氧化,而且酯化完全,样品转移简便,易于操作;用毛细管气相色谱法进行检测,选择性好,能一次性准确测定低分子量有机酸及高级脂肪酸。实验表明,该方法分离度好、精密度高、重现性好(保留时间变化在±1.5%以内)、回收率及最小检出限均满足要求,是一种对凋落物样品中有机酸进行定性、定量分析的可靠方法。
将本文分析结果与王晓水等(1997)、吴俊民等(2000)所做的结果进行对比,发现亚油酸所占比例较大这一点是一致的,但其二人均未涉及低分子量有机酸,如草酸、丙二酸、反丁烯二酸、丁二酸、顺丁烯二酸、苹果酸等。Pohlman等(1988)发现北美翠柏(Calocedrus decurrens)、美国黄松(Pinus ponderosa)未分解凋落物亚层中草酸含量最大,在这点上本研究也与此结果相符。同时还发现Pohlman等(1988)、Fox等(1990a)所检测的有机酸数量远低于本文结果,原因很可能在于他们测定有机酸时采用稀NaOH/HNO3溶液或调节到一定pH值的去离子水进行凋落物淋洗处理,接收淋洗液进行分析,所测得的主要是游离低分子有机酸(高级脂肪酸以水相溶剂是无法提取的);而本文则是在60℃密闭条件下,采用甲醇浸提有机酸并直接进行甲酯化,游离有机酸可直接浸提酯化,结合态有机酸亦可在酸的作用下完成酯交换,使游离及结合态有机酸得以同时测定。此外,凋落物中有机酸的专门定性分析采用了气相色谱-质谱(GC-MS)联用法,将另文论述。
胡红青, 贺纪正, 李学垣, 等. 1997. 有机酸对酸性土壤吸附磷的影响. 华中农业大学学报, 16(1): 37-42. |
刘百战, 徐亮, 詹建波, 等. 1999. 云南烤烟中非挥发性有机酸及某些高级脂肪酸的分析. 中国烟草科学, (2): 28-31. |
陆文龙, 王敬国, 曹一平, 等. 1998. 低分子量有机酸对土壤磷释放动力学的影响. 土壤学报, 35(4): 493-499. DOI:10.3321/j.issn:0564-3929.1998.04.008 |
莫淑勋. 1986. 土壤中有机酸的产生、转化及对土壤肥力的某些影响. 土壤学进展, 14(4): 1-10. |
沈阿林, 李学垣, 吴受容. 1997. 土壤中低分子量有机酸在物质循环中的作用. 植物营养与肥料学报, 3(4): 363-370. DOI:10.3321/j.issn:1008-505X.1997.04.012 |
王晓水, 刘广平, 吴保国.落叶松水曲柳混交林树体淋洗物和枯枝落叶分解产物的作用.见: 沈国舫, 翟明普主编.混交林研究.北京: 中国林业出版社, 1997: 164-167
|
吴俊民, 王会滨, 唐利疆, 等. 2000. 混交林落叶松枯枝落叶对水曲柳生长的影响. 东北林业大学学报, 28(2): 1-3. DOI:10.3969/j.issn.1000-5382.2000.02.001 |
Fox T R, Comerford N B. 1990a. Low-molecular-weight organic acids in selected forest soils of the southeastern USA. Soil Sci Soc Am J, 54: 1139-1144. DOI:10.2136/sssaj1990.03615995005400040037x |
Fox T R, Comerford N B, McFee W W. 1990b. Kinetics of phosphorus release from spodosols: Effects of oxalate and formate. Soil Sci Soc Am J, 54: 1441-1447. DOI:10.2136/sssaj1990.03615995005400050038x |
Fox T R, Comerford N B. 1992. Influence of oxalate loading on phosphorus and aluminum solubility in spodosols. Soil Sci Soc Am J, 56: 290-294. DOI:10.2136/sssaj1992.03615995005600010046x |
McColl J G, Pohlman A A, Jersak J M et al.Organic acids and metal solubility in California forest soils. In: Gessel S P (ed). Sustained productivity of forest soils. Vancouver: University of British Columbia, Faculty of Forestry Publication, 1999: 178-195
|
Pohlman A A, McColl J G. 1988. Soluble organics from forest litter and their role in metal dissolution. Soil Sci Soc Am J, 52: 265-271. DOI:10.2136/sssaj1988.03615995005200010047x |
Sollins P, Cromack K, Fogel R et al. Role of low-molecular-weight organic acids in the inorganic nutrition of fungi and higher plants. In: Wicklow D T, Carroll G C (ed).The fungal community. NewYork: Marcel Dekker, 1999: 607-619
|
 2004, Vol. 40
2004, Vol. 40