文章信息
- 金则新, 李钧敏.
- Jin Zexin, Li Junmin.
- 七子花种群遗传多样性的RAPD分析
- RAPD Analysis on Genetic Diversity of Populations of Heptacodium miconioides
- 林业科学, 2004, 40(4): 68-74.
- Scientia Silvae Sinicae, 2004, 40(4): 68-74.
-
文章历史
- 收稿日期:2003-02-17
-
作者相关文章
七子花(Heptacodium miconioides)为我国特有的落叶小乔木,属忍冬科(Caprifoliaceae)的单种属植物,是国家首批二级重点保护植物(国家环境保护局等,1987)。多生于悬崖峭壁、沟谷和山坡灌丛,分布范围窄,野生资源很少。有关七子花的研究不多,仅对其种群结构(金则新,1997)、分布格局(金则新,1999)、群落特征(金则新,1998)、物种多样性(金则新,2000)、光合生理生态特性(金则新等,2002)以及细胞学(张朝阳等,2000)等方面进行了研究,对其濒危现状也有一定的了解。七子花种群幼龄个体极少,天然更新困难,年龄结构呈衰退型模式,其濒危状况日趋严重,对这一濒危物种的遗传多样性的研究未见报道。遗传多样性的研究不仅有助于了解物种的进化历史和适应潜力以及探讨物种濒危的机制,同时也关系到能否或如何采取科学有效的措施来保护物种(葛颂等,1999)。
RAPD技术作为一种简便、快速、易行的分子标记技术,近年来被广泛地应用于木本植物遗传多样性和遗传结构的研究中(夏铭等,2001;Palacios et al., 1997;Wachira,1995)。本研究利用RAPD技术对分布在浙江省天台山的七子花天然种群的遗传多样性水平以及动态变化进行了分析,为进一步阐明七子花的遗传变异、进化潜力及采取合理的保护措施提供科学依据。
1 材料与方法 1.1 材料样地位于浙江省天台山华顶国家森林公园的狮子岩坑处,此地沿山沟及两侧呈带状分布着一小片天然七子花群落,有关其自然概况、群落特征、种群结构研究已有报道(金则新,1997;1998)。由于七子花是生命周期很长的树木,很难追踪种群的整个发育过程来研究种群遗传结构的动态变化。在植物种群分布格局研究中,常采用立木级结构分析的方法来研究动态变化。植物种群遗传变异的动态变化也可通过检测不同年龄级个体之间的遗传差异来判断种群遗传结构的时间变化,因此也采用大小级的方法进行研究(陈小勇等,1999)。将七子花种群按胸径(DBH)的大小分为4级:A级,大树,DBH>22.5 cm;B级,中树,DBH 7.5~22.5 cm;C级,小树,DBH 2.5~7.5 cm;D级,幼树,DBH<2.5 cm;由于样地中几乎见不到七子花幼苗,所以幼苗未研究。于2001年7月随机选取七子花的大树、中树、小树各12株;幼树因个体数有限,仅取9株;各采样点基本覆盖七子花自然分布区。取植株的叶片,置于保鲜袋中,封口,于样品贮藏箱(由超低温冰袋保持冷藏条件)带回实验室,-70℃超低温冰箱保存,供DNA提取。
1.2 DNA提取-70℃冻存叶片加入液氮研磨成粉状,0.1 g转入1.5 mL离心管中;加入500 μL提取缓冲液[100 mmol·L-1 Tris·HCl(pH8.0),3%可溶性聚乙烯吡咯烷酮(PVP),20 mmol·L-1 β-巯基乙醇,20 mmol·L-1 EDTA(pH8.0)],8 000 rpm离心5 min,弃上清,取沉淀加入500 μL裂解缓冲液[100 mmol·L-1 Tris·HCl(pH8. 0),20 mmol·L-1 EDTA(pH8.0),500 mmol·L-1 NaCl,1.5% SDS],65℃水浴30 min,不时轻轻颠倒;取出加入500 μL氯仿/异戊醇(v:v=24:1),颠倒成乳浊状,10 000 rpm离心10 min,取上清加入0.25(v/v)乙醇和0.11(v/v) 5 mol KAc(pH4. 8),10 000 rpm离心10 min,取上清加入0.6(v/v)异丙醇,置-20℃冰箱30 min;12 000 rpm离心10 min,取沉淀溶于30 μL TE缓冲液(含RNase 5 μg·mL-1)中,备用(李钧敏等,2002)。
1.3 DNA定量采用日本岛津UV-7401PC紫外可见分光光度计与琼脂糖凝胶电泳双重定量。紫外分光光度法以λDNA为标准品,以A260对DNA进行定量;电泳图谱经UTHSCSA Image Tool软件分析荧光面积,与标准DNA分子量参照物比较定量而得。
1.4 RAPD扩增及产物鉴定 1.4.1 扩增反应条件15 μLPCR反应体积,1×Taq酶缓冲液,0.1 mmol·L-1 4×dNTP,1U Taq酶(上海华美公司),10 ng模板DNA,20 pmol引物(上海生物工程公司);2.5 mmol·L-1 MgCl2;3 μg·μL-1 BSA。对照加入除模板DNA外的以上各成分,用双蒸水代替总DNA(边才苗等,2002b)。
1.4.2 扩增程序使用上海高机公司生产的SRX-481 PCR仪,适合七子花RAPD分析的PCR反应程序(用6℃循环水冷却):94℃预变性5 min,94℃变性1 min,40℃退火1 min,72℃延伸2 min,共35个循环;72℃完全延伸5 min。
1.4.3 电泳检测RAPD产物用1.4%琼脂糖凝胶电泳,缓冲液为0.5×TBE,用200 bp DNA梯度标准作分子量参照物。在凝胶中加入0.5 μg·mL-1溴乙锭,电泳完毕于紫外透射仪上观察拍照,Leica数码相机拍照保存。
1.5 数据处理 1.5.1 RAPD多样性表型带计数用200 bp DNA梯度标准作分子量参照物,对照反应产物在胶上的对应位置,有带记为“1”,无带记为“0”,记录后备用。
1.5.2 数据处理采用POPGENE32软件进行多态位点比率、等位基因显性频率、Shannon表型多样性指数、Nei指数、遗传分化系数、基因流的统计分析,并进行聚类分析。
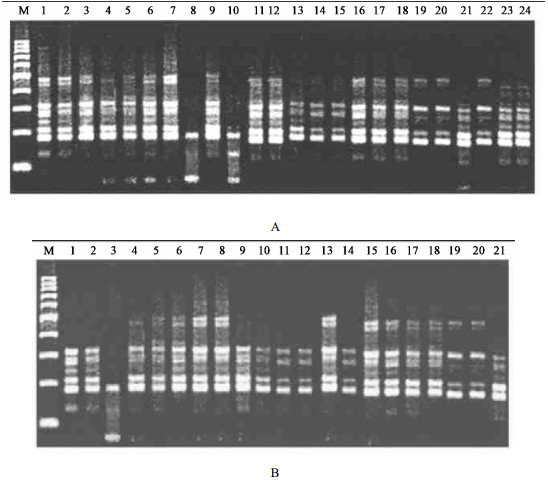
2 结果与分析 2.1 引物筛选对七子花叶片DNA进行RAPD扩增,对每次扩增的DNA产物电泳分离并拍照。从60个引物中共筛选出扩增条带清晰、重复性好的12个随机引物作为本研究的试验用引物。现将这12种引物的碱基序列列于表 1,其中由引物S71得到的4个大小级种群的扩增图谱如图 1所示。
|
|
|
图 1 七子花(S71)的RAPD扩增结果 Fig. 1 The result of RAPD of H. miconioides amplified with primer S71 M. 200 bp DNA梯度标准200 bp DNA ladder. A: 1—12: A级大树种群1—12个体RAPD扩增结果RAPD amplification of sample1—12 of A class big tree population;13—24: B级中树种群1—12个体RAPD扩增结果RAPD amplification of sample1—12 of B class middle tree population. B: 1—12: C级小树种群1—12个体RAPD扩增结果RAPD amplification of sample1—12 of C class arboret population;13—21: D级幼树种群1—9个体RAPD扩增结果RAPD amplification of sample1—9 of D class young tree population. |
12种引物在七子花4个大小级种群45个个体中共扩增出64个位点,平均5.33条带/引物,其中多态位点有39个,总多态位点百分率为60.94%。由表 2可知,每个引物所扩增出产物的多态性在各大小级种群中的分布数量不同,A级大树12个引物共扩增出23个多态位点,多态位点百分率为35.94%;B级中树共扩增出20个多态位点,多态位点百分率为31.25%;C级小树共扩增出19个多态位点,多态位点百分率为29.69%;D级幼树共扩增出15个多态位点, 多态位点百分率为23.44%。各大小级种群的多态位点百分率明显低于总多态位点百分率。七子花4个大小级种群的多态位点百分率为大树>中树>小树>幼树,由此可知,从大树到幼树多态位点百分率呈不断下降趋势。
|
|
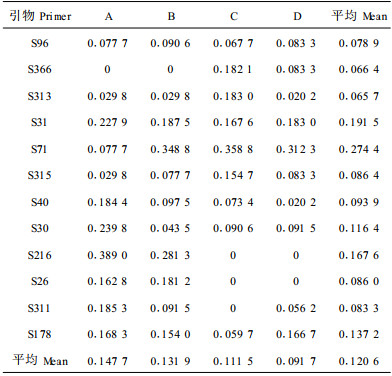
由Shannon信息指数估计的七子花不同大小级种群内的遗传多样性有一定的差异(表 3),变动范围为0.133 7~0.214 2,平均为0.175 4。4个大小级种群的遗传多样性大小顺序为大树>中树>小树>幼树。用不同引物检测的遗传多样性大小也是有差异的,其中引物S71检测的遗传多样性最高,4个大小级种群平均为0.394 9,而用引物S366检测的则最低,平均为0.093 5。
|
|
Shannon表型遗传多样性指数可分为大小级种群内遗传多样性和大小级种群间遗传多样性两部分,从表 4可以看出,各数值在引物间变动较大,说明各引物扩增出的不同多态位点对遗传多样性的贡献是不同的。七子花不同大小级种群总的遗传多样性平均为0.322 3,4个大小级种群内的遗传多样性平均为0.175 4。大小级种群内的遗传变异占总变异的54.41 %,大小级种群间占总变异的45.59%,这表明七子花不同大小级种群内、种群间个体均存在一定的遗传分化,但大小级种群内遗传分化要高于大小级种群间。
|
|
由Nei指数估计的七子花4个大小级种群内的基因多样性见表 5,虽然由Nei指数估计的基因多样性指数值比Shannon信息指数估计的值低,但二者估计的不同大小级的遗传多样性高低是一致的,也是大树最高,其余依次为中树、小树与幼树。用不同引物检测的基因多样性大小也是有差异的,其中引物S71检测的基因多样性最高,4个大小级种群平均为0.274 4,而用引物S313检测的则最低,平均为0.065 7,这与Shannon信息指数估计的结果有所差异。
|
|
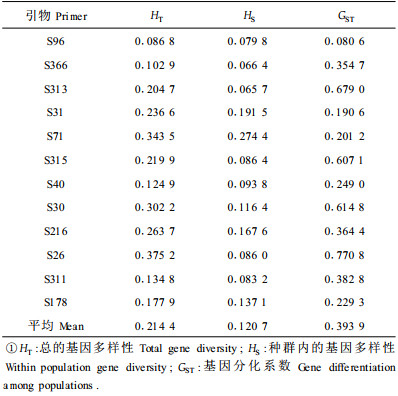
由表 6可知,Nei指数估算的七子花4个大小级种群总的基因多样性平均为0.214 4,大小级种群内的基因多样性平均为0.120 7,大小级种群间的基因多样性平均为0.093 7,大小级种群间的基因分化系数为0.393 9。表明七子花的遗传变异主要来自大小级种群内,不同大小级种群之间的个体也有一定的分化。由Gst估算的七子花大小级种群间的基因流为0.769 4,显示大小级种群间的基因流较小。
|
|
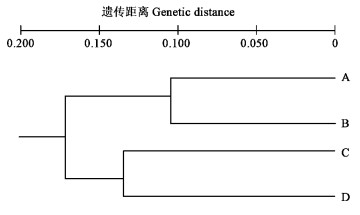
通过POPGENE软件按Nei's(1972)方法计算七子花不同大小级间的遗传相似度,其变化范围为0.812 9~0.900 9(表 7),变幅较小。从表 7可知,大树与中树的遗传相似度最高(0.900 9),而大树与幼树的遗传相似度最低(0.812 9)。通过UPGMA法制作系统树(图 2),可将大树与中树聚成一组,而小树与幼树聚成另一组,2组再聚在一起。
|
|
|
图 2 七子花不同大小级种群间的UPGMA聚类分析图 Fig. 2 The dendrogram of 4 populations of H. miconioides in different size classes generated by UPGMA |
多态位点百分率可作为度量遗传多样性高低的指标,虽然近来不少研究发现有些特有和濒危物种保持较高的变异水平(葛颂等,1999),但是一般认为特有种和狭窄分布的植物种与广布种相比,其遗传多样性较低。汪小全等(1996)对银杉(Cathaya argyrophylla)进行RAPD分析时,检测到银杉的多态位点比率仅为32%,认为低水平的遗传多样性是银杉濒危的原因之一。经过RAPD分析,七子花4个大小级种群中,A级大树种群多态位点百分率为35.94%,B级中树种群多态位点百分率为31.25%,C级小树种群多态位点百分率为29.69%,D级幼树种群多态位点百分率为23.44%。此外,Shannon信息指数、Nei指数均显示大树种群的遗传多样性最高,其余依次是中树种群、小树种群和幼树种群。从大树种群到幼树种群,出现了遗传上的衰退,也即遗传变异的下降。
造成遗传衰退的原因还有选择作用、种群有效规模下降、遗传漂变以及自交等(邹喻苹等,2001)。由Gst估算的七子花大小级种群间的基因流为0.769 4,显示4个大小级种群间的基因流较小。七子花虽是虫媒花,但自花受粉的比例很高(边才苗等,2002a), 并且种子的休眠期长,萌发率极低(王诗云等,1995)等,这些都限制了七子花的基因交流,导致大量遗传变异的丧失,使其遗传结构趋于简单和单调。另一方面,由于人类的过度樵砍,使个体数锐减,人为干扰造成了很大程度的近亲繁殖,增加了整个群体遗传上的同源性(李进等,1998),这些也会降低七子花的遗传水平。由于七子花的分布区狭小、缺乏基因交流及生境退化等,使得遗传多样性水平随着时间的变化而下降,导致不同大小级个体间出现了遗传衰退。另外,七子花4个不同大小级种群的多态位点百分率较低,平均只有30.08%,但总的多态位点百分率可达60.94%,这主要由于七子花自花受粉的比例高,基因流小,导致遗传漂变,使各大小级种群间出现较大的遗传分化。
从遗传相似度来看,通过POPGENE软件按Nei's(1972)方法计算七子花不同大小级间的遗传相似度,大树与中树的遗传相似度最高,大树与幼树的遗传相似度最低。通过UPGMA法制作系统树可知,大树与中树聚成一组,而小树与幼树聚成另一组,2组再聚在一起。其原因除不同大小级个体间出现了遗传衰退外,还与七子花的生物学特性有关。七子花在自然状态下对光的要求较为独特,性喜光,不耐荫蔽,也不耐强光,对光适应的生态幅度较窄(金则新等,2002)。由于七子花林下光合有效辐射强度低,幼树、小树等因光合产物积累少,不能满足植株正常生长和发育的需要,常因光合产物不足而死亡。因此,在七子花林内,小树、幼树并不多见。而在林缘光照充足的开阔地带有七子花小树、幼树的分布,但林缘地带由于人为干扰严重而造成近交衰退进而导致七子花遗传多样性的降低。
利用Shannon指数和Nei指数估计七子花不同大小级种群的遗传分化,Shannon指数显示大小级种群内的遗传变异占总变异的54.41%,大小级种群间的遗传变异占总变异的45.59 %;而Nei指数显示大小级种群内的遗传变异占总变异的56.30%,大小级种群间的遗传变异占总变异的43.70%。2种计算方法估计的遗传变异虽然大小有所差异,但均表明不同大小级种群内、大小级种群间个体均存在一定的遗传分化,大小级种群内的遗传分化比大小级种群间高。种群内个体的遗传分化主要与该物种的生殖特性有关。种群间个体的遗传分化,可能是不同年份交配格局以及繁殖个体的变化所致(陈小勇等,1999)。七子花不同大小级种群间的基因流较小,从大树到幼树出现了遗传衰退,加上七子花的生活能力弱,在生存竞争中处于不利地位,在立地条件较好的山坡等地有让位于其它常绿阔叶树种的趋势,不得不退到土层瘠薄、岩石裸露的沟谷等恶劣的生境中(金则新,1999)。因此,七子花在不同大小级别建立时,都会受到当时环境选择的压力,产生一定的变异,适应于环境的变异被保留下来,使不同大小级种群间的遗传多样性有所差异。
近些年来,对遗传多样性在物种保护中所起的作用不同学者有不同的说法。一些学者认为,遗传多样性对物种的生存和发展起着决定作用;而另一些学者则认为生态因素(如生境的破坏和环境的变迁等)是物种濒危和灭绝的直接原因,因此是物种多样性保护中应首先要考虑的问题(葛颂,1999)。事实上,物种的遗传多样性水平、生活史特性以及生态因素等均会影响到物种的生存和发展。因此,对七子花实施保护,不能仅仅运用单一的手段和简单的方法,而应采取综合措施,抑制其种群衰败趋势。首先要制止乱砍滥伐,努力保存现有的种群和个体;其次在原地保护的基础上,创造七子花生存的适宜生境;第三,进一步对七子花种子的活力进行研究,打破种子的休眠期,提高种子的萌发率,并在较大的空间上进行补播,增加种群中幼苗的数量,创造基因交流和重组的条件,以达到保护遗传多样性的目的。
边才苗, 金则新, 李钧敏. 2002a. 七子花的繁殖生物学研究. 云南植物研究, 24(5): 613-618. |
边才苗, 李钧敏, 金则新, 等. 2002b. BSA在植物RAPD扩增反应中的应用. 遗传, 24(3): 279-282. |
陈小勇, 宋永昌. 1999. 黄山青冈种群时间遗传结构. 华东师范大学学报(自然科学版), (4): 79-84. DOI:10.3969/j.issn.1000-5641.1999.04.014 |
国家环境保护局, 中国科学院植物研究所. 1987. 中国珍稀濒危保护植物名录(第1册). 北京: 科学出版社, 11.
|
葛颂, 洪德元. 1999. 濒危植物裂叶沙参及其广布种泡沙参遗传多样性的对比研究. 遗传学报, 26(4): 410-417. |
金则新. 1997. 浙江天台山七子花种群结构和分布格局研究. 生态学杂志, 16(4): 15-19. DOI:10.3321/j.issn:1000-4890.1997.04.004 |
金则新. 1998. 浙江天台山七子花群落研究. 生态学报, 18(2): 127-132. DOI:10.3321/j.issn:1000-0933.1998.02.003 |
金则新. 1999. 浙江天台山七子花群落种群分布格局研究. 广西植物, 19(1): 47-52. DOI:10.3969/j.issn.1000-3142.1999.01.008 |
金则新. 2000. 浙江天台山七子花群落物种多样性. 武汉植物学研究, 18(1): 26-32. DOI:10.3969/j.issn.2095-0837.2000.01.006 |
金则新, 柯世省. 2002. 浙江天台山七子花群落主要植物种类的光合特性. 生态学报, 22(10): 1645-1652. DOI:10.3321/j.issn:1000-0933.2002.10.010 |
李进, 陈可咏, 李渤生. 1998. 不同海拔高度川滇高山栎群体遗传多样性的变化. 植物学报, 40(8): 761-767. DOI:10.3321/j.issn:1672-9072.1998.08.012 |
李钧敏, 金则新, 柯世省. 2002. 濒危植物七子花RAPD条件的优化. 植物学通报, 19(4): 452-456. DOI:10.3969/j.issn.1674-3466.2002.04.010 |
王诗云, 徐惠珠, 赵子恩, 等. 1995. 湖北及其邻近地区珍稀濒危植物保护的研究. 武汉植物学研究, 13(4): 354-368. |
汪小全, 邹喻苹, 张大明, 等. 1996. 银杉遗传多样性的RAPD分析. 中国科学(C辑), 26(5): 436-441. |
夏铭, 周晓峰, 赵士洞. 2001. 天然蒙古栎群体遗传多样性的RAPD分析. 林业科学, 37(5): 126-133. DOI:10.3321/j.issn:1001-7488.2001.05.022 |
张朝阳, 顾志建, 岳中枢. 2000. 七子花的细胞学研究. 云南植物研究, 22(4): 428-430. DOI:10.3969/j.issn.2095-0845.2000.04.022 |
邹喻苹, 葛颂, 王晓东. 2001. 系统与进化植物学中的分子标记. 北京: 科学出版社, 140-149.
|
Nei M. 1972. Genetic distance between populations. Am Nat, 106: 283-292. DOI:10.1086/282771 |
Palacios C, Gonzalez C F. 1997. Lack of genetic variability in the rare and endangered Limonium cavanillesii (Plumbaginaceae) using RAPD markers. Molecular Ecology, 6(7): 671-675. DOI:10.1046/j.1365-294X.1997.00232.x |
Wachira F N. 1995. Detection of genetic diversity in tea(Camellia sinensis) using RAPD markers. Genome, 38: 201-210. DOI:10.1139/g95-025 |
 2004, Vol. 40
2004, Vol. 40