文章信息
- 肖祥希, 刘星辉, 杨宗武, 郑蓉, 陈立松.
- Xiao Xiangxi, Liu Xinghui, Yang Zongwu, Zheng Rong, Chen Lisong.
- 铝胁迫对龙眼叶和根细胞超微结构的影响
- EFFECT OF ALUMINUM STRESS ON CELL ULTRA-STRUCTURE OF LEAF AND ROOT OF LONGAN(DIMOCARPUS LONGAN)
- 林业科学, 2003, 39(专刊1): 58-61.
- Scientia Silvae Sinicae, 2003, 39(专刊1): 58-61.
-
文章历史
- 收稿日期:2003-03-21
-
作者相关文章
2. 福建农林大学园艺学院 福州 350002
2. College of Horticulture, Fujian Agriculture and Forestry University Fuzhou 350002
植物在逆境胁迫下, 超微结构遭破坏的研究已有一些报道(陈立松等, 2001; 闫先喜等, 1991; 李荣富等, 1996), 但有关铝胁迫下植物超微结构的研究鲜见报道(刘东华等, 1995)。铝对植物产生毒害作用, 这已被很多研究所证实。铝可与蛋白质结合, 也可与脂质、糖类、核酸等结合, 影响质膜结构和功能, 干扰植物细胞内一些离子代谢, 影响各种生理生化过程正常进行, 从而抑制植物的生长。铝很容易在植物根尖富集(Samuels et al., 1997), 通过作用于根伸长区使植物根尖变短变粗, 影响根对水分和养分的吸收, 限制整个植株的生长(孔繁翔等, 2000)。但铝胁迫下植物细胞内部结构的变化目前还不清楚, 为此, 本文以龙眼(Dimocarpus longan)为材料, 探讨铝胁迫下龙眼叶、根细胞超微结构的变化。
1 材料与方法 1.1 材料供试的材料为龙眼乌龙岭品种, 苗龄为7个月的实生苗。苗木从圃地取出移入培养液中, 经过2个月恢复培养后于2001年7月开始进行铝胁迫, 水培试验营养液采用李延1)的配方, 容器采用外壁漆黑的塑料桶, 每桶3株, 每桶装培养液5 L, 每14 d更换1次培养液, 更换培养液时调节pH至4.2, 每天定时通气3次、每次20 min。试验采用随机区组设计, 铝(Al3+)浓度设0(CK)、0.185、0.370、0.740、1.110、1.850 mmol·L-16个处理, 重复5次, 每个处理共15株。铝胁迫采用在营养液中加铝进行培养的方法进行。胁迫5个月后采叶、根样供电镜观察。
1) 李延.龙眼缺镁胁迫生理及调控技术研究.福建农业大学博士学位论文, 1999
1.2 方法 1.2.1 扫描电镜观察取须根0.3 ~ 0.5 cm左右(含根尖), 用蒸馏水清洗, 浸泡于0.1 mol·L-1PBS (pH =7.4)配制的2.5 %戊二醛内固定。固定后用蒸馏水清洗3次, 每次15 min, 然后用系列梯度酒精(30 %, 50 %, 70 %, 80 %, 90 %, 95 %, 100 %)脱水, 每个梯度脱水10 ~ 15 min, 然后临界点干燥(PVT-3B干燥仪), 在JFC-120镀膜仪上镀上一层金膜, 最后在JSM-5310LV扫描电镜下观察、拍照。
1.2.2 透射电镜观察沿叶脉取叶样1.0 cm ×0.1 cm, 须根0.2 ~ 0.3 cm(根尖2 cm以上部位), 迅速投入5 %的戊二醛(0.1 mol·L-1PBS配制, pH =7.0)固定液中, 抽气直到材料下沉为止, 于冰箱中4 ℃固定24 h, 用0.1 mol·L-1PBS冲洗, 而后用1 %锇酸溶液固定4 h, 再经重蒸水冲洗, 乙醇系列脱水, Epon 812环氧树脂包埋, LKB V型超薄切片机切片, 经醋酸双氧铀和柠檬酸铅染色, 于JEM-1010透射电镜下观察、拍照。
1.2.3 DAPI荧光染色观察取须根根尖0.5 cm进行压片, 加入5 μg·mL-1的DAPI(4, 6-二脒-2-苯基吲哚)染色液5 μL, 甘油-PBS(1:1)封片, ZEISS荧光显微观察, 用ASA400柯达胶卷拍照。
2 结果与分析 2.1 扫描电镜观察的结果铝首先是对根系产生毒害。铝毒害最容易识别的症状就是根的生长抑制, 本试验从龙眼根系铝胁迫下外观结构的变化也证明了铝对根系的毒害作用。龙眼根系在未经胁迫时, 根尖匀称, 表皮结构均匀而有规则, 尖削度大小适度(图版Ⅰ-1)。在铝胁迫下, 首先根端膨大, 变粗变短(图版Ⅰ-2、3、4), 且随铝胁迫浓度的增大, 膨大程度也不断增大, 说明根冠细胞和组织的结构已经发生了变化, 根冠细胞已经受到破坏; 其次, 根尖表皮出现某种程度的龟裂(图版Ⅰ-2、3、4), 龟裂程度随铝胁迫浓度的增大而不断加重, 铝浓度为1.850 mmol·L-1时, 可见到龟裂程度不仅限于外皮层、皮层, 甚至到达内皮层或中柱, 说明铝毒害造成根尖从外皮层、皮层、内皮层到中柱等各层细胞不断深入的破坏。

|
图版Ⅰ Plate Ⅰ 图版Ⅰ~ Ⅲ :C.叶绿体; S.淀粉粒; N.细胞核; V.液泡; CW.细胞壁; CY.细胞质; G.基粒片层; M.线粒体; NE.核膜; NU.核仁; MR.线粒体核糖体; PM.细胞质膜; ER.内质网; T.液泡膜。Plate Ⅰ ~ Ⅲ :C.Chloroplast; S.Starch vacuole; N.Nucleus; V.Vacuole; CW.Cell wall; CY.Cytoplasm; G.Stroma lamellae; M.Mitochondria; NE. Karyotheca; NU.Nucleolus; MR.Mitochondria ribosome; PM.Cytoplasm membrane; ER.Endoplasm reticulum; T.Vacuole membrane. 1.正常根尖(CK), ×200;2.0.185 mmol·L-1铝胁迫下的根尖, 根冠稍有膨大和龟裂, ×50;3.0.740 mmol·L-1铝胁迫下的根尖, 根尖部分变短变粗, 龟裂明显, ×50;4.1.850 mmol·L-1铝胁迫下的根尖, 根尖膨大且严重龟裂, 受害严重, ×50;5.(×3 000), 6.(×3 000), 7.(×40 000), 8.(×30 000)正常龙眼叶片细胞的超微结构; 9.0.740 mmol·L-1铝胁迫下龙眼叶片细胞的超微结构, ×3 000。1.Natural root tip of Longan (CK), ×200;2.Root tip of Longan under 0.185 mmol·L-1 aluminum stress, ×50;3.Root tip of Longan under 0.740 mmol·L-1 aluminum stress, ×50;4.Root tip of Longan under 1.850 mmol·L-1 aluminum stress, ×50;5.(×3 000), 6.(×3 000), 7.(×40 000), 8. (×30 000)Cell ultra-structure of natural Longan leaf; 9.Cell ultra-structure of Longan leaf under 0.740 mmol·L-1 aluminum stress, ×3 000. |
正常(未经胁迫)的龙眼叶片的海绵组织和柱状栅栏组织细胞内含有大量的叶绿体, 这些叶绿体及细胞质和细胞核被细胞内大液泡挤在紧贴细胞壁的部位, 叶绿体呈梭形, 大量的淀粉粒分散在叶绿体的基质中, 细胞核完整, 核膜清晰(图版Ⅰ-5、6)。叶绿体结构完整, 基粒片层整齐有序, 呈平行排列。在叶绿体周围有许多线粒体, 线粒体呈圆形或肾形, 双层膜清晰, 外膜平滑, 内膜内折形成许多形式不同的嵴, 线粒体内有大量的核糖体(图版Ⅰ-7、8), 说明细胞正在进行着比较旺盛的能量代谢。在铝胁迫下, 龙眼叶片细胞的超微结构发生了很大变化。铝浓度为0.740 mmol·L-1时, 叶片细胞的细胞壁开始降解, 叶绿体膜消失, 叶绿体与细胞质混在一起, 基粒片层扭曲, 分布混乱, 淀粉粒明显变少甚至看不到(图版Ⅰ-9, 图版Ⅱ-1), 线粒体变形, 线粒体膜局部破裂, 嵴的数量减少且结构模糊(图版Ⅱ-2)。随铝浓度的增大, 细胞超微结构破坏更严重, 细胞壁局部降解甚至几乎破裂, 细胞质和细胞器完全溶在一起, 叶绿体基粒片层更加混乱, 线粒体膜消失, 线粒体几乎解体(图版Ⅱ-3、4、5)。

|
图版Ⅱ Plate Ⅱ 1.(×40 000), 2.(×30 000)0.740 mmol·L-1铝胁迫下龙眼叶片细胞的超微结构; 3.(×3 000), 4.(×40 000), 5.(×40 000)1.850 mmol·L-1铝胁迫下龙眼叶片细胞的超微结构; 6.(×4 000), 7.(×40 000), 8.(×15 000)正常龙眼根尖伸长区细胞的超微结构; 9.0.740 mmol·L-1铝胁迫下龙眼根尖伸长区细胞的超微结构, ×4 000。 1.(×40 000), 2.(×30 000)Cell ultra-structure of Longan leaf under 0.740 mmol·L-1 aluminum stress; 3.(×3 000), 4.(×40 000), 5.(×40 000) Cell ultra-structure of Longan leaf under 1.850 mmol·L-1 aluminum stress; 6.(×4 000), 7.(×40 000), 8.(×15 000)Cell ultra-structure of elongation part of natural Longan root tip; 9.Cell ultra-structure of elongation part of Longan root tip under 0.740 mmol·L-1 aluminum stress, ×4 000. |
龙眼须根伸长区细胞在正常情况下, 细胞中含丰富的淀粉粒和细胞质, 细胞与细胞之间间距较大, 细胞核完整, 核膜和核仁清晰可见, 线粒体数量较多, 双层膜清晰(图版Ⅱ-6、7、8 )。在0.740 mmol·L-1铝胁迫下, 细胞壁开始降解, 细胞间距变小, 淀粉粒消失, 但线粒体数量增加, 其结构尚完好, 核膜局部破裂, 核仁消失, 核仁内物质外流(图版Ⅱ-9; 图版Ⅲ-1、2)。当铝胁迫浓度为1.850 mmol·L-1时, 细胞壁严重降解, 细胞之间几乎粘在一起, 看不到淀粉粒, 线粒体结构遭破坏, 膜破裂, 嵴散落在细胞质中, 形成内质网, 核膜破裂, 细胞核几乎解体(图版Ⅲ-3、4、5)。
|
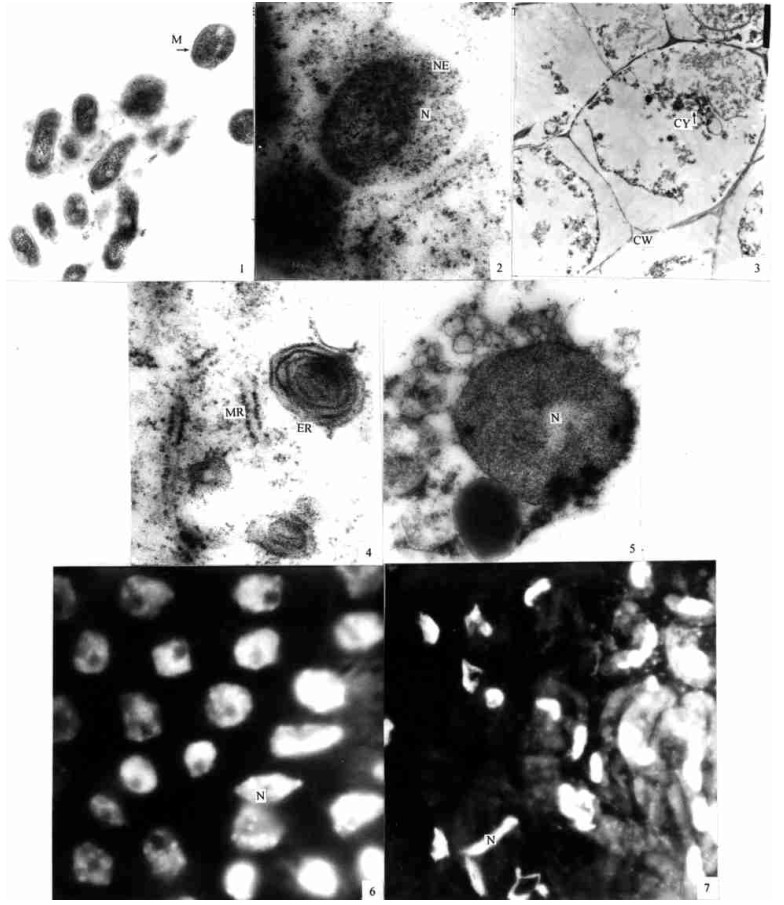
图版Ⅲ Plate Ⅲ 1.(×15 000), 2.(×40 000)0.740 mmol·L-1铝胁迫下龙眼根尖伸长区细胞的超微结构; 3.(×3 000), 4.(×40 000), 5.(×30 000)1.850 mmol·L-1铝胁迫下龙眼根尖伸长区细胞的超微结构; 6.正常龙眼根尖分生区细胞的超微结构, ×100;7.0.740 mmol·L-1铝胁迫下龙眼根尖分生区细胞的超微结构, ×100。 1.(×15 000), 2.(×40 000)Cell ultra-structure of elongation part of Longan root tip under 0.740 mmol·L-1 aluminum stress; 3.(×3 000), 4.(×40 000), 5.(×30 000)Cell ultra-structure of elongation part of Longan root tip under 1.850 mmol·L-1 aluminum stress; 6.Cell ultra-structure of division part of natural Longan root tip, ×100;7.Cell ultra-structure of division part of Longan root tip under 0.740 mmol·L-1 aluminum stress, ×100. |
铝胁迫下大多数植物中, 大部分铝位于根尖分生组织细胞, 且其中大部分存在于细胞核和细胞壁中(刘东华等, 1995)。本试验也观察了铝胁迫下龙眼根尖分生组织细胞核的变化。未经铝胁迫时, 分生组织细胞核形状比较规则透明, 呈圆形、椭圆形或近圆形, 且细胞核数量比较多; 铝胁迫下(0.740 mmol· L-1), 细胞核形状发生较大变化, 呈长柱状、棒状或弯月状, 而且细胞核的数量也大大减少(图版Ⅲ-6、7)。说明铝毒害造成根尖分生组织细胞的破坏, 使细胞核变形, 抑制细胞分裂。
3 讨论 3.1 铝胁迫造成龙眼叶片超微结构的破坏铝胁迫下龙眼叶片细胞超微结构最明显的变化是叶绿体的破坏, 表现为叶绿体膜系统受损加重, 基粒片层扭曲紊乱, 淀粉粒明显减少甚至消失; 其次是细胞壁的降解, 细胞之间间隙变小, 液泡膜破裂, 液泡消失; 线粒体膜系统受到破坏, 嵴数量明显减少甚至消失。说明龙眼叶片细胞叶绿体是铝胁迫比较敏感的细胞器。叶绿体是植物细胞最需O2的分区(Navari-izzo et al., 1999), 同时叶绿体类囊体膜富含不饱和脂肪酸(Nilsen et al., 1996), 因而对活性氧诱发的膜脂过氧化特别敏感。叶绿体是产生活性氧的主要部位, 在正常情况下活性氧的产生和清除维持在一个动态平衡, 不会导致伤害, 但在逆境胁迫下, 活性氧清除系统受到破坏, 这种平衡被打破, 从而导致膜的伤害, 这或许就是叶绿体对铝胁迫敏感的原因。同时也表明铝胁迫下龙眼的光合作用受到抑制, 这从细胞淀粉粒的减少也可以证实。植物体的细胞壁具有很强的积累阳离子的能力, 铝主要与细胞壁的成分(细胞壁的胶质、蛋白质等)结合, 降低细胞壁的弹性和导水性, 影响植物正常的代谢活动(Zhang et al., 1992); 铝易与细胞质膜上的磷酸基、羟基等极性基团结合, 影响膜的结构和功能(孔繁翔等, 2000)。另外, 线粒体是三羧酸循环和生物氧化进行的部位, 铝胁迫下线粒体膜的破坏、嵴数量减少, 必将影响到三羧酸循环和生物氧化进行, 从而影响到龙眼叶片的能量代谢。
3.2 铝胁迫对龙眼根系形态与超微结构的影响铝对植物的毒害首先是对根系产生危害, 表现为根尖外观形态的变化和结构的破坏, 这已为许多学者的研究所证实(田仁生等, 1990; Clarkson, 1996; 沈金雄等, 1998; Samuels et al., 1997; Macklon et al., 1992)。本试验结果表明, 铝胁迫下龙眼根端膨大, 根尖变粗变短, 从外表皮到中柱出现不同程度的龟裂, 且随铝浓度的提高, 这种伤害程度不断加重。说明当龙眼发生铝毒害, 根冠组织和细胞、根尖的皮层组织和细胞受到破坏, 根冠和根表皮外的粘质分泌物被认为是铝胁迫下起保护作用的一道防线(刘东华等, 1995), 因此龙眼根尖这种外部结构的变化, 一方面严重影响植株对水分和养分的吸收, 另一方面, 削弱了阻止铝侵入体内的功能。
铝胁迫下, 龙眼须根伸长区细胞细胞壁发生降解, 细胞间距变小, 细胞壁弹性变小, 僵硬度增加; 膜系统也遭到破坏, 核膜、线粒体膜破裂; 线粒体在中度铝胁迫(0.740 mmol·L-1)时, 数量有所增加, 可能是植株通过短暂增加呼吸, 来提供维持其它生理活动的能量, 至于此时呼吸效率如何, 尚须进一步探讨, 因为铝可与ATP结合, 形成Al-ATP复合物, 从而影响ATP的利用(田仁生等, 1990)。水稻的铝胁迫研究也证明了这一点, 铝胁迫下水稻根系线粒体的呼吸耗氧速率ADP:O降低, 呼吸效率降低(郝鲁宁等, 1989)。高浓度的铝胁迫导致线粒体结构遭破坏, 甚至解体。铝胁迫下, 根伸长区细胞的淀粉粒明显减少, 甚至消失, 说明铝影响了根系碳水化合物的积累。另外, 根尖分生组织细胞在铝胁迫下也发生变化, 细胞核变形, 数量大大减少, 说明细胞的分裂受到了抑制。
陈立松, 刘星辉. 2001. 水分胁迫对荔枝叶片超微结构的影响. 福建农业大学学报, 30(2): 171-174. |
郝鲁宁, 刘厚田. 1989. 铝对水稻幼苗的生理影响. 植物学报, 31(11): 847-853. |
孔繁翔, 桑伟莲, 蒋新, 等. 2000. 铝对植物毒害及植物抗铝作用机理. 生态学报, 20(5): 855-862. DOI:10.3321/j.issn:1000-0933.2000.05.023 |
李荣富, 王丽雪. 1996. 低温胁迫对葡萄叶片及根系细胞亚显微结构的影响. 华北农学报, 11(4): 109-113. DOI:10.3321/j.issn:1000-7091.1996.04.022 |
刘东华, 蒋悟生, 李懋学. 1993. 铝(Al3+)对洋葱根生长和细胞分裂的影响. 华北农学报, 8(1): 35-41. DOI:10.3321/j.issn:1000-7091.1993.01.007 |
刘东华, 蒋悟生. 1995. 铝对植物的毒害. 植物学通报, 12(1): 24-32. |
沈金雄, 徐巧珍. 1998. 大豆耐铝酸毒害研究概况. 中国油料作物学报, 20(2): 91-96. |
田仁生, 刘厚田. 1990. 酸化土壤中铝及其植物毒性. 环境科学, 11(6): 41-46. |
闫先喜, 赵坦芳, 叶宝兴, 等. 1991. 盐胁迫对大麦胚根细胞膜系统的影响. 植物学报, 36(增): 33-36. |
Clarkson D T. 1996. Effect of aluminum on the uptake and metabolism of phosphorus by barley seeding. Plant physiol, 41: 165-172. |
Macklon A E S, Sim A. 1992. Modifying effects of non-toxic levels of aluminum on the uptake and transports of phosphate in ryegrass. J Exp Bot, 43: 915-923. DOI:10.1093/jxb/43.7.915 |
Navari-izzo F, Rascid N. Plant responses to water-deficit condition. In : PressarakliM. Handbook of plant and crop stress. 2nd edition. New York : Marcel Dekker, 1999: 231-270
|
Nilsen E T, Orcutt D M. 1996. The physiology of plants under stress. New York: John Wiley & Sons, 70.
|
Samuels T D, Kucukakyuz K, Magaly R Z. 1997. Al partitioning patterns and root growth as related to Al sensitivity and Al tolerance in wheat. Plant physiol, 113: 527-534. DOI:10.1104/pp.113.2.527 |
Zhang G, Taylor G J. 1992. Effects of biological inhibitions on kinetics of aluminum uptake by excised roots and purified cell wall material of aluminum-tolerant and aluminum-sensitive of Triticum aestivum L. J Plant Physiol, 138: 533-539. |
 2003, Vol. 39
2003, Vol. 39
