文章信息
- 詹福建, 巫光宏, 黄卓烈, 罗焕亮, 孟立科.
- Zhan Fujian, Wu Guanghong, Huang Zhuolie, Luo Huanliang, Meng Like.
- 马占相思树对低温冻害的抗性研究
- STUDY ON THE RESISTANCE OF ACACIA MANGIUM TO LOW TEMPERATURE STRESS
- 林业科学, 2003, 39(1): 56-61.
- Scientia Silvae Sinicae, 2003, 39(1): 56-61.
-
文章历史
- 收稿日期:2000-10-23
-
作者相关文章
2. 华南理工大学食品与生物工程学院 广州 510641
2. College of Food and Biological Engineering, South China University of Technology Guangzhou 510641
低温冷害是限制植物自然分布和栽培区带的主要因素(李红元等,1999),低温影响植物的生长代谢,引起植物相关生理指标变化。在植物抗寒性研究中,有许多报道(武惠肖等,2000;艾希珍等,1999;陈杰忠等,1999;简令成,1983)指出耐寒性植物在低温胁迫下,细胞膜渗透性、电导率、脯氨酸、水溶性糖、蛋白质含量发生变化,并与植物的抗冷性密切相关。同时,植物经低温胁迫后体内很多酶的活性,如ATP酶(ATPase)发生明显变化,并且酶活性与植物抗寒性呈一定的相关性(李美茹等,1997;1995;彭永康等,1995;刘鸿先等,1981;简令成等,1981)。相关研究表明,抗寒性强的植物在低温逆境下,超氧化物歧化酶(SOD)、过氧化氢酶(CAT)和过氧化物酶(POD)等保护酶系统仍能维持较高的活性水平,因而防止了因冷害产生的毒害物质如活性氧自由基的积累,减轻了由膜脂过氧化所引起的膜伤害,从而增加机体的抗寒能力(李晶等,2000;彭永康等,1994;陈贻竹等,1988)。
马占相思(Acacia mangium)是优良的造纸、防护、水土保持、庭院绿化树种,具有较高的经济价值。因而,选择耐寒性较强的家系成为目前降低栽种风险的主要措施之一,但有关马占相思的抗寒机理研究还未见系统报道。本文通过对马占相思PNE17868家系对低温冻害引起的相关生理生化指标变化与抗寒性关系的研究,为引种栽培和抗寒育种提供理论依据和实践指导。
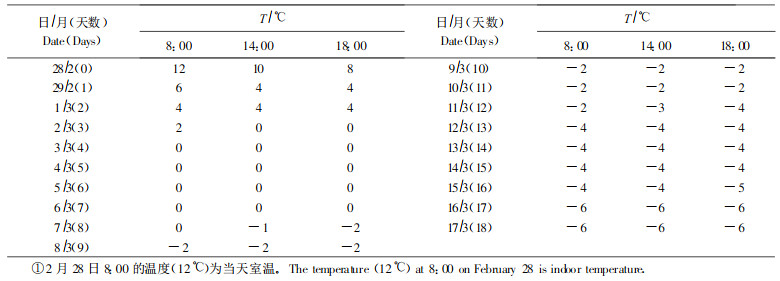
1 材料与方法 1.1 实验材料及低温处理本试验所用的材料是马占相思PNE17868家系(简称P家系)树苗,由广州市林业科学研究所提供。试验材料盆栽。低温处理在人工气候室中进行。人工降温程序见表 1。光照时间:8:00 ~18:00,10 h·d-1。光照强度为250 μE·m-2s-1,湿度为85%~95%,对照组于室外条件培植,室外平均温度为(20±2)℃。
|
|
各项检测项目采用随机区组设计,设3个处理组和3个对照组,每次处理设3个重复实验。在低温处理过程中,每2 d取样1次进行检测,采样时间均为8:00,每次分别取低温处理组和对照组各3盆植株(每盆1株),取每棵植株的第3位至第8位叶状体(叶柄)进行各种分析。
1.2 测定方法游离脯氨酸采用磺基水杨酸提取,酸性茚三酮显色,分光光度计比色法测定含量(张殿忠等,1990)。水溶性糖含量测定采用3,5-二硝基水杨酸比色法(北京大学生物系生化教研室,1987)。电导率采用电导仪(DDS-11AGA型)测定,以叶片杀死前的电导率占杀死后(全透性)电导率的百分数来表示膜的相对透性(西北农业大学植物生理教研室,1987)。可溶性蛋白质含量测定参照Bradford(1976)的考马斯亮蓝法,用牛血清蛋白作为标准。
酶液提取方法:称取0.5 g叶柄,用5 mL 0.05 mol·L-1磷酸缓冲液(pH7.8)冰浴研磨,10 000 r·min-1离心20 min,收集上清液,进行蛋白质含量及各种酶活性测定。过氧化氢酶(CAT)的活性测定采用碘量法(北京农业大学食品系,1984),酶活性以μg H2O2·mg-1protein min-1表示。过氧化物酶(POD)的活性测定采用愈创木酚法(高雯等,1991)测定,酶活性以ΔOD470nm·mg-1protein min-1表示。超氧化物歧化酶(SOD)的活性测定采用SOD抑制氮蓝四唑(NBT)光化还原法(Giannoplitis, 1977),以抑制NBT光化还原50%为一个酶活性单位,酶活性以U·mg-1protein min-1 表示。ATP酶(ATPase)活性测定采用孔雀石绿比色法(Lanzetta, 1979),酶活性以ATPase水解ATP生成无机磷的速率μmol Pi·mg-1protein min-1表示。
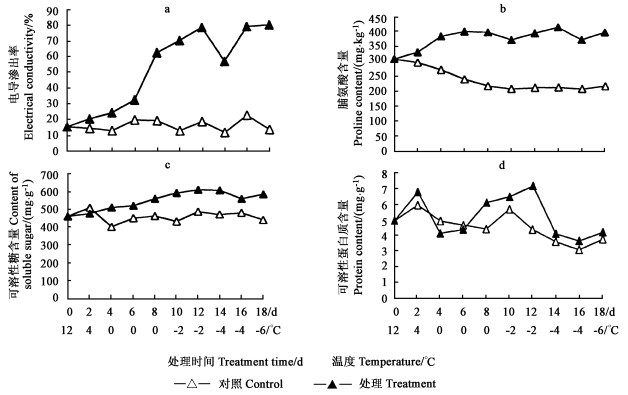
2 结果与分析 2.1 低温胁迫对P家系细胞质膜透性的影响马占相思P家系幼苗受到低温胁迫后,无论是随胁迫程度的加深还是随胁迫时间的延长,叶柄细胞质膜的相对透性均表现出递增的趋势。从图 1-a可见,当温度降至4℃时(即低温处理后第2天,简称2 d,以下同),与对照组相比,相对电导率增加了40.03%,降至0℃(8 d)时,相对电导率增加了2.19倍,降至-6℃(18 d),增加了4.89倍。实验结果表明,进一步降低温度使得细胞膜受到冻害,电解质大量外渗。可见,温度降至-6℃已给P家系树苗造成较严重的冻害。表 2电导率变化的方差分析表明,低温处理后植株的电导率极显著高于对照组(P<0.01)。说明随着温度逐渐下降,细胞有较显著的损伤。
|
图 1 低温处理对马占相思相对电导率、脯氨酸、可溶性糖和可溶性蛋白质含量的影响 Fig. 1 Effect of low temperature treatment on the electrical conductivity, the contents of proline, soluble sugar and protein in Acacia mangium |
|
|
图 1-b表明,当温度降至0℃,P家系树苗叶柄脯氨酸含量与对照组相比,不断增加。例如,0 ℃(4 d)增加了41.65%,陆续降低温度,到-6℃(18 d)增加83.70%。脯氨酸持续积累表明了P树苗具有较强的渗透调节能力。表 2脯氨酸含量变化的方差分析表明,低温处理后植株的脯氨酸含量显著高于对照组(P<0.01)。
2.3 低温胁迫对P家系可溶性糖含量的影响随着低温胁迫程度加深和时间的延长,马占相思P家系树苗可溶性糖含量稍微下降,然后持续增加(图 1-c)。当温度降至4℃(2 d),可溶性糖含量比对照组下降了6.32%,降至0℃(6 d)增加了27.07%,降到-6℃(18 d)增加了32.74%。表 2列出了可溶性糖变化的方差分析,低温处理后植株的可溶性糖含量显著高于对照组(P<0.01)。可见,可溶性糖也是植物体内一种重要的渗透调节物质。因此,马占相思P家系树苗在低温胁迫下可溶性糖持续积累,增强了其对低温冻害的抵抗能力。
2.4 低温胁迫对P家系可溶性蛋白质的影响从图 1-d中可看出,处理刚刚开始时可溶性蛋白质含量有一定波动。例如温度下降到0℃(4 d)时,蛋白质含量下降了16.00%;下降到-2℃(12 d)上升了63.51%,而下降到-6℃(18 d)上升了11.85%。从表 2方差分析结果看出,经低温处理后植株的可溶性蛋白质含量与对照组比较没有显著的差异(P>0.05),但在低温处理期间,可溶性蛋白质含量大多都高于对照组,这也有利于增强P家系树苗的抗寒性。
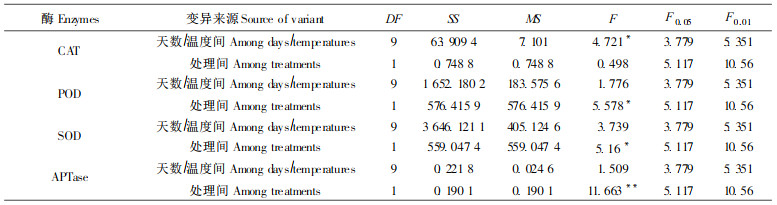
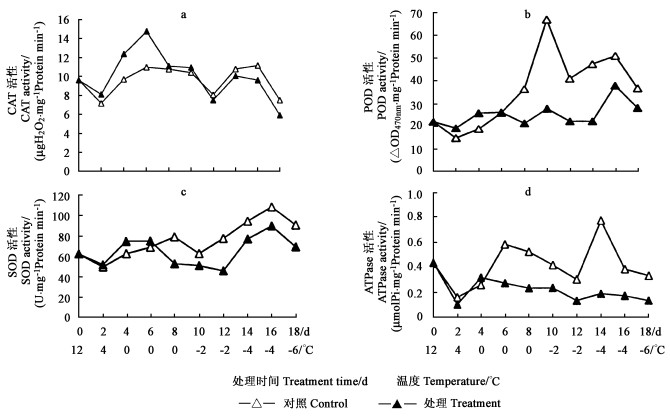
2.5 低温胁迫对P家系过氧化氢酶(CAT)活性的影响由图 2-a可看出,与对照组相比,低温处理下P家系树苗CAT活性随着温度的降低而变化。先是逐渐上升,然后下降。当温度降至4℃(2 d),升高了12.95%;降到0℃(6 d)时升高了34.73%;而到-2℃(10 d)时升高5.08%,可见升幅很小,然后开始下降。到-6℃(18 d)时下降21.14%。方差分析(表 3)表明,低温处理期间植株的CAT活性与对照组相比没有显著的差异(P>0.05),但保持有较高的CAT活性,增强了细胞的保护能力。
|
图 2 低温处理对CAT、POD、SOD和ATPase活性的影响 Fig. 2 Effect of low temperature treatment on CAT, POD, SOD and ATPase activities in Acacia mangium |
在低温处理下,P树苗POD活性先是升高,然后随着低温胁迫程度加深而缓慢下降(图 2-b)。例如温度降至0℃(4 d),POD活性升高了37.00%,而到0℃(8 d)下降了41.32%,到-6℃(18 d)下降23.48%。实验结果表明,-6℃(18 d)、-4℃(16 d)POD活性下降幅度较小,表明树苗对低温冻害已有一定的抗性而使POD活性维持在较高水平,消除寒害产生的有毒物质对细胞的伤害。方差分析结果(表 3)表明,低温处理后植株的POD活性显著低于对照组(P<0.05)。
|
|
从图 2-c中看出,最初温度下降的时候,与对照相比,处理的SOD活性呈上升状态,如温度降至0℃(4 d),SOD活性比对照组增加了19.23%,0℃(6 d)增加了8.56%。说明P家系体内的保护酶SOD和CAT、POD一样,对温度有一个适应过程,具有一定的抗寒性。随温度下降,SOD活性有所下降但幅度不大,如下降到-6℃(18 d),SOD活性下降了23.61%。而方差分析结果(表 3)表明,经低温处理的植株SOD活性没有显著低于对照组(P>0.05)。特别是随着温度的进一步降低,SOD活性下降幅度不大,这表明P家系树苗对低温冻害有较高的抗性。
2.8 低温处理对P家系APT酶(ATPase)活性的影响ATPase是一种与细胞膜结合的酶,执行着膜内外离子传递的作用,而低温对树苗伤害首先从损伤膜的结构开始。所以,低温冻害的程度与ATPase活性下降呈一定的相关性。这可从图 2-d中看出,当温度下降至4℃(2 d),ATPase活性下降了36.65%,0℃(8 d)下降了55.45%,-6℃(18 d)下降了63.60%。方差分析结果(表 3)表明,低温处理后植株的ATPase活性显著低于对照组(P<0.05)。
3 讨论生物膜与植物寒害和抗寒性的密切关系已为许多实验结果所证实(简令成,1983;李美茹等,1995;陆旺全等,2000;武惠肖等,2000),且寒害与细胞膜的半透性的破坏有关。电导率大小与组织受寒害的程度成正相关。在本实验中,随着低温胁迫程度加深和时间的延长,P家系树苗叶柄细胞膜电解质的相对渗出率与对照组相比逐渐升高(图 1-a),表明低温冻害对树苗具有一定伤害。当温度下降时,P家系树苗细胞质膜ATPase活性下降(图 2-d)。这也表明低温胁迫对P家系树苗的细胞膜有伤害作用。ATPase变化与低温处理直接相关。ATPase是一种与细胞膜相结合的功能蛋白,在低温胁迫下,植物细胞膜结构受到破坏而使ATPase活性下降(简令成等,1981;彭永康等,1994;Kasamo, 1988),使细胞对物质主动吸收与运输功能降低,细胞的渗透调控降低,导致细胞内溶质外渗,结果引起机体内整个生理过程受到破坏。如果ATPase活性下降太严重,甚至丧失,那么就会导致机体死亡;如果ATPase活性虽有所下降,但仍保持一定活性,仍能维持细胞的正常功能,则植物具有一定的抗寒性。相关的研究结果表明,经低温锻炼而具有抗寒性的冬小麦(简令成,1983)、黄瓜(戴金平等,1991),其质膜的ATPase活性升高,或保持一定稳定性。而对低温敏感的番茄(简令成等,1981)、玉米(彭永康等,1995)、白菜(李美茹等,1997),遭到低温冻害时,质膜ATPase活性下降很快,甚至完全丧失。可见,ATPase活性与植物抗寒性具有密切关系。本实验结果表明,P家系树苗对低温胁迫具有一定的适应性和抵抗性。
细胞膜是细胞对外界的屏障。当细胞面临环境的低温胁迫时,需要进行渗透调节以维持细胞内外的渗透平衡,因此必然会使机体内参与渗透调节的物质如脯氨酸、糖、蛋白质等发生变化,从而避免冻害,提高植物抗寒能力。有证据表明,脯氨酸、可溶性糖和可溶性蛋白质参与调控抗冷力的形成(艾希珍等,1999;陈杰忠等,1999;李美茹等,1995;陆旺全等,2000;柴团耀等,1999;武惠肖等,2000),在植物抗寒中起重要作用。在本实验中,马占相思P家系树苗脯氨酸随着低温胁迫程度加深和时间延长,表现出持续增加趋势(图 1-b);同时,可溶性糖含量也随着温度降低逐渐升高,这与某些经冷驯化而获得一定抗寒能力的植株如落叶松(武惠肖等,2000)、黄瓜(艾希珍等,1999)、香蕉(陈杰忠等,1999)的实验结果相符。表明脯氨酸、可溶性糖持续积累使得P家系树苗具有较强渗透调节能力。另一方面,脯氨酸、可溶性糖在细胞质中大量积累,不仅保持了蛋白质的水合度,防止原生质脱水,而且还起到了平衡细胞质与液泡间的渗透势等多种作用,减低质膜受冻害的程度,从而增强了植物对冻害的适应能力。有关研究表明,植物可溶性蛋白质升高也有利于抗寒性提高(武惠肖等,2000;万琳琛等,2001;陈杰忠等,1999;简令成,1983;李美茹等,1995;刘鸿先等,1981)。在本实验中,在低温胁迫下,P家系树苗的可溶性蛋白质含量先是下降,然后随着温度下降呈上升趋势,这可能是在低温胁迫下,某一类特殊的蛋白质合成会增加,以保护植物。
在正常情况下,植物体内存在着有效的保护酶系统(SOD、POD、CAT),以清除潜在的有毒物质。遇到低温逆境时,这种清除机制就会受阻,导致体内活性氧积累,造成对膜的伤害和生物大分子破坏,使DNA产生损伤,影响蛋白质合成与稳定,进而造成代谢功能失效和细胞死亡。在低温胁迫下,植物体内保护酶活性变化已有较多报道(万琳琛等,2001;李晶等,2000;陈贻竹等,1988;彭永康等,1994;刘鸿先等,1985;戴金平等,1991)。一般认为,抗寒植物在低温胁迫下,CAT、POD、SOD活性有些表现为先升后降,如豌豆(彭永康等,1994);有些则表现为维持恒定或略有增高的趋势,如经冷驯后的黄瓜(戴金平等,1991)、红松(李晶等,2000);而不耐寒的植物其保护酶活性则表现为一直降低趋势,如番茄(陈贻竹等,1988)。本实验中,随着温度逐渐下降,P家系树苗的CAT活性在4℃(2 d),0℃(8 d),-2℃(12 d)升高,然后随着温度进一步降至-4℃, -6℃,CAT活性有所下降(图 2-a),而SO D、POD活性亦是随着温度下降先是升高,然后缓慢降低,但降幅不大(图 2-b, c)。实验结果表明,马占相思P家系树苗受低温胁迫时,体内的CAT、POD、SOD保护酶的活性仍能维持较高水平,因而避免了活性氧等各种自由基的大量积累,减轻了膜脂过氧化作用,降低了细胞膜的破坏程度。这也是P家系树苗有较强抗寒能力的原因。
艾希珍, 于贤昌, 王绍辉, 等. 1999. 低温胁迫下黄瓜嫁接苗与自根苗某些物质含量变化(简报). 植物生理学通讯, (1): 26-28. |
北京大学生物系生化教研室. 1987. 生物化学实验指导. 北京: 高等教育出版社, 22-24.
|
北京农业大学食品系. 1984. 食品化学实验指导. 北京: 北京农业大学出版社, 103.
|
柴团耀, 张玉秀. 1999. 菜豆富含脯氨酸、蛋白质基因在生物和非生物胁迫下的表达. 植物学报, 41(1): 111-113. DOI:10.3321/j.issn:1672-9072.1999.01.022 |
陈杰忠, 徐春香, 梁立峰. 1999. 低温对香蕉叶片中蛋白质和脯氨酸的影响. 华南农业大学学报, 20(3): 54-58. |
陈贻竹, B.帕特森. 1988. 低温对植物叶片中超氧化物歧化酶、过氧化氢酶和过氧化氢水平的影响. 植物生理学报, 14(4): 323-328. |
戴金平, 沈征言, 简令成. 1991. 低温锻炼对黄瓜幼苗几种酶活性的影响. 植物学报, 23(8): 627-632. |
高雯, 姜培荣, 张之佳, 等. 1991. 食品酶学原理与方法. 哈尔滨: 黑龙江科学技术出版社.
|
简令成. 1983. 生物膜与植物抗寒害和抗寒性的关系. 植物学通报, 1(1): 17-23. |
简令成, 董合铸, 孙龙华. 1981. 番茄子叶细胞内三磷酸腺苷酶活性的超微结构定位及其在冷害中的变化. 植物学报, 23(4): 257-264. |
李纪元, 高传璧, 郑学为, 等. 1999. 两个相思树种的耐寒性评估. 林业科学研究, 12(1): 87-91. DOI:10.3321/j.issn:1001-1498.1999.01.015 |
李晶, 阎秀峰, 祖元刚. 2000. 低温下红松幼苗活性氧的产生及保护酶的变化. 植物学报, 42(2): 148-152. DOI:10.3321/j.issn:1672-9072.2000.02.007 |
李美茹, 刘鸿先, 王以柔. 1995. 植物细胞中的抗寒物质及其与植物抗冷性的关系. 植物生理学通讯, (5): 328-334. |
李美茹, 刘鸿先, 王以柔. 1997. 植物细胞膜ATP酶及其与植物低温生理过程的关系(综述). 热带亚热带植物学报, 5(3): 74-82. |
刘鸿先, 曾韶西, 李平. 1981. 植物抗寒性与酶系统多态性的关系. 植物生理学通讯, (6): 6-11. |
刘鸿先, 曾韶西, 王以柔, 等. 1985. 低温对不同耐寒力的黄瓜(Cucumis sativus)幼苗子叶各细胞中超氧物歧化酶(SOD)的影响. 植物生理学报, 11(1): 48-57. |
陆旺全, 李雪萍, 季作梁. 2000. 植物耐寒性的诱导及其与蛋白质的合成、基因表达的关系. 华南农业大学学报, 21(1): 82-86. DOI:10.3969/j.issn.1001-411X.2000.01.025 |
彭永康, 郝泗城. 1995. 低温对玉米、高梁和白菜幼苗生长的伤害与ATPase同工酶的关系. 西北植物学报, 15(4): 294-300. DOI:10.3321/j.issn:1000-4025.1995.04.007 |
彭永康, 郝泗城, 王振英. 1994. 低温处理对豌豆幼苗生长和POD、COD、ATPase同工酶的关系. 华北农学报, 9(2): 76-80. DOI:10.3321/j.issn:1000-7091.1994.02.015 |
万琳琛, 肖尊安, 王英典, 等. 2001. 猕猴桃属种间体细胞杂种试管苗的抗寒性. 果树学报, 18(3): 148-151. |
武惠肖, 吉艳芝, 何海龙, 等. 2000. 落叶松几个抗寒生理指标研究. 河北林果研究, 15(2): 105-109. DOI:10.3969/j.issn.1007-4961.2000.02.002 |
西北农业大学植物生理教研室. 1987. 植物生理学实验指导. 西安: 陕西科学技术出版社.
|
张殿忠, 汪沛洪, 赵云贤, 等. 1990. 测定小麦叶片游离脯氨酸含量的方法. 植物生理学通讯, (4): 62-65. |
Bradford M M. 1976. A rapid and sensitive method for the quantation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal Biochem, 72: 248-254. DOI:10.1016/0003-2697(76)90527-3 |
Giannoplitis C N, Ries S K. 1977. Superoxide dismutases:I.Occurrence in higher plants. Plant Physiol, 59: 309-314. DOI:10.1104/pp.59.2.309 |
Kasamo K. 1988. Response of tonoplast and plasma membrane ATPase in chilling-sensitive and insensitive rice(Oryza sativa L.)culture cell to low temperature. Plant Cell Physiol, 29(7): 1085-1094. |
Lanzetta P A, Alvarez L J, Reinach P S, et al. 1979. An improved assay for nanomole amounts of inorganic phosphate. Anal Biochem, 100: 95-97. DOI:10.1016/0003-2697(79)90115-5 |
 2003, Vol. 39
2003, Vol. 39