文章信息
- 郭志华, 臧润国, 奇文清, 余让才, 刘正宇.
- Guo Zhihua, Zang Runguo, Qi Wenqing, Yu Rangcai, Liu Zhengyu.
- 两种原始兰科植物生理生态特征的比较
- COMPARISON OF THE ECO-PHYSIOLOGICAL CHARACTERISTICS BETWEEN TANGTSINIA NANCHUANICA AND Cephalanthera falcata
- 林业科学, 2003, 39(1): 50-55.
- Scientia Silvae Sinicae, 2003, 39(1): 50-55.
-
文章历史
- 收稿日期:2000-10-10
-
作者相关文章
2. 华南农业大学生命科学学院 广州 510642;
3. 重庆市药物研究所 重庆 408435
2. College of Life Science, South China Agriculture University Guangzhou 510642;
3. The Research Institute of Pharmic Plants of Chongqing Chongqing 408435
金佛山兰(Tangtsinia nanchuanica S. C. Chen.)以其近辐射对称的花被、顶生柱头及5枚退化雄蕊等特征,显现出比兰亚科(Orchidoideae)中最原始的头蕊兰属(Cephalanthera)更原始的特征,它的发现对研究兰亚科的系统发育具有十分重要的意义(陈心启,1965)。金佛山兰是单属单种,属国家二级保护植物,仅散生于重庆南川的金佛山及其附近地区,且种群数量极小,在南川观测到的数量小于50株。在其分布区内,金佛山兰多单株散生、且与其亲缘种金兰(Cephalanthera falcata)生长在一起;两者加在一起,至多20~30株散生。除了在花特征上的差异外,金佛山兰与金兰的其他形态特征甚相似而难以区分。但金兰的分布范围很广,从我国西南、华中至日本均有分布(陈心启,1965)。对于金佛山兰的属性和功用,至今还知之不多,甚至还没有人工栽培的成功例子。因此,对金佛山兰及其亲缘种金兰的生理生态研究,可为就地保护或迁地保护提供依据。
1 生境条件金佛山兰分布的海拔高度为800~1 300 m,主要分布在800~900 m的范围内。金佛山兰可见于马尾松(Pinus massoniana)林、稀疏灌丛边缘、林窗和草坡(陈心启,1965);现在,金佛山兰仅见于灌木及草本不发达、林中透光良好的马尾松林下。金佛山兰对光照条件需求较高。分布区土壤为山地黄壤,腐殖质层薄(多<2 cm)。气候为典型的亚热带山地气候,夏季短、气温不高,冬季漫长、冷,霜期较长。
2 材料与方法金佛山兰种群数量稀少,难以在野外自然条件下测定其生理生态特征,因此将其与金兰一起移植至温室,同时定期和不定期观测其生长、光合等指标及其受精过程。2000-04-16~19,将刚发芽的金佛山兰和金兰一起移栽至北京植物园兰花温室。
在花期,同时测定金佛山兰和金兰的光合等生理生态指标。5月上、中旬,选第2~4位完全展开叶片的中部进行光合测定, 测2~5个叶片,每叶片重复3~5次。用LI-COR6400便携式光合作用测定仪开放系统主要测定:光合有效辐射(PAR, μmol photons·m-2s-1), 净光合速率(Pn, μmol CO2·m-2s- 1), 蒸腾速率(E, mmol·m-2s-1), 气温(Ta, ℃), 叶温(Tleaf, ℃), 空气相对湿度(RH, %), 水分亏缺(Vpdl, kPa),参比室气体CO2浓度(Cam, μmol·mol-1), 胞间CO2浓度(Ci, μmol·mol-1)和气孔导度(Con, mol·m-2s-1)。用开放系统进行测定, 可以有效地减少以往用闭路系统测定因叶室改变了测定叶周围的水气条件而造成的实验误差(郭志华等,1997;1998;1999a;1999b)。利用光控系统准确控制光合有效辐射的强度,由高到低, 直到PAR为0,以测定光响应和暗呼吸速率(Rd, μmol CO2·m-2s-1); 用温控系统逐渐改变叶温,以测定气体交换的温度响应。叶气温差(Δt, ℃)由计算获得; 光补偿点(LCP, μmol photons·m-2s-1)和光饱和点(LSP, μmol photons·m- 2s-1)根据Pn的光响应曲线估计。金佛山兰和金兰的光合速率在9:00左右达到高峰,因此,将这一时段内测定的各项指标作为金佛山兰和金兰的特征值。瞬时光能利用率(SUE)和瞬时水分利用率(WUE)的定义参照Field等(1989),分别表示Pn与PAR的比值、Pn与E的比值,旨在表示植物的潜在资源利用效率(郭志华等,1999a)。由于金佛山兰和金兰的营养体形态近似,因此其叶面积以最大叶的长与宽的积表示,旨在比较两者叶之间的异同而非准确值。
统计分析利用SAS软件。
3 结果与讨论 3.1 各项生理生态指标的比较金佛山兰和金兰的各项生理生态指标见表 1。从表 1可以看出,金佛山兰和金兰在气孔导度和水分利用率等方面有显著差异, 在胞间CO2浓度方面有极显著差异,而在植株高度、最大叶面积、净光合速率、暗呼吸速率、蒸腾速率、胞间CO2浓度和光利用率等方面两者均无显著差异。
|
|
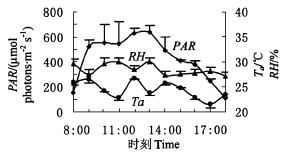
考虑到温室的特殊条件,在测定期间尽量使温室内的光照等生态因子的日变化规律与室外一致。相对地,光合有效辐射PAR的日变化更接近室外晴天。5月上旬,温室内PAR在9 :00左右就可高达近600 μmol·m-2s-1,中午在550~800 μmol·m-2s-1之间波动,16:00以后显著下降到400 μmol·m-2s-1以下。室外PAR可高达1 500 μmol·m-2s-1以上。由于屋顶等的影响,晴天温室内的PAR偶尔因阻挡可以下降到400 μmol·m-2s-1以下,但持续时间多在10 min以下。因为温控设备的作用,温室内的相对湿度和气温有不规则的波动,叶面温度也随之一起波动(图 1)。
|
图 1 光合有效辐射(PAR)、气温(Ta)、相对湿度(RH)的日变化 Fig. 1 Diurnal changes of photosynthetic active radiation (PAR), air temperature (Ta) and relative humidity (RH) |
金佛山兰净光合速率的日变化呈单峰型,峰值持续时间很长, 无明显午休。9:00左右, Pn达到1 d的最高峰, 约6 μmol·m-2s-1左右,直到13:00Pn均可保持在一个很高的水平, 之后逐渐下降,17:00的净光合速率也高达3.0 μmol·m-2 s-1以上(图 2)。蒸腾速率在9:00左右达到1 d的最高峰,约2.7 mmol·m-2s-1左右,之后显著下降,10:00~15:00间E在1.2~1.6之间波动,16:00~ 17:00下降至1 mmol·m-2s-1左右,18:00略有回升。气孔导度在8:00开始测量时最高,约0.11 mol·m-2s-1左右;之后缓慢下降,13:00左右略有回升;1 7:00左右的Con全天最低,约为0.05 mol·m-2s-1左右。胞间CO2浓度的日变化为典型的午间降低型,8:00约为230 μmol·mol-1, 12:00下降至150 μmol ·mol-1左右,之后又显著回升,到18:00左右高达280 μmol·mol-1。金佛山兰的光能利用率在8:00最高,可达近25%以上,9:00显著下降至10%左右,之后在6%~12%之间波动。金佛山兰的水分利用率的日变化表现为双峰型,10:00及17:00达到峰值,14:00达到低谷。与金佛山兰生长在一起的金兰,其净光合速率、蒸腾速率、气孔导度、胞间CO2浓度、光能利用率和水分利用率等的日变化趋势与金佛山兰完全一致,并且净光合速率、蒸腾速率和光能利用率等的大小也很接近,仅仅在气孔导度、胞间CO2浓度和水分利用率等值的大小方面有显著差异(图 2)。

|
图 2 金佛山兰和金兰的净光合速率(Pn)、蒸腾速率(E)、气孔导度(Con)、胞间CO2浓度(Ci)、光能利用率(SUE)、水分利用率(WUE)的日变化 Fig. 2 Diurnal changes of the net photosynthetic rate (Pn), transpiration rate (E), stomatal conductance (Con), internal CO2 concentration (Ci), solar energy use efficiency (SUE) and water use efficiency (WUE) in the leaves of Tangtsinia nanchuanica and Cephalanthera falcata |
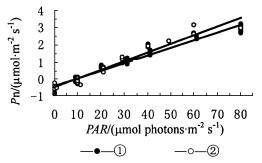
从图 3可知,金佛山兰和金兰的光补偿点均在10 μmol·m-2s-1左右,比木本植物银杏和鹅掌楸(25 μmol·m-2s-1左右)(郭志华等,1999b)低。同时,根据金佛山兰和金兰的光响应曲线可知,金佛山兰和金兰的光饱和点均在200 μmol·m-2s-1左右,两者相差不大(图 4)。这表明金佛山兰和金兰均具有较强的耐荫能力,属于比较典型的耐荫植物。
|
图 3 强光下金佛山兰和金兰叶片的表观量子效率 Fig. 3 Apparent quantum yield in Tangtsinia nanchuanica and Cephalanthera falcata under strong sunlight ①金佛山兰 Tangtsinia nanchuanica Pn=0.050 2 PAR-0.461 9(R2=0.952, n=39); ②金兰 Cepalanthera falcata Pn=0.044 4 PAR-0.436 7(R2=0.972, n=41) |

|
图 4 金佛山兰和金兰光合作用的光响应 Fig. 4 Light response of photosynthesis in Tangtsinia nanchuanica and Cephalanthera falcata ①金佛山兰 Tangtsinia nanchuanica ;②金兰 Cepalanthera falcata. |
温室内PAR最高可达约800 μmol·m-2s-1。在此PAR条件下,金佛山兰和金兰的净光合速率并未显著下降,因此,可以认为金佛山兰和金兰可以忍受相当程度的强光照。在亚热带地区自然条件下的空旷地带,PAR最高可达2 000 μmol·m-2s-1以上,而林下的光照条件变化极大。在郁闭度高的阔叶林下PAR多在100 μmol·m-2s-1 以下,而林下光斑处PAR可达1 000 μmol·m-2s-1以上。从光补偿点和光饱和点来看,两者均是能忍受一定强光的耐荫植物。因此,维持金佛山兰和金兰的正常生长发育,需要经常的不小于其光饱和点的光照条件。这就是金佛山兰仅见于稀疏马尾松林下的根本原因。
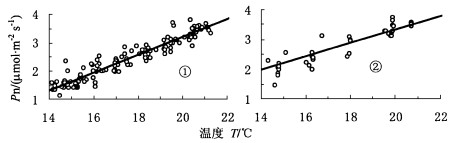
3.4 温度响应从图 5看出,在约14~22℃的气温范围内,金佛山兰和金兰的光合作用对温度的响应表现为,随气温的增加,净光合速率呈线形增加。假设净光合速率随气温的变化规律不变,则在约9~10℃时,金佛山兰和金兰的净光合速率为0。因此,二者的正常生长发育至少需要>10℃的条件。从多天的温室观测看,在日最高气温约30℃以下时,金佛山兰和金兰的净光合速率无显著下降。因此,二者花期阶段正常生长发育所需的气温大约在10~30℃之间,最适温度约在18~25℃左右。这仅是金佛山兰和金兰Pn短时间内的温度响应,并不一定真实代表它们在自然条件下的温度需求。因此,气温对金佛山兰和金兰在各个发育时期以及在野外条件下Pn的影响,还有待进一步研究,上述仅是初步的研究结果。
|
图 5 金佛山兰和金兰光合作用温度响应 Fig. 5 Temperature response of photosynthesis in Tangtsinia nanchuanica and Cephalanthera falcata ①金佛山兰 Tangtsinia nanchuanica Pn=0.314 1 T-3.076 1(R2=0.884 7, n=142); ②金兰 Cepalanthera falcata Pn=0.336 5 T-3.096 1(R2=0.892 8, n=61) |
另一方面,由于气温对植物净光合速率的影响很大,因此,在观测时应尽量减小由于叶室导致的叶室内温度的变化。方法是,每次观测时间不宜太长或利用仪器的温控系统附件。
3.5 光合速率的影响因子分析由于净光合速率的影响因子很多,再加上各因子的影响程度不同且各因子之间的相关程度很高,因此,可以用逐步回归分析的方法找出对净光合速率影响最大的因子(方开泰等,1988),并且该方法在其它珍稀濒危植物生理生态学的研究中取得了良好效果(郭志华等,1998;1999b)。
根据Pn, Con, Ci, Cam, E, Vpdl, Tleaf, PAR, Ta, RH, SUE, WUE, PAR2, Δt等因子的观测结果,每小时选取次数大致相当的观测数据用于Pn影响因子分析。这样,金佛山兰和金兰分别选取了185和204组观测数据进行逐步回归分析。由于统计分析仅考虑因子的数量变化,并不关心所得结果的生态学意义,因此,不断改变挑选和剔除因子的显著度水平,以获得显著度水平高、同时又符合现有生态学理论的统计结果。最后,分别得出金佛山兰和金兰净光合速率的回归模型:
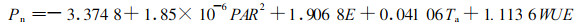
|
(1) |

|
(2) |
显著性检验:(1)式和(2)式的复相关系数分别为0.980 3和0.972 6,F检验值分别为1 145.2和1 210.8。检验结果表明,回归方程及方程中的每一项系数及常数项均达到极显著水平(p>0.01)。
从(1)式可知,金佛山兰净光合速率随光合有效辐射的平方、蒸腾速率、气温和水分利用率的增加而增加, 并且蒸腾速率对净光合速率的影响很大。从(2)式可知,在自然光照条件下,气孔导度、胞间CO2浓度和大气CO2浓度等因子对净光合速率的影响很大,并且,金兰的净光合速率随光照、气孔导度、大气CO2浓度、蒸腾速率、相对湿度的增加而增加,随胞间CO2浓度和光能利用率的增加而降低。从图 1也可看出,在1 d中,净光合速率大致与光能利用率和胞间CO2浓度呈负相关。此外,有许多影响净光合速率的重要因子未包含在(1)和(2)式中,如(1)式中未包含CO2浓度、气孔导度、叶温等,(2)式中未包含叶温等,但这并不表明这些因子对净光合速率的影响不大或没有影响,只能说明它们的影响相对较小或它们的影响已被方程中的因子所包含、反映。这种情况与银杏和鹅掌楸相似(郭志华等,1998;1999b)。
4 保护金佛山兰的建议作为一种珍稀濒危植物,金佛山兰的分布区有逐年减少的趋势。20世纪60年代,金佛山兰的分布区较大,可以分布在金佛山海拔700~2 100 m以上的山地(陈心启,1965),而近期已很难见其踪迹,最高分布界限也不超过1 200 m。金佛山国家级自然保护区的主要保护对象是银杉。金佛山兰的分布区并不位于自然保护区的核心区,而是位于缓冲地带。因此,目前的保护措施对金佛山兰的保护力度还很不够。由于历史原因,该地带有不少药农种植各类药材和粮食,药农的放牧、毁林开荒、种植和挖掘药材等对金佛山兰的影响很大。在此,极力呼吁加大对金佛山兰的保护力度和提高其保护等级。药农在该地区生活极为艰苦,他们的农业活动对本地区植被和环境的破坏很大,建议对这些药农移民。
除了在花特征上的差异外,金佛山兰与金兰的其他形态特征相似甚至完全相同而难以区分,并且金佛山兰均与金兰生长在一起。两者之间的相互作用机制还有待于进一步研究。无疑地,要实现对金佛山兰的有效保护,就必须同时加强对该地区金兰的保护。
陈心启. 1965. 一个原始的兰科新属进兰属(Tangtsinia)及其在系统发育上的意义. 植物分类学报, 10(3): 193-206. |
方开泰, 全辉, 陈庆云. 1988. 实用回归分析. 北京: 科学出版社, 204-232.
|
郭志华, 张宏达. 1997. 银杏(Ginkgo biloba)光合特性的研究. 生态科学, 16(1): 30-33. |
郭志华, 彭少麟, 王伯荪, 等. 1999a. 磷的有效性对菜豆生理生态特征的影响. 中山大学学报, 38(4): 82-85. |
郭志华, 王伯荪, 张宏达. 1998. 银杏的蒸腾特性及其对遮荫的响应. 植物学报, 60(6): 567-572. DOI:10.3321/j.issn:1672-9072.1998.06.014 |
郭志华, 张宏达, 李志安, 等. 1999b. 鹅掌楸(Liriodendron chinense)苗期光合特性的研究. 生态学报, 19(2): 164-169. |
Field C, Merino I, Mooney H A. 1983. Compromises between water-use efficiency and nitrogen-use efficiency in five species of California evergreens. Oecologia, 60: 384-389. DOI:10.1007/BF00376856 |
 2003, Vol. 39
2003, Vol. 39

