文章信息
- 翁尧富, 陈源, 郑康乐, 赵勇春, 黄少甫.
- Weng Yaofu, Chen Yuan, Zheng Kangle, Zhao Yongchun1, Huang Shaofu.
- 板栗优良品种(无性系)苗木分子标记鉴别研究
- DNA FINGERPRINTING OF CASTANEA MOLLISSIMA ELITE VARIETY (CLONE)SEEDLINGS
- 林业科学, 2001, 37(2): 51-55.
- Scientia Silvae Sinicae, 2001, 37(2): 51-55.
-
文章历史
- 收稿日期:2000-02-14
-
作者相关文章
2. 中国水稻研究所 杭州 310006;
3. 中国林业科学研究院亚热带林业研究所 富阳 311400
2. China National Rice Research Institute Hangzhou 310006;
3. Subtropical Forestry Institute, CAF Fuyang 311400
板栗是我国特产, 它是我国利用最早的经济树种之一。近年来, 我省板栗发展迅速, 板栗苗需求量很大, 由于板栗苗采用嫁接繁殖, 落叶后从外形上很难区分各品种(无性系)。一些不法分子乱用接穗或不嫁接, 甚至砍一刀形成愈伤组织假冒嫁接苗等手段迷惑买主。由于板栗生产周期较长, 待结果时发现品种不真实, 已给买方造成了巨大的经济损失。因此, 板栗品种(无性系)苗木的分子标记鉴别已成为生产上的迫切需要。随着分子生物学的发展, 分子标记技术为板栗品(无性系)的鉴别提供了一种有力的工具。由于在大部分林木种及种以下的不同层次上均存在着明显的遗传差异, 因此总能找到一些特殊的而又不受发育阶段或环境条件影响的遗传特征。RAPD标记可以直接从基因水平上研究板栗的遗传变异, 从而对品种或无性系加以确切的鉴别。本研究选用8个板栗品种(无性系), 利用RAPD技术构建其基因组指纹图谱, 并有效地鉴别板栗品种(无性系)。
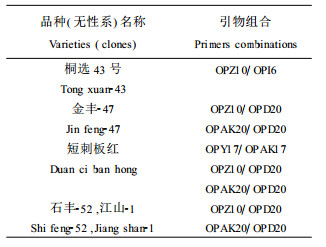
1 材料和方法 1.1 材料实验材料为浙江省诸暨市林业科学研究所采集的短刺板红和长刺板红, 浙江省桐庐县板栗研究所采集的石丰-52、金丰-47, 桐选43号、桐选32号、三门-4和江山-1。短刺板红和长刺板红为浙江省林木良种委员会审定的品种, 石丰-52和金丰-47为浙江省林木良种委员会认定的品种, 桐选43号和桐选32号为浙江省林木良种委员会认定的无性系, 三门-4和江山-1为通过省级鉴定的无性系。其特性见表 1。实验以板栗冬芽为材料。每个品种(无性系)选取3个样品, 所用的随机引物购自OPeron公司, Taq酶购自中国农业大学农业生物技术国家重点实验室, dNTP购自上海生物工程公司。
|
|
板栗DNA提取参考Murray等的方法, 取板栗冬芽(剥去苞片)于液氮中研磨成粉末, 用CTAB提取液提取, 然后用等体积的饱和酚、氯仿和异戊醇抽提两次, 无水乙醇沉淀DNA, 最后提取的DNA溶于TE缓冲液中。
1.2.2 RAPD分析本研究参考了标准的方法, 结合板栗的特点, 建立了板栗RAPD分析的技术体系。扩增反应在20 μL的体系中进行, 其中含有100 mmol L Tris-HCl, 500 mmol L KCl, 20 mmol L MgCl2, 0.01 % Gelatin, dNTP为100 μmol/L, 2 μLPrimer, 4.8 μLdi, 3 μL DNA, 0.2 μL Taq酶。扩增反应在Perkin-Elomer 9600型DNA扩增仪上进行。实验程序为:首先在94 ℃预变性2 min, 再按94 ℃ 30 sec、40 ℃ 30 sec、72 ℃ 1.5 min扩增38个循环, 最后在72 ℃延伸7 min。扩增产物在1.0 %琼脂糖凝胶中电泳, 经EB染色后在紫外灯下观察照相。每个品种(无性系)设3个重复, 个别情况因为泳道不够, 只有2个重复。
2 结果分析 2.1 RAPD扩增结果对684个RAPD随机引物的初筛和复筛, 共获得6个有稳定多态且带型清晰的引物, 共扩增出9个多态片段, 片段大小在500bp至1500bp之间变化, 平均每个引物产生1.5个多态片段。6个多态引物名称、碱基序列及其标记名称见表 2; 各品种(无系性)的特异性的RAPD扩增谱带见图 1~5。
|
|

|
图 1 板栗的RAPD指纹图谱(引物OPY17) Fig. 1 RAPD fingerprints of Castanea mollissima (Primer OPY17) |
|
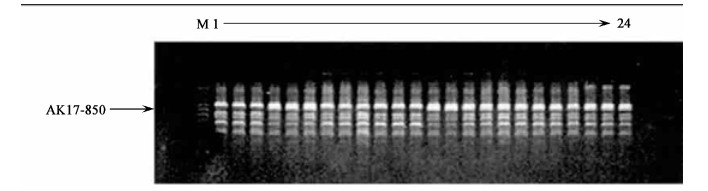
图 2 板栗的RAPD指纹图谱(引物OPAK17) Fig. 2 RAPD fingerprints of Castanea mollissima (Primer OPAK17) |

|
图 3 板栗的RAPD指纹图谱(引物OPZ10) Fig. 3 RAPD fingerprints of Castanea mollissima (Primer OPZ10) |

|
图 4 板栗的RAPD指纹图谱(引物OPAK20) Fig. 4 RAPD fingerprints of Castanea mollissima (Primer OPAK20) |

|
图 5 板栗的RAPD指纹图谱(引物OPD20) Fig. 5 RAPD fingerprints of Castanea mollissima (Primer OPD20) 图 1~5中第1~3条泳道为长刺板红; 第4~6条泳道为石丰-52;第7~9条泳道为三门-4;第10~12条泳道为酮选43号; 第13~15条泳道为江山-1;第16~18条泳道为金丰-47;第19~21条泳道为短刺板红; 第22~23(24)条泳道为酮选32号。图 1~5中M是分子量标记。 Fig 1~5, Lanes1~3:Chang ci ban hong; Lanes4~6:Shi fen-52;Lanes7~9:San men-4;Lanes10~12:Tong xuan-43;Lanes13~15:Jiang shan- 1;Lanes16~18:Jin fen-47;Lanes19~21:Duan ci banhong; Lanes22~23(24):Tong xuan-32.M :Molecular weight. |
长刺板红、三门-4和桐选32号有各自特异的分子标记。在引物OPI6的指纹图谱中, 长刺板红比其它品种(无性系)多1条约850 bp的带, 即特异标记为OPI6- 850。同样在引物OPI6的指纹图谱中, 三门-4比其它品种(无性系)多1条约690 bp的带, 即它的特异标记为OPI6-690。在引物OPZ10的指纹图谱中, 桐选32号比其它品种(无性系)少1条约1000 bp的带, 即它的特异标记为OPZ10-1000。特异分子标记鉴别品种见表 3。
|
|
三门-4、桐选43号和桐选32号在引物OPZ10的指纹图谱中比其它品种(无性系)多1条约630 bp的带, 而桐选32号在同种引物OPZ10中有特异标记OPZ10-1000, 可以区别于三门-4和桐选43号, 但三门-4可以利用它在OPI6指纹图谱中的特异分子标记OPI6-690区别于桐选43号, 所以引物组合OPZ10/OPI6可以鉴别桐选43号。长刺板红、三门-4、桐选43号和短刺板红在OPY17的指纹图谱中比其它品种(无性系)多1条约1150 bp的带, 而长刺板红、三门-4和桐选43号在OPAK17的指纹图谱中比其它品种(无性系)少1条约850 bp的带, 所以引物组合OPY17/OPAK17可以鉴别短刺板红。石丰-52、江山-1和金丰-47在OPZ10的指纹图谱中比其它品种(无性系)多1条约750 bp的带, 而在OPAK20的指纹图谱中比其它品种(无性系)少1条约1100 bp的带; 但石丰-52、江山-1和短刺板红在OPD20的指纹图谱中比其它品种(无性系)多1条约750 bp的带, 所以引物组合OPZ10/OPD20可以鉴别金丰-47、短刺板红及(石丰-52、江山-1), 另一组引物组合OPAK20/OPD20也可以鉴别金丰-47、短刺板红及(石丰-52、江山-1)。石丰-52与江山-1的主要谱带完全相同, 虽然经过600多个引物的筛选仍未能分开, 可能这两个品种是同物异名。
引物组合鉴别品种见表 4。
|
|
用当地的大田苗(每个品种或无性系20株)进行初步验证, 结果显示, 短刺板红苗中有18株苗的图谱与标准图谱一致, 准确率为90 %; 长刺板红苗中17株苗的图谱与标准图谱一致, 准确率为85 %; 金丰- 47、桐选43号、桐选32号、三门-4、石丰-52和江山-1各有17株苗、16株苗、16株苗、18株苗和17株苗的图谱与标准图谱一致, 准确率分别为85 %、80 %、80 %、90 %、85 %。因此, 8个板栗品种(无性系)大田苗初步验证准确率在80 %~90 %之间, 表明研究结果可靠。
3 结果讨论本研究的结果表明, 在板栗品种(无性系)间存在着广泛的遗传多态性。利用RAPD标记可以把亲缘关系很近的浙江省8个板栗主栽品种(无性系)的基因型区分开来, 根据RAPD标记遗传差异达到了鉴别板栗品种(无性系)苗木的目的, 具有重要的实用价值。在现有的基础上, 如果再筛选并增加某些板栗的特异性谱带, 则会进一步提高板栗品种(无性系)鉴别的准确率。
本研究针对当前林木种苗工作的实际, 采用RAPD技术进行浙江省主要经济品种板栗的DNA分子标记鉴别研究, 为今后开展板栗新品种(无性系)及其它名特优经济林木、花卉等品种鉴别和新品种保护打下了良好的基础。
RAPD技术应用于品种(无性系)的鉴别及指纹图谱的构建, 不仅具有快速、方便、直观等特点, 而且成本低, 为板栗苗木的鉴别提供了一个有效、可靠的方法, 拓宽了种苗检验的内容, 为修订新的种苗检验标准提供了一条崭新的途径。
利用分子标记不但能对板栗进行苗期鉴别, 避免假苗坑农, 同时为选育新品种提供从DNA水平上进行分析的一种高新技术。
陈洪, 朱立煌, 徐吉臣, 等. 1995. RAPD标记构建水稻分子连锁图. 植物学报, 37: 677-684. |
郭旺珍, 张天真, 潘家驹, 等. 1996. 我国棉花主栽品种的RAPD指纹图谱研究. 农业生物技术学报, 4(2): 129-134. |
惠东威, 陈受宜. 1992. RAPD技术及其应用. 生物工程进展, 12(6): 1-5. |
王冰冰, 孙宝启. 1997. RAPD技术进展及其在小麦遗传育种中的应用(综述). 农业生物技术学报, 5(3): 227-232. |
闫文昭, 王大一, 李晋涛, 等. 1997. 22个甘薯品种(系)遗传背景的RAPD图谱分析. 农业生物技术学报, 5(1): 40-46. |
尹佟明, 朱立煌, 黄敏仁, 等. 1997. 利用RAPD标记和单株树大配子体构建马尾松的分子标记连锁图谱. 植物学报, 39(7): 1-6. |
尹佟明, 韩正敏, 黄敏仁, 等. 1999. 林木RAPD分析及实验条件的优化. 南京林业大学学报. |
张超良, 孙世孟, 等. 1998. RAPD技术在12个玉米骨干自交系快速鉴定中的应用. 作物学报, 24(6): 718-722. DOI:10.3321/j.issn:0496-3490.1998.06.012 |
Torres A M. 1993. Identifying rose cultivars using random amplified polymorphic DNA markers. Hort.Science, 28(4): 333-334. DOI:10.21273/HORTSCI.28.4.333 |
Lodhi M A, Ye G N, Weeden N F, Reisch B I. 1994. A Simple and Efficient Method for DNA Extraction from Grapevine Cultivars and vitisSpecies. Plant Mol.Biol.Rep., 12(1): 6-13. DOI:10.1007/BF02668658 |
Murray M G, Thompson W F. 1980. Rapid isolation of high molecular weight plant DNA. Nuc.Acids Res, 8: 4321-4325. DOI:10.1093/nar/8.19.4321 |
Rhonda J. 1992. Honeycutt, Bruno W.S.Sobral, Paul Keim, and James E Irvine.A Rapid DNA Extraction Method for Sugarcane and its Relatives. Plant Mol.Biol.Rep., 10(1): 66-72. DOI:10.1007/BF02669266 |
Sue Porebski, Grant Bailey L, Bernard R Baum. 1997. Modification of a CTAB DNA Extraction Protocol for Plants Containing High Polysaccharide and Polyphenol Components. Plant Mol.Biol.Rep., 15(1): 8-15. DOI:10.1007/BF02772108 |
Weeden N F, Lamb R C. 1985. Identification of apple cultivars by isozyme phenotypes. J.Amer.Soc.Hort.Sci., 110: 509-515. |
 2001, Vol. 37
2001, Vol. 37