文章信息
- 易能君, 韩正敏, 尹佟明, 黄敏仁, 曹汉洋.
- Yi Nengjun, Hang Zhengmin, Yin Tongming, Huang Minren, Cao Hanyang.
- 湿地松抗病种子园的遗传多样性分析
- GENETIC VARIATION OF RAPD MARKERS IN A DISEASE RESISTANT SEED ORCHARD OF PINUS ELLIOTTII ENGELM
- 林业科学, 2000, 36(专刊1): 51-55.
- Scientia Silvae Sinicae, 2000, 36(专刊1): 51-55.
-
文章历史
- 收稿日期:1998-05-04
-
作者相关文章
2. 福建沙县官庄林场 沙县 366500
2. Fujian Guanzuang Forest Farm Sha county 366500
湿地松(Pinus elliottii Engelm)原产于美国西南部,是重要的工业用材树种。中国自1973年起从美国的佛罗里达、佐治亚、南卡罗来纳、密西西比、阿拉巴等州大量引种,在南方各省大面积造林。该树种对松针褐斑病(Mycosphaerella dearnessii Barr)严重感病,特别在闽西北地区,造成大面积死亡。为有效地控制松针褐斑病,南京林业大学树木病理研究室进行了湿地松的抗病育种研究,以抗病性状和生长性状为选择依据,从大约146 hm2严重发病的湿地松幼林中选择了47株抗病单株,并在此基础上建立了湿地松抗病种子园(叶建仁等,1986)。种子园是林木遗传改良的重要环节,应具有广阔的遗传基础和显著的遗传增益。在多世代改良研究中,保持遗传多样性是改良的关键之一。70年代以来,国内外广泛利用同工酶电泳技术研究森林树种的群体遗传变异。葛颂(1988)曾总结了25种针叶树种和6种阔叶树种的天然群体同工酶位点的研究结果,其基因多样度H平均为0.206,相对而言,林木群体遗传变异程度比其它物种要高。Hamrick和Godt (1989)综述了55种裸子植物遗传结构,研究也表明类似结果。近些年来,研究者已开始使用遗传标记研究林木群体遗传结构,并证实标记是揭示群体遗传变异的有利工具。Yeh等(1995)利用RAPD研究了欧州山杨(Trembling aspen) 8个天然群体的结果说明,群体的变异较大,Shannon信息指数I平均为0.65。苏晓华等(1997)对7个大青杨(Populus ussuriensis kom.)天然群体进行了研究,RAPD标记的Shannon指数平均为0.310。
连锁不平衡分析是现代群体遗传学的核心研究内容之一(Brown,1984),它更能深刻地揭示林木的遗传变异和分化,对遗传资源保存及改良策略的制定具有重要意义(Yang,1992)。
本文以有效等位基因数目,基因多样度和Shannon信息指数等遗传参数度量湿地松抗病种子园的遗传多样性,为制定遗传改良策略提供理论依据。
1 材料和方法 1.1 研究材料材料采自福建沙县官庄林场,选择感病指数小于1.0的植株22棵,从树上采取尚未木质化的嫩梢用于DNA提取。
1.2 DNA提取与随机扩增DNA提取程序根据Murray等(1990)的方法稍加改进。将3~5cm嫩梢一段放入研钵中,加入2 mL CTAB DNA提取液[10 mmol/L Tris (pH 8.0),20 mmol/L EDTA (pH 8.0),1.4 mol/L NaCl,1% CTAB,5%PVP,350 mmol/L β-mercaptoethanol]和少量石英砂,在研钵中研磨,匀浆转入10 mL离心管中,充分摇匀;8000×g离心10 min,将上清液转入新的10 mL离心管中,再加入2 mL酚:氯仿(1:1),充分摇匀;8000×g离心10 min,将上清液转入新的10 mL离心管中,再加入2 mL氯仿;摇匀;8000×g离心10 min,将水相转移至新的10 mL离心管中,加入5 mL无水乙醇沉淀DNA、-4℃下冰冻30 min,8000×g离心10 min,去上清然后用无水乙醇洗沉淀1次,将离心管倒置在吸水纸上,于空气中干燥沉淀;加入100 μL TE溶解。
DNA扩增在美国Idaho技术公司生产的气热式PCR仪上进行,反应管为玻璃毛细管,反应体系(15 μL)组成如下:5 ng左右模板DNA,5 pmol引物,dATP、dTTP、dCTP、dGTP的量各为200 μmol/L,1.5 μL 10×的反应缓冲液[100 μmol/L Tris-HCl (pH 8.3),500 mmol/L KCl,20 mmol/L MgCl2,0.01%明胶,5.0 g/L BSA,10 mmol/L酒石黄],1 U Taq-G聚合酶(中国农业大学农业生物技术重点实验室产品)。扩增条件为:94℃变性20 s,39℃退火10 s,72℃延伸1 min,反应2个循环后,接着进行94℃变性1 s,40℃退火10 s,72℃延伸1 min,反应8个循环,然后94℃变性1 s,37℃退火10 s,72℃延伸1 min,反应35个循环,最后72℃链延伸10 min,扩增产物用1.5%琼脂糖凝胶检测分析。
2 数据分析RAPD扩增带(见图 1)用1代表有,用0代表无。RAPD数据的遗传分析通常建立在下列条件之下:RAPD标记位点呈孟德尔式分离,每位点有两个等位基因M、m,到为显隐性,因此,数据'1'代表基因型MM或Mm,数据`0'代表基因型mm;任何RAPD位点达到Hardy—Weinberg平衡,因此,若'0'的频率为P0,m的频率为q,则q2=P0 (Apostol,1996)。由于本次研究的样本容量偏小,为了减小偏差,各位点等位基因M,m的频率根据Lynch和Milligan (1994)的公式计算。

|
图 1 引物J14的RAPD片段在样品中的分离 Fig. 1 Segregating of RAPD bands amplified with primer J14 in Slash pine under analyzing M. 分子量标记(PGM-3DNA被HinfI, RsaI及SinI酶切的产物) 0. 对照 1~22. 湿地松样品 M. Molecular weight marker (Product of PGM-3DNA digested by HinfI, RsaI and SinI); 0. Blank contrast; 1~22. Slash pine under analyzing |
以各基因位点的等位基因频率为基本数据,计算有效等位基因数目Ne (Effective number of alleles per locus)、基因多样度H (Gene diversity)和Shannon信息指数I (Shannons information index)。

|
其中:L为RAPD位点个数;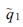
两位点间的连锁不平衡系数的估计和假设检验采用Hill (1974)关于显性位点间的方法。
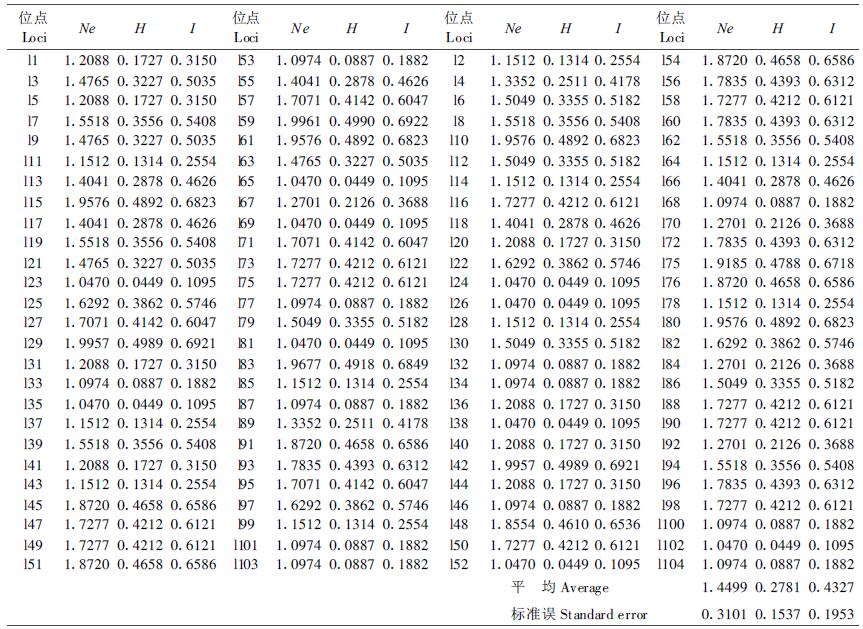
3 试验结果所有位点的平均有效等位基因数目、基因多样度和Shannon信息指数的结果列于表 1。
|
|
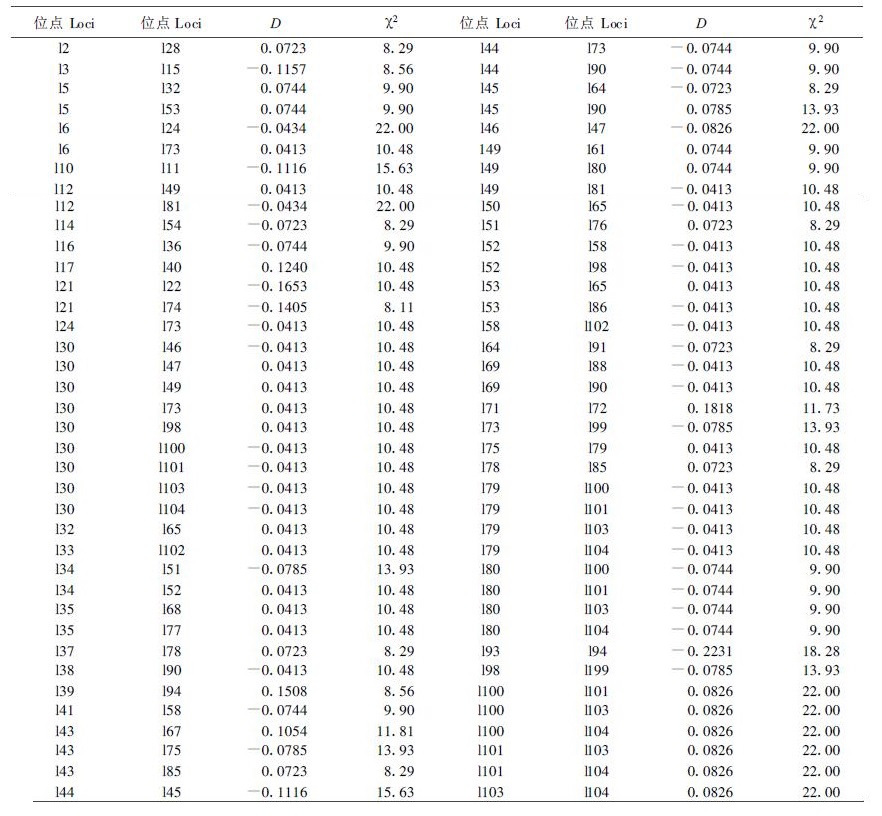
结果表明,104个分离位点均为多态性位点(Polymorphic loci),各位点的等位基因频率有较大差异。等位基因频率是描述群体遗传结构的基本参数,它们是计算其参数的前提。有效等位基因数目Ne和基因多样度H有明显的遗传学意义,是衡量遗传变异的最常用的两个遗传指标(Hamyick et al.,1989),Shannon信息指数没有遗传学意义,但为了与同类研究进行比较,本研究也进行了计算。研究结果显示:各位点上遗传多样性程度存在较大差别,Ne的最大值为1.9961,最小值为1.047,H的最大值为0.499,最小值为0.0449,I的最大值为0.6922,最小值为0.1095。对于相应位点,I值均大于H值,但这3个遗传指标在各位点的大小顺序基本一致。所有位点的平均有效等位基因数目为1.4499,平均基因多样度为0.2781,平均信息指数为0.4327。表 1中也列出了平均有效等位基因数目、平均基因多样度和平均Shannon信息指数估计的均方,它们均达较小,分别为0.3101、0.1537、0.1953,说明相应的估计值精度较高。这3个遗传多样性度量均表明该种子园具较高的遗传多样性。104个位点共有C1042=5356对连锁不平衡系数,根据Hill的方法估计各连锁不平衡系数,并由自由度为1的χ2分布作假设检验。表 2中列出了达到显著性水平为α=0.005的位点对的连锁不平衡系数的估计值D、检验统计量值χ2。可见共有76对位点处于连锁不平衡状态,超出了由于统计检验的随机性将可能产生的连锁不平衡系数达到显著的位点对数26。我们也进行了显著性水平为α=0.05的假设检验,共有355对位点处于连锁不平衡状态,超出了由于统计检验的随机性将可能产生的连锁不平衡系数达到显著的位点对数267 (结果未列出)。表明湿地松抗病种子园RAPD位点对大部分处于平衡状态,但依然有一部分位点对存在显著程度的连锁不平衡。
|
|
本文所研究的湿地松种子园具有较高的遗传多样性,其104个分离的RAPD位点的基因多样度H平均达到0.2781,Shannon信息指数I平均达0.4327。这两个度量值均超过或与林木天然群体同类研究的相应值相当,由于本研究仅取分离的RAPD位点进行分析,因此过高地估计了该种子园的遗传多样性,但总的来说,该种子园具有较为广泛的遗传基础。这与赖焕林关于马尾松种子园的研究结果相似1)。由于种子园大都从各天然林经过选择的个体而建立的,如果这些天然林在地理上和遗传上有分化,那么从中选择便有可能维持较高水平的遗传多样性。
1) 赖焕林. 马尾松群体交配系统研究. 1995, 南京林业大学博士学位论文.
该湿地松种子园的连锁不平衡程度也与林木天然群体相似,由于该种子园材料来自于湿地松很多种源,因此其连锁不平衡可能主要由群体融合导致,并且可粗略推测各天然群体在基因频率上存在一定差异(Feldman,1975)。易能君(1997)研究了16个杉木群体22合同工酶位点的连锁不平衡,发现各群体的连锁不平衡程度不一样,达到显著性水平的位点对数最大为22,最小为11。另外,针对某些性状的高强度选择会使基因组局部区域受到选择的影响而使该局部区域的基因频率发生较大变化,从而使种子园处于连锁不平衡状态。连锁不平衡是性状之间遗传相关的重要原因,保持群体处于连锁不平衡是进行遗传标记辅助选择(MAS)的唯一途径。因此,该种子园连锁不平衡的存在为将来进行MAS研究提供了基础。
葛颂. 1988. 同工酶与林木群体遗传变异研究. 南京林业大学学报, 1: 68-77. |
苏晓华, 等. 1997. 利用RAPD分析大青杨天然群体的遗传结构. 林业科学, 33(6): 504-511. DOI:10.3321/j.issn:1001-7488.1997.06.004 |
叶建仁, 韩正敏, 李传道, 等. 1986. 湿地松、火炬松种源抗褐斑病试验和抗病优树选择. 南京林业大学学报, (2): 27-36. |
易能君, 施季森, 王明庥. 1996. 林木群体遗传多样性和多位点遗传结构. 生物多样性, 4: 153-159. DOI:10.3321/j.issn:1005-0094.1996.03.006 |
Apostol B L, Blackiv W C, Reiter P, et al. 1996. Population genetics with RAPD-PCR markers: the breeding structure of Aedes aegypti in Puerto Rice. Heredity, 76: 325-334. DOI:10.1038/hdy.1996.50 |
Brown A H D. 1984. Multilocus organization of plant populations. Population Biology and Evolution: 159-169. |
Feldman M V , Christiansen F B. 1975. The effect of population subdivision on two loci without selection. Genet. Res. Camb., 24: 151-162. |
Hill W G. 1974. Estimation of linkage disequilibrium in randomlymating populations. Heredity, 33: 229-239. DOI:10.1038/hdy.1974.89 |
Hamrick J L, Godt M J W. Allozyme diversity in plant species. In: Plant Population Genetics, Breeding and Genetic Resource. Sinauer, Sunderland, 1989, 43~63
|
Kimura M , Crow J F. 1964. The number of alleles that can be maintained in a finite population. Genetics, 49: 725-738. |
Lynch M , Milligan B G. 1994. Analysis of population genetic structure with RAPD markers. Mol. Ecol., 3: 91-99. DOI:10.1111/j.1365-294X.1994.tb00109.x |
Murray H G , Thomson W F. 1990. Rapid isolation for high molecular weight DNA. Nucleic Acids Research, 8: 4321-4325. |
Nei M. 1973. Analysis of gene diversity in subdivded populations. Proc. Nat. Acad. Sci. USA, 70: 3321-3323. DOI:10.1073/pnas.70.12.3321 |
Weir B S. Genetic Data Analysis Ⅱ, 1996, Sinauer, Sunderland
|
Yang R C , Yeh F C. 1992. Genetic consequences of in situ and ex situ conservation of forest trees. The Forestry Chronicle, 68: 720-729. DOI:10.5558/tfc68720-6 |
Yeh F C, Chong D K X, Yang R C. 1995. RAPD variation within and amog natural populations of Trembling aspen (Populus tremuloides Michx.) from Alberta. The Journal of Heredity, 86(6): 454-459. DOI:10.1093/oxfordjournals.jhered.a111620 |
 2000, Vol. 36
2000, Vol. 36