文章信息
- 贺伟, 任飞娟, 郭利民, 李永, 常聚普.
- He Wei, Ren Feijuan, Guo Limin, Li Yong, Chang Jupu
- 欧美杨溃疡病的病原鉴定
- Pathogen identification of Populus × euramericana Canker Disease
- 林业科学, 2009, 45(6): 104-108.
- Scientia Silvae Sinicae, 2009, 45(6): 104-108.
-
文章历史
- 收稿日期:2009-04-02
-
作者相关文章
2. 中国林业科学研究院森林生态环境与保护研究所 北京 100091;
3. 河南省濮阳市林业科学研究所 濮阳 457000
2. Research Institute of Forest Ecology, Environment and Protection, CAF Beijing 100091;
3. Forestry Research Institute of Puyang, Henan Province Puyang 457000
近几年,优良品种欧美杨107杨(Populus × euramericana cv.‘74/76’)等在河南、山东等省得到迅速推广,仅河南省欧美杨树种植面积达近133万hm2。但是,在大面积发展速生杨造林的同时,病虫害问题成为制约生产发展的因素之一。2005年5月在河南濮阳首次观察到在6年生107杨树上出现树皮开裂、从树皮裂缝中流出大量汁液、树干韧皮部局部坏死、坏死处组织肿胀的症状。2006年在河南濮阳、山东兖州多块林地观察到此病害的发生。2007年在上述2地的107杨和中林46杨(P.×euramericana ‘zhonglin 46’)上普遍发生,发病率一般为30%~50%,病害严重的林分病株率达70%以上。2008年病害发生的面积和严重程度又有所增加。感病树木病部枝条和树干顶梢枯死,树木材积和其他可利用部分减少;大量伤流的产生,损耗树木养分,严重影响树木的健康生长。
在欧美杨上,此症状国内未见报道。类似的症状在美国见于北美鹅掌楸(Liriodendron tulipifera)(Dochinger et al., 1962),另外,在糖槭(Acer saccharum),枫香树属(Liquidambar)也有发生(Skelly,1964)。Boyce(1961)报道了在加拿大魁北克省发生在美洲黑杨(Populus deltoids)上由茄镰孢菌(Fusarium solani)引起的溃疡病。同年,在美国密西西比河沿岸的美洲黑杨上也出现由茄镰孢引起的溃疡病(Toole,1963)。1965年春,在美国衣阿华州7年生的威斯康星5号杨(美洲黑杨的一个无性系)和杂交杨上发生了由茄镰孢引起的杨树溃疡病,进一步的调查表明,2个有白杨派树种亲缘的无性系也受到感染。它们是5年生的大齿杨(Populus grandidentata)和银白杨(P. alba)的天然杂交种。发病树木树干上出现线形的裂缝,干形受到明显损害。1年生的溃疡斑可扩展到0.3 m,病害严重时溃疡病环割树干(Dochinger et al., 1967)。
从症状看,该病与以前普遍发生在毛白杨等杨树上由冻害造成的破腹病不同,而与北美报道的阔叶树溃疡病的特征相似。生产上迫切需要明确病原,本文在对病害标本分离、纯化、接种、致病性测定,明确病原的基础上,根据病原菌形态特征和病菌的核糖体DNA (rDNA)内转录间隔(internal transcribed spacer,ITS)的序列特征,鉴定速生杨伤流溃疡病的病原。以明确病原菌的种类,为进一步研究病害的发生规律、制定防治措施提供参考依据。
1 材料与方法 1.1 供试材料 1.1.1 接种杨树品种2年生107杨,由中国林科院中林公司提供。
1.1.2 培养基包括以下2种(灭菌条件:121℃,20 min):1) PDA培养基;2)稻秆培养基:将3 g稻秆洗干净后剪成0.5 cm长的小段,加入有10 g琼脂粉的1 L水中,加热搅拌至琼脂溶化后灭菌。
1.1.3 引物真菌核糖体基因转录间隔区ITS1(5′-TCCGTAGGTGAACCTGCGG-3′) /ITS4:(5′-TCCTCCGCTTATTGATATGC-3′)由上海英骏生物技术有限公司合成。
1.2 试验方法 1.2.1 病样的采集与微生物分离纯化于2007年9月28日、2008年5月5日、7月23日和10月2日先后4次在河南省清丰县、濮阳县、南乐县和山东菏泽等地发病严重的林地,观察和记录病害的症状特点,调查林地的病株率,采集具有典型症状的病组织,用常规组织分离方法,在实验室用PDA培养基进行分离,25 ℃下培养,纯化后对分离物进行归类、编号和转管保存。
1.2.2 致病性测定采用无伤接种和苗干伤皮接种2种方式对盆栽2年生苗木和玻璃缸水培2年生主干干条进行接种。1)接种体:将PDA上培养7~10天的分离物,真菌制取菌饼(Φ 6 mm),细菌则用无菌水稀释成107·mL-1的菌悬液,备用。2)树苗的培育:将来自中国林业科学研究院房山育苗基地的2年生107杨苗木分别栽植于盛有灭菌的土壤花盆中和北京林业大学森保研究室院内土壤中。水培接种时,从生长旺盛的健康苗木上截取直径约2.5~3 cm,长30 cm的2年生苗干,放入经消毒的玻璃缸内,缸底部盛2 cm深的无菌水,使苗干下端截面被水淹没,每隔2天换1次水,苗干上端包裹透明胶带,防止水分散失,室内自然光下培养。3)接种(1)伤皮接种:真菌接种:用湿棉球清洁苗干表皮,再用蘸有75%酒精的棉球擦洗苗干,待酒精挥发后,用孔径6 mm的打孔器在苗干上切去树皮块,将备好的同样直径的真菌分离物菌饼,菌丝体与苗干木质部相贴接入伤口处,对照接入无菌的培养基饼。细菌接种:在苗干接种点用消毒的大头针刺伤皮层,用滴管吸取0.1 mL细菌悬液,滴加到刺伤处,对照在刺伤处滴无菌水。接种后用透明胶带包裹接种点,防止水分散失,6天后去掉透明胶带。(2)无伤真菌接种:接种处表面清洁消毒后,用分离物真菌孢子悬浮液(15×40倍镜下,30个分生孢子/视野)浸湿棉球,对照用无菌水浸湿棉球,包裹在苗干表面,外面包裹塑料薄膜,上下两端用线绳扎紧。每根苗干和每株盆栽苗各接种3个点,每个处理5根苗干或5株苗木,2次重复,每处理共接种10株。接种后的杨树苗木和苗干在室内培养(温度23~25 ℃)。4)发病植株的再分离:接种后3天开始观察记录发病情况。取接种发病组织分离,并以分离物的培养性状和孢子形态等特征与最初的接种分离物进行比较。
1.2.3 调查统计方法接种发病率(%) =接种发病点数/接种点数×100%。
1.2.4 病原菌的生长及形态学观察均在25℃下培养。1)生长速率:将病原菌接种于PDA平板上,黑暗条件下培养5天后用十字交叉法测量菌落生长直径,计算生长速率。2)孢子形态:将病原菌接于稻秆培养基上,14天后在显微镜下观察其分生孢子形态,并照相记录。3)孢子着生方式:在灭菌培养皿中放置无菌载玻片,加1%水琼脂,将病原菌接于其上,盖上盖玻片,保温培养3天后,观察并照相记录。4)分生孢子的测量:取用Mz01菌株接种发病组织上产生的分生孢子和稻秆培养基上产生的厚垣孢子,用蒸馏水作浮载剂,在Nikon光学显微镜下(15×40)用测微尺测量,每种类型的分生孢子均测量30个。
1.2.5 病原菌的分子鉴定用真菌的通用引物对ITS1/ITS4对病原菌进行PCR扩增(White,1990),对获得的扩增产物进行测序,将得到的序列在GenBank中进行比对,通过同源性分析对病原菌进行鉴定。1)病原菌总DNA的提取:试验菌株为Mz01和培养性状与之相似,同样来自107杨病株的Mz02。菌丝培养用PDA培养基,25 ℃培养7天,DNA提取采用CTAB提取方法。2) rDNA ITS的扩增与序列测定:采用真菌核糖体基因转录间隔区(ITS)通用引ITS1/ITS4,扩增该病原菌的ITS和5.8S rDNA。PCR反应采用50 μL反应体系,包括模板DNA溶液2 μL (约10 ng)、10 ×PCR buffer 5.0 μL、2.5 mmol·L-1 dNTP 4.0 μL、7.5 pmol·μL-1的ITS1和ITS4引物各1.5 μL、5U·μL-1 Taq酶(含MgCl2) 0.5 μL、加ddH2O至50 μL。扩增反应程序为:94 ℃预变性5 min;94 ℃变性1 min、55 ℃退火1 min、72 ℃延伸1.5 min,35个循环,72 ℃延伸8 min。PCR产物经琼脂糖凝胶电泳检测后,直接委托上海英骏生物技术有限公司进行纯化和序列测定。3)病原菌rDNA ITS序列同源性比较:将菌株Mz01和Mz02的rDNA ITS序列在NCBI网站上(http://blast.ncbi.nlm.nih.gov/Blast.cgi)用BLAST软件与GenBank中已知种属的rDNA序列进行比对和同源性分析
2 结果与分析 2.1 病害症状与危害程度在107杨和中林46杨上,病害主要出现树木的主干上。树干上从基部向上0.5~10 m的范围内均可出现溃疡斑,而以4~6 m处较多。1株树上可产生1到多个病斑,最多的有8处病斑。4月下旬至5月中旬,在枝干上形成小型病斑,树皮呈湿润状,随着气温的升高,病斑逐渐扩展,病部皮层开裂,裂口边缘的皮层组织腐烂,皮层下的木质部表层产生白色乳状粘液,发出酸臭味,自发病部位流出大量黑褐色液体,发病部位流出的液体可自6~8 m的树干上流至干基部(图版Ⅰ-A)。8月份液流最多。发病后期,病部皮层干枯,树皮翘起,撕裂状,与木质部剥离,病部木质部浅层(1~2mm)变褐,少数严重的木质部变色深度达2cm。在病部树皮上出现肉桂色垫状物,为病菌的分生孢子座和分生孢子(图版Ⅰ-B)。溃疡斑长20~30cm,宽3~5cm。少数病株在出现溃疡斑的地方风折,风折处木质部变色深达2~3mm。在侧枝和1年生主干,常局部出现疙瘩状肿胀,剖开肿胀处,皮层变色处呈不规则线纹,其下木质部表层少许变色。病害在10月上旬停止发展。病害引起树体生长衰弱,在病斑周围常出现杨树腐烂病和杨树水疱型溃疡病的病斑。少数发病严重的植株枯死。已发病株第2年不再复发,但也有少数病株,第2年5月份在先年病斑的边缘向外扩展,流出树液。从病害症状看,此病害为典型的1年生溃疡病。

|
图版Ⅰ Plate Ⅰ |
该病2005年5月在河南省濮阳县海通乡刘吕丘村4年生的中林46杨树林地首次发现;2006年该病在濮阳县、清丰县相继出现,在林地零星发生,个别地块病株率为17%;2007年部分林地已造成严重危害,清丰县阳邵乡南阳建村,5年生中林46杨林地,病株率达50%。2008年在清丰县柳格乡面积约4 hm2,分别栽植中林46杨和欧美107杨的杨树林中,各随机抽取100株调查,中林46杨,病株率达75%,而与之相邻的6年生欧美107杨,病株率为60%。
2.2 病样的采集及分离结果分别于2007—2008年共4次从濮阳市清丰县、濮阳县、山东菏泽等地,采集到杨树伤流溃疡病典型症状的树皮皮层、木质部变色、肿胀组织共96份样品,经分离、纯化、共获得108个菌株,根据菌落形态、色素产生情况和分生孢子的基本形态的相似性进行合并分类编号,鉴定出2株菌落颜色不同的细菌,2株有明显差异的镰孢菌和多种真菌。其中细菌21株、真菌87株。Mz01为优势菌株,其次是Cz02,Cz03和Cz05,分别为53.1%,17.7%,13.5%,8.3%,其他真菌分离频率较低(表 1)。
|
|
于2008年8月26日,选择分离频率较高的4个分离物进行离体苗干水培接种。伤皮接种中,Cz03和Cz05的2株细菌不致病,Cz02的真菌亦无致病力,Mz01的菌株则具强烈致病性,接种30点全部发病。接种后第4天,从接种点流出少量褐色的汁液(图版Ⅰ-C),第5天流汁量最大,第6天流汁量很少,第7天停止流汁,在苗干上留下褐色液渍,此时病斑开始扩展。在坏死的皮层上出现菌丝,病斑纵向扩展较横向扩展明显。接种后13天,横向扩展3.5~5 mm,纵向扩展5.5~13 mm,其上产生白色菌丝体和乳白色粘团,镜检为病菌的分生孢子堆;对照伤皮处无树液流出,伤口4周变褐约1.5~3 mm,其上未产生菌丝和孢子(图版Ⅰ-D)。接种点以外其余皮层组织为绿色,表明苗干组织仍保持生活力。接种23天后,接种Mz01的整个枝段皮层全部变黑,接种点周围的坏死皮层和皮孔组织上,长出大量白色菌丝体和乳白色粘团。无伤接种的各处理均未发病。2008年9月19日,选用在离体苗干上致病的Mz01菌株和分离频率仅次于Mz01的Cz02菌株,在花盆栽植的107杨健株上进行接种试验,结果Cz02不致病,Mz01致病,接种点发病率90%;但病斑扩展的范围较离体苗干水培接种小,从伤皮处向外扩展仅3 mm,坏死组织湿润、略肿胀,流出少量褐色汁液,20天后接种处未长出愈伤组织;对照伤皮组织边缘坏死组织仅1 mm,无树液流出,经过20天长出愈伤组织。从发病株病斑病健交接处分离,得到与接种菌完全相同的培养物,据此认为Mz01为欧美杨溃疡病的病原菌,病菌可通过伤口侵入。
2.4 病原菌的形态学鉴定 2.4.1 菌株Mz01的菌落和菌体形态在PDA上,气生菌丝较旺盛,开始为白色,逐渐中央变为雏菊黄(图版Ⅰ-E),培养皿背面为浅黄色(图版Ⅰ-F)。菌丝生长速度快,黑暗培养5 d菌落直径达57~59 mm。在PDA上易形成小型分生孢子。小型分生孢子无色,椭圆形、卵圆形至肾形(4. 5~10.3) μm×(2.0~4.3) μm,平均6.9 μm×3.2 μm(图版Ⅰ-G);团状聚生在分生孢子梗上(图版Ⅰ-H),或单生。分生孢子梗瓶状,顶部略细,生于菌丝侧面,单生,分枝或不分枝,长35~120 μm,基宽2.3~5.3 μm,中宽1.3~4.3μm;顶宽1.3~2.5μm,以单出瓶梗方式产孢。
大型分生孢子圆柱状,直或向一端弯曲,2~7隔,多5隔,顶细胞钝圆,基细胞圆形或呈脚状(图版Ⅰ-I)。3个隔膜的分生孢子,(19.0~38.0) μm×(2.8~5.0)μm,5个隔膜的分生孢子,(29.0~47.8) μm×(4.3~5.3) μm。在PDA培养基上,产生的孢子绝大多数为无隔单胞的小型分生孢子,偶尔可见3隔的大型分生孢子;而在稻秆培养基上,可产生与接种发病病组织以及田间自然发病组织上相同的大型分生孢子和厚垣孢子。厚垣孢子顶生或间生,单生或成对着生,球形,无色,光滑,直径9.6~12.9 μm。
2.4.2 形态学鉴定结果根据Mz01的以上形态学特征,以Nelson等(1983)对镰孢菌种的描述和Booth(1971)镰孢菌分种检索表为依据进行鉴定,Mz01为茄镰孢(Fusarium solani)。
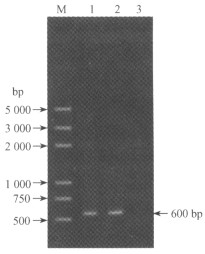
2.5 病原菌菌株Mz01的分子鉴定 2.5.1 PCR扩增结果采用真菌通用引物ITS1 / ITS4进行PCR扩增,Mz01和Mz02菌株都能扩增得到单一片段,大小约600 bp,而用水做为阴性对照的CK未能扩增到该片段(图 1)。
|
图 1 ITS区PCR扩增产物 Figure 1 PCR-amplified product of ITS region M.DNA marker; 1.PCR product of Mz01 strain; 2.PCR product of Mz02 strain; 3.CK |
ITS的序列分析及同源性比较本研究选取2个菌落形态相似的菌株进行rDNA ITS的序列测定和分析。菌株Mz01和Mz02的PCR扩增产物经琼脂糖凝胶电泳检测,获得大小约600 bp的特异性片段,PCR产物序列测定获得572个碱基的核苷酸序列。菌株Mz01和Mz02的rDNA ITS序列同源性为99.8%(GenBank的登录号:Mz01为FJ886799;Mz02为FJ874633),572个碱基中2者仅存在1个碱基的差异;与GenBank中已有的DNA序列同源性比较结果显示,与其序列同源性最高的有5个ITS序列,其中有2个菌株为Fusarium solani(GenBank登录号分别为:FJ459973.1,EF062312.1),同源性高达99.12%,570个碱基中存在5个碱基的差异,另外3个序列同源性均达100%,分别为Ascomycete sp.(GenBank登录号:AY770412.1,546个碱基完全相同)、Uncultured Ascomycota clone(GenBank登录号:EU862818.1,563个碱基完全相同)和Chloridium sp.(GenBank登录号:EU394444.1,54个碱基完全相同)。这2株菌株与GenBank中其他菌种序列的同源性均小于98%。
GenBank中与待测菌株序列同源性达100%的3株菌,前2者都是子囊菌,说明待测菌株属于子囊菌,但范围大,无法确定其种类;据魏景超(1984),暗梗单孢霉属(Chloridium)分生孢子单生,不聚成头状,分生孢子梗暗色。这与待测菌株的形态明显不同,因此待测菌株非暗梗单孢霉属真菌。综合形态学特点和分子鉴定的结果,菌株Mz01和Mz02均为茄镰孢菌(Fusarium solani)。
3 结论与讨论本研究证明分离自杨树的菌株Mz01具有致病性,其形态与茄镰孢菌相似,而rDNA-ITS的序列和GenBank中F.solani对应的序列同源性最高,达99.12%;表明引起欧美杨溃疡病的病原菌是茄镰孢菌。从病斑处还可分离到其他镰孢菌菌株,如Cz02,以及2种细菌,试验证明它们不具致病性。这阐明了欧美杨溃疡病的病原,为开展病害侵染和发生发展规律、流行学研究和综合防治的研究奠定基础。
由茄镰孢引起的树木溃疡病在国外早有报道,除了在杨树上,在美国宾夕法尼亚州的红花槭(Acer rubrum)、美国黑樱桃(Prunus serotina)、红栎(Quercus rubra)、多个白蜡属树种(Fraxinus)(Skelly,1964);在密西西比州的Quercus nuttallii,Q. hellos,Q. nigra上也产生由茄镰孢引起的溃疡病(Toole,1966)。近年来,在南非的胡桃(Jugans regia)(Chen et al., 2000),土耳其的NFDA5叶槭(Acer negundo)(Demirci et al., 2006),意大利的悬铃木(Platanus acerifolia) (Pilotti et al., 2002)上都报道了由茄镰孢引起的溃疡病。
在我国未见有茄镰孢菌引起杨树溃疡病的报道(李传道,1979;徐梅卿等,2008),引起其他树种溃疡病的茄镰孢菌则有花椒溃疡病(曹支敏等,1994),银鹊树溃疡病(梁英梅等,1994)等。
茄镰孢菌是1个复合种,其下分为多个专化型(O'Donnell,2000)。发生在欧美杨上的茄镰孢菌与其他树种上已报道的茄镰孢菌之间的关系,除了107杨、中林46杨等杨树品种,是否侵染其他杨树种类和品种,病菌是由国外传入的,还是在国内通过其他寄主侵染欧美杨引起病害的,需要进一步研究。近年来,欧美杨在华北等地得到大面积栽培,目前仅在河南濮阳和山东菏泽2地采集到病害的标本,在其他地方是否有发生,需要对病害发生的范围进行广泛调查。分离过程中,Cz02的镰孢菌分离频率较高,接种试验表明它单独不致病,但它是否与茄镰孢菌有协同作用,有待进一步作接种试验。
曹支敏, 田呈明, 梁英梅, 等. 1994. 陕甘两省花椒病害调查. 西北林学院学报, 9(2): 39-43. |
李传道. 1979. 树木的溃疡病. 南京林产工业学院学报, (Z1): 22-35. |
梁英梅, 田呈明, 高爱琴, 等. 1999. 银鹊树溃疡病病原菌的研究. 西北林学院学报, 14(4): 53-58. DOI:10.3969/j.issn.1001-7461.1999.04.011 |
徐梅卿, 何平勋. 2008. 中国木本植物病原总汇. 哈尔滨: 东北林业大学出版社.
|
魏景超. 1979. 真菌鉴定手册. 上海: 上海科学技术出版社, 534-540.
|
Booth C. 1971. 镰刀菌属. 陈其煐. 北京: 农业出版社, 31-37.
|
Boyer M G. 1961. A Fusarium canker disease of Populus deltoids Marsh. Can J Botany, 39: 1195-1204. DOI:10.1139/b61-104 |
Chen W, Stewart W J. 2000. First report of stem canker of English walnut caused by Fusarium solani in South Africa. Plant Disease, 84: 592. |
Demirci F, Maden S. 2006. A severe dieback of box elder (Acer negundo) caused by Fusarium solani (Mart.) Sacc. in Turkey. Australasian Plant Disease Notes, 1: 13-15. DOI:10.1071/DN06007 |
Dochinger L S, Seliskar C E. 1962. Fusarium canker found on yellow poplar. Journal of Forestry, 60: 331-333. |
Dochinger L S, Leon S. 1967. Occurrence of poplar cankers caused by Fusarium solani in Iowa. Plant Disease Reporter, 11: 900-903. |
Nelson P E, Toussoun T A, Marasas W F O. 1983. Fusarium species, an illstrated manual for identification. The Pennsylvania State University Press, 146-150.
|
O'Donnell K. 2000. Molecular phylogeny of the Nectria haematococca-Fusarium solani species complex. Mycologia, 92: 919-938. DOI:10.2307/3761588 |
Pilotti M, Ponzio V, Motta E. 2002. Isorders of Platanus × acerifolia in Italy associated with Fusarium solani. For Path, 32: 249-264. DOI:10.1046/j.1439-0329.2002.00289.x |
Skelly J M. 1964. The nature and occurrence of an annual canker of Acer saccharum Marsh. in Pennsylvania. M. S. thesis. Pennsylvania State University.
|
Toole E R. 1963. Cottonwood canker caused by Fusarium solani. Plant Disease Report, 47(11): 1032-1035. |
Toole E R. 1966. Stem canker of red oaks caused by Fusarium solani. Plant Disease Report, 50: 160-161. |
White T J, Bruns T, Lee S, et al. 1990. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics//Innis M A, Gelfand D H, Sninsky J J, et al., PCR Protocols: A Guide to Methods and Applications. Academic Press, New York, 315-322.
|
 2009, Vol. 45
2009, Vol. 45