文章信息
- 阎伟, 骆有庆, 宗世祥, 宝山, 孙耀武, 李月华.
- Yan Wei, Luo Youqing, Zong Shixiang, Bao Shan, Sun Yaowu, Li Yuehua
- 油蒿不同演替阶段钻蛀性害虫数量变动与环境的关系
- Woodborers Abundance and the Relationship with Environmental Factors at Different Successional Stages of Artemisia ordosica (Asterales: Compositae)
- 林业科学, 2009, (${metaVo.issue}): 87-91.
- Scientia Silvae Sinicae, 2009, (${metaVo.issue}): 87-91.
-
文章历史
- 收稿日期:2008-08-07
-
作者相关文章
2. 宁夏森林病虫害防治检疫总站 银川 750004;
3. 宁夏灵武市林木检疫站 灵武 751400;
4. 宁夏盐池县林业局检疫站 盐池 751500
2. 2. Forest Diseases and Insect Pests Control and Quarantine Station of Ningxia Hui Autonomous Region Yinchuan 750004;
3. Forest Quarantine Station of Lingwu Ningxia Lingwu 751400;
4. Quarantine Station of Yanchi Forestry Bureau Ningxia 751500
油蒿(Artemisia ordosica)(黑沙蒿)分布于以鄂尔多斯高原为中心的温带半干旱沙区,是我国温带沙漠的优良固沙半灌木,在固定流沙、维持区域生态系统健康和保育生物多样性等方面发挥了重要作用(北京大学地理系等,1983;张新时,1994;杨洪晓等,2004;张德魁等,2007),许多学者对其进行了比较深入的研究(王庆锁等,1997;郭柯,2000;卢建国等,2006;Zhao et al., 2006;王海涛等,2007;Li et al., 2007;Cheng et al., 2007;李慧勇等,2008;杨洪晓等,2008),然而涉及油蒿钻蛀性害虫混合种群危害及其与沙地环境关系研究的报道很少。
近年来,油蒿林钻蛀性害虫沙蒿大粒象(Adosopius sp.)、沙蒿木蠹蛾(Holcocerus artemisiae)、沙蒿圆吉丁虫(Sphenoptera sp.)和一种卷蛾科的蛀茎害虫在内蒙古、宁夏、陕西、甘肃等地大面积暴发,造成油蒿大面积死亡。油蒿群落经历半固定沙丘、固定沙丘、生草沙丘后,最终被较为稳定的后期群落所代替(中国科学院兰州沙漠研究所沙坡头沙漠科学研究所,1991;王庆锁等,1997;郭柯,2000)。针对在油蒿群落演替过程中,油蒿钻蛀性害虫的种类和数量如何波动,影响波动有哪些环境因子等问题,笔者于2006—2007年在毛乌素沙地就油蒿演替的3个阶段,对钻蛀性害虫混合种群的组成结构和环境因子的关系进行了研究。
1 材料与方法 1.1 研究区概况盐池县位于宁夏回族自治区中东部,毛乌素沙地西南缘(37°04′20″—38°10′30″N、106°33′10″—107°47′30″E)。气候属于温带半干旱季风气候,年均气温6.0~8.5 ℃,年均降水量250~350 mm,7—9月占年降水量的68.3%,年均蒸发量为2 000 mm以上。地表形态主要表现为梁地与滩地、沙丘与滩地相间分布。样地土壤主要有沙地上的各类风沙土,以及梁地上的栗钙土或淡栗钙土。调查地油蒿林的基本情况为:半固定沙丘,总盖度≤20%,油蒿盖度13.9%,地表几乎无结皮;植被主要以油蒿为主,仅有沙米(Agirophyllum pungens)、虫实(Corispermum heptapotamicum)等少量伴生种。固定沙丘,总盖度25%~50%,油蒿盖度26.1%,地表具灰白色降尘结皮并逐渐演变为土壤生物结皮;植被以油蒿为建群种,伴生种主要有糙隐紫草(Cleistogenes squarrosa)、兴安胡枝子(Lespedeza davurica)、草木栖状黄芪(Astragalus melilotoides)、乳浆大戟(Euphorbia esula)、雾冰藜(Bassia dasyphylla)、沙葱(Allium prostratum)、赖草(Leymus secalinus)等。生草沙丘,总盖度35%~60%,油蒿盖度31.4%,地表具具发育良好的土壤生物结皮;植被以油蒿为建群种,常见种主要为狗尾草(Setaria viridis)、画眉草(Eragrostis pilosa)、刺藜(Chenopodium aristatum)、山苦荬(Ixeris chinensis)、乳浆大戟、地锦(Euphorbia humifusa)等杂草。
1.2 调查方法根据林分踏查及油蒿群落的演替特点(中国科学院兰州沙漠研究所沙坡头沙漠科学研究所,1991;王庆锁等,1997;郭柯,2000),选择总面积约6 km2的半固定沙丘(Ⅰ)、固定沙丘(Ⅱ)、生草沙丘试验区(Ⅲ),根据钻蛀性害虫对油蒿的危害程度,在Ⅰ、Ⅱ、Ⅲ试验区中分别选取14、13、12块样方,样方大小为10 m×10 m(CCICCD,1997;何志斌等,2004)。在每块样方内,首先,采用双对角线抽样方法,从每个样方内抽取20株油蒿分别测其冠幅、主根粗和树龄等,详细调查这20株油蒿上钻蛀性害虫的种类、虫态、数量,计算每种钻蛀性害虫的虫口密度。然后,采用5点式抽样方法,即在样方的中心和四角共设定5个1 m×1 m的小样方,详细记载每个小样方内出现的草本植物的种类、个体数、土壤含水量、地表结皮类型、坡位、坡向、油蒿盖度和油蒿密度。
其中,油蒿盖度为样地内油蒿冠幅的总和/样地面积(%),油蒿冠幅计算公式为π×CL/2×CW/2(cm2),式中CL为油蒿冠幅的最长距离(cm),CW为油蒿冠幅的最宽距离(cm)(Sah et al., 2004);油蒿密度为样地内油蒿株数/样地面积(株·m-2);油蒿树龄采用切断根径基部后按照年轮数确定;坡位以1=丘间地、2=平地、3=坡下、4=坡中、5=坡顶(于九如等,1997)表示;坡向以0=平地、1=迎风坡、2=背风坡表示;地表结皮类型以1=基本无结皮、2=灰白色降尘结皮、3=具点状黑斑生物结皮、4=具灰黑色藻类和苔藓生物结皮(王庆锁等,1997)表示;土壤含水量(%)采用ML2x型号土壤水分速测仪测定。
1.3 数据处理对油蒿群落演替3个阶段的环境变量以及油蒿钻蛀性害虫个体数量的差异采用非参数检验Kruskal-Wallis方差分析(non-parametric Kruskal-Wallis analysis of variance)以及Tukey多重比较(Tukey post-hoc pairwise comparisons)分析。油蒿钻蛀性害虫密度与环境因子间的关系采用线性逐步回归分析(丁岩钦,1994),以上的数据分析均使用数理统计软件SPSS11.5完成(余建英等,2003)。
2 结果与分析 2.1 油蒿不同演替阶段油蛀性害虫混合种群物种的组成调查结果表明:不同演替阶段油蒿林的钻蛀性害虫主要有4种,分别是危害油蒿根部的沙蒿大粒象(鞘翅目:象甲科)、根部的沙蒿木蠹蛾(鳞翅目:木蠹蛾科)、根部和茎基部的沙蒿圆吉丁虫(Sphenoptera sp.)(鞘翅目:吉丁虫科)和根部和茎基部的一种卷蛾科(鳞翅目:卷蛾科)的蛀茎害虫,这4种害虫以幼虫危害油蒿根和茎基部并导致油蒿死亡。
由图 1可见:上述4种油蒿钻蛀性害虫在油蒿演替的各个阶段均有危害,在生草沙丘阶段油蒿钻蛀性害虫个体数量最多,半固定沙丘阶段最少。但由于在油蒿的演替过程中,油蒿群落的物种组成、多样性、丰富度及周围的环境都会发生一系列的变化(张新时,1994;王庆锁等,1997;郭柯,2000;于云江等,2002),该4种害虫的危害程度也有一定的差异。在半固定沙丘阶段,卷蛾科的蛀茎害虫的个体数量显著(P<0.05)大于其他3种钻蛀性害虫,其个体数量占该阶段钻蛀性害虫总数的46.8%;在固定沙丘阶段,沙蒿大粒象和沙蒿木蠹蛾的个体数量显著(P<0.05)大于其他2种钻蛀性害虫,其个体数量分别占到该阶段钻蛀性害虫总数的35.7%和33.1%;在生草沙丘阶段,沙蒿圆吉丁虫的数量极显著(P<0.01)大于其他3种钻蛀性害虫,其个体数量占该阶段钻蛀性害虫总数的69.6%。在油蒿群落演替的3个阶段中,危害油蒿的钻蛀性害虫的优势种各不相同;沙蒿木蠹蛾、沙蒿大粒象、沙蒿圆吉丁的个体数量在油蒿演替的3个阶段差异均显著(P<0.01),沙蒿木蠹蛾和沙蒿大粒象的个体数量在固定沙丘阶段的个体数量显著高于其他2个阶段,沙蒿圆吉丁的个体数量表现为逐渐增多、在生草沙丘阶段其个体数量达到最大;卷蛾科的蛀茎害虫的个体数量在油蒿演替的3个阶段没有显著差异(P>0.05)。

|
图 1 油蒿不同演替阶段钻蛀性害虫的虫口密度 Figure 1 Population densities of insect borers at different successional stages of A. ordosica |
油蒿群落在演替的时间序列过程中,各演替阶段的环境因子组合作用于昆虫,必然影响其种群数量,可通过线性回归模型检验影响油蒿钻蛀性害虫虫口密度的主要环境因子。
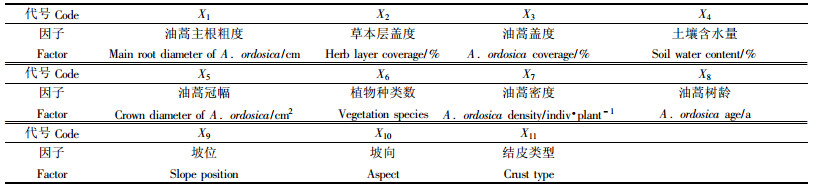
表 1为油蒿钻蛀性害虫密度与环境因子回归模型中的自变量及其代码。其中,半固定沙丘因变量为:Y1为油蒿钻蛀性害虫虫口密度(用头·株-1表示,下同),Y11为沙蒿木蠹蛾的虫口密度,Y12为沙蒿大粒象的虫口密度,Y13为沙蒿圆吉丁虫的虫口密度,Y14为卷蛾科的蛀茎害虫的虫口密度;固定沙丘和生草沙丘阶段的因变量设置依此类推。
|
|
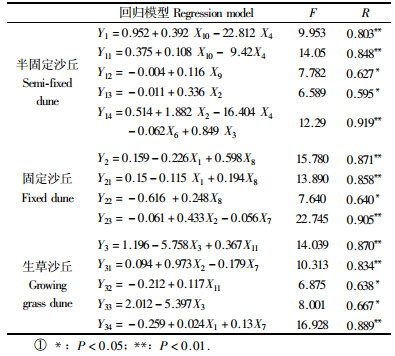
根据上述变量设置,对4种油蒿钻蛀性害虫的虫口密度与环境因子进行线性逐步回归检验得表 2。由表 2可见:随着油蒿群落演替的进行,影响油蒿钻蛀性害虫危害的环境因子也发生着相应的变化。在半固定沙丘阶段,坡向和土壤含水量是影响油蒿钻蛀性害虫虫口密度的主要环境因子;固定沙丘阶段,油蒿主根粗度和树龄是影响油蒿钻蛀性害虫虫口密度的主要环境因子;生草阶段,油蒿盖度和结皮是影响油蒿钻蛀性害虫虫口密度的主要环境因子。
|
|
其次,同一种油蒿钻蛀性害虫,在油蒿演替的不同的阶段,影响其虫口密度的环境也不完全相同。如在半固定沙丘阶段,坡向和土壤含水量是沙蒿木蠹蛾虫口密度的主要影响因子;固定沙丘阶段,油蒿主根粗度和树龄是其虫口密度的主要影响因子;到生草阶段,草本层盖度和油蒿密度是决定其虫口密度的主要环境因子。
此外,虽然4种油蒿钻蛀性害虫属于同一营养层生物,但是在油蒿演替的同一阶段,影响油蒿钻蛀性害虫的环境因子也不完全相同。以生草沙丘阶段来说,影响沙蒿木蠹蛾虫口密度的环境因子是草本层盖度和油蒿密度,结皮类型则是影响沙蒿大粒象虫口密度的主要环境因子,油蒿盖度是沙蒿圆吉丁虫虫口密度的主要影响因子,油蒿主根粗度和油蒿密度是影响卷蛾科的蛀茎害虫密度的主要环境因子。
3 小结与讨论在植被演替的过程中,植物群落的物种组成、多样性、丰富度及周围的环境都会发生一系列的变化(张新时,1994;郭柯,2000;于云江等,2002)并直接影响到群落中昆虫种群数量的变动(Southwood et al., 1979;Erja et al., 2000;Ingolf et al., 2002;Heybornea et al., 2003;易兰等,2005;Edwin et al., 2006)。因此,研究油蒿群落不同演替阶段的钻蛀性害虫种群动态与环境的关系,对于揭示钻蛀性害虫在油蒿演替过程中的危害规律及防治有重要意义。
本研究结果表明:随着油蒿群落演替的进行,油蒿钻蛀性害虫混合种群的总体数量逐渐增多,但只有沙蒿圆吉丁虫的个体数量明显增多,卷蛾科的蛀茎害虫的个体数量则逐渐减少,而沙蒿大粒象和沙蒿木蠹蛾的个体数量则是先增加再减少。在油蒿林演替的过程中,油蒿林钻蛀性害虫混合种群的优势种由最初半固定沙丘阶段卷蛾科的蛀茎害虫→固定沙丘阶段沙蒿大粒象和沙蒿木蠹蛾→生草沙丘阶段沙蒿圆吉丁虫。造成这一现象的原因可能与该钻蛀性害虫的生物学特性有关,即沙蒿木蠹蛾和沙蒿大粒象与沙蒿圆吉丁相比其体型和食量较大,且沙蒿木蠹蛾有转移危害的现象,前2种害虫的雌成虫只在未被其危害的油蒿上产卵,而沙蒿圆吉丁虫也在被其他害虫危害后的油蒿上、甚至在距离地表 20 cm的油蒿茎部危害取食;另一方面,在油蒿群落的演替过程中,群落的生态环境也发生了变化,这些变化也对油蒿林钻蛀性害虫的演替施加了影响。在半固定沙丘阶段沙地质地疏松,植物种类少而稀疏,群落冠层温度变化剧烈,相对湿度低;在固定沙丘阶段,植物种类增多,覆盖度大,生物量高,缓冲气象因子的能力增强;在生草沙丘阶段,植物种类最多,密度最大,但土壤紧实,稳定性较高(王庆锁等,1997;王新平等,2005;张德魁等,2007)。因此,可以推断在油蒿群落从半固定沙丘到生草沙丘的演替过程中,系统逐渐趋于相对稳定的平衡状态,为钻蛀性害虫提供了更加稳定的栖息微环境;同时因为演替前期钻蛀性害虫的危害,使得油蒿生长势降低,从而更有利于钻蛀性害虫的发生。
综上所述,油蒿林钻蛀性害虫混合种群的变化受油蒿群落演替阶段的影响较大,在防治中应根据油蒿林的演替情况,采取合适的调控策略进行防治。
北京大学地理系, 中国科学院自然资源综合考察委员会, 中国科学院兰州沙漠研究所, 等. 1983. 毛乌素沙区自然条件极其改良利用. 北京: 科学出版社, 83-84.
|
丁岩钦. 1994. 昆虫数学生态学. 北京: 科学出版社, 399-403.
|
郭柯. 2000. 毛乌素沙地油蒿群落的循环演替. 植物生态学报, 24(2): 243-247. DOI:10.3321/j.issn:1005-264X.2000.02.020 |
何志斌, 赵文智, 常学向, 等. 2004. 荒漠植被物种多样性对空间尺度的依赖. 生态学报, 26(6): 1146-1149. DOI:10.3321/j.issn:1000-0933.2004.06.008 |
李慧勇, 李慧卿, 李清河, 等. 2008. 几种人工固沙林多种群多尺度格局及种间关联. 应用生态学报, 19(4): 741-746. |
卢建国, 王海涛, 何兴东, 等. 2006. 毛乌素沙地半固定沙丘油蒿种群对土壤湿度空间异质性的响应. 应用生态学报, 17(8): 1469-1474. DOI:10.3321/j.issn:1001-9332.2006.08.022 |
王海涛, 何兴东, 高玉葆, 等. 2007. 油蒿演替群落密度对土壤湿度和有机质空间异质性的响应. 植物生态学报, 31(6): 1145-1153. |
王庆锁, 董学军, 陈旭东, 等. 1997. 油蒿群落不同演替阶段某些群落特征的研究. 植物生态学报, 21(6): 531-538. DOI:10.3321/j.issn:1005-264X.1997.06.005 |
王新平, 李新荣, 肖洪浪, 等. 2005. 干旱半干旱地区人工固沙灌木林生态系统演变特征. 生态学报, 25(8): 1974-1980. DOI:10.3321/j.issn:1000-0933.2005.08.021 |
杨洪晓, 张金屯, 吴波, 等. 2004. 油蒿(Artemisia ordosica)对半干旱区沙地生境的适应及其生态作用. 北京师范大学学报(自然科学版, 40(5): 684-690. DOI:10.3321/j.issn:0476-0301.2004.05.020 |
杨洪晓, 张金屯, 李振东, 等. 2008. 毛乌素沙地油蒿(Artemisia ordosica)种群空间格局对比. 生态学报, 28(5): 1901-1910. DOI:10.3321/j.issn:1000-0933.2008.05.003 |
易兰, 由文辉, 宋永昌. 2005. 天童常绿阔叶林五个演替阶段凋落物中的土壤动物群落. 生态学报, 25(3): 466-473. DOI:10.3321/j.issn:1000-0933.2005.03.013 |
于九如, 韦少敏, 朱灵益. 1997. 数量化理论(Ⅰ)与专家评分多元回归方法在荒漠地区生物量估测上的比较. 林业科学, 3(6): 481-487. DOI:10.3321/j.issn:1001-7488.1997.06.001 |
余建英, 何旭宏. 2003. 数据统计分析与SPSS应用. 北京: 人民邮电出版社.
|
于云江, 林庆功, 石庆辉, 等. 2002. 包兰铁路沙坡头段人工植被区生境与植被变化研究. 生态学报, 22(3): 433-439. DOI:10.3321/j.issn:1000-0933.2002.03.021 |
张德魁, 王继和, 马全林, 等. 2007. 油蒿研究综述. 草业科学, 24(8): 30-35. DOI:10.3969/j.issn.1001-0629.2007.08.006 |
张新时. 1994. 毛乌素沙地的生态背景极其草地建设的原则与优化模式. 植物生态学报, 18(1): 1-16. DOI:10.3321/j.issn:1005-264X.1994.01.008 |
中国科学院兰州沙漠研究所沙坡头沙漠科学研究所. 1991. 腾格里沙漠沙坡头地区流沙治理研究(二). 银川: 宁夏人民出版社, 27-57.
|
CCICCD (Chinese Committee for Implementing UN Convention to Combat Desertification). 1997. China Country Paper to Combat Desertification. Beijing: China Forestry Publishing House, 40.
|
Cheng X, An S, Chen J, et al. 2007. Spatial relationships among species, above -ground biomass, N, and P in degraded grasslands in Ordos Plateau, northwestern China. Journal of Arid Environments, 68: 652-667. DOI:10.1016/j.jaridenv.2006.07.006 |
Rowe E C, Healeyc J R, Jonesc G E, et al. 2006. Fertilizer application during primary succession changes the structure of plant and herbivore communities. Biological Conservation, 131: 510-522. DOI:10.1016/j.biocon.2006.02.023 |
Huusela-Veistola E, Vasarainen A. 2000. Plant succession in perennial grass strips and effects on the diversity of leafhoppers (Homoptera, Auchenorrhyncha). Agriculture Ecosystems and Environment, 80: 101-112. DOI:10.1016/S0167-8809(00)00143-2 |
Heybornea W H, Millera J C, Parsons G L. 2003. Ground dwelling beetles and forest vegetation change over a 17-year-period, in western Oregon, USA. Forest Ecology and Management, 179: 123-134. DOI:10.1016/S0378-1127(02)00490-5 |
Li C P, Xiao C W. 2007. Above and belowground biomass of Artemisia ordosica communities in three contrasting habitats of the Mu Us desert, northern China. Journal of Arid Environments, 70: 195-207. DOI:10.1016/j.jaridenv.2006.12.017 |
Sah J P, Ross M S, Koptur S, et al. 2004. Estimating aboveground biomass of broadleaved woody plants in the understory of Florida Keys pine forests. Forest Ecology and Management, 203: 319-329. DOI:10.1016/j.foreco.2004.07.059 |
Steffan-Dewenter I, Tscharntke T. 2002. Insect communities and biotic interactions on fragmented calcareous grasslands—a mini review. Biological Conservation, 104: 275-284. DOI:10.1016/S0006-3207(01)00192-6 |
Southwood T R E, Brown V K, Reader P M. 1979. Relationships of plant and insect diversities in succession. Biological Journal of the Linnean Society, 12: 327-348. DOI:10.1111/bij.1979.12.issue-4 |
Zhao L J, Xiao H L, Liu X H. 2006. Variations of foliar carbon isotope discrimination and nutrient concentrations in Artemisia ordosica and Caragana korshinskii at the southeastern margin of China's Tengger Desert. Environmental Geology, 50: 285-294. DOI:10.1007/s00254-006-0209-1 |
 2009, Vol.
2009, Vol.