文章信息
- 侯英杰, 苏晓华, 焦如珍, 黄秦军, 褚延广.
- Hou Yingjie, Su Xiaohua, Jiao Ruzhen, Huang Qinjun, Chu Yanguang
- 转基因银腺杂种杨对土壤微生物的影响
- Effects of Transgenic Populus alba×P.glandulosa on Soil Microorganism
- 林业科学, 2009, 45(5): 148-152.
- Scientia Silvae Sinicae, 2009, 45(5): 148-152.
-
文章历史
- 收稿日期:2008-03-07
-
作者相关文章
近20年来,转基因林木已开始进行田间试验,其中部分还获得商品化许可。与此同时,转基因林木的生态安全问题也逐渐受到关注,但这方面研究报道还很少。目前,已开展的转基因林木安全性研究多集中在转抗虫Bt毒蛋白基因和蛋白酶抑制剂基因林木上(高素红等, 2005),而很少涉及抗逆境等其他性状基因。
土壤是生态系统中物质循环和能量转化的重要场所,转基因植物体内外源基因的表达产物有可能通过植物残留物及根系分泌物对土壤生态系统特别是对土壤微生物造成影响。评价转基因林木对土壤微生物的影响也具有重要的生态学意义(胡建军等, 2004)。
为探讨外源基因数量、种类以及不同种植年限对土壤微生物数量变化的影响程度,本研究以转基因银腺杂种杨(Populus alba×P. glandulosa)及其非转基因对照共4个株系为材料,利用PCR技术对转基因株系外源基因的稳定性进行检测,并连续2年对其根圈土壤微生物数量进行监测,初步探讨转基因银腺杂种杨对土壤微生物数量的影响,为进一步深入研究其生态安全性提供依据。
1 材料与方法 1.1 试验设计试验林位于北京市房山区韩村河东营苗圃,2006年春季造林,造林面积为0.66 hm2。试验林共种植3种转基因杨树及其非转基因对照15个株系,分别为银腺杂种杨、银中杨(Populus alba ×P. berolinensis)和库安托杨(P.×euramericana‘Guariento')。所有转基因株系均已经分子检测及功能验证(张冰玉等, 2005; 2006)。每个株系按正方形种植100株(行10株,列10株),株行距为2 m × 2 m。
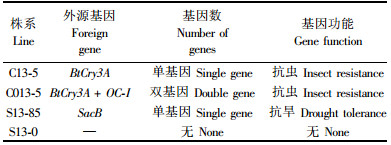
本试验仅选取银腺杂种杨3个转基因株系及1个非转基因对照株系进行研究,参试株系及其转化的外源基因列于下表(表 1)。
|
|
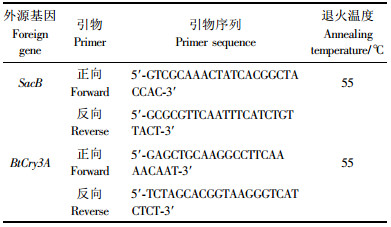
于2007年10月分别取C13-5,C013-5,S13-85,S13-0等4个参试株系幼嫩叶片,迅速置于-40 ℃保存备用。采用DNeasy Plant Mini Kit (Qiagen,Germany)提取银腺杂种杨叶片基因组DNA,具体操作按试剂盒使用手册进行。以4个株系基因组DNA为模板,用基因特异性引物对外源基因SacB和BtCry3A进行PCR扩增,外源基因及其PCR引物与退火温度情况见表 2。
|
|
在所选取的每个株系林分内随机选取1个样点采集土样,每个样点按等边三角形3次重复取样,进行土壤理化性质的测定。对测定结果进行单因素方差分析与多重比较,发现来自4个参试株系林分土壤样品的理化性质并无显著差异,说明本试验的本底一致。4个样点土壤的理化性质各指标平均值分别为:pH 8.24;全氮(N)含量1.04 g·kg-1;全磷(P)含量0.77 g·kg-1;全钾量K 21.29 g·kg-1;碱解氮(N)含量93.56 mg·kg-1;速效磷(P)6.91 mg·kg-1;速效钾(K) 94.69 mg·kg-1;有机质含量22.36 g·kg-1。试验林按常规方法进行田间管理,在整个生长季节内均不使用农药。
1.4 土壤微生物数量测定1)取样方法 分别于2006年8—10月及2007年4—10月在试验林内用土钻取根圈土壤。每个株系林分内随机选取3个样点进行取样,每个样点位于以植株为中心的等边三角形的3个顶点上,将土样装入灭菌布袋中混合均匀,于4 ℃保存备用。
2)测试方法 配制孟加拉红培养基、牛肉膏蛋白胨培养基和改良淀粉铵培养基,采用稀释平板法对土样中的真菌、细菌、放线菌进行培养,各设3次重复。称取一定量的待测土样于烘箱中,105 ℃烘烤,恒重后称量,计算含土量。用SPSS13.0软件进行数据的统计分析。
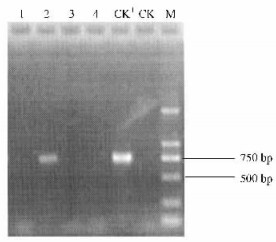
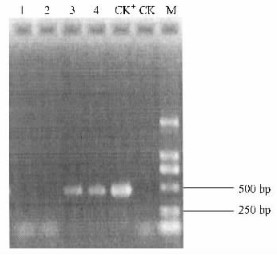
2 结果与分析 2.1 目的基因遗传稳定性分析对银腺杂种杨3个转基因株系和1个非转基因对照株系基因组DNA进行的外源基因PCR检测。在图 1和图 2中,泳道1为非转基因对照株系S13-0,泳道2~4分别为转基因株系S13-85,C013-5和C13-5,泳道CK+为外源基因阳性质粒对照,泳道CK-为无模板水对照,泳道M为DL2000分子量标准。PCR反应结果显示:参试的3个转基因银腺杂种杨株系中,株系C13-5和C013-5检测到BtCry3A基因的存在(PCR产物440 bp),株系S13-85检测到SacB基因的存在(PCR产物743 bp)。由于转基因株系C013-5中BtCry3A和OC-I基因位于同一个T-DNA骨架上,因此可以认为OC-I基因也存在于该转基因株系中。此外,非转基因株系S13-0及无模板水对照中无目的条带产物,说明PCR结果可信,转基因银腺杂种杨中所有目的基因仍稳定存在于其基因组中。
|
图 1 SacB基因的PCR产物电泳检测结果 Figure 1 Results of electrophesis of PCR products of SacB gene |
|
图 2 BtCry3A基因的PCR产物电泳检测结果 Figure 2 Results of electrophesis of PCR products of BtCry3A gene |
对2年试验得到的数据进行整理分析,根据含土量得出每克干土中土壤微生物菌落数[菌落平均数×稀释倍数]/[接种量毫升数×(1-含水量)]。银腺杂种杨林分内单位土壤样品中细菌数量最多,放线菌数居中,真菌数最少,这与自然条件下土壤微生物数量的分布比例一致。3种土壤微生物数量在不同月份表现出一致的变化趋势,不同微生物的数量在转基因株系及非转基因株系林分内的变化趋势也基本一致。在自然条件下,土壤微生物数量通常会随土壤温度、湿度的加大在一定程度上有所增加,本试验林分内3种土壤微生物的数量随土壤温度、湿度的变化趋势也与此规律基本一致。
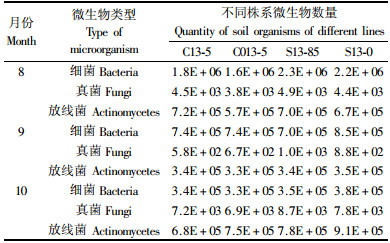
1)当年生林地不同株系土壤中主要微生物数量情况 2006年8—10月3次对土壤样品的检测所得微生物数量平均值见表 3。微生物数量以每克干土中土壤微生物菌落数表示。本年8,9月份土壤中细菌数量最多,放线菌数居中,真菌数最少,但9月份细菌、真菌及放线菌数量较8月份有所减少;细菌数量在10月份时继续减少,但真菌和放线菌数量则增加到高于8月份的水平。总体来看,土壤中细菌数量随时间呈现出逐步减少的趋势,而真菌和放线菌数量则呈现出先降后升的趋势。
|
|
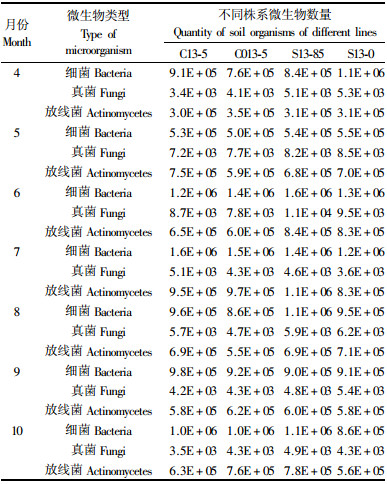
2)次年生林地不同株系土壤中主要微生物数量情况 2007年4—10月7对土壤样品的检测所得微生物数量平均值见表 4。5月份细菌数量较低,但随着气温的升高和湿度的加大而呈逐渐增加的趋势;4,5,6月真菌数量随着气温的升高而逐渐增加,7月份由于湿度的加大而有所降低;放线菌数在整体上呈逐渐增加的趋势,但其数量在6月时较5月份有所减少,该变化并无明显的规律性。
|
|
由表 4中可以看出:8月份,3种微生物中细菌数量最多,放线菌数居中,真菌数最少,9月份后随气温的降低,3种微生物数量均不断减少;真菌数量在10月份时继续减少,而细菌和放线菌数量却略有增加,且放线菌数量达到8,9,10月中的最高水平,其原因尚不明。总体来看,2007年8,9和10月份细菌和放线菌数量呈现出先降后升的趋势,而真菌则呈现出逐渐减少的趋势。这与2006年的变化趋势略有不同,推测可能是由于不同年份相同月份间温度、湿度和植株根系分泌物等情况的不同综合作用的结果。
2.3 土壤微生物数量的单因素方差分析对2006年造林当年林地内银腺杂种杨4个株系在3个月份内(8,9和10月)的3种土壤微生物数量分别进行单因素方差分析与多重比较。银腺杂种杨各株系间在3种微生物数量上并无显著差异。对2007年7个月份的调查数据进行单因素方差分析与多重比较,4月份株系间细菌数量和放线菌数量差异显著,其中非转基因对照株系S13-0林分内细菌数量高于转基因株系C013-5和S13-85林分,转基因株系C013-5林分内土壤放线菌数量高于其他3个株系;6月份株系间真菌数量差异显著,其中转基因株系S13-85林地内的真菌数量高于C13-5和C013-5;其他各月份内株系间3种微生物数量无明显差异(表 5)。
|
|
总体看来,参试林地内大部分株系林地间(不同转基因株系间、转基因株系与对照株系间)土壤微生物数量并无明显差异,个别月份中个别株系间虽有差异但并无明显的规律性,说明外源基因种类和数量的不同并未对土壤微生物数量造成影响。
将3个转基因株系所得数据综合后作为转基因林分的总数据,对当年生林地内银腺杂种杨转基因林分与非转基因林分在3个月份内的3种土壤微生物数量进行单因素方差分析,结果显示:大部分参试转基因株系与对照株系林地内微生物数量无明显差异。10月份时,转基因与其非转基因对照林分的土壤细菌数量呈极显著差异(P≤0.01),表现为非转基因林分内土壤细菌数量高于转基因林分。对2007年获得的7个月份数据进行的单因素方差分析结果表明:4月份非转基因林分与转基因林分土壤细菌数量差异显著,非转基因林分土壤微生物数量高于转基因林分;但7月份非转基因林分与转基因林分土壤细菌和真菌数量差异显著,但表现为转基因林分内其数量高于非转基因林分(表 6)。总的来看,转基因林地与非转基因林地土壤微生物数量变化并明显的规律性,个别月份中的数量的差异可能为自然条件所致,说明本试验地内的转基因银腺杂种杨尚未对土壤微生物数量造成影响。
|
|
对不同年份(2006年和2007年)同一月份(8,9和10月)的土壤3种微生物数量进行均值比较与单因素方差分析的结果见表 7。
|
|
分析结果表明:土壤细菌数量在2006年8月达最高,在2006年10月最低,所有月份年份间土壤细菌数量的差异均达极显著水平(P<0.05)。土壤真菌数量在2007年9月达最高,在2006年10月最低,其数量在8月份的差异达到显著水平,在7月和9月达极显著水平(P<0.01)。土壤放线菌数量也在2006年8月达最高,在2006年10月最低,其数量在9月份差异达极显著水平,而其余月份均无显著差异。3种微生物数量年份间的变化及差异情况并无明显的规律性,推测可能为不同年份相同月份间自然条件的差异所致,说明转基因杨树种植年限的增加并未对土壤微生物系统造成影响。
3 结论与讨论转基因植物对土壤微生物可能造成的影响一直是人们进行转基因植物安全性评价的焦点,2000年美国环保署(EPA)将转基因植物对土壤生态系统的影响列为风险评价的重要组成部分,相关报道也在不断增多(Glandorf et al., 1997; Oger et al., 1997; 赵海泉等, 2007)。本研究通过对试验地内银腺杂种杨4个株系土壤微生物数量进行10个月的调查分析,结果发现大部分株系间土壤微生物数量无显著差异,个别株系间虽存在差异但并无规律性,说明外源基因种类和数量的不同并未对土壤微生物数量造成影响。同时,转基因林地与非转基因林地土壤微生物数量变化也无规律性,证明本试验地内的转基因杨树尚未对土壤微生物数量造成影响。对不同年份同1月份的土壤微生物数量进行均值比较与单因素方差分析,结果发现3种微生物数量差异较大,但却无规律可寻,说明转基因杨树种植年限的增加并未对土壤微生物系统造成影响。这一结论与胡建军等(2004)等对田间试验7年的转Bt基因欧洲黑杨(Populus nigra)的研究基本一致,该研究通过土壤微生物类群数量分析,发现转基因与非转基因植株间、林地间土壤3大类微生物(细菌、放线菌和霉菌)数量无显著差异,证明转基因欧洲黑杨对土壤微生物系统尚未有明显影响。
虽然对转基因植物风险评价的研究大多未发现参试转基因植物对土壤微生物造成不利的影响(Saxena et al., 2000; Griffiths et al., 2000; Devare et al., 2004),但与本研究结果不同的是,少数研究发现转基因作物对土壤微生物有着不同程度的影响,如阮妙鸿等(2007)利用平板法对转基因(ScMV-CP)甘蔗(Saccharum sinensis)土壤中主要微生物数量变化进行了测定,发现转基因甘蔗显著增加了根际土壤可培养的细菌和真菌数量,但对放线菌影响很小。这些结果有可能同时受不同的环境条件和农业田间作业过程的影响,且所观察到的转基因作物对土壤微生物的影响常是不稳定的。对于大田条件下的生态安全性评价,由于立地条件、温度、湿度和光照等各项影响因子很难控制,给检测增加了难度。此外,转基因植物各项安全性评价目前国际上还没有一个共同的评价标准,这些问题可能会使不同的研究者在类似的试验中得到了不同的结论,因此,有必要继续摸索科学合理的检测技术与手段,尽快建立一套国际认可的评价体系。
本试验涉及了SacB、BtCry3A和OC-I等3个不同的目的基因,在多个月份对土壤细菌、真菌、放线菌的数量进行连续监测,获得大量相关数据,并通过统计分析得到了初步的结论,为深入研究转基因杨树的生态安全性奠定了基础。林木普遍具有类型复杂、生命周期长,基因组巨大等特点,因此对转基因林木生态安全性的了解还需要进行长期、深入、系统的研究。一些研究发现土壤生态系统的变化是多因素综合作用的结果,如Rui等(2005)发现纯的Bt毒蛋白进入到根际土壤后,土壤微生物的数量没有发生明显的改变,由此推断土壤微生物数量如果发生改变并不单是Bt毒蛋白直接作用的结果,或许还有其他因子的参与作用。本试验中个别转基因株系及非转基因株系之间土壤微生物数量差异达到显著水平,虽然目前未发现其存在规律性,但该现象需引起我们的注意,还要进行进一步的追踪调查。
高素红, 毛富玲, 王江柱, 等. 2005. 转双抗虫基因741杨节肢动物群落生态安全性评价. 河北农业大学学报, 28(3): 77-80. DOI:10.3969/j.issn.1000-1573.2005.03.020 |
胡建军, 张蕴哲, 卢孟柱, 等. 2004. 欧洲黑杨转基因稳定性及对土壤微生物的影响. 林业科学, 40(5): 105-109. DOI:10.3321/j.issn:1001-7488.2004.05.017 |
阮妙鸿, 许燕, 郑瑶, 等. 2007. 转ScMV-CP基因甘蔗对根际土壤酶活性及微生物的影响. 中国农学通报, 23(4): 381-386. DOI:10.3969/j.issn.1000-6850.2007.04.088 |
张冰玉, 苏晓华, 黄秦军, 等. 2005. 转果聚糖蔗糖转移酶基因银腺杂种杨的获得. 林业科学, 41(3): 48-53. DOI:10.3321/j.issn:1001-7488.2005.03.008 |
张冰玉, 苏晓华, 李义良, 等. 2006. 转抗鞘翅目害虫基因银腺杂种杨的获得及其抗虫性的初步研究. 北京林业大学学报, 28(2): 102-105. DOI:10.3321/j.issn:1000-1522.2006.02.018 |
赵海泉, 曹珂珂, 王凤娟, 等. 2007. bar基因对盆栽小麦根际微生物的影响. 安徽农业大学学报, 34(1): 1-7. |
Devare M H, Jones C M, Thies J E, et al. 2004. Effect of Cry3Bb Transgenic corn and tefluthrin on the soil microbial community: biomass, activity, and diversity. J Environ Qual, 33(3): 837-843. DOI:10.2134/jeq2004.0837 |
Glandorf D C M, Bakker P A H M, Van Loon L C, et al. 1997. Influence of the production of antibacterial and antifungal proteins by transgenic plants on the saprophytic soil microflora. Acta Bot Neerl, 46(1): 85-104. DOI:10.1111/plb.1997.46.issue-1 |
Griffiths B S, Geoghegan I E, Robertson W M. 2000. Testing genetically engineered potato, producing the lectins GNA and Con A, on non-target soil organisms and processes. J Appl Ecol, 37: 159-170. |
Oger P, Petit A, Dessaux Y. 1997. Genetically engineered plants producing opines alter their biological environment. Nature Biotechnol, 15(4): 369-372. DOI:10.1038/nbt0497-369 |
Rui Y K, Yi G X, Zhao J, et al. 2005. Changes of Bt toxin in the rhizosphere of transgenic Bt cotton and its influence on soil functional bacteria. World Journal of Microbiology and Biotechnology, 21: 1279-1284. DOI:10.1007/s11274-005-2303-z |
Saxena D, Stotzky G. 2000. Insecticidal toxin from Bacillus thuringiensis is released from roots of transgenic Bt corn in vitro and in situ. FEMS Microbial Ecol, 33: 35-39. DOI:10.1111/fem.2000.33.issue-1 |
 2009, Vol. 45
2009, Vol. 45