文章信息
- 左航, 黄文, 李天宏, 龚国华, 魏蒙.
- Zuo Hang, Huang Wen, Li Tianhong, Gong Guohua, Wei Meng
- 杜仲叶中绿原酸的提取条件优化及其提取物的降血脂作用
- Optimization of Extracting Chlorogenic Acid from Eucommia ulmoides Leaf and the Effect of the Extract on Hyperlipemia in Mice
- 林业科学, 2009, 45(1): 158-160.
- Scientia Silvae Sinicae, 2009, 45(1): 158-160.
-
文章历史
- 收稿日期:2007-12-03
-
作者相关文章
2. 北京大学环境工程系 水沙科学教育部重点实验室 北京 100871;
3. 四川大学纳米生物医学技术与膜生物学研究所 四川大学华西医院肿瘤生物治疗国家重点实验室 成都 610041
2. Environmental Engineering Department of Peking University Key Laboratory for Water and Sediment Sciences of Ministry of Education Beijing 100871;
3. Institute for Nanoblomedical Technology and Membrane Biology, Sichuan University State Key Laboratory of Biotherapy, West China Hospital, Sichuan University Chengdu 610041
杜仲叶为杜仲科植物杜仲(Eucommia ulmoides)的干燥叶,具有补肝肾、强筋骨的功效,用于肝肾不足,头晕目眩,腰膝酸痛,筋骨痿软(国家药典委员会,2005)。绿原酸是杜仲叶中的主要化学成分,具有多种生物活性,杜仲叶中含有1%~5.5%绿原酸,是目前国内绿原酸提取的主要原料。现代医学根据药理实验和临床应用证明了杜仲叶能有效治疗高血压病,降低血脂,抗炎、抗病毒,同时还具有增强机体免疫力、抗衰老、抗癌等作用(叶文峰,2004),因此杜仲叶也被广泛地应用于保健品行业。张瑛朝(2000)、张瑛朝等(2001)对复方杜仲叶合剂进行了大鼠(Rattus norvegicus)和人体的降血脂作用研究,结果显示由杜仲叶、葛根及山楂组成的复方合剂具有降脂作用。
本文在优化杜仲叶中绿原酸提取工艺的同时,对杜仲叶提取物进行了抗小鼠高血脂作用的研究,为将来对杜仲叶的资源化利用提供基础数据,提高杜仲叶资源开发,利用的经济社会效益。
1 材料与方法 1.1 材料与仪器1)药品与试剂 杜仲叶于2006年秋季采摘自湖北郧西杜仲基地。其他包括:胆固醇(日本进口分装);脱氧胆酸钠、磷酸、吐温-80(分析纯);猪油(自制);绿原酸对照品(中国药品生物制品检定所,生产批号为110753-200413)。总胆固醇(TC)试剂盒、总甘油三酯(TG)试剂盒、高密度脂蛋白胆固醇(HDL-C)试剂盒及低密度脂蛋白胆固醇(LDL-C)试剂盒(中生北控生物科技股份有限公司)。
2)仪器 包括:Shimadzu UV-1700型紫外-可见分光光度计(日本岛津);Beckman Micofuge 18 Centrifuge台式微型离心机(美国贝克曼);CHB-100恒温金属浴(杭州博日科技有限公司)。
3)动物 小鼠(Mus musculus):昆明种,40只,雌雄各半,体质量30~40 g,由四川省医科院实验动物研究所提供,动物合格证号为SCXK[川]2004-15。
1.2 试验方法1)绿原酸含量测定(周军等,2008) 精密称取绿原酸标准品4.92 mg,以60%乙醇水溶液定容致100 mL,摇匀为标准母液。准确吸取上述标准母液1.00 mL,用60%乙醇水溶液稀释到10 mL,以体积分数60%乙醇水溶液作为参比溶液,在200~500 nm范围内进行紫外扫描,得其最大吸收波长328 nm。
分别准确吸取标准母液0.05, 0.10, 0.20, 0.50, 1.00, 2.00和5.00 mL,以10 mL容量瓶定容,配成梯度浓度,在328 nm下测定吸光度A。测定结果由最小二乘法进行线性回归,得绿原酸标准曲线,C=39.29A+0.196,R2=0.999。这表明绿原酸在0~20 mg·L-1范围内呈良好的线性关系。
称取2.00 g杜仲叶,以不同条件,在水浴中以乙醇回流提取,提取液定容至100 mL,再稀释100倍,以紫外扫描仪在328 nm波长下扫描,测得吸光度,代入标准方程,计算可得含量。
2)高血脂症小鼠造模 采用灌胃高脂乳剂的方法造模,高脂乳剂配方参照文献(张加雄等,2004;2006;熊静悦等,2006)并加以改进:取1 g丙硫氧嘧啶和20 g胆固醇于研钵中分别研细,备用。取40 g猪油于40 ℃水浴加热融化,置研钵中,加入20 g胆固醇、1 g丙硫氧嘧啶,充分搅拌,溶解。再徐徐加入10%的脱氧胆酸钠水溶液20 mL,并不断搅拌,然后加入3.0 mL吐温-80,研磨乳化均匀,最后加蒸馏水至100 mL。装入密闭容器,冷藏,使用时置37 ℃水浴中融化。
3)动物分组及给药 小鼠随机分为4组,每组10只,雌雄各半:正常对照组(A组CON)、模型组(B组HLM)、地奥组(C组DIAO)、杜仲叶醇提物组(D组ETDZ)。A组动物上午灌胃2%吐温-80(TW)溶液,下午灌胃蒸馏水;B、C、D组动物每天上午分别灌胃2%TW溶液、90 mg·mL-1地奥心血康2%TW溶液、600 mg·mL-1杜仲提取物2%TW溶液,下午灌胃脂肪乳剂。各组上午灌胃量为10 mL·kg-1体质量,下午灌胃量为15 mL·kg-1体质量,连续灌胃14 d。
4)指标测定 小鼠灌胃14 d后,禁食不禁水,12 h后摘眼球取血,3 000 r·min-1离心15 min分离血清。参照试剂盒说明书方法,利用紫外分光光度计测定吸光度,换算血清TC、TG及LDL-C含量,并由Friedwald.WT公式:HDL-C=TC-(1/5TG + LDL-C)计算血清中HDL-C的含量。
5)统计学处理 所有数据用x±s表示,采用Spss12.0软件进行统计学分析。
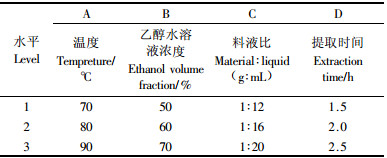
2 结果与分析 2.1 杜仲叶中绿原酸提取条件优化杜仲叶中绿原酸的提取受回流时间、提取温度、乙醇水溶液浓度和乙醇水溶液用量等因素的影响。为探索最佳提取条件,在单因素实验的基础上,对每个因素分别取3个水平,采用L9(34)正交实验设计,各因素和水平如表 1所示。
|
|
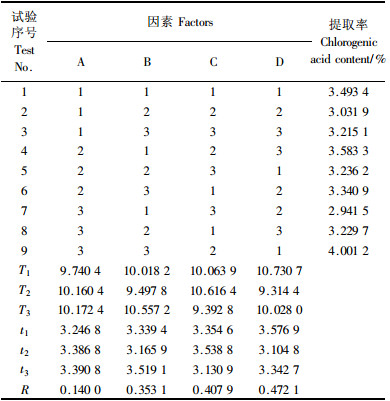
由表 2的数据可以得到,杜仲叶中绿原酸提取的最佳工艺组合为A3B3C2D1,即提取温度90 ℃,乙醇水溶液浓度为70%,料液比1:16,提取1.5 h。由极差分析可得,各因素对绿原酸提取影响的大小为D>C>B>A,即提取时间的影响最大,其次是料液比,提取剂中乙醇的含量,提取温度的影响最小。
|
|
依上述优化条件对湖北郧西产杜仲叶中的绿原酸进行提取,绿原酸的提取率可以达到4%以上,与刘军海等(2004;2006)报道的研究结果比较,其提取率有所提高,原因可能为所采用的检测方法不同及所采用杜仲叶原料不同。
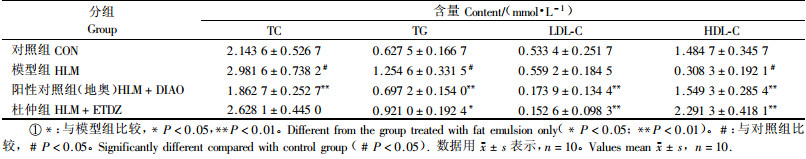
2.2 以绿原酸为主成分的杜仲叶提取物对小鼠高血脂症的抑制作用药物对动物血脂的影响体现在血清中TC、TG、LDL-C及HDL-C含量的变化。表 3列出了不同给药组小鼠体内上述指标水平的变化情况及方差分析结果。
|
|
采用脂肪乳剂灌胃的方法对小鼠进行高脂血症造模是一种简便可行的方法。已有研究(张家雄等,2004;2006;熊静悦等,2006)表明脂肪乳剂中猪油和胆固醇的含量在造模过程中起到至关重要的作用,笔者在本研究中探索造模方法时亦尝试了不同猪油、胆固醇含量的脂肪乳剂对模型的影响,结果与先前学者的研究一致,猪油和胆固醇的含量越高,造模越容易。表 3数据表明采用该方法建立小鼠高脂血症模型是成功的,TC和TG都比对照组有了显著的增加,HDL-C也明显降低。
张瑛朝(2000)曾报道,杜仲叶和山楂、葛根的水提物组成的一种调节血脂的制剂可使血清中TC、TG、LDL-C明显降低,使HDL-C有一定程度的升高。本文的研究结果亦显示了杜仲叶乙醇提取物具有降低血脂含量,调节机体血脂代谢的作用。
从表 3数据可以看出:与模型组小鼠相比,杜仲叶提取物组小鼠血清TC含量降低,TG(P<0.05)和LDL-C(P<0.01)含量显著降低,同时血清HDL-C(P<0.01)含量显著增高。表明杜仲叶乙醇提取物可以提高体内HDL-C的含量,提高体内胆固醇、甘油三酯的转运速度,加快代谢,从而降低血清TC、TG及LDL-C含量。
阳性对照组地奥心血康具有明显降低TC(P<0.01)、TG(P<0.01)及LDL-C(P<0.01)含量以及升高HDL-C(P<0.01)含量的作用,其主要成分为甾体皂苷,国内外的研究早已证实该物质具有良好的调节血脂作用。
杜仲叶醇提物成分复杂,降血脂的有效成分和作用机制尚需进一步的研究,目前国外学者研究表明口服绿原酸有降低大鼠内脏脂肪堆积和体质量的趋势(Shimoda et al., 2006);绿原酸静脉给药能显著降低大鼠血浆中胆固醇和甘油三脂的含量,以及肝脏中的甘油三脂水平(Rodriguez et al., 2002)。因此纯化杜仲叶中的绿原酸及其他主要活性成分,探索其调脂作用具有现实意义。
刘军海, 裘爱泳. 2004. 杜仲叶绿原酸提取纯化工艺的研究. 中药材, 27(12): 942-946. DOI:10.3321/j.issn:1001-4454.2004.12.024 |
刘军海, 裘爱泳. 2006. 杜仲叶中绿原酸提取工艺研究. 食品科学, 27(12): 450-454. DOI:10.3321/j.issn:1002-6630.2006.12.110 |
熊静悦, 周桢昊, 赵璐, 等. 2006. 脂肪乳剂建立高脂血症模型小鼠的比较研究. 中医药学刊, 24(8): 1507-1508. DOI:10.3969/j.issn.1673-7717.2006.08.050 |
叶文峰. 2004. 杜仲叶中化学成分、药理活性及应用研究进展. 林产化工通讯, 38(5): 40-44. DOI:10.3969/j.issn.1673-5854.2004.05.010 |
张加雄, 万丽, 陈芳, 等. 2004. 用脂肪乳剂建立小鼠高脂血症模型. 成都中医药大学学报, 27(3): 36-37. DOI:10.3969/j.issn.1004-0668.2004.03.017 |
张加雄, 范开华, 万丽, 等. 2006. 小鼠高脂血症模型建立方法的改进. 中国药师, 9(8): 723-724. DOI:10.3969/j.issn.1008-049X.2006.08.017 |
张瑛朝. 2000. 复方杜仲叶提取液对大鼠血脂的调节作用实验研究. 中成药, 22(4): 291-292. DOI:10.3969/j.issn.1001-1528.2000.04.020 |
张瑛朝, 张延敏, 郭代立, 等. 2001. 复方杜仲叶合剂对人体降压作用的实验研究. 中成药, 23(6): 418-421. DOI:10.3969/j.issn.1001-1528.2001.06.011 |
中国药典委员会.2005.中国药典: 2005版(一部), 114-115.
|
周军, 黄琼, 李志光, 等. 2008. 超声波法提取金银花中的绿原酸. 化学与生物工程, 25(1): 31-33. DOI:10.3969/j.issn.1672-5425.2008.01.010 |
Rodriguez D S, Hadley M. 2002. Chlorogenic acid modifies plasma and liver concentrations of cholesterol, triacylglycerol, and minerals in (fa/fa) Zucker rats. J Nutr Biochem, 13: 717-726. DOI:10.1016/S0955-2863(02)00231-0 |
Shimoda H, Seki E, Aitani M. 2006. Inhibitory effect of green coffee bean extract on fat accumulation and body weight gain in mice. BMC Complement Altern Med, 17(6): 9. |
 2009, Vol. 45
2009, Vol. 45