文章信息
- 王光军, 田大伦, 闫文德, 朱凡, 李树战.
- Wang Guangjun, Tian Dalun, Yan Wende, Zhu Fan, Li Shuzhan
- 马尾松林土壤呼吸对去除和添加凋落物处理的响应
- Response of Soil Respirations to Litterfall Exclusion and Addition in Pinus massoniana Plantation in Hunan, China
- 林业科学, 2009, 45(1): 27-30.
- Scientia Silvae Sinicae, 2009, 45(1): 27-30.
-
文章历史
- 收稿日期:2008-06-30
-
作者相关文章
森林凋落物是森林生态系统的重要组成成分,凋落物的分解是森林生态系统物质循环和能量流动的一个重要方面(Martin,1963;Maguire,1994),在很大程度上影响着土壤有机质的形成和植物养分的供应,以及土壤CO2通量(Prescott, 2005)。土壤呼吸作用是全球碳循环的主要通量过程(Raich et al., 1992),Raich等(1992)估算的全球土壤呼吸释放CO2通量约为68 Pg C·a-1,其中50 Pg C·a-1来自于凋落物和土壤有机质分解。添加和去除凋落物能显著影响凋落物分解速率及土壤呼吸速率(Bowden et al., 1993; Boone et al., 1998; Jonasson et al., 2004; Maier et al., 2000; Sayer et al., 2006;Sulzman et al., 2005; Nadelhoffer et al., 2004)。DIRT(detritus input and removal treatments), 是一种测定凋落物分解对土壤呼吸贡献的方法,是一种控制土壤碳输入来源和速率的长期野外试验(Holub et al., 2005),这种试验最初由Wisconsin大学于1956年在草地和森林生态系统中建立,并一直运行到现在(Nadelhoffer et al., 2004)。在意大利地中海橡树(Quercus palustris)林生态系统中,移除凋落物的试验结果表明,地上凋落物对土壤呼吸的贡献量为21.9%(Rey et al., 2002),Wan等(2003)在美国Oklahoma高草草原中移走凋落物,土壤呼吸降低了14%。在国内,关于凋落物添加和去除试验的报道并不多,仅Peng等(2003)研究了去除凋落物对华南热带桉树(Eucalypus)林中植物物种多样性的影响,以及Zhang等(2006)进行了马尾松(Pinus massoniana)林去除凋落物的碳氮动态模拟。
马尾松是中国南方主要造林树种之一,在我国森林资源中占有十分重要的地位。研究添加和去除凋落物后马尾松林土壤呼吸的季节动态变化,有助于掌握马尾松林土壤碳循环过程及环境变化对其产生的影响。
1 试验地概况试验地位于湖南省长沙市南郊的天际岭国家森林公园(113°01′—02′ E,28°06′—07′ N),核心区面积约4 356 hm2,海拔46~114 m,坡度5°~25°。年平均气温17.2 ℃,1月最冷,平均4.7 ℃,极端最低气温-11.3 ℃;7月最热,平均气温29.4 ℃,极端最高气温40.6 ℃;全年无霜期270~300 d,年均日照时数1 677.1 h;年均降水量1 422 mm。属典型的亚热带湿润季风气候。其地层主要是第四纪更新世的冲积性网纹红土和砂砾,属典型红壤丘陵区,园内小生境众多,植物达2 200余种,以人工林为主。
2006年12月,选择林龄30 a左右的马尾松人工林作为研究对象,林分密度平均为690株·hm-2,植株平均胸径18.65 cm,树高13.6 m,林分郁闭度0.7。林分以马尾松为优势种,其他树种有樟树(Cinnamomum camphora)、山矾(Symplocos caudata)、青冈(Cyclobalanopsis glauca)及大青(Clerodendron cyrtophyllum)。草本植物有肾蕨(Nephrolepis auriculata)、淡竹叶(Lophantherum gracile)、酢浆草(Oxalis comiculata)、鸡矢藤(Paederia scandens)、五节芒(Miscanthus floridulus)和商陆(Phytolacca acinosa)等。
马尾松群落的凋落物年归还量为1 157.5 g·m-2a-1,凋落物层厚1.2~2.5 cm,针叶占总凋落物量的54.44%。
2 研究方法 2.1 样地设置2006年12月在天际岭国家森林公园选择马尾松林进行调查,设立4块半径15 m的圆形固定样地,样地间相隔100 m以上。在每个固定样地内均匀设置3个凋落物正常进入的PVC土壤环,为对照,同时在旁边设置3个去除凋落物和3个添加凋落物的PVC土壤环处理,共36个PVC土壤环测点。PVC土壤环内径10.5 cm,高4.5 cm,平放压入土中2 cm左右。测量在安放土壤环24 h之后开始,并保持土壤环在整个测定期间位置不变(Wang et al., 2002)。对于去除凋落物处理,首先将地上凋落物(腐殖质层以上)移走,放置PVC土壤环后,在土壤环上方安置1.5 m×1.5 m有1 mm大小网眼的凋落物收集网,网离地面0.5 m,收集凋落物并防止凋落物进入;对于添加凋落物处理,首先是收集腐殖质层以上凋落物,平均撒在以土壤环为中心的1.5 m×1.5 m的范围内,每个月将凋落物收集网收集的等面积凋落物均匀撒在添加凋落物处理范围内。
2.2 土壤呼吸测定将LI-6400-09(土壤呼吸室)连接到LI-6400便携式CO2/H2O分析系统(LI-COR Inc., Lincoln, NE, USA)测定土壤呼吸速率。测量时间为2007年1—12月。每隔15 d,在上午9:00—11:00测定1次,全年共测定24次。
2.3 凋落物的测定在样地内放置3个1.5 m×1.5 m的凋落物收集网。凋落物每月收集1次,在80 ℃下烘干至恒质量后称重,确定凋落物量。
土壤有机碳用重铬酸钾氧化-外加热法测定;全氮用半微量凯氏法测定;pH值采用电位法测定;土壤密度用环刀法测定(中国科学院南京土壤研究所,1978)。
2.4 数据统计分析所有的统计分析都在SPSS13.0软件中进行,用Repeated measured ANOVA检验土壤呼吸季节变化的显著性,用SigmaPlot 9.0软件作图。月土壤呼吸速率是每月2次测量值的平均值,年土壤呼吸速率是全年24次测量的平均值。Q10值通过下式确定(Xu et al., 2001):Q10=e10b,b为温度反应系数。
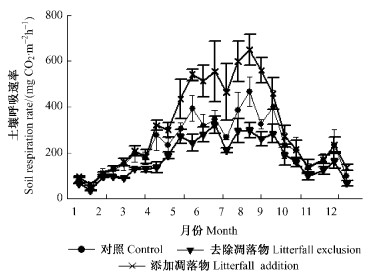
3 结果与分析 3.1 去除和添加凋落物对土壤呼吸速率的影响去除、添加凋落物处理和对照的土壤呼吸速率均呈现显著的季节变化(P < 0.001)(图 1),3者曲线格局相似,土壤呼吸速率分别为34.45~321.16,61.26~649.44和38.6~466.49 mgCO2·m-2h-1。土壤呼吸速率最小值均出现在1月土壤温度最低时,去除凋落物处理的最高值均出现在7月下旬,而添加凋落物处理和对照均出现在8月下旬土壤温度最高时。3者年均土壤呼吸速率分别为175.18,310.36和234.97 mgCO2·m-2h-1。可见去除凋落物会降低土壤呼吸速率,反之会增加土壤呼吸速率。
|
图 1 土壤呼吸速率季节动态 Figure 1 Seasonal dynamics of soil respiration rate |
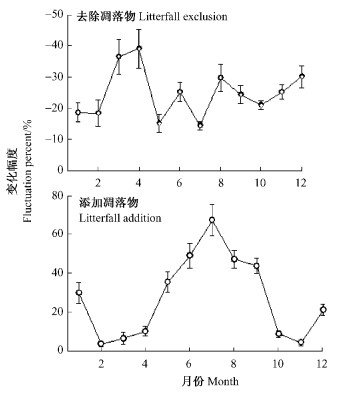
去除、添加凋落物处理的土壤呼吸速率与对照之间差异显著(P < 0.01)。用每月2次测得数值的平均值作为月平均值,计算出去除凋落物使土壤呼吸速率年均降低24.96%,影响最小月份是7月,降低了14.48%±1.44%,影响最大月份是4月,降低了39.25%±6.23%;添加凋落物使土壤呼吸速率年均增加27.36%,影响最小月份是2月,增加了3.78%±1.30%,影响最大月份是7月,增加了67.26±7.91%(图 2)。
|
图 2 土壤呼吸速率月变幅 Figure 2 Month fluctuation percent of soil respiration rates |
马尾松去除和添加凋落物的土壤呼吸Q10值分别为2.16和2.56,比对照点Q10值2.13稍高。我们按四季分别计算Q10值:春(3—5月)、夏(6—8月)、秋(9—11月)、冬(12月及次年1、2月)季去除凋落物的土壤呼吸Q10值分别为2.20,1.10,2.70和2.53;添加凋落物的Q10值分别为2.16,1.07,4.07和2.54;对照的Q10值分别为1.60,0.70,2.54和2.46;Q10值均表现出夏季最小,秋、冬季高的特点。
4 结论与讨论植物凋落物分解是土壤呼吸的一个重要组成部分(Bowden et al., 1993; Sulzman et al., 2005)。凋落物的去除或添加会改变有机碳供应,从而显著降低或增加土壤呼吸,其中添加凋落物引起的土壤呼吸的增加程度远远大于去除凋落物引起的降低程度(Nadelhoffer et al., 2004; Sulzman et al., 2005)。而Boone等(1998)的哈佛森林控制凋落物试验表明:完全移走地上凋落物时土壤呼吸降低25%;添加凋落物则使土壤呼吸增加近20%。本试验表明:去除凋落物使土壤呼吸速率年均降低24.96%,添加凋落物使土壤呼吸速率年均增加27.36%,添加凋落物土壤呼吸的增加幅度比去除凋落物土壤呼吸的降低幅度大,这与Nadelhoffer等(2004)和Sulzman等(2005)的研究结果一致。这种情况可能是去除或添加凋落物引起了有机质分解的增加(正激发效应)或减少(负激发效应)。
去除和添加凋落物直接改变凋落物分解、向土壤碳输入的过程,而且还影响植物萌发和生长(Nzila et al., 2002; Sybille et al., 2005; Matsushima et al., 2006)从而间接地影响对土壤的碳输入。在刚果森林,去除凋落物2年后树木生长明显受到抑制,添加凋落物则刺激树木生长(Nzila et al., 2002)。另外,凋落物输入途径和量的变化可以改变凋落物层和土壤微生物群落:添加凋落物增加了凋落物层的真菌和细菌的总生物量(Nadelhoffer et al., 2004),并导致土壤细菌群落结构的变化(Nadelhoffer et al., 2004;Brant et al., 2006)。
温度敏感性指数(Q10值)多为1.8~4.1(Ohashi et al., 1999;Xu et al, 2001;Erland et al., 2003)。本试验中,马尾松林去除和添加凋落物的Q10值分别为2.16和2.56,比对照点Q10值2.13稍高,表明去除和添加凋落物使土壤呼吸的温度敏感性增强。Boone等(1998)的结果是去除和加倍凋落物的Q10值为3.1和3.4,比对照点的Q10值3.5小。这可能是由估算Q10值试验的地理位置和生态系统类型的差异所造成的。本试验还表明,去除和添加凋落物的土壤呼吸的Q10值与对照一样,存在秋、冬季高,春、夏季低的特征,这与土壤呼吸受光、温度和湿度的复合影响有关(Davidson et al., 2005;Atkin et al., 2000)。
由于本研究只有1 a的试验数据,得出的结论具有一定的局限性,今后仍然需要对马尾松林及其他森林生态系统进行长期定位监测,为准确预测未来森林生态系统土壤碳库的动态变化提供参考。
中国科学院南京土壤研究所. 1978. 土壤理化分析. 上海: 上海科学技术出版社.
|
Atkin O K, Edwards EJ, Loveys B R. 2000. Response of root respiration to changes in temperature and its relevance to global warming. New Phytologist, 147: 141-154. DOI:10.1046/j.1469-8137.2000.00683.x |
Brant J B, Sulzman E W, Myrold D D. 2006. Microbial community utilization of added carbon substrates in response to long-term carbon input manipulation. Soil Biology and Biochemistry, 38: 2219-2232. DOI:10.1016/j.soilbio.2006.01.022 |
Bowden R D, Nadelhoffer K J, Boone R D, et al. 1993. Contributions of aboveground litter, below ground litter and root respiration to total soil respiration in a temperate hardwood forest. Canadian Journal of Forest Research, 23: 1402-1407. DOI:10.1139/x93-177 |
Boone R D, Nadelhoffer K J, Canary J D, et al. 1998. Roots exert a strong influence on the temperature sensitivity of soil respiration. Nature, 396: 570-572. DOI:10.1038/25119 |
Davidson E A, Richardson A D, Savage K E, et al. 2006. A distinct seasonal pattern of the ratio of soil respiration to total ecosystem respiration in a spruve-dominated forest. Global Change Biology, 12: 230-239. DOI:10.1111/gcb.2006.12.issue-2 |
Erland B, Hakan W. 2003. Soil and rhizosphere microorganisms have the same Q10 for respiration in a model system. Global Change Biology, 9: 1788-1791. DOI:10.1046/j.1365-2486.2003.00692.x |
Holub S M, Lajtha K, Spears J D H, et al. 2005. Organic matter manipulations have little effect on gross and net nitrogen transformations in two temperate forest mineral soils in the USA and central Europe. Forest Ecology and Management, 214: 320-330. DOI:10.1016/j.foreco.2005.04.016 |
Jonasson S, Castro J, Michelsen A. 2004. Litter, warming and plant affect respiration and allocation of soil microbial and plant C, N and P in arctic mesocosms. Soil Biology and Biochemistry, 36: 1129-1139. DOI:10.1016/j.soilbio.2004.02.023 |
Maguire D A. 1994. Branch mortality and potential litter fall from Douglas-fir trees in stands of varying density. Forest Ecology and Management, 70: 41-53. DOI:10.1016/0378-1127(94)90073-6 |
Maier C A, Kress L W. 2000. Soil CO2 evolution and root respiration in 11 year-old loblolly pine(Pinus taeda)plantation as affected by moisture and nutrient availability. Canadian Journal of Forest Research, 30: 347-359. DOI:10.1139/x99-218 |
Martin W. 1963. Microbial populations of leaf litter in relation to environ- mental conditions and decomposition. Ecology, 44: 370-377. DOI:10.2307/1932184 |
Nadelhoffer K J, Boone R D, Bowden R D, et al. 2004. The DIRT experiment: litter and root influences on forest soil organicmatter stocks and function // Foster D, Aber J. Forests in time: the environmental consequences of 1000 years of change in New England. New Haven: Yale University Press, 300-315.
|
Nzila D J, Bouillet J P, Laclau J P, et al. 2002. The effects of slash management on nutrient cycling and tree growth in Eucalyptus plantations in the Congo. Forest Ecology and Management, 171: 209-221. DOI:10.1016/S0378-1127(02)00474-7 |
Ohashi M, Gyokusen K, Saito A. 1999. Measurement of carbon dioxide evolution from a Japanese cedar(Cryptomeria japonica)forest floor using an open-flow chamber method. Forest Ecology and Management, 123: 105-114. DOI:10.1016/S0378-1127(99)00020-1 |
Peng S L, Ren H, Wu J G, et al. 2003. Effects of litters removal on plant species diversity: a case study in tropical Eucalypus forest ecosystems in South China. Journal of Environment Sciences-China, 15: 367-371. |
Raich J W, Schlesinger W H. 1992. The global carbon dioxide efflux in soil respiration and its relationship to vegetation and climate. Tellus, 44(B): 81-99. |
Rey A, Pegoraro E, Tedeschi V, et al. 2002. Annual variation in soil respiration and its components in a coppice oak forest in Central Italy. Global Change Biology, 8: 851-866. DOI:10.1046/j.1365-2486.2002.00521.x |
Prescott C E. 2005. Do rates of litter decomposition tell us anything we really need to know. Forest Ecology and Management, 220: 66-74. DOI:10.1016/j.foreco.2005.08.005 |
Sayer E J, Tanner V J, Lacey A L. 2006. Effects of litter manipulation on early stage decomposition and mesoarthropod abundance in a tropical moist forest. Forest Ecology and Management, 229: 285-293. DOI:10.1016/j.foreco.2006.04.007 |
Sulzman E W, Brant J B, Bowden R D, et al. 2005. Contribution of aboveground litter, belowground litter, and rhizosphere respiration to total soil CO2 efflux in an old growth coniferous forest. Biogeochemistry, 73: 231-256. DOI:10.1007/s10533-004-7314-6 |
Sybille H, Richard K. 2005. Aspen plant community response to organic matter removal and soil compaction. Canadian Journal of Forest Research, 35: 2030-2044. DOI:10.1139/x05-133 |
Xu M, Qi Y. 2001. Spatial and seasonal variations of Q10 determined by soil respiration measurements at a Sierra Nevadan forest. Global Bio-geochemical Cycles, 15: 687-696. DOI:10.1029/2000GB001365 |
Wan S Q, Luo Y Q. 2003. Substrate regulation of soil respiration in a tallgrass prairie, Resuts of a clipping and shading experiment. Global biogeochemical cycles, 17(1054). DOI:10.1029/2002GB001971 |
Wang C K, Bond_Lamberty B, Gower S T. 2002. Soil surface CO2 flux in a boreal black spruce fire chronosequence. Journal of Geophysical Research Atmospheres, 108: 8224. DOI:10.1029/2001JD000861 |
Zhang G L, Jiang H, Niu G D, et al. 2006. Simulating the dynamics of carbon and nitrogen in litter-removed pine forest. Ecological Modeling, 195: 363-376. DOI:10.1016/j.ecolmodel.2005.11.041 |
 2009, Vol. 45
2009, Vol. 45
