文章信息
- 王艳娜, 王贵禧, 梁丽松, 赵晓芳.
- Wang Yanna, Wang Guixi, Liang Lisong, Zhao Xiaofang
- 低温及轮纹病菌胁迫对鸭梨果肉ATP含量及H+-ATPase、Ca2+-ATPase活性的影响
- Effect of Low Temperature and Pathogen Stress during Storage Periods on Pear Fruit Pulp ATP Contents, H+-ATPase and Ca2+-ATPase Activity
- 林业科学, 2008, 44(12): 72-76.
- Scientia Silvae Sinicae, 2008, 44(12): 72-76.
-
文章历史
- 收稿日期:2007-03-31
-
作者相关文章
2. 中国林学会 北京 100091
2. Chinese Society of Forestry Beijing 100091
ATP是生物体的能量来源,它作为植物维持生命活动最重要的能量库,其含量在一定程度上能够反映植物本身的生理状态。ATP酶存在于组织细胞及细胞器的膜上,在物质运送、能量转化以及信息传递方面具有重要作用,H+-ATPase具有利用水解ATP产生的能量将细胞质膜内侧的H+泵到质膜外侧的特性,维持胞内H+浓度,调节pH值;Ca2+-ATPase水解ATP为Ca2+的主动运转提供能源,将Ca2+泵出胞液,在维持细胞钙稳定和钙信使系统中起重要作用(Bush, 1993;1995;Braam, et al., 1996)。低温、高温、盐胁迫等逆境条件可以导致植物ATP含量、质膜H+-ATPase活性、Ca2+-ATPase活性的变化(张宗申等,2001;周晓阳,2007;陈海燕等,2007)。果实采后即进入衰老阶段,为了延缓果实采后的衰老代谢,常常采取低温措施控制果实的生命活动;此外,果实在贮藏过程中还会因为病原菌的侵染而腐烂。对于果实在遭受低温和病害逆境胁迫下的能量和H+-ATPase、Ca2+-ATPase活性的变化以及与正常衰老过程中的差异还未见报道。本试验以鸭梨为试验材料,通过测定低温及病原菌胁迫条件下果肉组织的主要能量相关指标的变化,研究果实低温贮藏过程中和发病过程中能量变化规律,以探讨胁迫条件下能量和ATP酶活性的反应机理。
1 材料与方法 1.1 试验材料鸭梨(Pyrus bretschneideri cv.‘Yali')果实取自河北省赵县无公害梨果研究所果园,盛花期4月12日,套袋期5月28日,采收期9月26日。梨果采收后当天运至中国林业科学研究院林业研究所采后实验室,一部分入冷库低温贮藏,入库温度10 ℃,梯度降温,30 d降至0 ℃恒温保存;另一部分鸭梨在室温(20~25 ℃)放置作为对照。
病原菌为轮纹病菌梨生囊孢壳(Physalospora piricola),采自当地典型轮纹病病果,进行分离纯化(方中达,1999),经国家林业局林业菌种保藏中心鉴定。
1.2 试验方法 1.2.1 样品制备贮藏鸭梨样品的取样:分别在常温和低温贮藏0,10,20,30,40,50 d取样,液氮冷冻后置-80 ℃冰箱备用。用于ATP含量、H+-ATP活性和Ca2+-ATP活性的测定。
病原菌接种与取样:选择大小一致、健康的梨果实,经75%酒精表面消毒。用梨轮纹病菌孢子悬液(含量为1×105个·mL-1)针刺接种于果实,以涂抹无菌水的鸭梨为对照,用蘸有无菌水棉花团保湿,27 ℃贮藏。每个果实接种20点,重复接种6个果实。接种病原菌梨果和对照梨果分别在0,12,24,36,48,60 h测定ATP含量、H+-ATPase活性和Ca2+-ATPase活性。
1.2.2 ATP含量测定荧光素酶法。取5 g果肉加50 mL蒸馏水在沸水浴中煮沸15 min冷却至室温后定容至50 mL,12 000×g离心20 min,取上清液,置25 ℃恒温水浴中保温。取10 μL提取液加入滨松光子BHP9504型微孔板发光分析仪样品槽中,迅速加入100 μL全效裂解发光体系,记下峰值从标准曲线上查得相应的ATP含量。AFA和测定均由中科靓马科技公司提供。
1.2.3 果肉质膜的提取方法参照Lassron等(1990)和文彬等(2004)方法,略有改进。称取5 g果肉,加提取缓冲液[EGTA 5 mmol·L-1,PMSF 1 mmol·L-1,Tris-Mes25 mmol·L-1,蔗糖0.25 mol·L-1,MgSO4 1 mmol·L-1,0.2%(W/V) BSA,0.5%(W/V) PVP,10%(W/V)甘油,ATP 2 mmol·L-1,巯基乙醇15 mmol·L-1,DTT 1 mmol·L-1]。冰浴研磨,4层纱布过滤,滤液在4 ℃下、12 000×g离心15 min。取上清液,4 ℃、80 000×g离心30 min;倒去上清液,取沉淀,加入1 mL悬浮缓冲液[含Tris-Mes 25 mmol·L-1,蔗糖0.25 mol·L-1,0.2% (W/V) BSA,DTT 1 mmol·L-1,10%(W/V)甘露醇],溶解沉淀物。将悬浮液置于两相系统[20%(W/W) Dextran T500,40%(W/W)PEP3350,KCl 120 mmol·L-1,DTT 1 mmol·L-1,蔗糖0.25 mol·L-1,pH值7.8磷酸缓冲液。8 g两相系统的配比:1.37 g蔗糖,0.002 4 g DTT,1.8 mLH2O,0.4 mL KCl,1.3 g PEG3350,2.6 g DextranT500, 0.4 mL磷酸缓冲液]中上下摇匀40次,4 ℃、4 200×g离心5 min,取上相。下相继续加入两相系统,分离3次,合并上相,稀释3~5倍,4 ℃、80 000×g离心30 min。加入保存缓冲液1~2 mL悬浮沉淀、分装,迅速放入液氮冷却,然后置于-80 ℃冰箱中保存。
1.2.4 质膜H+-ATP酶水解活力的测定采用Ames钼蓝法(Ames, 1966),略有改进。在酶反应缓冲体系[Tris-Mes 30 mmol·L-1 pH值7.0,KCl 50 mmol·L-1,MgSO4 3 mmol·L-1,NaNO3 50 mmol·L-1,Na2MoO4 0.1 mmol·L-1,NaN3 10 mmol·L-1,ATP 3 mmol·L-1]中,加入鸭梨果肉质膜蛋白20~60 μg,终体积为1 mL,从加入ATP开始计时,37 ℃恒温下反应30 min,然后加入10%SDS 200 μL终止反应,加入1 mL显色液液[1 g VtC,0.252 g (NH4)2MoO4,1.716 mL H2SO4,蒸馏水定容至70 mL],在820 nm下测OD值,计算酶活力。活力单位为μmol·mg-1·min-1。
1.2.5 质膜Ca2+-ATPase活性测定反应体系含蔗糖250 mmol·L-1,Hepe-Tris(pH值7.5)30 mmol·L-1,NaN3 1 mmol·L-1,0.1 mmol·L-1钼酸氨,EDTA-Na2 0.1 mmol·L-1,0.02%(V/V)的TritonX-100,加入鸭梨果肉质膜蛋白20~60 μg,加与不加Ca(NO3)2 3 mmol·L-1引起的酶活性之差为Ca2+-ATPase活性,反应启动用50 μL 30 mmol·L-1的ATP-tris pH值7.5,其后步骤同H+-ATP酶活性测定。
1.2.6 数据处理数据采用SPSS(11.0)软件进行分析处理,采用“paired-sample T Test"进行差异显著性检验,P < 0.05为差异显著,P < 0.01为差异极显著。
2 结果与分析 2.1 低温贮藏对ATP含量、H+-ATPase活性、Ca2+-ATPase活性的影响常温和低温贮藏鸭梨果实ATP含量均呈下降趋势(图 1)。与常温贮藏相比,鸭梨果实在降温20 d内果实中的ATP含量快速下降至2.76×10-9 mol·g-1,显著低于对照果实(P < 0.05)。贮藏30 d后库温稳定在0 ℃,30~60 d果肉ATP依然下降明显,至60 d其含量比采收时下降53.97%,且均显著低于常温果实中ATP含量(P < 0.05)。这可能是由于冷藏果实受低温胁迫影响,果实的呼吸强度降低,ATP的生成速率也受到抑制(潘瑞炽,2001)。但随着贮藏期的延迟,果实生理代谢机制逐渐衰老,常温和低温贮藏的果实的ATP含量的积累也呈下降趋势。

|
图 1 低温贮藏对鸭梨果肉ATP含量的影响 Figure 1 The effects of cold storage on ATP content in `Ya' pear pulp |
常温和低温贮藏H+-ATPase活性随贮藏时间延长而逐渐上升(图 2)。低温贮藏0、10、20、30 d的果实中H+-ATPase活性差异显著(P < 0.05),且匀速上升。30 d时库温降至0 ℃时H+-ATPase活性比0 d活性增强48.38%,当温度稳定后H+-ATPase活性仍然增强,但是差异不显著。与低温贮藏相比,常温贮藏至30 d时果实中H+-ATPase活性升高幅度较小,整个贮藏期酶活性显著低于常温贮藏果实(P < 0.05)。说明低温胁迫增强了果实的H+-ATPase活性,活性增强幅度与温度相关。

|
图 2 不同贮藏条件H+-ATPase活性的变化 Figure 2 The changes of activity of H+-ATPase in different storage condition |
鸭梨果实在常温和低温贮藏期间Ca2+-ATPase活性呈现先升高后下降的趋势(图 3),冷藏果实在降温10 d时的Ca2+-ATPase活性略有下降而后逐渐增高,至30 d(缓慢降温到0 ℃时),其活性达到最高值1.27 μmol·mg-1min-1,而后急剧下降。常温贮藏的鸭梨也呈现前在10 d略有下降,而后升高,贮藏20 d时活性达峰值0.83 μmol·mg-1min-1,随后逐渐下降。质膜是Ca2+-ATPase的主要存在场所(Kasamo,1998),与常温贮藏相比,低温贮藏能显著提高质膜Ca2+-ATPase活性的峰值,推迟其高峰时间,且峰值显著高于低常温贮藏的峰值。说明低温有利于质膜Ca2+-ATPase活性的提高,细胞控钙能力加强,延缓果实的衰老。

|
图 3 不同贮藏条件Ca2+-ATPase活性的变化 Figure 3 The changes of activity of Ca2+-ATPase in different storage condition |
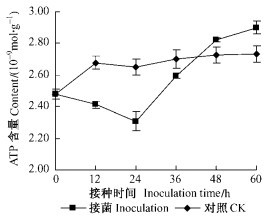
图 4为鸭梨果实在接种病原菌60 h内的ATP含量变化。果实在接种24 h内果肉中的ATP含量快速下降至最低值1.91×10-9mol·g-1,显著低于对照(P<0.05),而后又逐渐上升,至48 h后ATP含量显著高于对照果实的ATP含量(P < 0.05)。对照果实仅在处理24 h时ATP含量小幅升高,这可能是由于果实受刺伤处理造成呼吸速率加强,果肉中ATP含量积累增加,随后含量保持稳定,差异不显著。接种病原菌果实在36 h前ATP含量一直低于对照果肉中ATP含量,至48 h ATP含量高于对照果肉中含量,这说明在病原菌侵入果肉前期,虽然可溶性糖含量降低转变为果肉中ATP,由于果肉抵御病原菌侵然一系列抗性活动大量消耗ATP,仍表现为耗能大于贮能;随着病原菌的侵入抵御反应减弱能耗降低而且病原菌生理活动也产生了少量ATP。
|
图 4 鸭梨接种病原菌后ATP含量变化 Figure 4 The changes of ATP content of `Ya' pear fruit after inoculation with B.berengriana |
图 5为鸭梨果实接种病原菌后60 h内质膜H+-ATPase活性变化。鸭梨果实对照处理12 h时的H+-ATPase活性显著增加,而后缓慢增加但是测量值之间差异不显著(P>0.05),果肉受到刺伤后也会发生短时的应激反应。鸭梨果实接种病原菌后,果肉中的H+-ATPase活性迅速提高,在36 h时出现活性最高值0.396 μmol·mg-1min-1,随后缓慢下降但活性仍显著高于对照处理(P<0.05)。

|
图 5 鸭梨接种病原菌后H+-ATPase活性变化 Figure 5 The changes of H+-ATPase activity of `Ya' pear fruit after inoculation with B.berengriana |
图 6为鸭梨果实接种病原菌后果肉内Ca2+-ATPase活性变化。鸭梨果实在接菌后12 h果肉中Ca2+-ATPase活性升高,与对照相比差异不显著(P>0.05)。接菌24 h后果肉中的Ca2+-ATPase活性快速下降至60 h的0.201 μmol·mg-1min-1,对照活性变化不明显。说明果实在受到胁迫时细胞调控Ca2+的能力在逐渐增强,当病害胁迫稳定时,Ca2+-ATPase活性下降,使得细胞调控Ca2+能力降低,Ca2+含量过高或维持时间过长,会使细胞受到伤害,而细胞伤害又加剧了果实衰老。

|
图 6 鸭梨接种病原菌后Ca2+-ATPase活性变化 Figure 6 The changes of Ca2+-ATPase activity of `Ya' pear fruit after inoculation with B.berengriana |
ATP是光合磷酸化和氧化磷酸化的产物, 是活细胞中最活跃的能量通货, 也是活细胞进行新陈代谢最重要的生理指标。在胁迫下对能量进行分析,有3个方面:一是呼吸增强,碳同化减少;二是渗透调节物质的合成和积累是一个耗能的过程;三是ATP作为植物维持生命活动最重要的能量,其含量在一定程度上能够反映植物本身的能量状况(李美茹等,1999)。本试验中无论是低温还是在病原菌侵染的逆境胁迫条件下,ATP含量均显著降低。果实采收后由于果实停止光合作用,碳同化减少,ATP生成量显著降低,而梨果采后呼吸增强,且在低温下呼吸强度更高,维持渗透势耗能,即维持细胞内低渗透势是一个耗能的过程,因此ATP大量消耗,虽然可溶性糖及有机酸等物质代谢产生能量,但仍表现为耗能大于贮能。低能量状态下果实的抗性降低,潜伏侵染的病原菌易发病,在采后40~60 d为果实发病高峰期(王艳娜等,2008;赵晓芳等,2008),即果肉ATP降低显著时病原菌易发病。接种病原菌后ATP含量显著低于对照,可能是由于果肉感染病原菌后呼吸强度增强,果实中H+-ATPase、Ca2+-ATPase活性变化,细胞抵御病原菌将Ca2+和H+等离子泵出细胞外维持低渗透势此过程为耗能过程。柠檬酸和苹果酸的跨膜运输需要ATP(潘瑞炽,2001),梨果实在受病原菌侵染后果肉中2种有机酸变化最为显著,因此该过程也大量消耗ATP。接种病原菌果肉细胞发生抵御反应如呼吸强度增强,维持细胞渗透势等生理反应,而这些互作过程大量消耗ATP,虽然可溶性糖被大量消耗而转化成ATP,但是由于此过程大量消耗能量与常温贮藏对照果肉相比ATP含量仍然较低,当病原菌侵入果肉中,果肉抵御病原菌生理活动减缓,而此时可溶性糖继续降低补给果肉中ATP,菌丝在果肉中的的生长繁殖,此时所测得的ATP含量不仅源自果肉有氧呼吸还源自菌丝无氧呼吸,因此腐烂果肉中ATP含量高于未接菌的对照果肉。
3.2 低温和病原菌胁迫对H+-ATPase活性的影响H+-ATPase活性增强有利于加强胞内H+外排的能力,以便在质膜H+-ATPase活性下降导致胞质H+增加的条件下,维持胞质pH值的稳定,保持细胞壁酸化(Ratajczak,2000)。在盐胁迫和水分胁迫等逆境下植物细胞H+-ATPase活性增强(邸娜,2007)。环境应力刺激可能提高线粒体跨膜电位,为ATP合成提供更多潜在能量,或者对内膜H+-ATPase合成酶有激活作用,从而使细胞内合成更多的ATP(潘瑞炽,2001)。本试验结果显示在低温和病原菌胁迫下H+-ATPase活性均会显著增高,低温和病害使得果实呼吸作用加强,在果实受病原菌侵染过程中,苹果酸和柠檬酸也增加说明合成酶活性增加,因此推测鸭梨果肉细胞在胁迫下激活H+-ATPase合成更多的ATP应对逆境,还可以通过调节细胞渗透压和pH值来抵御逆境条件。
3.3 低温和病原菌胁迫对Ca2+-ATPase活性的影响Ca2+-ATPase对维持细胞内Ca2+稳定、保持细胞内外Ca2+平衡及神经细胞的兴奋和传导起到非常重要的作用(崔洪宇等,2007)。一般认为,胞外在维持质膜功能的同时抑制乙烯生成,延缓衰老;过量Ca2+进入细胞质,促进乙烯的生成和衰老(苏梦云,2003)。定位于细胞膜上的Ca2+-ATPase对维持细胞内低钙水平起着重要的调控作用。研究发现在受病原菌胁迫下,Ca2+-ATPase先是缓慢升高,随着病原菌在果肉中大量繁殖,Ca2+-ATPase的活性迅速下降,而酶活性的下降,使得细胞调控Ca2+的能力下降,结果导致细胞内Ca2+积累,对胞内Ca2+含量过高或维持时间过长时,会对细胞产生毒害作用,达到一定程度后使得质膜过氧化加剧,又进一步促进了果实衰老的进程。鸭梨果实在贮藏的前40 d,Ca2+-ATPase总活性先上升而后下降,并且低温贮藏果实的Ca2+-ATPase活性峰值明显提高,这种酶活性的升高可能是钙信使系统对细胞质Ca2+含量升高的一种反馈调节机制,反映出此时细胞膜维持稳态Ca2+的能力较强。因此进一步促进果实衰老和果肉细胞的坏死。而在病原菌侵染过程中Ca2+-ATPase由于刺伤活性略有上升,而后一直下降,病原菌侵染主要破坏细胞膜导致细胞信使系统紊乱,胞内积累,同时伴随活性氧自由基的产生与积累,质膜过氧化作用增强,加剧了膜脂过氧化物对膜的伤害。
陈海燕, 崔香菊, 陈熙, 等. 2007. 盐胁迫及La3+对不同耐盐性水稻根中抗氧化酶及质膜H+-ATPase的影响. 作物学报, 33(7): 1086-1093. DOI:10.3321/j.issn:0496-3490.2007.07.007 |
崔洪宇, 孙玉河. 2007. 植物抗病的Ca2+信号研究进展. 天津农业科学, 13(1): 48-51. DOI:10.3969/j.issn.1006-6500.2007.01.016 |
邸娜. 2007. 拟南芥液泡H+-ATPase C亚基基因功能研究进展. 河套大学学报, 4(2): 157-162. |
方中达. 1999. 植病研究方法. 北京: 中国农业出版社.
|
李美茹, 杜延茹, 郭立波. 1999. 花生幼苗下胚轴质膜Ca2+-ATP酶及其对低温胁迫的反应. 武汉植物学研究, 17(2): 110-114. DOI:10.3969/j.issn.2095-0837.1999.02.004 |
潘瑞炽. 2001. 植物生理学. 北京: 高等教育出版社.
|
苏梦云. 2003. 杉木幼苗在渗透胁迫下脯氨酸积累及Ca的调节作用研究. 林业科学研究, 16(3): 335-338. DOI:10.3321/j.issn:1001-1498.2003.03.015 |
王艳娜, 王贵禧, 梁丽松, 等. 2008. 鸭梨果实轮纹病潜伏侵染时期及采后发病规律的研究. 林业科学研究, 21(5): 630-634. DOI:10.3321/j.issn:1001-1498.2008.05.007 |
文彬, 宾金华, 王小菁. 2004. 茉莉酸甲酯处理对绿豆下胚轴质膜H+-ATPase水解活力及磷酸化水平的影响. 植物生理与分子生物学学报, 30(6): 665-670. |
张宗申, 利容千, 王建波. 2001. Ca2+预处理对热胁迫下辣椒叶肉细胞中Ca2+-ATP酶活性的影响. 植物生理学报, 27(6): 451-454. DOI:10.3321/j.issn:1671-3877.2001.06.002 |
赵晓芳, 王贵禧, 王艳娜, 等. 2008. 鸭梨几丁质酶和β-1, 3-葡聚糖酶活性与其对轮纹病抗性的关系. 林业科学, 44(3): 162-165. DOI:10.3321/j.issn:1001-7488.2008.03.030 |
周晓阳.2007.胁迫条件下胡杨与意大利杨细胞内Ca2+水平和Ca2+-ATPase活性的变化.北京林业大学博士学位论文.
|
Ames B N. 1966. Assay of inorganic phosphate total phosphate and phosphatases. Methods Enzymol, 8: 115-118. DOI:10.1016/0076-6879(66)08014-5 |
Braam J, Sistrunk M L, Polisensky D H, et al. 1996. Life in a changing world: TCH gene regulation of expression and responses to environmental signals. Physiol Plant, 98: 909-916. DOI:10.1111/ppl.1996.98.issue-4 |
Bush D S. 1993. Regulation of cytosolic calcium in plants. Plant Physiol, 103: 7-13. DOI:10.1104/pp.103.1.7 |
Bush D S. 1995. Calcium regulation in plant cells and its role in signaling. Annu Rev Plant Physiol Plant Mol Biol, 46: 95-122. DOI:10.1146/annurev.pp.46.060195.000523 |
Kasamo K. 1988. Response of tonoplast and plasma membrane ATPase in chilling-setmitive and insensitive rice (Oryza sativa L.)culture cells to low temperature. Plant Cell Physiol, 29: 1085-1094. |
Lassron C, Morre D J. 1990. The plant plasma membrane. Berlin Heidelberg: Springer-Verlag.
|
Ratajczak R. 2000. Structure, function and regulation of the plant vacuolar H+-translocating ATPase. Biochim Biophys Acta, 1465: 17-36. DOI:10.1016/S0005-2736(00)00129-2 |
 2008, Vol. 44
2008, Vol. 44

