文章信息
- 王茜龄, 周金星, 余茂德, 徐立, 李镇刚.
- Wang Xiling, Zhou Jinxing, Yu Maode, Xu Li, Li Zhengang.
- 桑树组织培养诱导多倍体植株
- Induction of Polyploids on Mulberry in Tissue Culture
- 林业科学, 2008, 44(6): 164-167.
- Scientia Silvae Sinicae, 2008, 44(6): 164-167.
-
文章历史
- 收稿日期:2007-05-25
-
作者相关文章
2. 中国林业科学研究院林业研究所 国家林业局林木培育重点实验室 北京 100091
2. Key Laboratory of Tree Breeding and Cultivation of State Forestry Administration Research Institute of Forestry, CAF Beijing 100091
桑(Morus)为多年生落叶木本植物,是我国重要的经济树种,桑叶为家蚕饲料。人工选育的三倍体桑树品种,细胞体积较二倍体桑大1倍以上,不育,营养生长旺盛,产叶量与叶质明显高于目前生产上使用的二倍体桑树品种。作为叶用植物的桑树,选育和推广人工三倍体新桑品种已成为国内外桑树育种与栽培新的方向(南泽吉三郎,1984;林寿康,1989;柯益富,1997)。
在人工三倍体桑树新品种选育中,桑树二倍体材料多,容易获得优良的育种材料,而四倍体亲本材料非常缺乏,在自然界野生四倍体桑树极其稀少,并且经济性状低下,还不能选作三倍体育种亲本。因此,目前国内外桑树四倍体育种材料只能通过人工途径获得,在国内主要是在大田中采用物理辐射方法即60Co-γ射线等辐射,或者化学诱导方法即秋水仙碱处理二倍体桑的无性繁殖器官获得四倍体(杨今后,2004)。这种传统育种周期长,受天气、季节影响大,获得的四倍体桑育种材料也局限在已有的一些地方桑树品种中,基因资源多样化有限。利用植物组织培养技术和化学诱变相结合的方法获取桑树四倍体育种材料的研究,在国内尚未见报道。在国外,印度Chakraborti等(1998)采用二倍体桑树器官作为外植体,对其培养并进行化学诱导研究。为了丰富遗传育种资源,改良现有的某些栽培品种,缩短育种进程,本研究采用桑树多倍体化学诱变技术与桑树组织培养技术相结合的方法,在试管内获取桑树四倍体育种材料。
1 材料与方法 1.1 材料中桑5801(Morus atropurpurea)×纳溪桑(Morus multicaulis)的杂交桑种(该杂交桑种的亲本组合由西南大学生物技术学院选育,在西南大学生物技术学院技术指导下,由重庆市西里蚕种场制种)。
1.2 方法1) 不定芽的诱导 参考王茜龄等(2005)。
2) 多倍体诱导 (1)将获得的不定芽转移到已灭过菌的浓度分别为1、1.5、2.5 g·L-1的秋水仙碱溶液中分别浸渍2 d、3 d,对照用无菌水处理1 d。轻轻摇动使其充分接触,处理完毕后用无菌水冲洗4~5次,再接入到新鲜的培养基中,待得到完整植株后进行染色体倍性鉴定,确定为多倍体的株系予以保留并繁殖。(2)待不定芽有4片嫩叶时,以浓度为1.5、2、2.5 g·L-1的秋水仙碱滴液滴定不定芽5 d。8:30—9:00滴定1次,15:00—16:00滴定1次。待得到完整植株后鉴定细胞染色体数目,确定为多倍体的株系予以保留并繁殖。
1.3 多倍体检测1) 染色体数目鉴定 采用改良去壁低渗法(陈瑞阳等,1979)。取桑树茎尖或嫩叶置于8-羟基喹啉中预处理3~4 h,于新配的卡诺固定液中过夜,前低渗30 min吸干,3%的果胶酶和纤维素酶混合液酶解4~5 h,后低渗10 min,又用卡诺氏固定液再固定30 min。采用火焰干燥制片,玻片经空气干燥后,用5%Giemsa染色2 h,流水冲洗晾干,镜检观察。
2) 生物学性状鉴定 选取正常株与变异株代表部位,每株采集充分生长的叶片6片,比较其宽度、厚度、质量等生物学性状。采用光合测定仪CB-1101(北京恩爱迪生态科学仪器有限公司),选择阴天天气,空气中CO2浓度基本稳定,温度26~30 ℃,光照强度12000~13000 lx的条件下测试。采取测1个样品、测1个对照的方法,4个重复,每个重复测5片,取平均值作为这个重复的数据。记录每次测定的CO2初值和终值,采用CB-1101型光合测定仪自带的软件和计算公式计算出光合速率。
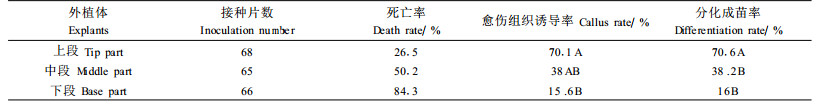
2 结果与分析 2.1 不定芽的诱导下胚轴上段(靠近胚芽的一段)、中段、下段,每段约0.2 cm,在诱导培养基中黑暗培养5 d,胚轴膨大,乳白色,转入光照条件下培养,第7天左右开始在切口处形成愈伤组织,第12天后开始分化出不定芽,重复3次。其愈伤组织诱导率和分化成苗率见表 1。
|
|
对上述试验结果中下胚轴各区段的愈伤组织诱导率进行统计分析,其愈伤组织诱导率差异达到极显著水平;经多重比较,下胚轴上段(靠近胚芽的一段)愈伤组织诱导率显著高于下胚轴中段及下段。不定芽分化率差异达到极显著水平;经多重比较,下胚轴上段不定芽分化率极显著高于下胚轴中段及下段。这与王茜龄等(2005)以沙二×伦109杂交品种的胚轴为外植体的结果一致。
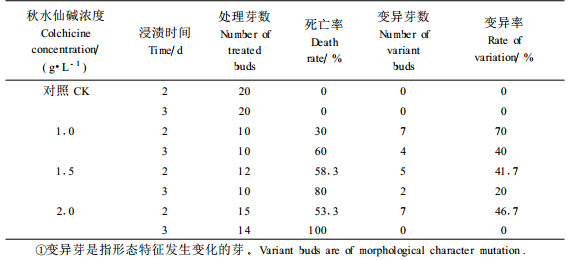
2.2 多倍体诱导经过秋水仙碱浸渍后的不定芽,生长受到抑制,叶片发生畸变,不定芽有严重腐烂现象,相同的秋水仙碱浓度分别处理不定芽2 d、3 d,其变异率差异明显(表 2)。浓度越大,差异越明显;随着浓度的增加,死亡率增高。处理后的不定芽的形态特征都发生了变化,随着秋水仙碱的浓度提高,叶片畸形越严重。从死亡率和变异率来看,以1.0 g·5L-1浸渍2 d死亡率最低,变异率最高。
|
|
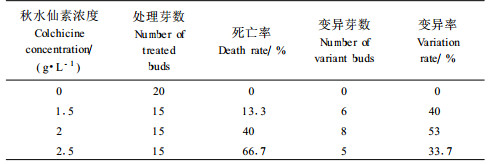
用秋水仙碱滴液滴定不定芽的试验结果见表 3。未经药液处理的丛生芽生长正常,经药液处理的丛生芽生长受到不同程度的影响。随着秋水仙碱浓度的提高,丛生芽死亡加重,生长迟缓,浓度为2.5 g·L-1死亡率最高,同时畸形芽增多; 秋水仙碱1.5、2.0、2.5 g·L-1的处理均有变异植株产生,但以浓度为2.0 g·L-1的处理最好,变异率达53%。
|
|
试管苗移栽成活后,对44株变异植株进行细胞染色体检测,显微镜下观察并计数染色体数目。每个植株观察30个细胞。仍为二倍体植株的染色体数目为2n=2x=28(图 1A),4株变异植株变为2n=4x=56(图 1B)。用2 g·L-1的秋水仙碱浸渍丛生芽获得的7株变异植株中有2株纯合四倍体植株,诱导频率为14%;用2.5 g·L-1的秋水仙碱滴定丛生芽获得5株变异植株中有1株纯合的四倍体植株,诱导频率为20%。

|
图 1 变异植株体细胞染色体图组(600×) Figure 1 the chromosomal number of somatic cells in diploid and tetraploid(600×) 二倍体 Diploid; B. 四倍体 Tetraploid |
四倍体植株(2n=4x=56)叶面凹凸不平,叶身较为扭曲,叶片宽大,叶色浓绿,节间密。与二倍体植株(2n=2x=28)外形特征比较如图 2所示。经显微测微计算,四倍体植株叶幅为(17.1±0.1) cm, 叶厚为(152.5±4.5) μm;测定其光合速率为(3.05±1.8) mgCO2·dm-2h-1; 二倍体植株的叶幅为(12.8±0.7) cm, 叶厚为(99.9±3.7) μm,光合速率为(1.14±0.4) mgCO2·dm-2h-1。经统计分析,其叶片宽度差异达显著水平(t=8.6*,n=3);其厚度达极显著水平(t=16.258**, n=9);光合速率达极显著水平(t=3.41*, n=4)。

|
图 2 桑四倍体与二倍体的叶片宽度比较(均为第6叶位) Figure 2 The comparison of blade width between tetraploid and diploid(the sixth leaf order) A. 四倍体 Tetraploid(4x);B.二倍体Diploid(2x). |
在多倍体诱导领域,理化诱变一直是首选的诱导方法。本试验将化学诱变剂与组织培养相结合,使化学诱变成为人工诱导多倍体的快捷途径,它与传统的多倍体诱变相比,具有较多优越性:可以在离体培养条件下,反复批量地在培养瓶中进行处理,从而大大提高诱导成功率;它可以不受季节、天气等自然条件的限制,诱导条件易于控制,可大大缩短诱导所需时间;同时,诱变后的植株易于早期筛选、鉴定,而且筛选鉴定以后,短期内可快速繁殖出大量的试管苗,以供田间鉴定、生产试验。
在化学诱变剂与组织培养相结合的这一技术中,建立高频再生体系是基础。桑为木本植物,在组培过程中容易褐化,较难获得高频再生体系,外植体的选择是关键因素之一。试验以中桑5801×纳溪桑下胚轴为外植体,取下胚轴上段(靠近胚芽的一段,约0.2 cm)在诱导培养基MS+6-BA 3.0 mg·L-1+IAA 0.3 mg·L-1+葡萄糖30 g·L-1+琼脂7.0 g·L-1+AgNO3 1.0 mg·L-1中诱导效果较好,诱导率可以达到70%,并且容易直接分化出不定芽,为诱导多倍体植株提供试管苗。李在留等(2006)在巨龙竹(Dendrocalamus sinicus)组织培养的研究中也表明巨龙竹组织培养与外植体采集部位有关。
秋水仙碱处理离体组织的方法主要有浸渍法、滴液法、混培法,不同的处理方法对诱导效果有一定影响。陈柏君等(2000)在诱导黄芩(Scutellaria baicalensis)多倍体时发现浸渍法优于混培法;而周嘉裕等(2002)在诱导辣椒(Capsicum annuum)多倍体时,认为混培法优于浸渍法。Chen等(2007)用2 g·L-1的秋水仙碱浸渍黄芪(Astragalus membranaceus)丛生芽36 h获得了35.3%的四倍体植株。本研究用2 g·L-1的秋水仙碱浸渍丛生芽2 d获得了纯合四倍体植株,其诱导率为14%;用2.5 g·L-1的秋水仙碱滴定丛生芽5 d也获得纯合的四倍体植株,其诱导率为20%。但是在采用浸渍法和滴液法中发现,滴液法耗费药液,浸渍法使用的秋水仙碱可以反复使用,省药,诱导率较高。由于秋水仙碱药品价格昂贵,因此在桑树多倍体离体诱导中从经济角度考虑还是选择浸渍法最佳。
本次试验通过组织培养与化学诱变相结合的方法已成功获得了四倍体桑植株,但其诱导纯合四倍体的频率还不高,有待进一步研究。
陈柏君, 高山林. 2000. 黄芩组织培养同源四倍体诱导. 植物资源与环境学报, 9(1): 9-11. DOI:10.3969/j.issn.1674-7895.2000.01.003 |
陈瑞阳, 宋文芹, 李秀兰. 1979. 植物染色体制备新方法. 植物学报, 21(3): 297-298. |
柯益富. 1997. 桑树栽培及育种学. 北京: 中国农业出版社, 267.
|
李在留, 辉朝茂. 2006. 珍稀竹种巨龙竹组织培养研究. 林业科学, 42(2): 43-49. |
林寿康. 1989. 实用桑树育种学. 成都: 四川科学技术出版社, 210-213.
|
南泽吉三郎. 1984. 栽桑学:基础与应用. 东京: 日本鸣风出版社, 171-190.
|
王茜龄, 余茂德, 徐立, 等. 2005. 桑子叶与胚轴不同区段离体再生植株的研究. 蚕业科学, 31(3): 334-336. DOI:10.3969/j.issn.0257-4799.2005.03.020 |
杨今后. 2004. 桑树四倍体的诱导及其应用. 蚕业科学, 30(1): 6-9. DOI:10.3969/j.issn.0257-4799.2004.01.002 |
周嘉裕, 卿人韦, 兰利琼, 等. 2002. 辣椒离体细胞多倍体的诱导研究. 四川大学学报:自然科学版, 39(4): 706-709. |
Chakraborti S P, Vijayan K, Roy B N, et al. 1998. In vitro induction of tetraploidy in mulberry(Morus alba L.). Plant Cell Reports, 17(10): 799-801. DOI:10.1007/s002990050486 |
Chen Lanlan, Gao Shanlin. 2007. In vitro tetraploid induction and generation of tetraploids from mixoploids in Astragalus membranaceus. Scientia Horticulturae, (112): 339-344. |
 2008, Vol. 44
2008, Vol. 44