文章信息
- 王海香, 申照静, 杜娟, 王有年, 师光禄.
- Wang Haixiang, Shen Zhaojing, Du Juan, Wang Younian, Shi Guanglu.
- 核桃青皮提取物对朱砂叶螨的毒力及相关酶活性的测定
- Insecticidal Activity of Juglans regia Extracts against Tetranychus cinnabarinus
- 林业科学, 2008, 44(5): 70-74.
- Scientia Silvae Sinicae, 2008, 44(5): 70-74.
-
文章历史
- 收稿日期:2007-11-18
-
作者相关文章
2. 北京农学院农业应用新技术北京市重点实验室 北京 102206
2. Key Laboratory of New Technology of Agricultural Application of Beijing Beijing 102206
植食性害螨个体小、繁殖快、种群密度高、为害重,是农业生产上的一个重要有害生物类群(师光禄等,1994;李连昌等,1992)。我国每年在柑橘、梨、苹果、桃等林果上使用化学杀螨剂防治此类有害生物,要花费巨额费用(曹挥等,2007)。然而频繁使用单一化学杀虫剂,不但会造成害螨天敌的大量死亡,而且会很快发展成一个具有该杀螨剂抗性的种群(Sachiko et al., 1999)。目前,从植物体内提取有效杀虫抑菌活性物质防治病虫害是国内外农药主要研究方向之一(张兴,2003)。植物源农药对环境污染小、害虫较难产生抗药性,且对有益生物较安全,可能具有降低害螨迅速产生农药抗性的潜能(何衍彪等,2004;张兴,2003;Wang et al., 2007)。很多学者纷纷应用现代科学技术,研制和开发了许多高效的植物源杀虫剂。
核桃(Juglans regia)在我国栽培历史悠久,资源丰富,具有显著的经济效益和药用价值。有关核桃叶、青果皮等的提取物在抗虫抑菌方面的活性作用已有较多的报道(翟梅枝,2003a;2003b)。但对杀螨方面的研究甚少,尤其对其机理方面的研究尚未见报道。朱砂叶螨(Tetranychus cinnabarinus)是农林生产上的重要有害生物,危害的林果及农作物已达百余种之多(Hazan et al., 1974;Ho et al., 1997)。为了有针对性的控制此类有害生物的危害,减少环境污染,笔者对核桃青皮提取物的杀螨活性成分及其机理进行了初步的研究,旨在为开发一种经济、安全、有效的植物源杀螨剂提供科学支撑。
1 材料与方法 1.1 供试材料核桃青皮采自北京市平谷区苏子峪,将收集的核桃青皮洗净阴干,磨碎后备用。供试朱砂叶螨为敏感品系,采自北京科技大学碧桃树(Prunus persica),以大豆(Glycine max)幼苗为螨的食料,温度为(25±1)℃,相对湿度为50%±5%,光照(L:D)为16:8的条件下饲养后获得。
1.2 核桃青皮活性成分的提取与分离 1.2.1 提取方法准确称取一定量的植物干粉,装入广口瓶内,加入干粉5倍量的有机溶剂(石油醚、氯仿、甲醇),室温下(25±2) ℃分别浸提3次,每次3~5 d,分别合并3种提取液并减压浓缩至膏状后,称重。
1.2.2 萃取分离采用液-液分配法。生物测定结果表明:核桃青皮石油醚提取物生物活性较强,因此,对其进一步分离纯化。称取核桃青皮提取物6 g,用10倍量石油醚溶解,装入分液漏斗中,用甲醇萃取3次,合并萃取液并减压浓缩至稠膏状,称重。
1.2.3 柱层析分离将规格为5 cm×80 cm的层析柱,洗净后烘干,垂直固定在铁架台上备用。称取需分离萃取物100倍量的硅胶(100~200目),与适量的洗脱液混匀,迅速注入层析柱中,并用橡胶锤轻敲柱壁,排除溶液中的气泡,同时,打开层析柱底端的旋塞,使溶液缓慢下移,带动硅胶颗粒向下移动,紧密沉集在柱底。取萃取物5 g用少量初始洗脱液溶解,待柱内溶液表面距硅胶表面1 cm左右时,用吸管将待分离物质沿柱内壁均匀注入,待需分离物质移动到硅胶表面以下时,覆盖一层石英砂,然后用石油醚、氯仿、甲醇溶剂系统进行洗脱淋柱:洗脱液的流速为3~4滴·s-1,每流分收集60 mL,共得流分299个,经薄层层析(TLC)后,置于碘蒸气中进行检测,做好标记。将相同成分者合并,最终得到流分19个,分别将其减压浓缩后,进行生物活性测定,确定活性成分所在部位。
1.3 触杀作用采用玻片浸渍法(FAO,1980)进行生物活性测定。用双面胶条将健康活泼、大小一致的30头雌成螨粘于载玻片的一端,于药液中浸5 s后取出,并用滤纸吸掉虫体周围多余药液,处理后置于室温(25±1)℃下,24 h后观察其死亡情况,接触动者为活,不动者为死,按Abbott公式计算校正死亡率(Abbort,1987)。
1.4 症状观察叶碟浸渍法(朱丽梅等,2002):将洗净的平展的大豆叶片于水培养台上,每一叶片挑入成螨30头以上,待成螨稳定后,夹取叶片浸入药液(10 mg·mL-1)中5 s,以清水处理为对照。叶片边缘用湿棉条围住,以防螨体逃逸。每6 h观察1次成螨的活动及反应状况,24 h记录4次。
1.5 酶液制备试虫采用触杀方法处理,分别取处理后4、8、12、16、20、24 h的雌成螨150头,加0.25 mL生理盐水在冰浴中匀浆后,10 000 r·min-1,4 ℃下离心15 min,取上清液备用。
1.6 蛋白质含量测定采用考马斯亮蓝G-250法(慕立义,1991)进行蛋白质含量的测定。加酶液0.1 mL于5 mL考马斯亮蓝G-250试剂中混匀,25 ℃水浴中恒温加热2 min,于595 nm波长处比色测定OD值,然后根据标准曲线得出蛋白质含量。
1.7 酶活性测定乙酰胆碱酯酶和Na+,K+-ATPase酶活性测定使用南京建成生物研究所的乙酰胆碱酯酶测试盒,超微量Na+,K+-ATPase测试盒进行测定。
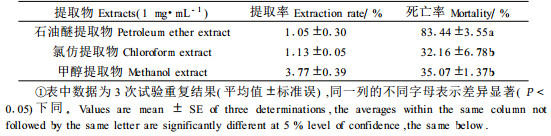
2 结果与分析 2.1 核桃青皮提取物对朱砂叶螨的触杀作用核桃青皮3种溶剂提取物的提取率分别为甲醇(3.77±0.39)%>氯仿(1.13±0.05) %>石油醚(1.05±0.30)%。将石油醚、氯仿和甲醇提取物分别配制成浓度为1 mg·mL-1药液,对害螨进行触杀试验,24 h后,毒力测定结果表明(表 1),核桃青皮石油醚提取物的触杀活性明显大于其余2种有机溶剂的提取物(p<0.05),对朱砂叶螨的触杀效果达到80.61%。为此作者选择了核桃青皮石油醚提取物作进一步的萃取与纯化。
|
|
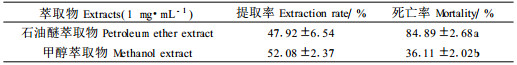
对触杀效果较好的石油醚提取物用甲醇进行萃取分离(表 2)。2种溶剂之间萃取率分别为:甲醇(52.08±2.37) % >石油醚(47.92±6.54) %;2种溶剂萃取物生物测定结果表明:石油醚萃取物的死亡率为(84.89±2.68)%,明显高于甲醇萃取物(36.11±2.02)%(P<0.05),由此可确定核桃青皮的杀螨活性物质主要存在于石油醚萃取物中。
|
|
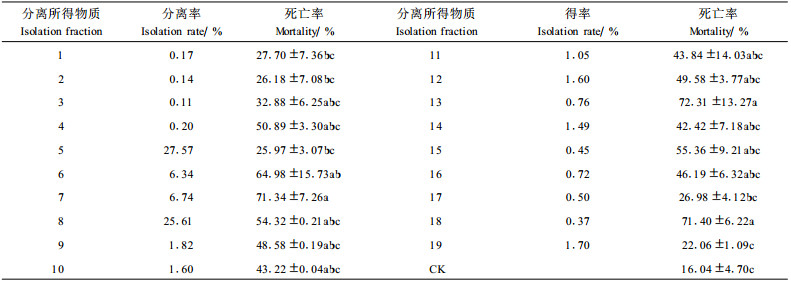
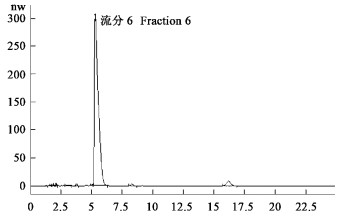
将柱层析分离及TLC检测后得到19个流分(表 3),生测结果表明,流分6、7、13、17对朱砂叶螨的触杀效果较好,均达到60%以上,其中,流分6、7的提取率较好,分别为6.34%,6.74%。TLC检测结果表明,流分6的纯度高于其他几种有效物质,通过高压液相色谱(图 1)证实,其纯度达90%以上,因此选择该物质首先进行毒理研究。
|
|
|
图 1 核桃青皮提取物流分6高压液相图谱 Figure 1 HTLC figure of the sixth fraction of J. regia |
将所得流分6配制成6个不同浓度的药液(1、2、4、5、8、10 mg·mL-1)进行生物活性测定,分别求出毒力回归方程(y=4.402+2.170x)及致死中量LC50(1.886 mg·mL-1),可见其有较好的生物活性。药液浓度为10 mg·mL-1时,24 h后害螨死亡率为98.45%,已大于95%,适于进行后续酶活性的进一步研究。因此选择10 mg·mL-1这一药剂浓度,进行症状观察及乙酰胆碱酯酶与Na+,K+-ATPase的活性测定。
2.4 症状观察用流分6(10 mg·mL-1)及清水处理雌成螨后,进行症状观察,发现0~6 h间,处理组害螨表现的十分兴奋,四处爬动,并急剧产卵,而对照组则缓慢的爬动,正常的取食叶片;6~12 h间,处理组试虫背部出现体液外渗现象,四处窜动或抽搐,产卵量有所下降,而对照组行为正常,并开始产卵;12~18 h间,处理组试虫体液一直保持外渗状态,兴奋与静止交替出现,身体开始收缩,对照组则正常爬动,未见异常;18~24 h间,处理组试虫身体逐渐收缩至死亡,对照组则身体饱满,活动正常。
经流分6处理后,表现的症状与神经毒剂有相似之处,如兴奋、抽搐等,由此推测,该活性物质对神经系统有一定的作用。
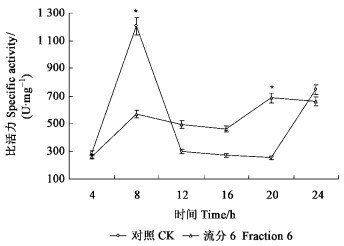
2.5 乙酰胆碱酯酶的活力测定将流分6(10 mg·mL-1)和清水分别喷施于朱砂叶螨体表,作为处理组和对照组,经测定两者乙酰胆碱酯比活力变化如图 2所示:8 h时,处理组比活力为570.90 U·mg-1 prot,是对照组的0.47倍,显著高于对照(P<0.01);12~20 h间,处理组比活力分别为494.81,461.73,686.98 U·mg-1 prot,对照组的分别为299.45,271.99,255.41;24 h时,处理组比活力低于对照组,为对照的0.89倍。从整体来看,流分6对朱砂叶螨的乙酰胆碱酯酶具有一定的抑制作用。
|
图 2 核桃青皮活性物质对朱砂叶螨乙酰胆碱酯酶活性的影响 Figure 2 Effect on the activity of Ache of the extracts of J. regia against T. cinnabarinus *表示差异极显著(P<0.01),下同。 *is significantly different at 1% level of confidence, the same below. |
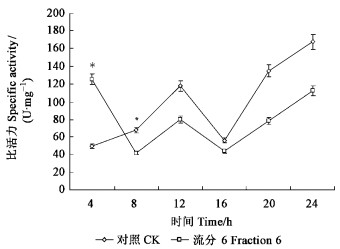
从图 3可以看出,害螨经流分6处理后Na+,K+-ATPase比活力变化趋势与对照(清水)基本相同,4~8 h间,处理组比活力从125.46降至41.68 U·mg-1 prot,8 h时,其为对照组的0.62倍,抑制效果显著(P<0.01);12、16 h时,处理组比活力分别为对照组的0.67、0.78倍;24 h时,处理组比活力为112.54 U·mg-1 prot,是对照的0.67倍。
|
图 3 核桃青皮活性物质对朱砂叶螨Na+,K+-ATPase活性的影响 Figure 3 Effect on the Na+, K+-ATPase activity of the extracts of J. regia against T. cinnabarinus |
大多数杀螨剂是通过干扰神经系统来发挥致死作用的,而且其中毒特征多表现为战栗、痉挛、麻痹或是其他行为上的改变。神经细胞间的化学信息传递主要依靠神经传递素的合成与分解,已经报道了许多被公认的神经传递素,如乙酰胆碱、伽马氨基丁酸、真硝胺等,其中已有一些被证明为杀螨剂的靶标(Mark et al., 1994)。作者所观察到的害螨施药后的症状与上述神经毒剂的症状有相似之处,因此作者选择神经系统中2个重要酶系,即乙酰胆碱酯酶与Na+,K+-ATPase 2种酶的活性进行测定。乙酰胆碱存在于突触间隙中并可被乙酰胆碱酯酶分解,从而终止神经兴奋的传导,一旦该酶被一定程度的抑制昆虫会过度兴奋后死亡(林忠莲等,2001)。试验结果表明,核桃青皮提取物流分6对乙酰胆碱酯酶的活性有一定的抑制作用,8 h时,与24 h内其他时间段相比,抑制效果较好。
神经细胞的离子组成不同于周围介质,它取决于细胞膜对不同离子的渗透性,周围介质中这些离子的浓度以及在细胞膜上离子泵的的活性(林忠莲等,2001)。Na+,K+-ATPase广泛分布于细胞膜及内质网等膜成分之中,与Na+,K+的传递有关,该酶受抑制时,膜对离子的通透性降低,Na+流受抑制,引起膜内Na+浓度升高,造成神经膜处于持续的兴奋状态,继而引发神经系统功能紊乱,最终导致昆虫死亡(张宗炳,1982)。试验结果表明,施以药剂的害螨Na+,K+-ATPase活性变化趋势与对照基本相同,且在8 h时抑制效果要好于24 h内其他时间段,与乙酰胆碱酯酶较强抑制点出现的时间段相同,且与观察到的与之相应症状出现的时间段也基本相符,由此可推断,活性物质可能通过对这两种酶活性的影响,引起神经传递的阻断从而导致螨体死亡。
核桃具有2千多年的栽培历史,我国是核桃的起源地之一,资源十分丰富,早在隋唐时期,其药用价值就已得到肯定并广泛应用(唐静成,2003)。现代研究表明,核桃叶提取物对粘虫(Leucania separata)与小菜蛾(Plutella xylostella)具有一定的拒食作用;核桃青皮提取物对粘虫与小菜蛾也均有一定的拒食和胃毒作用,对粘虫的作用效果更为明显,且其对杨毒蛾的触杀作用弱于对蚜虫的触杀作用(翟梅枝等,2001;2003)。本研究中,作者利用相似相溶的原理,以朱砂叶螨为试虫,从核桃青皮中分离出纯度为90%以上的杀螨活性物质,并探索性地对朱砂叶螨神经系统2个重要酶活性进行了初步的测定,为将来该活性物质的结构鉴定,毒理的深入研究及新型植物源农药的研发等后续工作奠定了良好的基础。今后将对其毒理进行深入的研究,并对该物质的结构进行鉴定,以求得到一种新型的植物源杀螨剂。
曹挥, 王有年, 刘素琪, 等. 2007. 地肤提取物对山楂叶螨体内几种酶活性的影响. 林业科学, 43(2): 68-72. |
何衍彪, 詹儒林, 赵艳龙. 2004. 植物源农药的研究和应用. 热带农业科学, 24(3): 58-62. |
林忠莲, 张立力. 2001. 磷化氢对谷蠢和玉米象成虫体内乙酰胆碱酯酶的影响. 郑州工程学院学报, 22(4): 35-41. DOI:10.3969/j.issn.1673-2383.2001.04.008 |
李连昌, 李利贞, 范永亮, 等. 1992. 中国枣树害虫. 北京: 中国农业出版社.
|
师光禄, 郑王义, 党泽普, 等. 1994. 果树害虫. 北京: 中国农业出版社.
|
唐静成.2003.核桃叶生物活性成分的研究.西北农林科技大学硕士学位论文.
|
张兴. 2003. 植物性农药在生防中的地位和作用. 世界农业, 2(1): 31-32. DOI:10.3969/j.issn.1002-4433.2003.01.009 |
翟梅枝, 李晓明, 林奇英, 等. 2003a. 核桃叶抑菌成分的提取及其抑菌活性. 西北林院学报, 18(4): 89-91. |
翟梅枝, 杨秀萍, 林奇英, 等. 2003b. 核桃叶提取物对杨毒蛾生物活性的研究. 西北林学院学报, 18(2): 65-67. |
翟梅枝, 杨秀萍, 刘路. 2001. 核桃叶提取物对蚜虫的触杀作用. 西北林学院学报, 16(4): 55-56. DOI:10.3969/j.issn.1001-7461.2001.04.015 |
张宗炳. 1982. 昆虫毒理学的新进展. 北京: 北京大学出版社.
|
朱丽梅, 倪钰萍, 黄春霞, 等. 2002. 螨的综合测试方法的研究. 南京农专学报, 17(1): 13-17. DOI:10.3969/j.issn.1672-755X.2002.01.003 |
Abbort W S. 1987. A method of computing the effectiveness of an insecticide. J Am Mosq Control Assoc, 3: 302-303. |
FAO. 1980. Revised method for spider mites and their eggs (Tetranychus spp. and Panonychus ulmi Koch). FAO Plant Production, 21: 49-54. |
Hazan A, Gerson U, Tahori A S. 1974. Spider mite webbing Ⅰ. the production of webbing under various enviromental conditions. Acarologia, 16: 68-84. |
Ho C, Maggi V. 1997. Spider mite (Acari:Tetranychidae) on various crops in Taiwan. J Agr Res China, 46: 333-346. |
Mahoney N, Molyneux R J, Mckenna J, et al. 2003. Resistance of 'Tulare' Walnut (Juglans regia cv. Tulare) to aflatoxigenesis. J Fo Sci, 68(2): 619-621. DOI:10.1111/jfds.2003.68.issue-2 |
Mark A, Roger G H. 1994. Downer biochemical and physiological targets for miticides. Pestic Sci, 40: 85-101. DOI:10.1002/ps.v40:2 |
Sachiko K, Youko K, Hamitsu K.1999. A novel miticide. Norio O and Tadakazu W* AKD-2023: Biological activity and mode of action IUPAC Congress.
|
Wang Younian, Shi Guanglu, Zhao Lilin, et al. 2007. Acaridical activity of Juglans regia leaf extracts on Teranychus viennensis and Tetranychus cinnabarinus (Acari: Tetranychidae). J Econ Entomo, 100: 1298-1303. DOI:10.1093/jee/100.4.1298 |
 2008, Vol. 44
2008, Vol. 44