文章信息
- 王娅丽, 李毅, 陈晓阳.
- Wang Yali, Li Yi, Chen Xiaoyang.
- 祁连山青海云杉天然群体表型性状遗传多样性分析
- Phenotypic Diversity of Natural Populations in Picea crassifolia in Qilian Mountains
- 林业科学, 2008, 44(2): 70-77.
- Scientia Silvae Sinicae, 2008, 44(2): 70-77.
-
文章历史
- 收稿日期:2006-12-04
-
作者相关文章
2. 北京林业大学林木花卉遗传育种教育部重点实验室 北京 100083
2. Key Laboratory of Forest and Flower Genetics and Breeding of Ministry of Education Beijing Forestry University Beijing 100083
青海云杉(Picea crassifolia)是我国西北地区特有树种,分布于甘肃、青海等省,是祈连山水源涵养林主要组成群系。长期以来,青海云杉不但是主要用材树种,同时以其为主体的水源涵养林更是该区人民赖以生存和发展的生态保证。近50年来,随着人口压力加大和环境条件变迁,祈连山森林体系遭到破坏,森林资源减少,青海云杉天然群体出现逆向演替。
遗传多样性是生物多样性的基本组成部分,其测定对于了解物种起源、预测种源适应性及估算基因资源分布具有重要意义。遗传标记是研究遗传多样性的主要方法,包括形态学(表型)、细胞学、生化和分子标记4大类(葛颂等,1994)。很多时候,当需要在短期内对变异性有所了解或在其他生化方法无法开展之时,利用形态性状来估测遗传变异是一种有价值的选择(李文英等,2005)。云杉属植物表型遗传多样性研究已取得了一些成果(El-Kassaby,1991;Putenikhin,1997;Li et al., 1997;乌弘奇,1989;江洪,1992;韦淑英等,2001;罗建勋等,2003;2005),但对于青海云杉,前人研究主要集中于立木资源调查、林分类型划分及间伐量等宏观方面,遗传多样性研究至今报道甚少,仅有孙雪新等(1990)、李萍等(2005)对青海云杉群体进行了同工酶变异初步分析和探讨,而表型遗传多样性研究尚未涉及。
本文通过对祁连山青海云杉10个天然群体的针叶、球果、种鳞、种翅、种子表型性状的研究,揭示青海云杉的表型变异程度与变异规律,为其保护与合理利用提供依据。
1 材料与方法 1.1 群体的确立与试验材料的采集在勘查的基础上,按经纬度和海拔梯度设置样地,于2006年10月完成所有性状的采集工作。在祁连山青海云杉天然分布区内,自西向东共选取10个群体:肃南1(SN1)、肃南2(SN2)、肃南3(SN3)、天祝1(TZ1)、天祝2(TZ2)、山丹(SD)、民乐(ML)、大通1(DT1)、大通2(DT2)。每群体选取30株平均木或亚优势木作为采种母树,株间距离50 m以上。由于正逢青海云杉结实小年,故采用非常规小样本试验取样,即每群体选取10个供种单株进行分析测定。在每个单株树冠中上部南向采集15~30枚成熟球果和2年生针叶30~50枚。针叶现场测定,球果带回实验室分析测定。
样地中实测经纬度、海拔、坡度、坡向和土壤因子;年均温、1月均温、7月均温和年降水等气象因子从当地气象部门查阅。
1.2 表型性状的测定方法参照Falkenhagen(1978)、Putenikhin(1997)、Li等(1997)、罗建勋等(2003)表型测定方法进行青海云杉表型性状测量。
针叶测定:每单株的2年生针叶混匀后,随机选取15枚针叶用游标卡尺测定针叶的长度、宽度(中央)。球果测定:直尺测定球果长度,游标卡尺测定球果径(中央直径),每单株测定15个球果;球果干燥脱粒后称量其干质量。种鳞测定:从上述15个球果中部随机各取2个完整的种鳞,用直尺测定其长度和宽度(最宽端)。种翅测定:从上述15个球果的中部随机各取2个完整的种翅,用直尺测定其长度和宽度(最宽端)。种子测定:群体分单株脱粒净种,随机取30粒种子,用游标卡尺测定每粒种子的长度和宽度;每单株随机取100粒种子称其质量,换算成千粒质量,重复3次,取平均值。
上述长宽测量精度均为0.01 cm,质量测量精度为0.01 g。
1.3 统计分析方法对各性状采用巢式设计方差分析(李斌等,2002;李梅等,2005;李文英等,2005),线性模型为:γijk=μ+τi+δj(i)+εk(ij),式中:γijk为第i个群体第j个家系第k个观测值,μ为总平均值,τi为群体间效应值,δj(i)为群体内家系效应值,εk(ij)为随机误差。
以表型分化系数(Vst)反映群体间表型分化(葛颂等,1998)。Vst=(σt/s2)/(σt/s2+σs2),式中:σt/s2为群体间的方差分量,σs2为群体内的方差分量。
采用常规统计方法,统计各表型性状的平均值、标准差;用变异系数CV表示表型性状的离散程度,CV=S/x,式中:S为标准差,x为平均值。采用双变量相关分析对青海云杉各表型性状之间以及各表型性状和采集点的地理生态因子进行相关分析。利用欧式平均距离方法进行分层聚类分析。其他统计运算按照常规方法并利用EXCEL2003, SAS11.5软件包提供的有关程序进行。
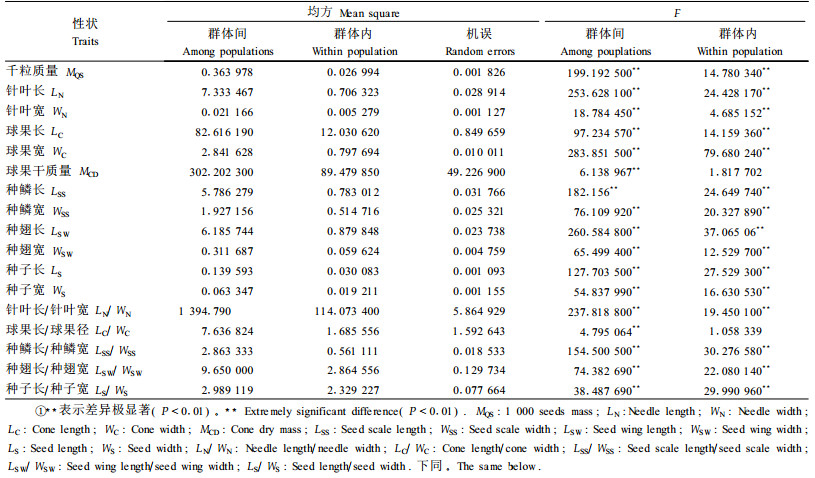
2 结果与分析 2.1 青海云杉群体间和群体内的形态变异特征青海云杉针叶、球果、种鳞、种翅、种子的17个表型性状在群体间和群体内2个层次上的差异分析见表 1;差异显著的性状多重比较结果见表 2。表 1表明,针叶、球果、种鳞、种翅、种子的17个表型性状在群体间都存在极显著差异,除球果干质量和球果长/球果径外,其余性状在群体内都存在着极显著的差异。说明青海云杉的表型性状在群体间和群体内存在着广泛的变异。
|
|
|
|
各性状平均值和多重比较表明,群体中17个表型性状间存在着显著差异。针叶长较大的群体是ML、SD和DT1,相互间差异不显著,针叶长和针叶宽较小的群体是MY,针叶宽最大的群体是SN1。叶形状指数较大的群体是ML和SD,较小的群体是TZ2和TZ1。球果长、球果径、球果干质量以及千粒质量变异特征相近,都是SN1和SN3两个群体较大,MY较小。球果形状指数最大的群体为DT2,最小为TZ2。种鳞长度较大的群体是SN3、SD、SN1,相互间差异不显著,与其他几个群体间差异显著。种鳞宽度较大的群体是SN1、SN2、SN3和DT2,与其他群体间差异显著。种翅长度、宽度最大的群体都是SN1,最小的群体分别是MY和TZ2。种鳞和种翅形状指数变异特征极其相似,最大的群体都是SD,最小的群体是MY。种子长度以SN3、SN1、SD、SN2、DT 5个群体较大,相互间无显著差异。种子宽度是SD、ML、SN3、SN2、DT2、TZ1、SN1 7个群体无显著差异,与TZ2、MY、DT1间差异显著。种子形状指数最大的群体是SN1,最小的群体是ML。针叶、球果、种鳞、种翅、种子都可概括为在采样分布区西北部的群体较大,中部群体较小,即随着纬度的减小,经度的增加,种鳞、种翅、种子形状都有变小的趋势。
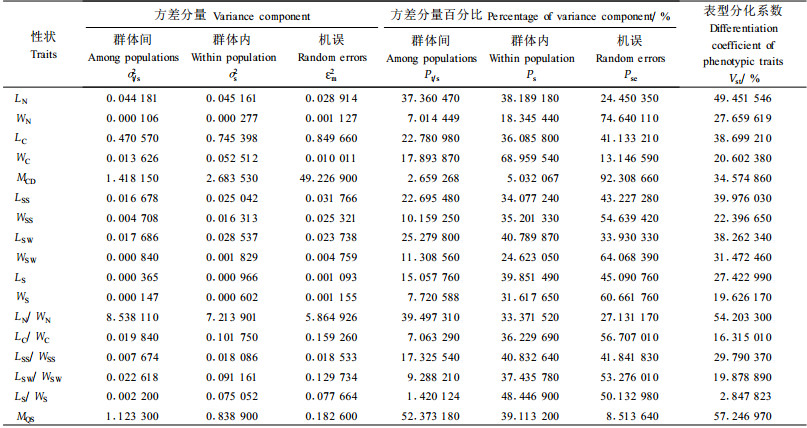
2.2 青海云杉各形态特征变异来源及群体间的表型分化为定量分析青海云杉17个表型性状变异来源,按照巢式设计将各表型性状的变异分解为群体间变异、群体内变异和个体内变异(机误),各层次上的方差分量百分比是说明变异来源的一个重要指标(张恒庆等,1999)。各方差分量占总变异比例及表型分化系数(表 3)表明,针叶、球果、种鳞、种翅、种子表型性状的表型分化系数(Vst)变异幅度为2.84%~57.25%,其中最大的是千粒质量,最小的是种子长/种子宽。Vst较大的是针叶形状指数54.20%和千粒质量57.25%,说明这2个性状在群体间的变异大于群体内的变异,群体间的变异占相对优势。种鳞、种翅、种子的形状指数的Vst相对较小,说明它们较其他性状在群体间相对稳定,以群体内变异为主。17个表型性状的平均表型分化系数为31.20%,说明群体间的变异小于群体内的变异(68.80%),青海云杉天然群体表型分化的变异以群体内变异为主。
|
|
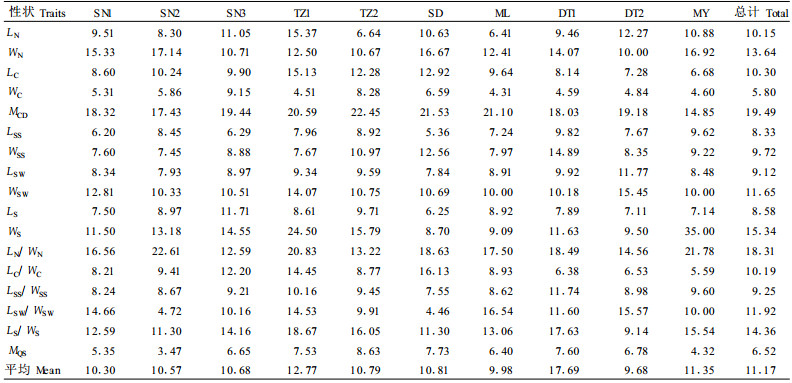
用变异系数表示性状值离散性特征,变异系数越大,性状值离散程度越大。青海云杉天然群体表型性状变异系数分析揭示(表 4),17个表型性状平均变异系数为11.17,变异幅度5.80~19.49。按针叶、球果、种鳞、种翅、种子性状的平均变异幅度由大到小顺序排列的是针叶(13.79)>球果(11.21)>种子(11.03)>种翅(10.60)>种鳞(8.84),这表明种鳞的稳定性较高。
|
|
同一性状在不同群体内的变异幅度也有差异,说明不同地区的环境异质性导致群体表型变异的差异。10个群体所有性状的平均变异系数从大到小排序为:DT1(17.69)>TZ1(12.77)>MY(11.35)>SD(10.81)>TZ2(10.79)>SN3(10.68)>SN2(10.57)>SN1(10.30)>ML(9.98)>DT2(9.68)。变异系数最大的群体,要比最小的群体大近2倍。说明DT1群体的表型多样性较高,而DT2群体的表型多样性程度较低。
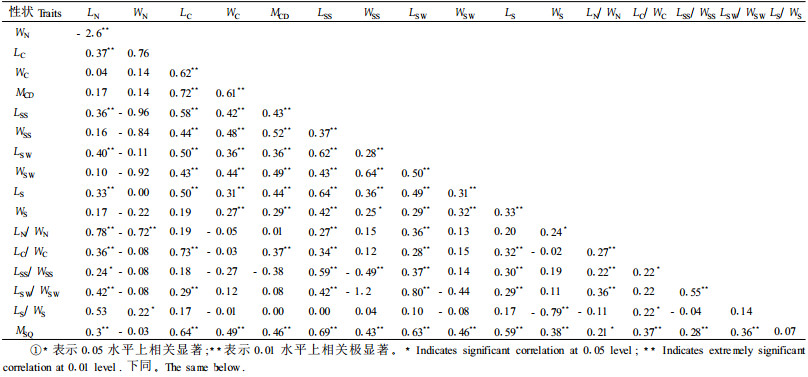
2.4 青海云杉表型性状间的相关关系对青海云杉针叶、球果、种鳞、种翅和种子17个表型性状进行双变量相关分析和检验(表 5)。结果表明:表型性状间相关系数较大的是针叶长与针叶长/针叶宽(0.78),球果长与球果长/球果宽(0.73),球果长与球果干质量(0.72),球果长与球果宽(0.62),球果长与种鳞长(0.58),球果长与种翅长(0.50),球果长与种子长(0.5),球果长与千粒质量(0.64), 球果宽与球果干质量(0.61),球果干质量与种鳞宽(0.52), 种鳞长与种子长(0.64),种鳞长与种翅长(0.62),种鳞长与种鳞长/种鳞宽(0.59),种鳞长与千粒质量(0.69),种翅长与种翅宽(0.62), 种鳞宽与种翅宽(0.64),种翅长与种翅宽(0.5),种翅长与千粒质量(0.63),种子长与千粒质量(0.59),种鳞长/种鳞宽与种翅长/种翅宽(0.55)。说明以上这些性状之间有着极强的相关性。17个表型性状中与10个以上的其他性状有极显著正相关的性状有种翅长(14个)、种鳞长(14个)、种子长(13个)、千粒质量(13个)、球果长(11个)、球果干质量(10个),与不足6个其他性状有相关关系的性状有针叶宽(0个)、种子长/种子宽(1个)、针叶长/针叶宽(5个)。
|
|
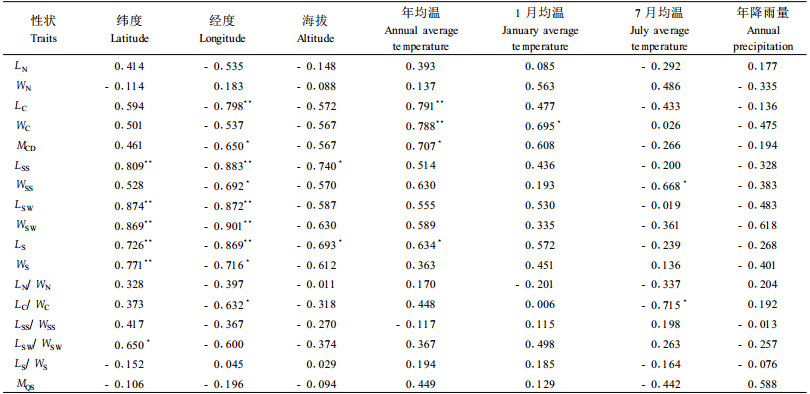
青海云杉针叶、球果、种鳞、种翅、种子17个表型性状与采样地地理生态因子双变量相关分析与检验结果(表 6)表明,球果长与经度呈极显著负相关,与年均温呈极显著正相关;球果宽与年均温和1月均温分别呈极显著和显著正相关;球果干质量与经度呈显著负相关,与年均温呈显著正相关;球果长/球果宽与经度和7月均温呈显著负相关。这说明随着经度和年均温升高,球果干质量减小,球果逐渐向长减小、宽增大的粗短圆柱形变异。种鳞长与纬度呈极显著正相关,与经度呈极显著负相关,与海拔呈显著负相关,种鳞宽与经度和7月均温呈显著负相关,种鳞长度和宽度都随着经度增大而减小。种翅长、宽都与经度呈极显著负相关,说明随着经度的增加,种翅变小。种子长宽变异特征相似,与纬度呈极显著正相关,与经度呈极显著负相关,种子长与海拔呈显著负相关,说明从南向北、从东向西种子长、宽都增大,即种子变大。
|
|
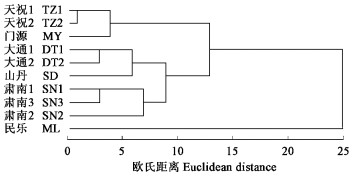
利用欧式平均距离法,对群体针叶、球果、种鳞、种翅、种子表型数据进行聚类分析(图 1)。根据聚类结果将10个群体划分为4个类群,其中TZ1群体与TZ2群体表型特征相似,MY群体与其距离相近,这3个群体归为一类;DT1与DT2群体和SD群体距离相近,归为一类;SN1、SN3、SN2 3个群体聚为一类,ML群体单独归为一类。
|
图 1 青海云杉天然群体表型性状的聚类结果 Figure 1 UPGMA cluster based on the phenotypic traits of 10 populations in P.crassifolia |
青海云杉10个天然群体表型性状分析表明,该群体表型变异极为丰富,这些变异是自身遗传因素和环境因素共同作用的结果。这种多层次的变异为优质种质资源和生物多样性保护提供了物质基础,同时也表明了生物多样性保护任务的艰巨性。
1) 青海云杉群体间和群体内方差分析表明,各性状在群体间和群体内存在着广泛变异且差异显著,表明其性状稳定性较差并受到一定环境压的影响(周连第等,2005;李梅等,2005),与粗枝云杉(Picea asperata)和红皮云杉(Picea koraiensis)表型变异研究结果一致。罗建勋等(2003;2004;2005)研究结果认为粗枝云杉表型性状在群体间和群体内都存在显著差异;张含国等(2003)认为红皮云杉表型性状群体间、群体内以及个体内都存在丰富的变异。
2) 青海云杉17个表型性状的平均表型分化系数为31.20%,群体内的变异为68.80%,说明青海云杉群体内多样性程度大于群体间多样性,表型变异以群体内为主。李萍等(2005)同工酶研究也表明,青海云杉群体间分化水平较低,大部分变异存在于群体内。这种结果反映了群体G×E的复杂性及其适应环境压的广泛程度,是不同环境选择的结果,是群体分化的源泉(庞广昌等,1995)。尽管群体内变异远远大于群体间变异,但群体间变异的意义却大于群体内的变异,因为存在于群体间的变异反映了地理、生殖隔离上的差异,它是种内多样性的重要组成部分。分布在群体间的变异真正反映了群体在不同环境中的适应状况,其大小在某种程度上说明了该生物对不同环境适应的广泛程度,值越大适应的环境越广(李斌等,2002)。青海云杉群体内表型多样性程度大于群体间,可能是因为所选群体间距离较小,导致群体间分化水平较低(李梅等,2005)。
与其他针叶树种相比青海云杉表型分化系数为中等偏高,和云南松(Pinus yunnanensis)(36%)、粗枝云杉(30.99%)非常接近,小于黑云杉(Picea mariana)(49.41%~57.04%)和白云杉(Picea glauca)(50%),高于西加云杉(Picea sitchensis)(10.1%)、红皮云杉(14.51%)、长白落叶松(Larix olgensis)(26.2%)和白皮松(Pinus bungeana)(22.86%)等(张含国等,2003;罗建勋等,2004;2005)。
3) 青海云杉不同群体内每一性状都存在着广泛差异,说明不同地区的环境异质性导致群体表型变异的差异。在10个群体中DT1群体的表型多样性最丰富,DT2群体表型多样性程度较低。17个表型性状中,球果干质量变异性较大,千粒质量稳定性较高,针叶和种子横向变异程度大于纵向变异。针叶、球果、种翅形状指数比其单个性状变异性大,而种鳞和种子形状指数比其单个性状稳定。罗建勋等(2005)对云杉表型多样性研究结果认为,云杉球果、针叶、种翅和种子4个性状的形状指数比单个性状的变异系数大,只有种鳞形状指数的变异系数小于单个性状的变异系数。
4) 青海云杉表型性状间相关分析表明,种鳞长、种子长、千粒质量、球果长、球果干质量是青海云杉较为关键和重要的表型性状,对表型性状的测定效率有着极为重要的影响。罗建勋等(2005)也认为云杉球果长度、球果径、种鳞长度和种翅长度以及种子千粒质量应视为云杉重要和关键的表型性状。
5) 一般而言,树种分布区较大,分布区环境条件越复杂,群体遗传变异越大。青海云杉表型与生态因子相关分析表明,多数性状与经度呈显著负相关,似有随经度增加性状减小的趋势,由此可得出表型变异呈现以经度变异为主的梯度规律性。这与Khalil(1984)对黑云杉研究结果相似,与挪威云杉(Picea abies)研究结果不同,Bergmann(1978)认为温度是挪威云杉地理变异的主要选择因子。
罗建勋等(2003)认为云杉针叶宽度随着纬度和经度变异,从南向北、从西向东针叶宽度逐渐变小;江洪(1992)认为云杉针叶宽度随海拔增高而增大,变异与适应性有关。而青海云杉针叶性状地理变异不明显。
青海云杉球果性状变异以经度和年均温变异为主,随着年均温增大,球果逐渐由细长向粗短变异,与挪威云杉研究结果(Khalil,1984)相同,与云杉和黑云杉研究结果相异。罗建勋等(2005)认为云杉球果的变异以纬度变异为主;江洪(1992)认为云杉球果长度和宽度都与海拔相关;Khalil(1985)认为黑云杉球果性状变异的地理趋势不明显,球果长、宽,球果干质量及千粒质量受较强的遗传控制。
青海云杉种鳞、种翅性状变异以纬度和经度变异为主,随经纬度增加性状变小;种鳞长与海拔呈显著负相关,种鳞宽与7月均温呈显著负相关。而Roche(1969)认为,白云杉、黑云杉、西加云杉和恩氏云杉(Picea engelmannii)种鳞性状受强遗传控制。
青海云杉种子受经度、纬度和海拔的影响,从南向北,从东向西,海拔越低的地方种子越大。年均温也影响种子的大小,年均温越大种子越大。种子随海拔升高体积变小的现象与杨玉坡等(1960)和罗建勋等(2003)研究结果一致,即认为海拔高的地方云杉植株上结的球果多,但种子的质量轻,发芽率也较低。
6) 青海云杉群体表型特征基本上按地理距离而聚类,说明了群体间表型性状变异的连续性。罗建勋等(2003)认为利用云杉群体表型性状进行群体的初步区划是可行的。Barzdajn(1996)认为表型是基因型和环境共同作用的结果, 可采用表型性状进行挪威云杉群体鉴别,并根据挪威云杉群体球果和种鳞等表型性状对其20个种源进行了区划。因此依据青海云杉天然群体主要表型性状聚类分析结果进行种源划分是可行的。
本文虽然只对祁连山青海云杉10个天然群体的表型多样性进行了探讨,但表型是遗传型和环境型共同作用的结果,表型变异必然蕴藏着遗传变异。表型变异越大,可能存在的遗传变异越大。一般认为表型变异往往具有适应意义, 自然群体中保持大的变异贮存对群体是有利的, 群体内多种基因型所对应的表型范围越广, 群体在整体上适应环境的能力更强,因此青海云杉丰富的表型变异, 也就是青海云杉抗逆性强适应性广的原因。根据青海云杉丰富的表型变异,可以推断青海云杉的遗传改良前景是广阔的,这对开展青海云杉天然群体遗传多样性和种质资源的保护、评价与利用具有重要的意义。
葛颂, 洪德元.1994.遗传多样性及其检测方法//钱迎倩, 马克平.生物多样性研究的原理和方法.北京: 中国科学技术出版社.
|
葛颂, 王明麻, 陈岳武. 1998. 用同工酶研究马尾松群体的遗传结构. 林业科学, 24(11): 399-409. |
江洪. 1992. 云杉种群生态学. 北京: 中国林业出版社, 120-143.
|
李斌, 顾万春, 卢宝明. 2002. 白皮松天然群体种实性状表型多样性研究. 生物多样性, 10(2): 181-188. DOI:10.3321/j.issn:1005-0094.2002.02.008 |
李梅, 韩海荣, 康峰峰, 等. 2005. 辽东栎天然群体表型多样性研究. 北京林业大学学报, 27(5): 10-16. DOI:10.3321/j.issn:1000-1522.2005.05.002 |
李萍, 李毅. 2005. 青海云杉遗传结构研究. 甘肃农业大学学报, 40(3): 363-367. DOI:10.3969/j.issn.1003-4315.2005.03.020 |
李文英, 顾万春. 2005. 蒙古栎天然群体表型多样性研究. 林业科学, 41(1): 49-56. DOI:10.3321/j.issn:1001-7488.2005.01.010 |
罗建勋, 李晓清, 孙鹏, 等. 2003. 云杉天然群体的表型变异. 东北林业大学学报, 31(1): 9-11. DOI:10.3969/j.issn.1000-5382.2003.01.003 |
罗建勋, 顾万春. 2004. 云杉天然群体种实性状变异研究. 西北农林科技大学学报:自然科学版, 32(8): 60-66. |
罗建勋, 顾万春. 2005. 云杉天然群体表型多样性研究. 林业科学, 41(2): 66-73. DOI:10.3321/j.issn:1001-7488.2005.02.011 |
庞广昌, 姜冬梅. 1995. 群体遗传多样性和数据分析. 林业科学, 31(6): 543-550. DOI:10.3321/j.issn:1001-7488.1995.06.002 |
孙雪新, 查天山, 陶毅. 1990. 青海云杉群体同工酶变异的研究. 甘肃林业科技, (2): 11-15. |
乌弘奇. 1989. 东北云杉的地理变异规律. 东北林业大学学报, 17(2): 27-33. |
杨玉坡, 李成彪. 1960. 四川大小金川冷、云杉林木结实规律性的初步研究. 林业科学, (3): 193-195. |
韦淑英, 陆卫林, 段喜华, 等. 2001. 红皮云杉亲代特征群体的多样性. 东北林业大学学报, 29(5): 5-10. DOI:10.3969/j.issn.1000-5382.2001.05.002 |
张含国, 孙立夫, 韩继凤, 等. 2003. 红皮云杉遗传多样性的研究. 植物研究, 25(5): 224-229. |
张恒庆, 安利佳, 祖元刚. 1999. 天然红松种群形态特征地理变异的研究. 生态学报, 19(6): 932-938. DOI:10.3321/j.issn:1000-0933.1999.06.029 |
周连第, 兰彦平, 曹庆昌, 等. 2005. 板栗叶片性状表型多样性研究. 林业科学, 21(9): 136-139. |
Barzdajn W. 1996. An assessment of diagnostic value of morphological traits of Norway spruce(Picea abies(L.) cones for discrimination of spruce provenances. Sylwan, 140: 61-75. |
Bergmann F. 1978. The allelic distribution at an acid phosphatase locus in Norway spruce(Picea abies) along similar climatic gradients. Theoretical and Applied Genetics, 52: 57-64. |
El-kassaby Y A. 1991. Genetic variation within and among conifer populations: review and evolution//Biochemical markers in the population genetics of forest tree. Hague, Etherland, 61-76.
|
Falkenhagen E R. 1978. Multivariate classification in provenance reaearch. Silvae Genetica, 27(1): 14-23. |
Khalil M A K. 1985. Genetic varation in eastern white spruce (Picea glauca(Moench) Voss) population. Can J For Res, 15: 444-452. DOI:10.1139/x85-071 |
Khalil M A K. 1984. Genetic of cone morphology of black spruce(Pice mariana(Mill).B.S.P.)in Newfound-land, Canada. Silvae Genetica, 33: 101-109. |
Li Peng, Beaulieu J, Bousquet J. 1997. Genetic structure and patterns of genetic variation among populations in eastern white spruce(Picea glauca). Canadian Journal of Forest Research, 27(2): 189-1981. DOI:10.1139/x96-159 |
Putenikhin V P. 1997. Phenotype analysis of Picea obovata in the southern Urals population structure. Lesovedenie, 6: 37-49. |
Roche L. 1969. A genecological study of the genus Picea in British Columbia. New Pbytol, 68: 505-554. |
 2008, Vol. 44
2008, Vol. 44