随着全球人口老龄化的到来,非传染性疾病已成为主要的死亡原因[1],全球对药品需求强劲。随着生命科学的发展和技术的进步,以抗体、疫苗、融合蛋白、细胞治疗和基因疗法等为代表的生物制药,因其具有较高的安全性和有效性,越来越获得市场和患者的认可。IQVIA公司数据显示,2018年全球处方药物市场近10698亿美元,虽然非生物药市场仍占据主导地位,但生物制药的市场份额在不断扩大,增速远超非生物制药。2018年全球生物制药市场份额超过3000亿美元,年复合增长率(CAGR)为11.5%。2019年全球销售额排名前10的药物中,有8种为生物制药[2]。在生物制药市场,美国市场占据主导地位,市场份额占全球市场的61.2%,其次是日本、德国、法国、意大利、中国、英国、西班牙、加拿大和澳大利亚。美国、中国和澳大利亚的生物制药市场增长较快,2014—2018年的CAGR都超过10%(图 1)。
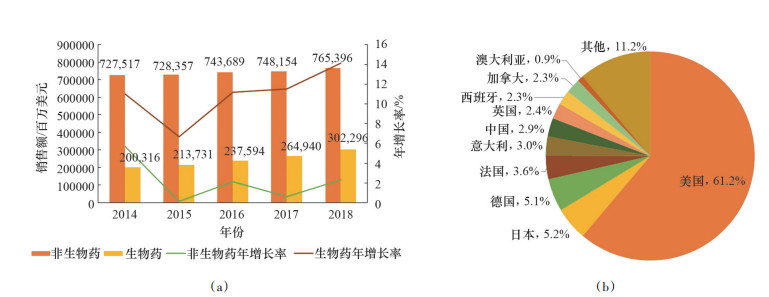 |
数据来源:IQVIA Analytic Link数据库(检索日期:2019年7月12日) 图 1 2014—2018年全球生物制药及非生物药市场概况(a)及2018年生物制药市场国家占比(b) |
专利对医药行业技术创新成果的保护作用非常重要,分析生物制药专利家族,可以在一定程度上反映目前研究的重点领域,技术的发展状况及未来趋势[3-6]。现代生命科学发展日新月异,生物制药技术更新迭代较快,全球每年都有上万件生物制药专利申请。新兴技术如CRISPR-Cas系统技术等崭露头角之时,专利申请量并不突出,但极大地推动了产业变革。选取合适的指标,对生物制药专利家族的强度、质量和相关价值进行深度分析,可以深度挖掘新兴技术的创新价值,了解生物制药产业的最新面貌和发展趋势。很多研究者通过国内外专利申请和授权对医药领域的区域分布、研发机构及技术研发重点等进行了分析[3, 5, 7-8],但综合专利申请、市场覆盖、高质量专利分析的深入挖掘尚未报道。本研究基于PatentSight®数据库,利用专利申请量、技术相关性(technology relevance,TR)、市场覆盖率(market coverage,MC)、竞争影响力(competitive impact,CI)、专利资产指数(patent asset index,PAI)等指标,深入分析了全球生物制药专利的申请趋势,并对热点技术CRISPR-Cas系统技术、PD-1/PD-L1免疫疗法和CAR-T细胞疗法的专利布局进行了重点分析。
1 数据来源与分析方法以相关字段对该数据集进行加工处理,并以专利申请量、TR、MC、CI、PAI等指标对检索得到的专利发展态势、国家创新力、疾病治疗领域和主要研发机构专利申请态势分析,并对本领域研究热点的专利进行深度挖掘(检索日期:2019年7月12日)。生物技术的不同应用领域常用颜色代码划分,“Red Biotech”是指生物技术在健康、医学和诊断领域的应用,PatentSight®以该分类形成“Biopharma”数据集。
TR反映了专利的技术相关性,主要来自于专利审查员引文的加权和。该指标是专利审查员作为独立技术专家对所有专利文献进行持续同行评审的结果。
MC反映了专利家族的规模所显示的发明的经济潜力(每个国家的国民总收入(GNI)和专利家族成员的法律地位所加权的管辖范围)。MC代表了申请人对该专利的看法:使用申请人的内部知识作为代理,以确定预期具有更大潜力的专利(与不重要的专利不同,这些专利通常在更多、更大的经济体中提交)。
CI是在单个专利家族(简单家族)的级别上计算的,显示了该专利家族的技术和战略价值。竞争影响力是由TR和MC两个指标的组合来计算的(即CI=TR×MC),每个指标都提供了不同的视角。数据库所有专利的CI平均分为1.0。
PAI是衡量一个企业或整个技术领域创新实力的指标。它是在专利组合水平上计算的,是该组合中包含的各个专利族的CI得分之和。根据要解决的问题,可计算公司整体的专利资产指数,或仅计算属于特定业务领域或技术领域的专利,显示公司在这些特定领域的实力。
2 生物制药行业专利态势分析 2.1 全球生物制药行业专利申请趋势自20世纪末,生物制药进入了蓬勃发展期,世界各国纷纷将生物制药的研发作为技术创新的主要驱动。截至检索日期,全球范围内的生物制药领域公开的专利申请达到32.5万件,其中有效专利近15万件。生物制药领域专利申请在1996—2001年实现井喷式发展,年申请量从5000件增长到1.3万件,之后趋于平稳,每年在1.2万件左右。而2013年之后,该领域专利年申请量又逐年增加,到2016年,年度申请量超过1.7万件,中国专利申请量占据多数(图 2)。
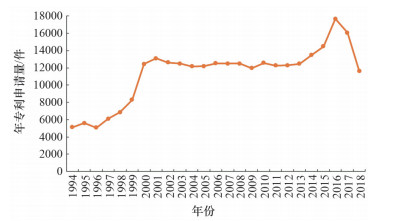 |
由于专利申请文件一般是自申请之后18个月公开,因而2017年之后提交的相当部分专利申请文件尚未公开,导致2017以后的申请量数据不完善 图 2 1994—2018年全球专利申请趋势 |
美国是生物制药创新的先驱国家,近年来中国生物技术蓬勃发展,市场重要性和技术影响力在不断扩张。1994—2000年,美国、日本申请的专利数量不断上升,而2000年之后,美国的专利申请量呈下降趋势,2013年申请量仅有约6900件,此后几年略有回暖。日本与美国该领域专利申请趋势一致。这两个国家的生物技术发展相对趋于成熟。
中国在该领域的专利申请量自1994年以来呈不断上升的趋势,自2010年首次超过日本、2015年首次超越美国后,2016年该领域的专利申请更是超过1万件,而同年美国有7217件,日本仅有4188件(图 3)。
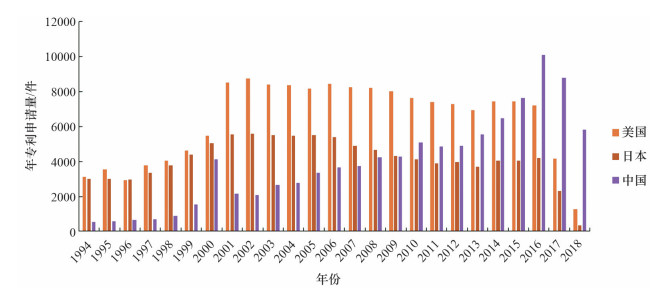 |
图 3 1994—2018年美国、日本和中国生物制药领域专利申请趋势 |
目前该领域活跃的专利以美国为优先权国家的有6.3万件,其PAI值高达22.8万,单件专利CI值高达3.6(全球生物制药专利的平均CI值为2)。欧盟地区也是全球重要医药市场和技术创新区域,虽然在该领域具有优先权的专利仅有8804件,但PAI值仅次于美国。
中国经过多年发展,生物制药领域的创新实力已有突破性进展,目前以本国专利为优先权的有效专利约3.6万件,PAI值(2.3万)居于全球第3。然而,专利质量尚有待提高,单件专利族的竞争影响力(CI值为0.7)在排名前20的国家/地区中仍处于较低水平,与韩国相当。
此外,印度本土的生物技术值得关注,虽然专利总量较少,但竞争影响力(CI值为2.2)不容小觑(图 4)。
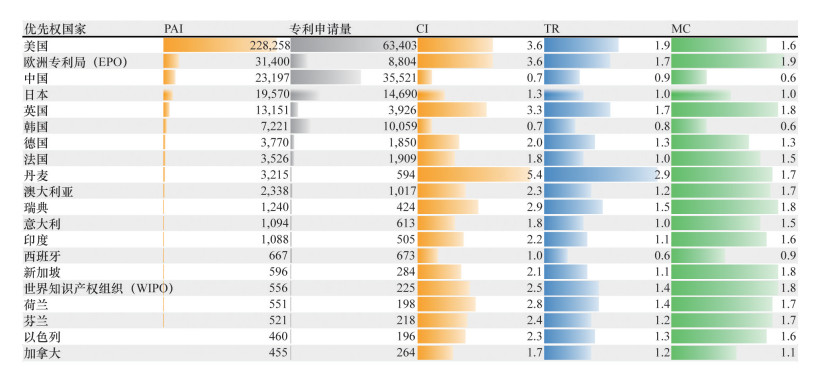 |
国家/地区为活跃专利的优先权国家/地区 图 4 以PAI值排序的各国/地区专利关键指标分析 |
从治疗领域看,抗肿瘤药物研发是全球生物制药的技术热点。抗肿瘤药的专利布局占生物制药总体专利资产(PAI)的33.7%,其次是免疫或过敏疾病治疗药(21.1%)、抗感染药物(20.2%)、神经系统疾病治疗药物(14.0%)、消化系统疾病治疗药(13.6%)。此外,非中枢镇痛药/非甾体抗炎药、心血管疾病治疗药、代谢紊乱治疗药、皮肤病治疗药、骨骼疾病治疗药物的专利布局占生物制药总体专利资产的比例均超过10%(图 5)。内分泌系统疾病治疗药物、抗寄生虫药、全身保护剂或抗毒素剂等方向还罕有生物技术专利申请。
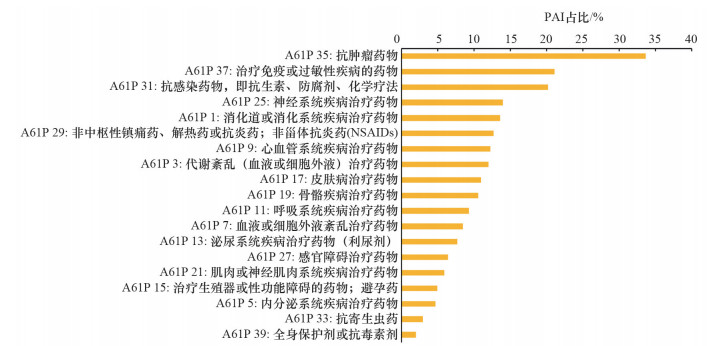 |
PAI百分比为各领域PAI值与全球生物制药专利总体PAI值的比例。由于一件专利可能涉及不同的治疗领域,有多个IPC分类号,统计有重复 图 5 全球生物制药专利治疗领域布局分析(按IPC分类号计的PAI百分比) |
各国对疾病领域的专利布局不尽相同。美国、欧盟和日本的生物制药专利布局与全球总体趋势一致,技术热点集中在抗肿瘤药、免疫或过敏疾病治疗药、抗感染药物、神经系统疾病治疗药物和消化系统疾病治疗药,其中美国对其他疾病领域也有均衡布局。
中国生物制药技术热点及竞争力集中在抗肿瘤药物领域,其次是抗感染药物领域、免疫或过敏疾病治疗药。但其他疾病领域的生物制药创新尚处于起步阶段,与欧美日尚有较大差距(图 6)。
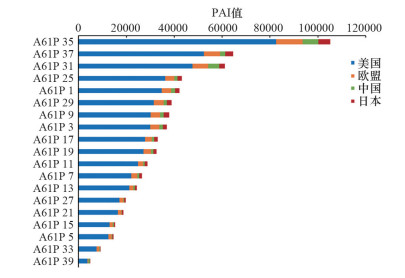 |
图 6 美国、欧盟、中国和日本生物制药专利治疗领域布局分析(按IPC分类号计的PAI值分析) |
在生物制药领域,罗氏的专利资产全球领先,PAI为17130,新技术的兴起带动了哈佛大学、麻省理工学院等相关机构竞争影响力不断增强。哈佛大学、加利福尼亚大学、麻省理工学院、诺华集团、百时美施贵宝公司、强生公司、葛兰素史克公司、宾夕法尼亚大学和安进公司都进入以PAI排序的排行榜前10(图 7)。此外,由于CRISPR-Cas系统技术的兴起,哈佛大学、麻省理工学院以及这两个机构共建的Broad Institute的竞争影响力呈直线上升趋势(PAI值未进入全球前10,未在图 7中显示)。
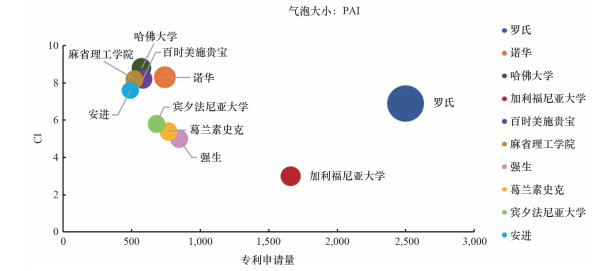 |
图 7 全球生物制药行业公司/机构专利概况(以PAI值排序) |
在中国生物制药领域,虽然科研机构在积极推动研发进展,但企业具有强劲的竞争力。目前,中国本土的机构/公司中,中国科学院活跃的专利族共计1770件,CI值为0.6,PAI为1101,专利资产指数在国内排名第一。江苏恒瑞公司、华大基因公司、上海交通大学、百济神州公司、清华大学、中山大学、中国医学科学院、浙江大学和复旦大学都进入以PAI排序的排行榜前10。百济神州公司的CI值国内领先,有多篇专利涉及其PD-1抗体药物,该公司的替雷利珠单抗已于2019年底在中国获批,另有多个抗体类药物在临床研究中(图 8)。
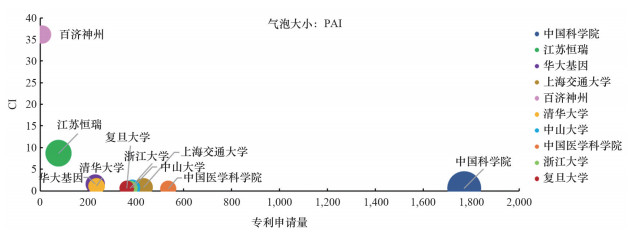 |
图 8 中国生物制药行业公司/机构专利概况(以PAI值排序) |
在生物制药领域近15万件有效专利中,按照CI排名的前100篇专利,要求保护的技术内容主要涉及CRISPR-Cas系统技术、免疫检查点抑制剂特别是PD-1/PD-L1免疫疗法、CAR-T细胞疗法、双特异性抗体、小分子IDO抑制剂、脂质纳米粒子制剂等方向,尤其集中在前3种技术主题。下文对CRISPR-Cas系统、PD-1/PD-L1免疫疗法以及CAR-T细胞疗法进行重点分析。
3.1 CRISPR-Cas系统 3.1.1 技术简介CRISPR-Cas系统是一种原核生物的免疫防御系统,用来抵抗外来遗传物质的入侵,如质粒和噬菌体内的遗传物质,从而提供获得性免疫[9]。CRISPR-Cas系统可分为2类:Class 1和Class 2。CRISPR-Cas系统被开发成一种高效的基因编辑工具,其中目前研究最深入、应用最成熟的是属于Class 2的CRISPR/Cas9系统[10]。CRISPR-Cas9由Broad研究所的张锋和加州大学伯克利分校的Jennifer Doudna提出,可作为简单、灵活的基因组编辑工具。
CRISPR-Cas技术随着研究的深入,已经被广泛地应用在基因敲除、基因替换等基础编辑方向,此外,还可以被用于基因激活,疾病模型构建,甚至是基因治疗。首例人体临床试验于2016年在中国展开,四川大学华西医院利用CRISPR技术编辑的T细胞,治疗化疗、放疗以及其他疗法治疗无效的转移性非小细胞肺癌患者[11]。至2019年,Clinicaltrials.gov数据库列出了10多个正在进行的CRISPR-Cas9的活跃临床研究,该疗法的适应症涉及从癌症到HIV和血液疾病等多种疾病[12]。
3.1.2 技术专利分析CRISPR-Cas技术在生物制药领域的应用在蓬勃发展中,美国和中国是专利布局的重要国家。自2013年以来,全球专利申请呈爆发式增长,至今还在持续发展中。目前该技术在生物制药领域活跃的专利共计1281件,其中以美国为优先权国家的专利有825件,以中国为优先权国家的专利有275件,活跃专利总量分别位居第一和第二位。
美国和丹麦、英国等欧洲国家在该技术方面具有核心竞争影响力。美国该技术专利的CI为10.0,TR为4.7,MC为2.1。以丹麦为优先权国的5篇专利,CI高达30.9,TR为15.8,MC为1.5。中国技术影响力在全球不容小觑,与法国、新加坡等国家相当,但市场覆盖较小,专利大多在国内进行申请(图 9)。
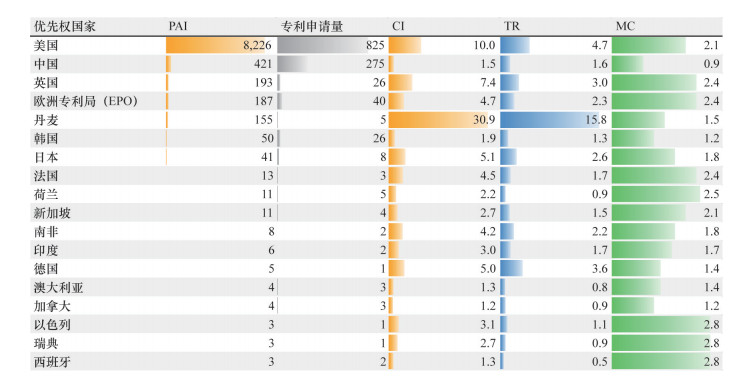 |
图 9 以PAI值排序的各国/地区生物制药领域CRISPR-Cas技术专利关键指标分析 |
目前科研机构是CRISPR-Cas技术在生物制药领域应用研发的主体,企业也在紧急布局。全球以PAI值统计的前10位研发机构中,有6家是科研机构,4家为药物公司,其中Broad研究所的竞争影响力和技术影响力均居于全球首位。以TR排名的前10篇相关专利中有7篇为Broad研究所申请的专利,要求保护的主题均涉及CRISPR-Cas技术及其应用。中国以PAI值统计的前10位研发机构中,科研机构和企业分别为6家和4家,中国科学院的专利申请量和PAI值居于国内首位,南京凯地生物科技有限公司竞争影响力国内最高。但中国以TR排名的前10篇相关专利仅涉及CRISPR-Cas技术在细胞制备、动物建模等方向的基因编辑应用,具有创造性的技术改进未见涉及。
3.2 PD-1/PD-L1免疫疗法 3.2.1 技术简介PD-1(程序性死亡受体1),也称为CD279(分化簇279),是一种重要的免疫抑制分子,PD-L1是PD-1配体之一。PD-1与PD-L1的结合会破坏T细胞与树突细胞之间稳定接触的产生,从而导致T细胞激活过程的中止。另外,PD-1信号通路对T细胞新陈代谢和肿瘤微环境都有影响[13]。
PD-1/PD-L1免疫疗法是当前备受瞩目,为患者带来新希望的新一类抗癌免疫疗法。自2006年首次进行了靶向PD-1的单克隆抗体Nivolumab的临床试验以来,当前已有10种PD-1/PD-L1单克隆抗体在全球获批。另据相关报道,截至2018年9月,全球共开展了2250项抗PD-1/PD-L1药物临床试验,其中既有单独用药也有联合试验研究,与2017年9月相比,共新增试验748项[14]。
3.2.2 技术专利分析该技术相关的专利申请自2013年以来蓬勃增长,尚无放缓趋势。目前生物制药领域该技术活跃的专利共计3463件,其中以美国为优先权国家的专利有2328件,以中国为优先权国家的专利有565件,活跃专利总量分别位居第一和第二位。
美国、中国、欧洲、英国、丹麦、印度、澳大利亚和荷兰在该技术方面具有核心竞争影响力。美国该技术专利的CI为9.7,TR为4.3,MC为2.1。中国该技术专利的CI为4.5,TR为2.5,MC为1.3,已走在世界前列(图 10)。
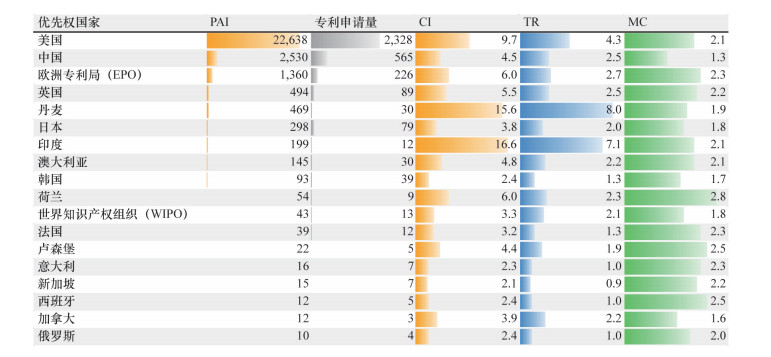 |
图 10 以PAI值排序的各国/地区生物制药领域PD-1/PD-L1技术专利关键指标分析 |
随着多个PD-1/PD-L1抗体药物的上市,制药公司已然成为该项技术的核心竞争者。全球以PAI值统计的前10位研发机构中,有6家是跨国制药公司,4家为科研机构。诺华公司的专利申请量虽然不是最多,但PAI居于全球首位,其核心专利值得关注。中国PD-1/PD-L1免疫疗法领域,也是企业具有核心竞争力,江苏恒瑞、百济神州、信达生物PAI值国内领先,排名前10的研发机构均为制药企业。国内外技术影响力最高的前10篇相关专利涉及的主题均为PD-1/PD-L1抗体及其用途。
3.3 CAR-T细胞疗法 3.3.1 技术简介CAR-T细胞疗法(Chimeric Antigen Receptor T-Cell Immunotherapy)为近年来涌现的明星抗癌疗法。CAR-T疗法是利用白细胞分离术收集患者的T细胞,然后在体外进行T细胞活化、转导含有嵌合抗原受体(CAR)的病毒载体、CAR-T细胞的扩增及回输患者体内。CAR是由抗体衍生的片段组成,该片段识别与共刺激分子偶联的肿瘤抗原,促进T细胞的扩增和持久性[15]。
目前全球已被批准上市的CAR-T细胞疗法共有两项,分别为诺华公司的Kymriah和由Kite公司原研的Yescarta。全球处于临床研发中的CAR-T细胞疗法有近200个。中国的CAR-T细胞疗法研究也在飞速发展。南京传奇生物科技、上海药明巨诺、西比曼生物科技、博生吉医药、安科生物、科济生物等公司的CAR-T产品都已进入临床研究,其中有部分产品已取得了积极的临床结果。
3.3.2 技术专利分析自2014年以来,该技术的专利申请量呈直线上升状态。目前生物制药领域该技术活跃的专利共计1733件,其中以美国为优先权国家的专利有997件,以中国为优先权国家的专利有486件,活跃专利总量分别位居第一和第二位。
美国、中国、欧洲的丹麦、英国等国家在该技术方面具有核心竞争影响力。美国该技术专利的CI为9.4、TR为4.3、MC为2.2,中国该技术专利的CI为2.5、TR为2.0、MC为1.0(图 11)。
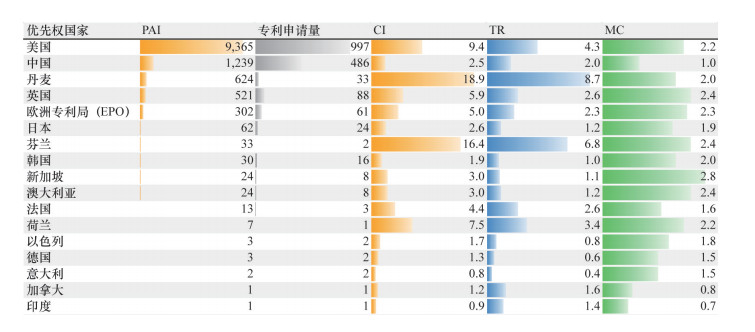 |
图 11 以PAI值排序的各国/地区生物制药领域CAR-T细胞疗法专利关键指标分析 |
科研机构在全球的CAR-T细胞疗法研发中具有核心竞争力,随着两款该类产品的上市,企业也在紧急布局;而中国的生物制药企业是CAR-T细胞疗法研发的驱动力。全球以PAI值统计的前10位研发机构中,有6家是科研机构,4家为药物公司,其中宾夕法尼亚大学和诺华公司的竞争影响力和技术影响力均居于全球前列。以TR排名的前10篇相关专利中,有6篇为宾夕法尼亚大学申请的专利,大多为和诺华共同申请。中国以PAI值统计的前10位研发机构中,有7家是药物企业,3家为科研机构,其中科济生物的专利申请量和PAI值居国内首位。国内外技术影响力最高的前10篇相关专利涉及要求保护的主题均含嵌合抗原受体及表达CAR的T细胞的构建及在疾病治疗中的应用。
4 结论随着全球对生物制药需求的不断上涨以及下一代生物技术的蓬勃发展,生物制药市场近年来始终保持高速增长态势。生物制药研发热点集中在抗肿瘤药物、免疫或过敏疾病治疗药、抗感染药物、神经系统疾病治疗药物和消化系统疾病治疗药;而以传统化药治疗为主的疾病领域如内分泌系统疾病治疗药物及抗寄生虫治疗药物等方向还罕有生物技术专利申请。跨国制药公司是生物医药研发的主力军,PAI前10位的公司机构中,有6家为制药公司,4家为科研机构,罗氏公司的PAI全球领先。然而,新兴技术如CRISPR-Cas技术、CAR-T细胞疗法的核心竞争力集中在科研机构,如Broad研究所、宾夕法尼亚大学等,科研机构对生物制药新兴技术的推动力日益突显。
中国生物医药研究已进入首创(First-in-class)阶段,在抗肿瘤药物研发及新技术如PD-1/PD-L1免疫疗法、CAR-T细胞疗法和CRISPR-Cas技术方向上已具有一定的国际竞争力。国内医药企业和科研机构都在对生物制药相关技术进行积极创新,但整体创新实力和国际市场关注度与顶尖机构尚有较大差距。国内的学术机构尽管拥有较多的专利,但核心竞争力却不强,原创性技术布局较弱。国内的制药企业已对国外热点技术进行跟进,但核心竞争力还局限于某一领域,国际市场关注度仍需增强。
综上所述,尽管中国的生物医药研发实力在不断增强,但技术创新力、市场竞争力还有待提高。这不仅要求我们重视并鼓励各类主体积极开展原创性生物制药技术研究,还需要进一步加强科技成果转化、促进学术机构与企业的合作创新。在药物研发方面,国内企业除了着重于抗肿瘤药物领域,还应多元化发展,着力解决中国人口诸多远未满足的突发性传染病及慢性疾病的临床需求。
| [1] | World Health Organization. The top 10 causes of death[EB/OL]. (2018-05-24)[2018-05-24]. https://www.who.int/en/news-room/fact-sheets/detail/the-top-10-causesof-death. |
| [2] | Lisa U. Top companies and drugs by sales in 2019[J]. Nature Reviews Drug Discovery, 2020(228):19. |
| [3] | 谢华玲, 陈芳, Cynthia, 等. 全球生物制药领域研发态势分析[J]. 中国生物工程杂志, 2019, 39(5):1-10. |
| [4] | 谌凯, 应向伟, 吴叶青, 等. 基于专利分析和文献计量的中国医药制造业发展态势研究[J]. 科技管理研究, 2018, 38(2):103-111. |
| [5] | 齐燕, 高东平, 杨渊. 中国医药专利70年发展态势分析[J]. 医学信息学杂志, 2019, 40(10):19-24. |
| [6] | 赵杨升, 徐俐颖, 褚淑贞. 中国医药制造业专利合作发展研究与分析[J]. 药学进展, 2019, 43(8):621-627. |
| [7] | 刘畅, 李硕, 李凤新, 等. 生物医药产业专利态势分析[J]. 科学观察, 2012, 7(4):40-43. |
| [8] | 傅俊英, 赵蕴华. 中国生物医药专利的分布及趋势分析[J]. 现代生物医学进展, 2012, 12(1):142-150. |
| [9] | Wright A V, Nuñez J K, Doudna J A. Biology and applications of CRISPR systems:Harnessing nature's toolbox for genome engineering[J]. Cell, 2016, 164(1):29-44. |
| [10] | Liang P P, Xu Y W, Zhang X Y, et al. CRISPR/Cas9mediated gene editing in human tripronuclear zygotes[J]. Protein & Cell, 2015, 6(5):363-372. |
| [11] | Cyranoski D. Chinese scientists to pioneer first human CRISPR trial[J]. Nature, 2016, 535(7613):476-477. |
| [12] | Nature. Quest to use CRISPR against disease gains ground[EB/OL]. (2020-01-06)[2020-01-06]. https://www.nature.com/articles/d41586-019-03919-0. |
| [13] | Longo D L, Boussiotis V A. Molecular and biochemical aspects of the PD-1 checkpoint pathway[J]. New England Journal of Medicine, 2016, 375(18):1767-1778. |
| [14] | Tang J, Yu J X, Hubbard-Lucey V M, et al. The clinical trial landscape for PD1/PDL1 immune checkpoint inhibitors[J]. Nature Reviews Drug Discovery, 2018(17):854-855. |
| [15] | Yip A, Webster R M. The market for chimeric antigen receptor T cell therapies[J]. Nature Reviews Drug Discovery, 2018(17):161-162. |