2. 武汉理工大学 船海与能源动力工程学院,湖北 武汉 430063;
3. 中国舰船研究院,北京 100192
2. School of Naval Architecture, Ocean and Energy Power Engineering, Wuhan University of Technology, Wuhan 430063, China;
3. China Ship Research and Development Academy, Beijing 100192, China
碳达峰、碳中和是我国搭建清洁低碳、安全高能源体系的重要措施,而构建以新能源为主体的新型电力动力系统是我国能源动力领域和水运交通行业实现双碳目标的主要方式。风电、光伏等清洁零碳能源具有波动性和间歇等特点,设计并配置适配的储能系统形成局域微电网络,可平缓清洁能源输出波动,提高能量输出稳定性,并有利于促进清洁能源联网使用,拓宽其应用场景。储能系统中锂离子电池的应用是发展最迅速且有望满足大规模储能应用需求的关键技术。锂离子电池储能系统可结合分布式/集中式的新能源发电架构,有效解决新能源发电并网问题。伴随清洁能源发电规模的快速增长及储能技术的飞速发展,锂离子电池储能系统将成为推动我国清洁能源战略发展的重大关键技术。
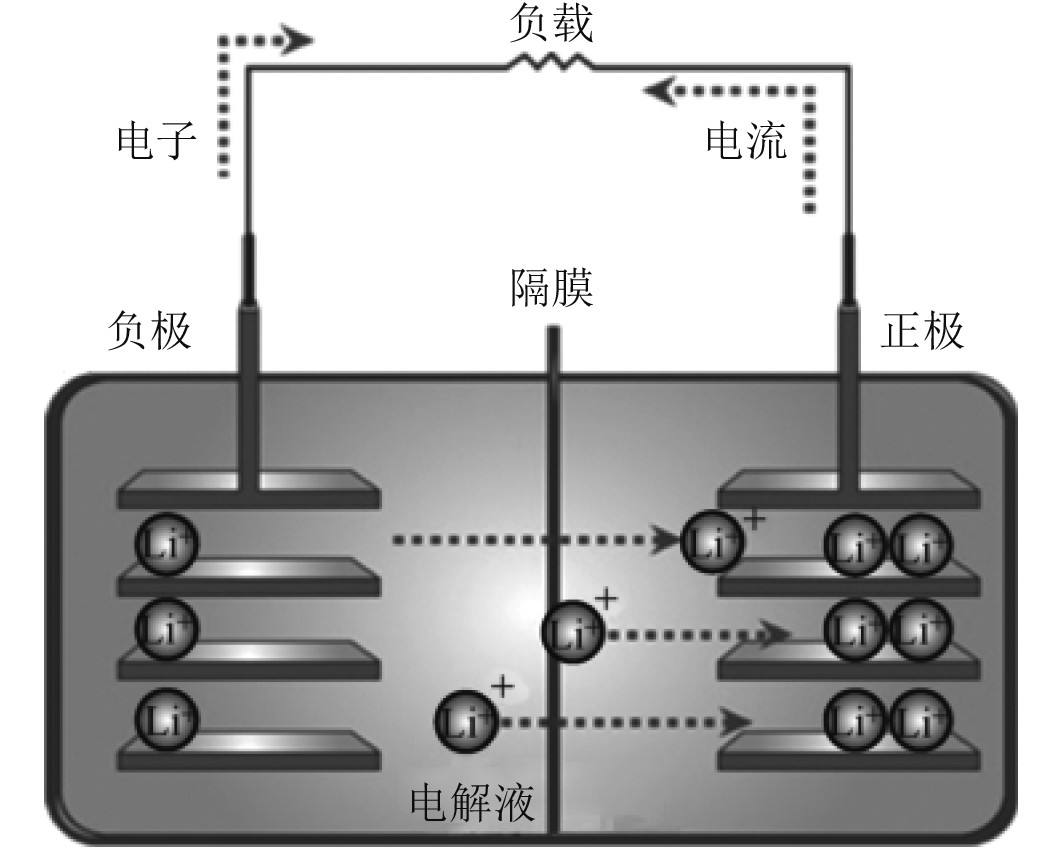
1 锂电池工作原理分析 1.1 锂电池充放电原理分析锂电池主要结构由正极材料、负极材料、隔膜和电解液4个部分组成。正极材料大多为锂化合物,为电池提供锂离子。负极材料主要是石墨,用于存储锂离子,实现充放电过程中锂离子的嵌入和脱嵌。隔膜是一种复合膜绝缘体,阻止电子通过电解液在正负极之间自由穿行。锂电池充放电过程中,锂离子能够通过隔膜,而电子脱离自身元素后通过外部电路到达新载体(正极材料或负极材料)。电解液是电池中锂离子传输的载体,通常由锂盐和有机溶剂组成,实现锂离子在电池正负极之间的传导。图1为对锂电池的内部结构原理,电池内包含锂离子、金属离子、氧离子和碳层。电池通过电池内部的锂离子移动来实现充放电反应,如图2所示,隔膜提供离子通道,同时使电池两极分开,避免两极接触造成短路。

|
图 1 锂电池结构原理图 Fig. 1 Lithium battery structure schematic diagram |
|
图 2 锂离子电池工作原理示意图 Fig. 2 The working principle of lithium ion battery |
总的来说,锂电池内部电化学反应过程为锂离子在正、负两极之间的来回交换,其正负极反应和总反应方程式如下所述[1]:
正极反应方程式为
| $ {\text{Li}}{{\text{M}}_x}{{\text{O}}_y} = {\text{L}}{{\text{i}}_{(1 - x)}}{{\text{M}}_x}{{\text{O}}_y} + x{\text{L}}{{\text{i}}^ + } + x{{\mathrm{e}}^ - } $ | (1) |
负极反应方程式为
| $ n{\text{C}} + x{\text{L}}{{\text{i}}^ + } + x{{\mathrm{e}}^ - } = {\text{L}}{{\text{i}}_x}{{\text{C}}_n} $ | (2) |
电池总反应方程式为
| $ {\text{Li}}{{\text{M}}_x}{{\text{O}}_y} + n{\text{C}} = {\text{L}}{{\text{i}}_{(1 - x)}}{{\text{M}}_x}{{\text{O}}_y} + {\text{L}}{{\text{i}}_x}{{\text{C}}_n} $ | (3) |
上述3个方程式中M为正极锂化合物中的金属离子。
1.2 锂电池产热和热失控机理分析任何化学反应都会伴随着热量的吸收或放出,锂电池充放电过程中的氧化还原反应也难以避免地产生热量。电极、电解液等材料在高温下的副反应会损害电池健康状况,甚至发生严重的热失控造成火灾及爆炸。为此有必要进行正常工况下的热机理分析。
充电过程中,正极锂原子发生氧化反应,属于吸热反应(Qr<0);与之互为逆过程的放电过程则属于吸热反应(Qr>0),且放出的热量与吸收的热量在数值上相等,总反应热的计算公式如下[2]:
| $ {Q_{{r}}} = nmQI/MF。$ | (4) |
式中:n为单体电芯数量;m为正负极材料质量,g;Q为正负极发生电化学反应所发出的热量之和,J;I为充放电电流大小,A;M为正负极摩尔质量,g/mol;F为法拉第常数,F=96484.5 C/mol。
另外,由于锂离子电池内部存在欧姆内阻,锂离子在正负极和电解液等中迁移克服阻力产生欧姆热,计算公式如下[3]:
| $ {Q_\Omega } = {I^2}{R_s} 。$ | (5) |
式中:I为充放电电流大小,A;Rs为总欧姆内阻。
此外,当锂离子电池不工作时,正负电极处于平衡状态,两者之间的电势差即为开路电压。当电池工作时会有一定的电流流过电极,正负电极平衡状态被打破,此时电压偏离平衡状态时开路电压的现象称之为极化。极化主要包括欧姆极化、电化学极化和浓度差极化。欧姆极化是由电池内阻引起,所产生的欧姆热见式(5)。电化学极化主要由正负极活性物质的电化学反应迟缓,反应速率小于电子运动速率造成;浓度差极化是由锂离子迁移速度小于正负极电化学反应速度引起的,它们所产生的热量称为极化热[4]。极化热与温度、电流等因素有关,其表达式为[5]:
| $ {Q_j} = {I^2}{R_j}。$ | (6) |
式中:I为充放电电流大小,A;Rj为等效极化内阻。
通常情况下电池的极化内阻无法直接获取,且会随放电深度的改变而变化。
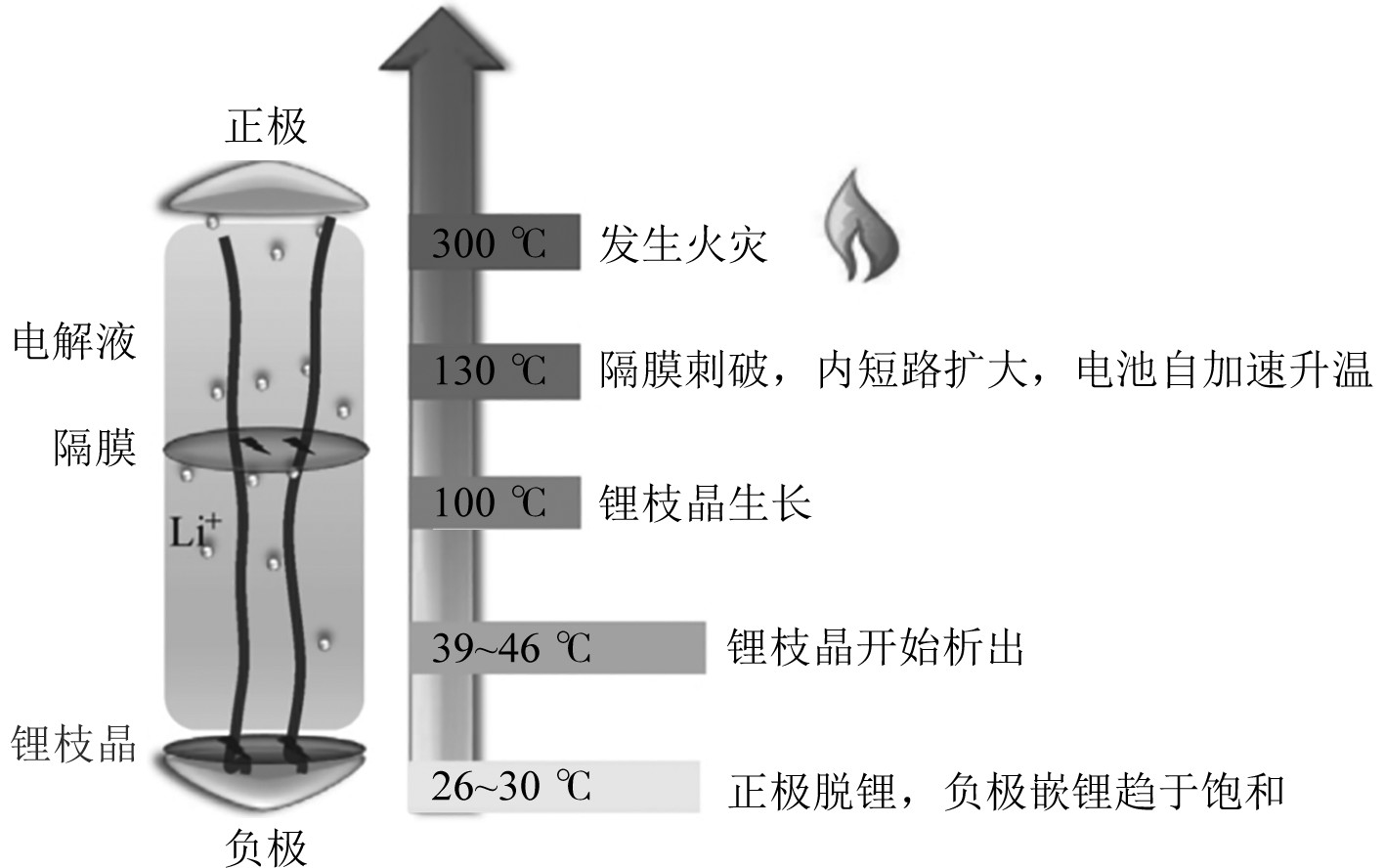
大量研究表明,当锂离子电池整体温度升高时,电池内部会引发一系列放热反应,从而导致电池温度持续升高。同时,高温又会促进放热反应的进行,最终电池温度失去控制[6]。其基本发生发展阶段如图3所示。
|
图 3 锂电池热失控基本发展阶段 Fig. 3 Basic development stage of thermal runaway of lithium battery |
第一阶段:正常充电时,电池表面温度较低(26~30℃)。锂离子从正极脱出,在负极嵌入,电池的电压缓慢升高[7]。当电池电压为3.6 V左右时,电池负极嵌锂趋于饱和。
第二阶段:轻微过充时,电池表面温度升高显著(39~46℃)。伴随充电过程持续进行,负极嵌锂过饱和,锂离子会在负极表面析出锂枝晶。由于正极脱锂超出正常范围,锂枝晶更容易析出在与正极相近的负极边缘表面。已有研究表明,负极表面析出的锂枝晶,会与负极的有机黏结剂发生反应生成氢气[8]。
第三阶段:锂枝晶与电解液发生副反应生成热量,导致电池内部温度升高,当温度超过90℃时,SEI膜会发生陆续分解,并产生C2H4、CO2、O2气体[9]。
随着电池内部温度的持续升高,电解液开始参与绝大多数副反应,如电解液与嵌锂负极、正极、金属锂等反应。电解液与嵌锂负极反应的产气机理与电解液的成分有关,不同电解液成分产生的气体成分和含量有所不同[10]。
第四阶段:当锂离子电池内部温度达到130℃左右时,隔膜熔融,引发电池大面积内短路并产生热量,热量集聚引起的高温对内部反应形成正反馈,电池开始发生不可控的自加速反应,进一步造成电池的温度上升,最终导致火灾甚至爆炸事故[11]。
一般由单体电池热失控所造成的危害有限,但在储能系统应用场景下,单体电池数量多、排列紧密,当某一个单体电池发生热失控后,其产生的热量可能会传导至周围电池,使得热失控发生蔓延,所造成的危害将被扩大。研究单体电芯在不同环境温度、不同放电倍率的工作温度是储能系统设计的基础和出发点,为此,本文将针对不同电芯进行不同场景的温度测试,通过实验获取真实有效温度数据,为储能模组及系统的热管理设计提供支持。
2 锂电池温度场测试分析 2.1 测试方法和测试过程本文以目前较为流行的280 Ah磷酸铁锂电芯为研究对象,在封闭的防爆温度箱(体积为1 m3且温度、湿度可控)内进行测试。温度箱可通过温湿度表监控并调整箱内温度。实验在环境温度分别为25℃、35℃、45℃,放电倍率分别为0.5C和0.65C条件下进行两充两放的充放电温升测试。设定7个测温区域,分别为正负极柱、上盖板、极柱下1/3、宽侧的中间部位、底部中间,通过无线数据采集仪采集温度数据。
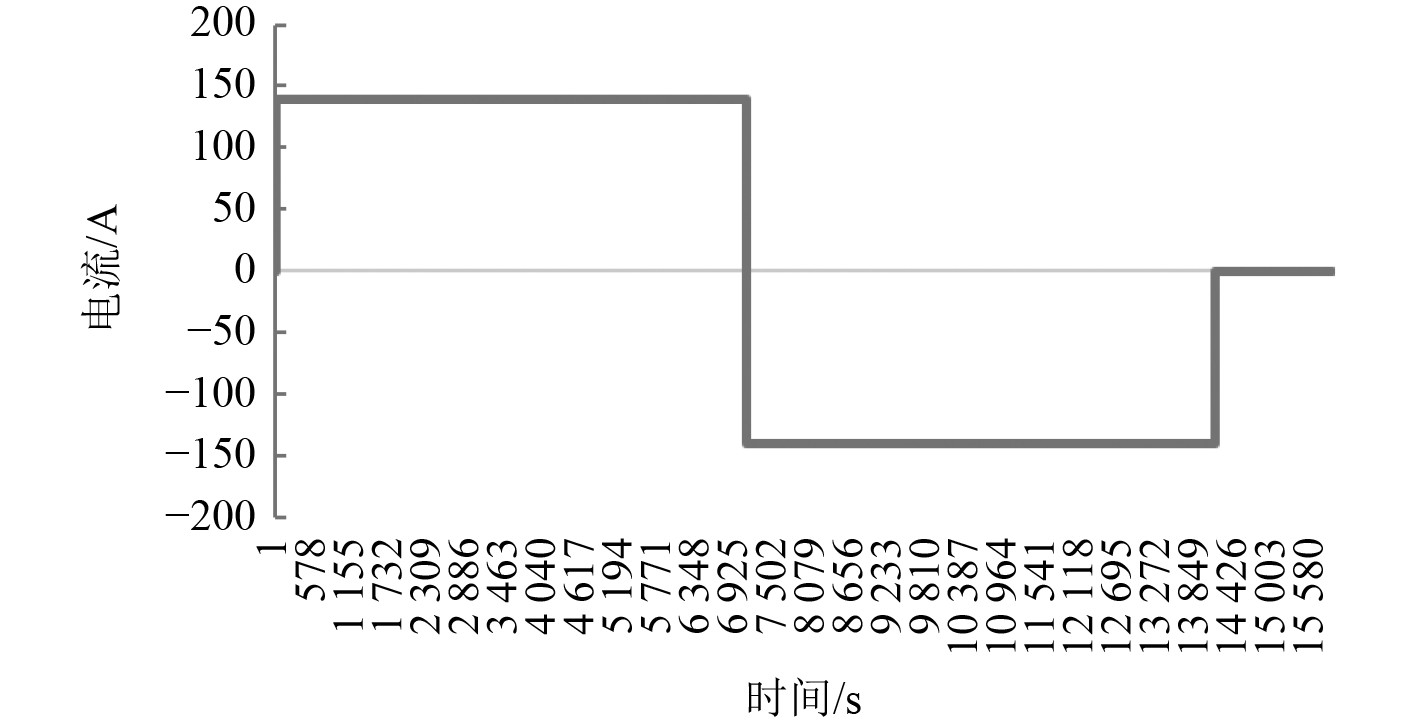
测试前先将电芯余电以0.1C倍率放空,静置1 h后在25℃下进行0.5 C(140 A)恒流充放电实验,起始电压为2.68 V,充电至截至电压3.65 V后静止30 min,该过程电压、电流随时间变化曲线如图4和图5所示。

|
图 4 25℃0.5C充放电电压变化曲线图 Fig. 4 Chart of charge and discharge voltage change curve at 25°C 0.5C |
|
图 5 25℃0.5C充放电电流变化曲线图 Fig. 5 Charging and discharging current change curve at 25°C 0.5C |
静止30 min后重复进行5次上述充放电实验,然后在同样环境温度(25℃)下进行0.65 C(182 A)恒流充放电实验并重复进行5次。
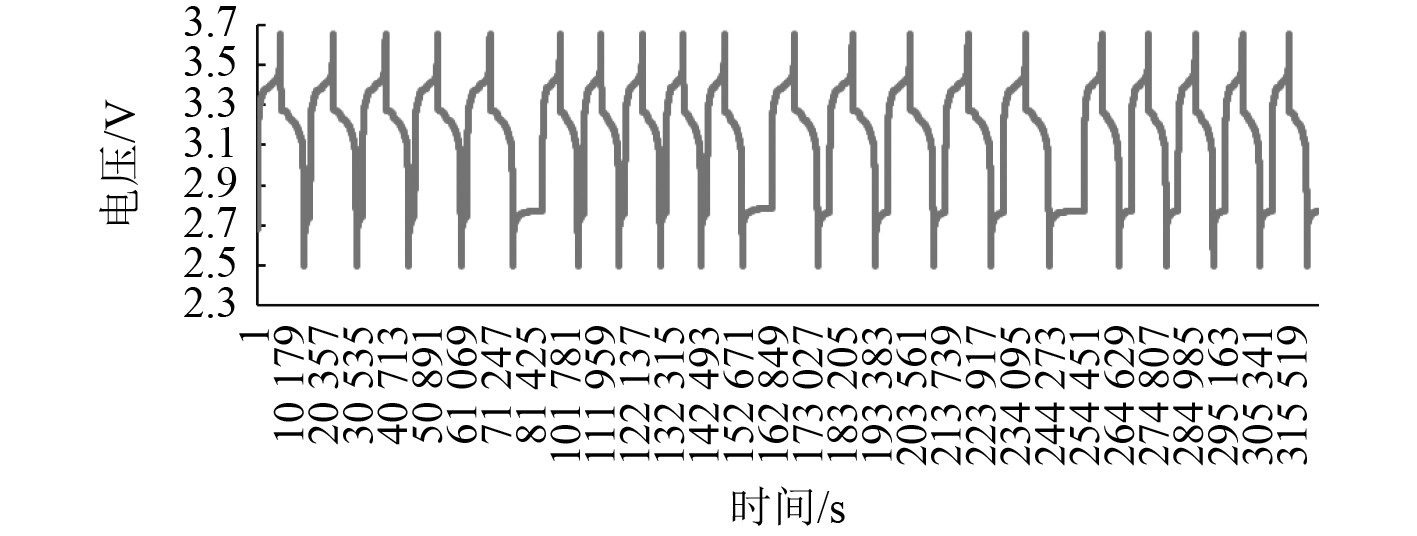
再重复进行25℃下0.5 C和0.65 C实验,数据显示电池的充放电电压、电流和7个温度测量点的温度随时间出现周期性、重复性变化,与实验设计的重复性一致。多周期的电压、电流、温度变化曲线如图6~图8所示。
|
图 6 25℃变倍率充放电电压变化曲线图 Fig. 6 Chart of charge and discharge voltage change at 25°C variable rate |

|
图 7 25℃变倍率充放电电流变化曲线图 Fig. 7 Chart of charge-discharge current at variable rate at 25°C |

|
图 8 各测温点25℃变倍率充放电温度变化曲线图 Fig. 8 The temperature change curve of 25°C variable ratecharge and discharge |
由图可知,实验过程中对于同一电芯0.5 ℃充电最高温度32.5 ℃(0.2)、放电最高温度33.6 ℃(0.2),0.65C充电最高温度33.9 ℃(0.2)、放电最高温度35.2 ℃(0.2),重复性较高、一致性较好。
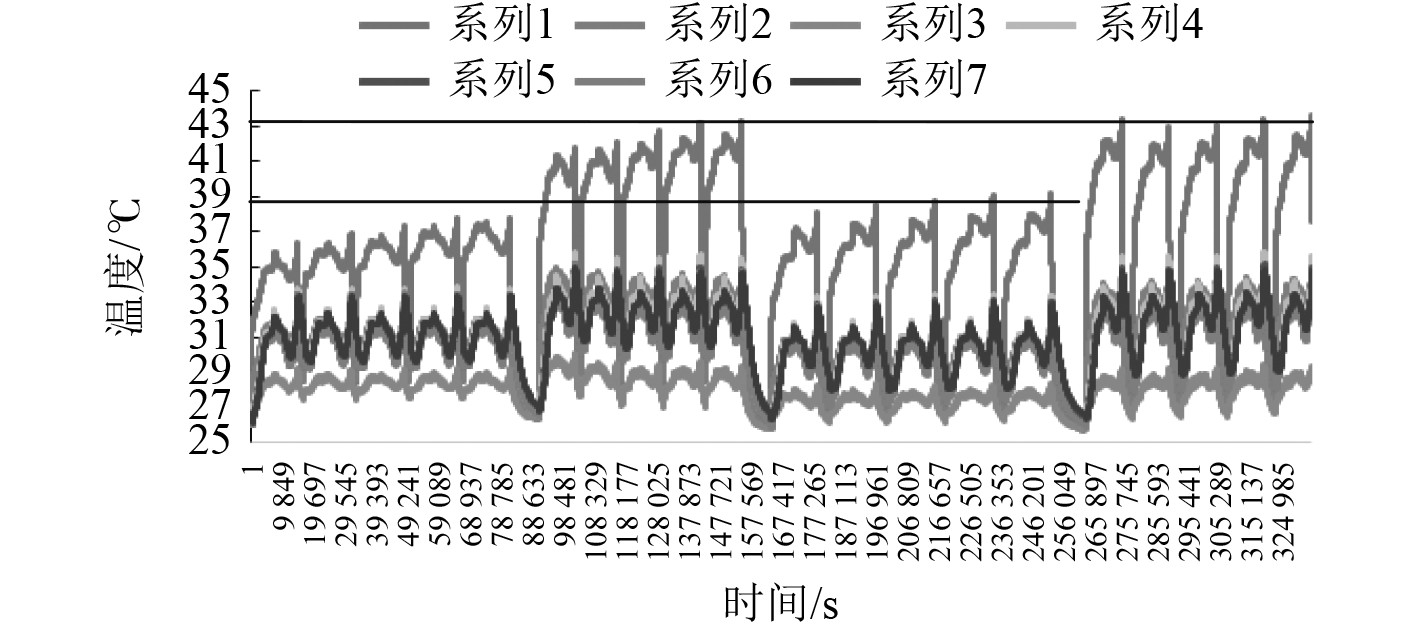
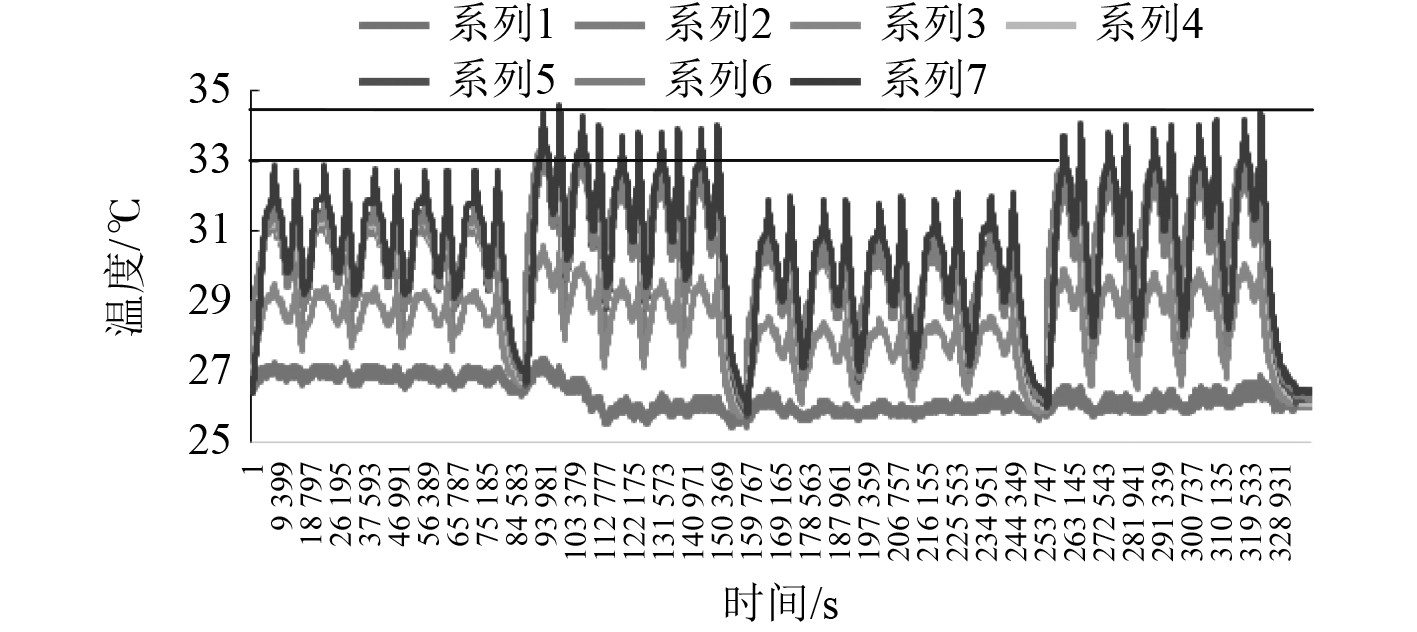
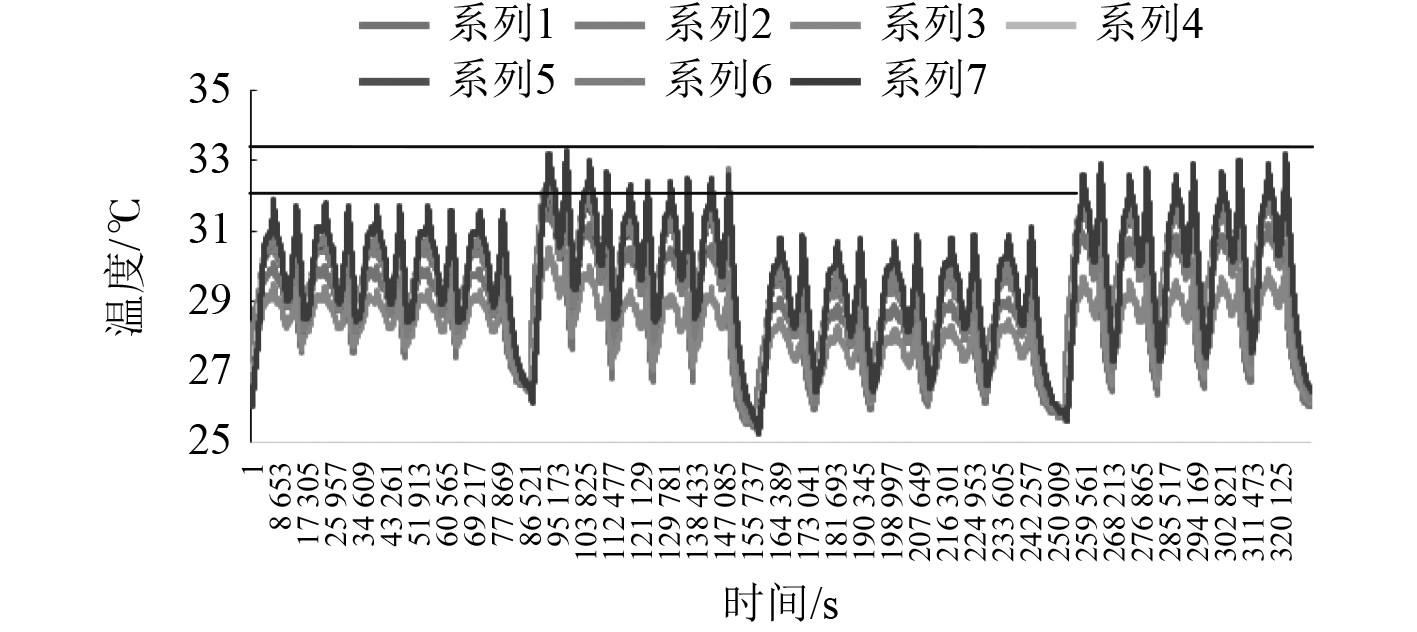
2.2 不同电芯的测试数据分析选取3种不同品牌的280 Ah电芯A、B、C,每个品牌分别选取2个电芯(A1/A2、B1/B2、C1/C2),分别在环境温度25℃、以放电倍率0.5C和0.65C恒流充放电实验,结果表明对于A品牌不同批次的电芯温度变化在2℃左右,电芯底面温度较高。对于B品牌不同批次的电芯温度变化大,在9℃左右,电芯极柱温度较高。对于C品牌不同批次的电芯温度变化在2℃左右,电芯底面温度较高。充放电温度变化详细数据及变化趋势如图9~图14所示。

|
图 9 A1芯25℃变倍率充放电温度变化曲线图 Fig. 9 A1 core 25°C variable rate charge and discharge temperature change curve |

|
图 10 A2芯25℃变倍率充放电温度变化曲线图 Fig. 10 A2 core 25°C variable rate charge and dischargetemperature change curve |
|
图 11 B1芯25℃变倍率充放电温度变化曲线图 Fig. 11 B1 core 25°C variable rate charge and dischargetemperature change curve |

|
图 12 B2芯25℃变倍率充放电温度变化曲线图 Fig. 12 B2 core 25°C variable rate charge and dischargetemperature change curve |
|
图 13 C1芯25℃变倍率充放电温度变化曲线图 Fig. 13 C1 core 25°C variable rate charge and dischargetemperature change curve |
|
图 14 C2芯25℃变倍率充放电温度变化曲线图 Fig. 14 C2 core 25°C variable rate charge and dischargetemperature change curve |
对于同一电芯在环境温度25℃、35℃、45℃时,均以0.5 C(140 A)进行2次恒流充放电实验,温度变化趋势如图15~图17所示。

|
图 15 25℃0.5C充放电温度变化曲线图 Fig. 15 Chart of charge and discharge temperature change at 25°C 0.5C |

|
图 16 35℃0.5C充放电温度变化曲线图 Fig. 16 Chart of charge and discharge temperature change at 35°C 0.5C |

|
图 17 45℃0.5C充放电温度变化曲线图 Fig. 17 45°C 0.5C charge and discharge temperaturechange curve diagram |
结果表明,电芯在25℃充放电过程中,温度变化呈现峰谷状,较为稳定,一致性较好,充放电最高温度分别稳定在极柱位置和底部位置,分别为32.5℃和33.6℃。环境温度为35℃和45℃时,充放电时,温度较高且变化较为平坦,最高温度基本一致分别为43℃和49.2℃。环境温度为35℃充放电时,最高温度出现在正极位置,其次为底部位置;环境温度为45℃充放电时最高温度出现在正极位置,其次为负极位置。
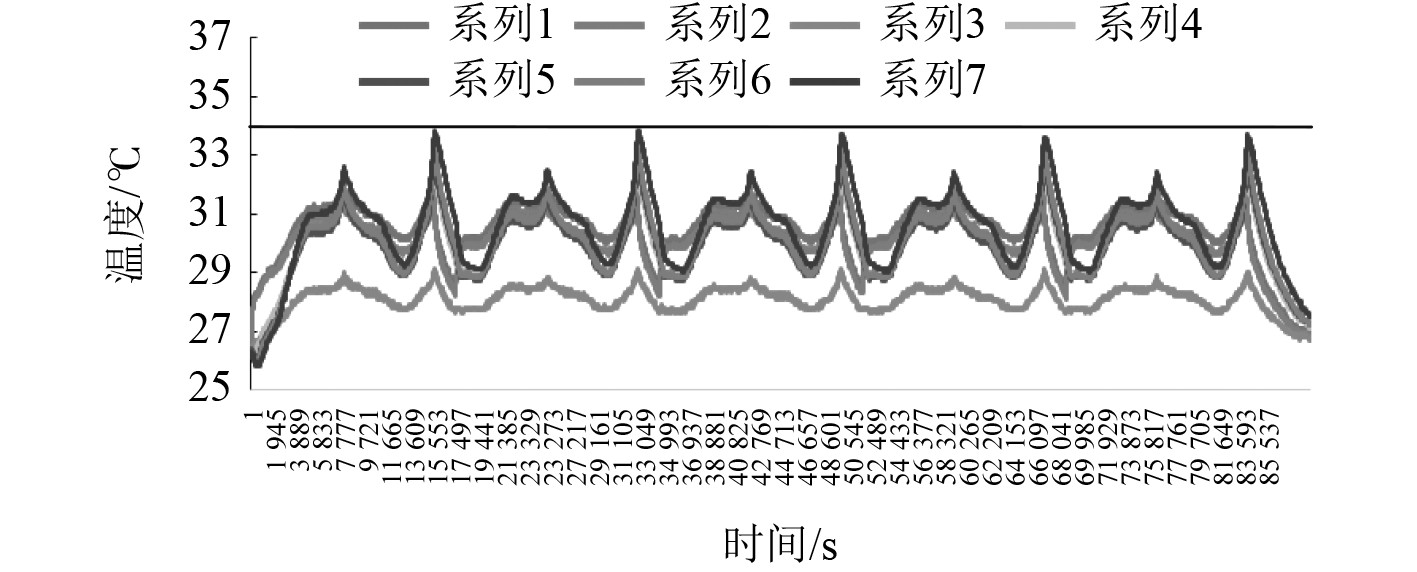
2.4 不同放电倍率的测试数据分析对于同一电芯在环境温度25℃、35℃、45℃时,以0.5C和0.65C进行恒流充放电实验,温度变化趋势如图18~图23所示。
|
图 18 25℃0.5C充放电温度变化曲线图 Fig. 18 Chart of charge and discharge temperaturechange at 25°C 0.5C |
|
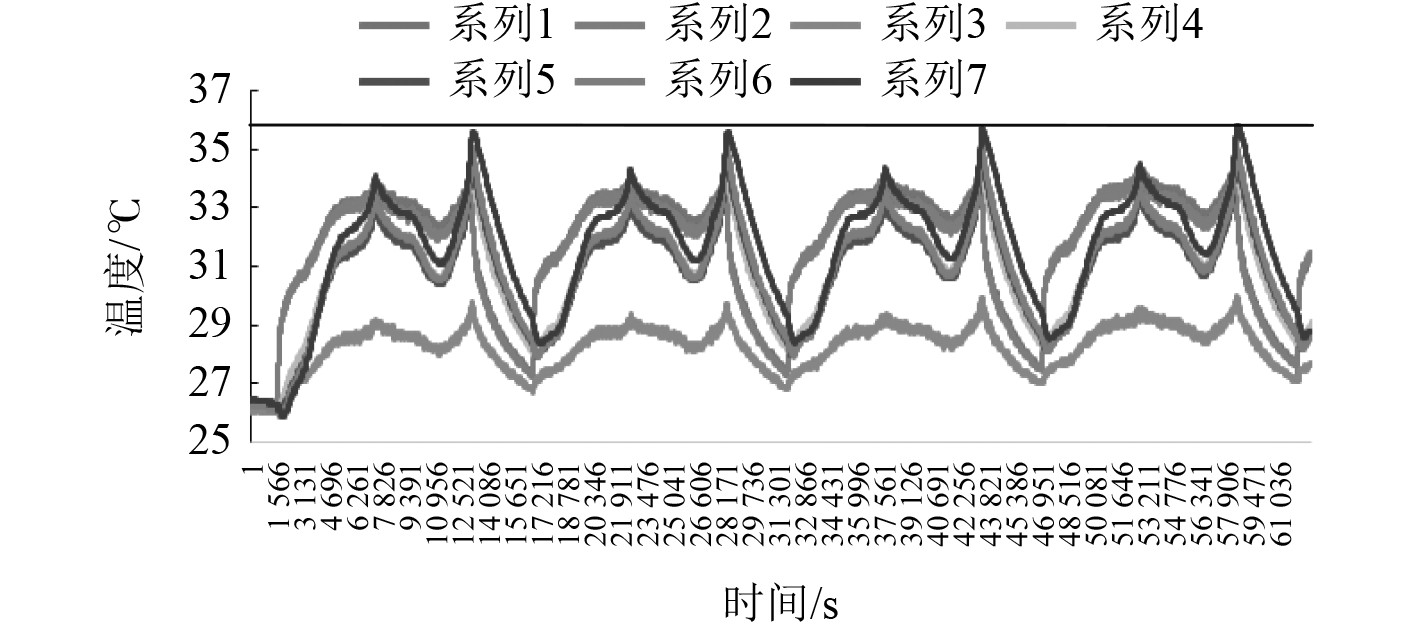
图 19 25℃0.65C充放电温度变化曲线图 Fig. 19 Chart of charge and discharge temperature change at 25°C 0.65C |
|
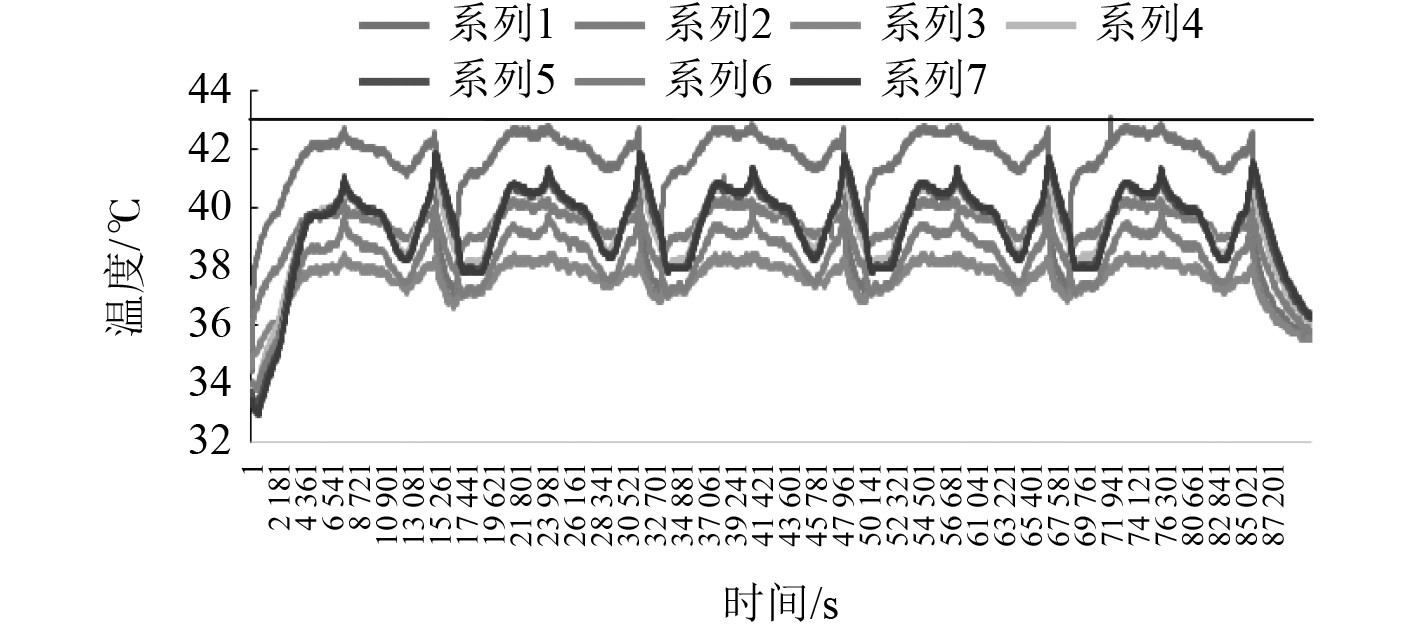
图 20 35℃0.5C充放电温度变化曲线图 Fig. 20 Chart of charge and discharge temperaturechange at 35°C 0.5C |
|
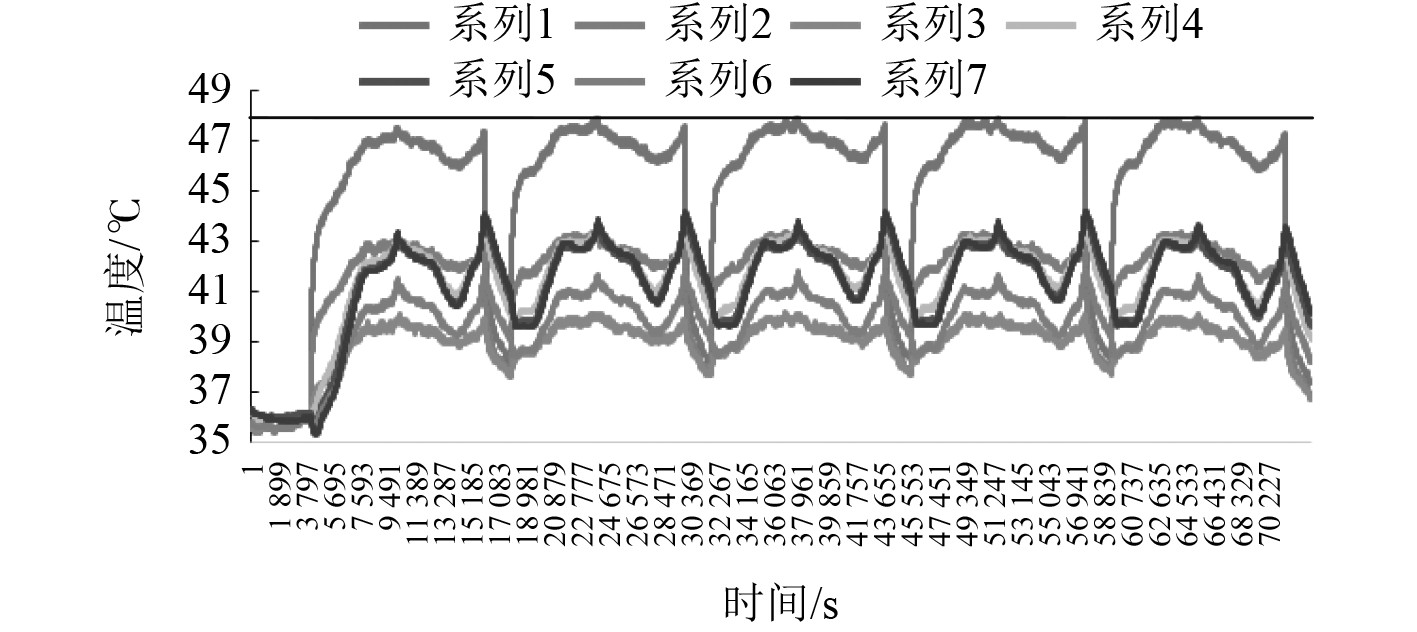
图 21 35℃0.65C充放电温度变化曲线图 Fig. 21 Chart of charge and discharge temperature change at 35°C 0.65C |
|
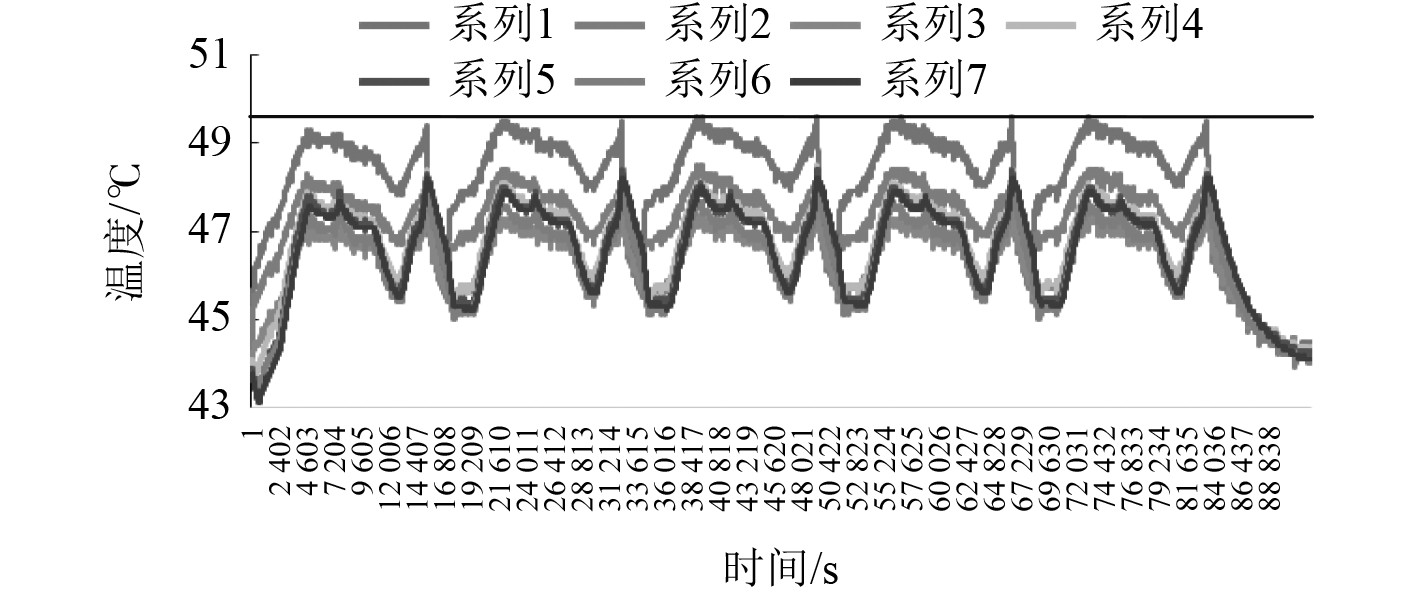
图 22 45℃0.5C充放电温度变化曲线图 Fig. 22 Chart of charge and discharge temperaturechange at 45°C 0.5C |
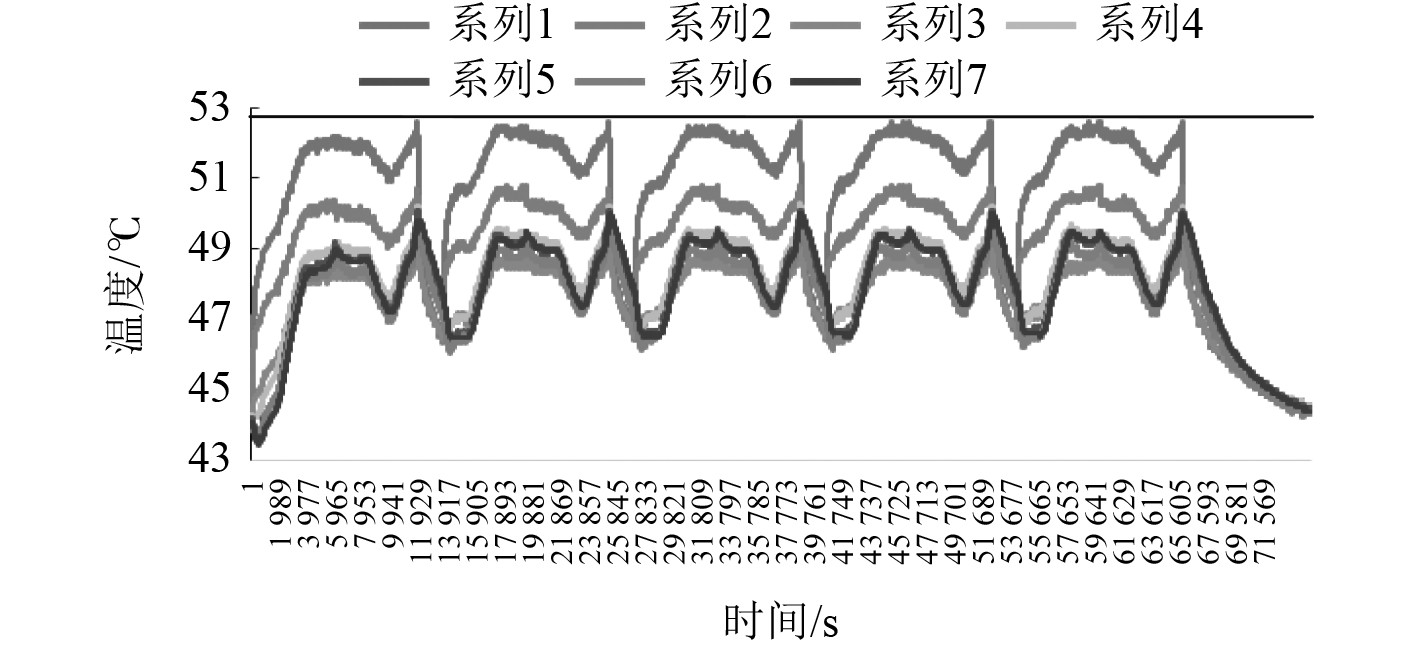
|
图 23 45℃0.65C充放电温度变化曲线图 Fig. 23 Chart of charge and discharge temperaturechange at 45°C 0.65C |
结果表明,电芯在高倍率充放电时,温升出现明显增加。在25℃时,0.5C和0.65C充放电过程中,温度变化呈现峰谷状,较为稳定,一致性较好,最高温度为33.6℃和35.4℃。35℃和45℃不同倍率充放电时,温度较高且变化较为平坦,最高温度基本一致分别为43℃和48℃、49.2℃和52.8℃。
3 结 语本文在分析锂电池工作原理和产热机理的基础上得出温度场分析在锂电池热管理和防热失控中的重要性。基于此重要性,针对280 Ah磷酸铁锂电芯进行不同电芯品牌、不同生产批次在不同环境温度、不同充放电倍率下的温度测试研究,研究结果表明:
1)不同品牌、不同批次的电芯充放电过程中,温度差异基本在2℃左右,个别会出现较大温升差异。电芯制造或者选取时应注意一致性控制。
2)电芯底部和极柱位置是高温度集中区域。冷却系统和冷却方式着重考虑区域。
3)环境温度升高,电芯充放电时温升较大。35℃和45℃充放电时,温度较高且变化较为平坦。
4)不同倍率充放电时,温升变化状况不同。高倍率充放电时,温升出现明显增加。
5)电芯在25℃、0.5C(标称工况)充放电倍率工作状况较为稳定。在船舶和港口储能系统中以确保电芯尽量在此状况下工作。
| [1] |
惠东, 金翼, 于冉. 电力储能用锂离子电池技术(第1版)[M]. 北京: 机械工业出版社, 20230203. 40−60.
|
| [2] |
金阳. 锂离子电池储能电站早期安全预警及防护(第1版)[M]. 北京: 机械工业出版社, 20211201. 60−80.
|
| [3] |
张兵, 叶树亮, 许金鑫, 等. 基于等温量热的锂离子电池熵热系数测量[J]. 电池, 2023, 53(4): 378-382. |
| [4] |
司云森, 杨显万. 电化学极化过程实验数据处理分析的研究[J]. 昆明理工大学学报(理工版), 2003(1): 164-167. |
| [5] |
白龙, 倪培永, 朱建新, 等. 混合动力汽车用锂电池组散热系统研究[J]. 电源技术, 2019, 43(11): 1813-1816. |
| [6] |
金远, 韩甜, 韩鑫, 等. 锂离子电池热管理综述[J]. 储能科学与技术, 2019, 8(S1). DOI:10.19799/j.cnki.2095-4239.2019.0218 |
| [7] |
康慨, 戴受惠, 万玉华. 固相配位化学反应法合成LiMn2O4的研究[J]. 功能材料, 2000, 31(3): 283-286. KANG Kai, DAI Shouhui, WAN Yuhua. Synthesis of LiMn2O4 by solid-state coordination chemical reaction[J]. Functional Materials, 2000, 31(3): 283-286. |
| [8] |
郑志坤. 磷酸铁锂储能电池过充热失控及气体探测安全预警研究[D]. 郑州: 郑州大学, 2021.
|
| [9] |
廉洁, 封星, 刘一凡, 等. 锂电池动力船舶电池热失控释放气体电池舱内扩散输运数值模拟研究[J]. 大连海事大学学报, 49(3): 122−128.
|
| [10] |
郎春艳. 低温环境下锂离子电池组热管理系统研究[D]. 广州: 华南理工大学, 2023.
|
| [11] |
徐振恒, 周晓燕, 付佳龙, 等. 锂离子电池热失控及其预警方法[J/OL]. 科学通报: 1−16 [2023-10-11].
|
 2024, Vol. 46
2024, Vol. 46
