五氯丙烷是合成环保型低碳制冷剂的重要原料中间体[1-3],为无色、透明、具有强刺激性气味的液体;不溶于水,易溶于乙醚,可混溶于多数有机试剂;主要作用是防治农作物害虫的有效熏蒸剂,在常温常压下稳定;经吸入、食入吸收,对肝脏有损害作用,具有较强的腐蚀性、刺激性,可致人灼伤。近些年来对五氯丙烷的研究一直停留在制备上面[4-8],由于五氯丙烷在市场上无法获得其标准品,所以在检测方法的研制开发上面欠缺。目前,国内仅在《生活饮用水卫生标准》(GB 5749-2006)[9]附录A中规定五氯丙烷的标准限值为0.03 mg/L,与《生活饮用水卫生标准》(GB 5749-2006)[9]标准配套的《生活饮用水标准检验方法》(GB/T 5750-2006)[10]也无五氯丙烷的推荐检测方法,国外也未见有权威机构制定的标准方法。国内外文献查询结果发现,只有国内少数关于1, 1, 2, 3, 3-五氯丙烷的方法研究报道[11],1, 1, 1, 3, 3-五氯丙烷和1, 1, 1, 2, 3-五氯丙烷的方法研究尚未见相关报道,因此建立饮用水中3种五氯丙烷的标准检验方法具有重要意义,可以填补方法空白。
顶空—气相色谱法(HS-GC法)和吹扫捕集—气相色谱质谱联用法(吹扫捕集-GC-MS法)已经成为挥发性有机物测试领域最为常用的分析技术[12-14],两种方法均具有操作简捷、无溶剂污染、可测定范围宽等优点;本文根据五氯丙烷的物理化学性质,结合国内《生活饮用水标准检验方法》(GB/T 5750.8-2006)附录A和美国国家环保署524.2方法[15],分别建立了顶空—气相色谱法(配ECD检测器)和吹扫捕集—气相色谱质谱联用法来测定饮用水中的3种五氯丙烷,并将两种方法的研究结果进行比较。
1 材料与方法 1.1 仪器与试剂 1.1.1 仪器气相色谱仪[7890B,附电子捕获检测器(ECD),中国安捷伦公司];自动顶空进样器(7697A,中国安捷伦公司);HP-5 MS色谱柱(30 m×0.25 mm×0.25 μm,美国安捷伦公司);气相色谱质谱联用仪(7890B/7000D,美国安捷伦公司);ATOMX吹扫捕集仪(配5 mL吹扫管,美国Tekmar公司);HP-624 MS色谱柱(30 m×0.25 mm×1.4 μm,美国安捷伦公司);XSE205DU十万分之一天平(瑞士METTLER TOLEDO公司)。
1.1.2 试剂标准品:1, 1, 1, 3, 3-五氯丙烷(纯度≥98%)、1, 1, 1, 2, 3-五氯丙烷(纯度≥97%)、1, 1, 2, 3, 3-五氯丙烷(2.0 g/L);内标:氟苯(纯度≥99%);以上标准品和内标均购于上海安谱公司。甲醇(色谱纯,上海安谱公司);抗坏血酸(优级纯,上海安谱公司);高纯氮气(99.999%);高纯氦气(99.999%);高纯水:不含有机物。
1.2 标准曲线的配制 1.2.1 标准储备液的配制1, 1, 1, 3, 3-五氯丙烷标准储备溶液[ρ(1, 1, 1, 3, 3-五氯丙烷)=1.0 g/L]:准确称取0.010 20 g 1, 1, 1, 3, 3-五氯丙烷(98%),于10 mL容量瓶中,甲醇定容至刻度。1, 1, 1, 2, 3-五氯丙烷标准储备溶液[ρ(1, 1, 1, 2, 3-五氯丙烷)=1.0 g/L]:准确称取0.010 31 g 1, 1, 1, 2, 3-五氯丙烷(97%),于10 mL容量瓶中,甲醇定容至刻度。内标物氟苯的制备:准确称取0.050 5 g氟苯(99%),于10 mL容量瓶中,甲醇定容至刻度,此溶液为5.0 g/L;临用前稀释为5.0 mg/L。
1.2.2 混合标准工作溶液的配制HS-GC法:根据1, 1, 1, 3, 3-五氯丙烷、1, 1, 1, 2, 3-五氯丙烷以及1, 1, 2, 3, 3-五氯丙烷的响应值,取相应体积的1, 1, 1, 3, 3-五氯丙烷、1, 1, 1, 2, 3-五氯丙烷以及1, 1, 2, 3, 3-五氯丙烷标准储备液于10 mL容量瓶中,用甲醇定容至刻度,得到相应浓度分别为2.0、2.0、10 mg/L的标准使用溶液。临用前用纯水配制1, 1, 1, 3, 3-五氯丙烷和1, 1, 1, 2, 3-五氯丙烷的质量浓度分别为0.00、0.020、0.10、0.20、0.50、1.0、2.0和5.0 μg/L;1, 1, 2, 3, 3-五氯丙烷的质量浓度分别为0.00、0.10、0.50、1.0、2.5、5.0、10和25 μg/L标准系列;取10.0 mL该系列标准溶液于20 mL顶空瓶中,密封混匀。吹扫捕集-GC-MS法:取相应体积的1, 1, 1, 3, 3-五氯丙烷、1, 1, 1, 2, 3-五氯丙烷、1, 1, 2, 3, 3-五氯丙烷标准储备液于10 mL容量瓶中,用甲醇定容至刻度,得到相应浓度均为5.0 mg/L的标准使用溶液。临用前用纯水进一步稀释得到0.00、0.10、0.20、0.50、1.0、2.0、5.0和10 μg/L标准系列。同时加入内标氟苯溶液,使其浓度为5.0 μg/L。
1.3 样品采集及前处理 1.3.1 样品采集100 mL棕色采样瓶,采样时先加入0.10 g抗坏血酸,取水至满瓶,瓶中不留顶上空间和气泡,加盖密封,保存在0 ℃~4 ℃冰箱中,48 h内完成分析。
1.3.2 样品前处理HS-GC法样品前处理:取水样10.0 mL于20 mL顶空瓶中,密封摇匀,放入顶空进样器,待测。吹扫捕集-GC-MS法样品前处理:40 mL吹扫瓶加满样品,同时加入内标氟苯溶液,使其浓度为5.0 μg/L;旋紧瓶盖放在吹扫捕集进样器上,待测。
1.4 方法 1.4.1 HS-GC法顶空进样器条件:平衡温度为70 ℃,定量管温度为90 ℃,传输线温度为100 ℃;样品平衡时间为15 min,进样时间为1 min。顶空进样系统采用中速振荡,进样量1.0 mL。色谱条件:气相色谱进样口温度250 ℃,分流比10 :1;柱温采用程序升温:60 ℃(保持1 min),以15 ℃/min升至180 ℃(保持1 min);恒流模式:2 mL/min;检测器温度300 ℃,尾吹60 mL/min。
1.4.2 吹扫捕集-GC-MS法吹扫捕集条件:吹扫取样量为5 mL;吹扫气体为高纯氮气;吹扫流量为50 mL/min;吹扫时间为11 min;吹扫温度为室温;解析温度为180 ℃;解析时间为3 min;解析后捕集阱在280 ℃焙烤2 min,焙烤流量200 mL/min。气相色谱条件:进样口温度为250 ℃,分流比为30:1;柱温采用程序升温:50 ℃(保持1 min),以10 ℃/min升至180 ℃(保持1 min);恒流模式:1 mL/min。质谱条件:离子源为电子轰击源(EI),离子源温度为230 ℃;传输线温度为200 ℃;电子轰击能量为70 eV;采用全扫描模式进行样品定性,选择离子监测模式进行定量。化合物经气相色谱、质谱条件优化后的保留时间、定量离子、定性离子信息见表 1。
| 化合物 | CAS号 | 分子量 | 保留时间/min | 定量离子 | 定性离子 |
| 1, 1, 1, 3, 3-五氯丙烷 | 13253-23-3 | 216 | 12.421 | 181 | 83,179 |
| 1, 1, 1, 2, 3-五氯丙烷 | 21700-31-2 | 216 | 13.396 | 117 | 119,83 |
| 1, 1, 2, 3, 3-五氯丙烷 | 15104-61-7 | 216 | 14.073 | 143 | 145,96 |
| 氟苯 | 462-06-6 | 96 | 5.185 | 96 | 70 |
1.5 定量分析 1.5.1 HS-GC法
分别取10.0 mL标准系列和水样于20 mL顶空瓶中,密封摇匀,放入顶空进样器。根据保留时间定性,以峰面积对浓度分别绘制标准曲线,进行定量分析。
1.5.2 吹扫捕集-GC-MS法分别取40 mL标准系列和水样于40 mL样品瓶中,同时加入内标氟苯溶液,使其浓度为5.0 μg/L;以组分峰面积与内标的峰面积比值为纵坐标,被测组分的浓度为横坐标,绘制标准曲线,进行定量分析。
1.5.3 检出限的计算配制接近检出限的空白加标样品,连续分析11次,计算其标准偏差s。方法检出限(MDL)按公式(1)计算:
| $ MDL = s \times {t_{(n - 1,0.99)}} $ | (1) |
式中:MDL—方法检出限,μg/L;
s—n次平行测定的标准偏差,μg/L;
n—样品的平行测定次数;
t—自由度为n-1,置信概率为99%时的t分布;由t界值表查得:t=2.76。
1.6 质量控制每批试验均须进行样品空白检测,空白试验结果均须低于方法的检出限。以实际水样为基质,分别加入低、中、高浓度的标准溶液,按照方法进行分析,计算准确度和精密度。准确度用回收率指标表示,加标回收率应在80.0%~120%之间;精密度用相对标准偏差(RSD)表示,RSD应小于20%。内标的定量离子的峰面积在一段时间内保持相对稳定,内标的漂移不得大于50%。
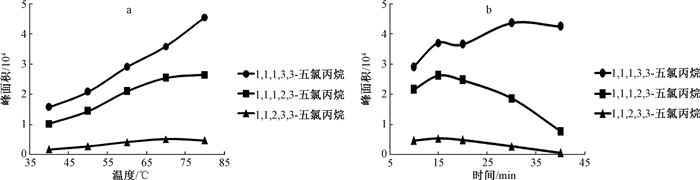
2 结果与讨论 2.1 顶空条件的优化不同的平衡温度和平衡时间会对试验结果有所影响;通过对平衡温度和平衡时间的优化,可最大限度提高方法的准确度和精密度。固定平衡时间为15 min,平衡温度分别设定为40、50、60、70和80 ℃,研究不同平衡温度下混合标样(20 μg/L)的峰面积的变化。结果(图 1a)显示平衡温度在70 ℃以下3种五氯丙烷的峰面积均随平衡温度的升高而增大,平衡温度超过70 ℃,1, 1, 1, 3, 3-五氯丙烷的峰面积继续增大,1, 1, 1, 2, 3-五氯丙烷和1, 1, 2, 3, 3-五氯丙烷的峰面积持平。考虑到平衡温度过高会造成蒸汽中水汽含量升高,进样后对色谱柱和检测器造成影响,故选择平衡温度为70 ℃。
|
| 注:a为平衡温度的优化;b为平衡时间的优化 图 1 顶空条件的优化 |
固定平衡温度为70 ℃,平衡时间分别设定为10、15、20、30和40 min,研究不同平衡时间下混合标样(20 μg/L)的峰面积的变化。结果(图 1b)显示平衡时间从10 min到15 min,3种五氯丙烷的峰面积随平衡时间的延长而增大,平衡时间超过15 min,1, 1, 1, 2, 3-五氯丙烷和1, 1, 2, 3, 3-五氯丙烷的峰面积随平衡时间的延长呈下降趋势,而1, 1, 1, 3, 3-五氯丙烷呈先下降后上升趋势,故选择平衡时间为15 min。
2.2 吹扫条件的优化在吹扫捕集过程中,吹扫效率是被关注的最重要参数,它是指被分析组分能被吹出回收的百分数。影响吹扫效率的因素主要有吹扫温度、吹扫时间、吹扫流量以及化合物在水中的溶解度。本方法针对吹扫温度、吹扫时间和吹扫流量进行了优化。
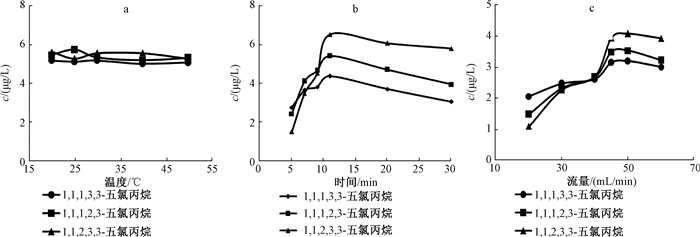
一般情况下,随着吹扫温度的提高,样品中有机化合物的扩散速率加快,有助于待测物的吹脱。固定吹扫时间为11 min,设定吹扫温度分别为20、25、30、40和50 ℃,研究不同吹扫温度下混合标样(5.0 μg/L)检出浓度的变化。结果(图 2a)显示不同吹扫温度下,3种五氯丙烷的检出浓度变化不大,因此选择吹扫温度为室温即可。
|
| 注:a为吹扫温度的优化;b为吹扫时间的优化;c为吹扫流量的优化 图 2 吹扫条件的优化 |
由于五氯丙烷是沸点较高的挥发性卤代烃,对此类挥发物来说,吹扫时间对其吹扫效率有着显著的影响,吹扫时间过短则待测物组分吹脱不完全,吹扫时间过长则试验效率降低。在保持吹扫温度为室温不变的条件下,设定吹扫时间分别为5、7、9、11、20和30 min,研究不同吹扫时间下混合标样(5.0 μg/L)检出浓度的变化。结果(图 2b)显示吹扫时间从5 min到11 min,3种五氯丙烷的检出浓度均随吹扫时间的延长而增大,11 min以后3种五氯丙烷的浓度值随吹扫时间的延长下降,故本试验选择吹扫时间为11 min。
同时吹扫流量的选择与样品中的待测物的浓度、挥发性、样品基质的相互作用以及其在捕集管中的吸附作用大小相关。理论上,吹扫流量越大,吹出效率越高。当吹扫流量太小时,样品组分不能完全吹扫出来。用氦气或氮气吹扫时,一般推荐流量范围(20~60) mL/min。保持吹扫时间为11 min和吹扫温度为室温不变的条件下,设定吹扫流量分别为20、30、40、45、50和60 mL/min,研究不同吹扫流量下混合标样(5.0 μg/L)检出浓度的变化,结果(图 2c)显示在吹扫流量为50 mL/min时,3种五氯丙烷的检出浓度最大,故本实验选择吹扫流量为50 mL/min。
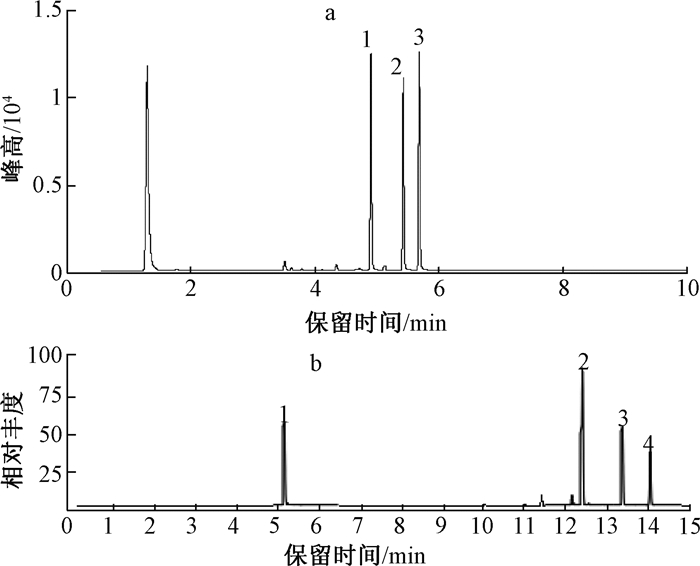
2.3 优化条件下的色谱分离图通过对顶空进样器条件、气相色谱条件、吹扫捕集进样器条件以及质谱条件优化后进行试验得到五氯丙烷标准混合溶液的色谱图和总离子流图(图 3)。图 3a为HS-GC法五氯丙烷的标准色谱图,出峰时间依次为空气峰1.284 min;1, 1, 1, 3, 3-五氯丙烷4.909 min;1, 1, 1, 2, 3-五氯丙烷5.432 min;1, 1, 2, 3, 3-五氯丙烷5.690 min;图 3b为吹扫捕集-GC-MS法五氯丙烷的标准总离子流图,出峰时间依次为氟苯5.185 min,1, 1, 1, 3, 3-五氯丙烷12.421 min,1, 1, 1, 2, 3-五氯丙烷13.396 min,1, 1, 2, 3, 3-五氯丙烷14.073 min。HS-GC法和吹扫捕集-GC-MS法得到的图谱均实现基线分离良好,峰型对称,满足定量分离的基本要求。HS-GC法出峰时间较快,较适合大量样品的分析。
|
| 注:a. HS-GC法色谱图(1-1, 1, 1, 3, 3-五氯丙烷; 2-1, 1, 1, 2, 3-五氯丙烷; 3-1, 1, 2, 3, 3-五氯丙烷);b.吹扫捕集-GC/MS法色谱图(1-氟苯; 2-1, 1, 1, 3, 3-五氯丙烷; 3-1, 1, 1, 2, 3-五氯丙烷; 4-1, 1, 2, 3, 3-五氯丙烷) 图 3 HS-GC法色谱图和吹扫捕集-GC-MS法色谱图 |
2.4 标准曲线、相关系数、检出限及定量限
HS-GC法和吹扫捕集-GC-MS法测定五氯丙烷,两种方法线性范围广,线性良好,相关系数r均大于0.999 0;方法灵敏度高,检出限均小于0.03 μg/L;相比较而言,吹扫捕集-GC-MS法的检出限比HS-GC法低一些,更适合痕量分析(表 2)。
| 目标化合物 | 方法 | 线性范围/ (μg/L) |
回归方程 | 相关系数 | s*/(μg/L) | 检出限/ (μg/L) |
定量限/ (μg/L) |
| 1, 1, 1, 3, 3-五氯丙烷 | HS-GC法 | 0.02~5.0 | y=1 466 x-77.4 | 0.999 5 | 0.001 8 | 0.005 | 0.02 |
| 吹扫捕集-GC-MS法 | 0.10~10 | y=0.390 6 x-0.016 5 | 0.999 5 | 0.001 4 | 0.004 | 0.02 | |
| 1, 1, 1, 2, 3-五氯丙烷 | HS-GC法 | 0.02~5.0 | y=852.3 x-39.3 | 0.999 5 | 0.002 0 | 0.006 | 0.02 |
| 吹扫捕集-GC-MS法 | 0.10~10 | y=0.432 4 x-0.004 8 | 0.999 8 | 0.002 5 | 0.007 | 0.03 | |
| 1, 1, 2, 3, 3-五氯丙烷 | HS-GC法 | 0.10~25 | y=235.2 x-69.5 | 0.999 1 | 0.010 | 0.03 | 0.10 |
| 吹扫捕集-GC-MS法 | 0.10~10 | y=0.271 9 x-0.005 1 | 0.999 5 | 0.002 9 | 0.008 | 0.03 | |
| 注:“*”s为1.5.3中11次平行测定的标准偏差。 | |||||||
2.5 方法的准确度与精密度试验
以自来水(本底为未检出)为基质添加一定浓度的五氯丙烷,配制成低、中、高3个浓度水平的样品,每个浓度点做6个平行样,按照试验方法进行分析,对照标准曲线计算精密度和准确度(表 3),实测浓度值取6次平行测定均值。结果表明,HS-GC法:1, 1, 1, 3, 3-五氯丙烷、1, 1, 1, 2, 3-五氯丙烷、1, 1, 2, 3, 3-五氯丙烷的回收率为86.4%~118%,精密度为1.9%~6.5%。吹扫捕集-GC-MS法:1, 1, 1, 3, 3-五氯丙烷、1, 1, 1, 2, 3-五氯丙烷、1, 1, 2, 3, 3-五氯丙烷的回收率为80.5%~112%,精密度为0.9%~5.6%。
| 化合物 | 本低值/(μg/L) | HS-GC法 | 吹扫捕集-GC-MS法 | ||||||
| 加标浓度/(μg/L) | 平均测定值/(μg/L) | 回收率范围/% | RSD/% | 加标浓度/(μg/L) | 平均测定值/(μg/L) | 回收率范围/% | RSD/% | ||
| 1, 1, 1, 3, 3-五氯丙烷 | 未检出 | 0.10 | 0.11 | 110~116 | 2.9 | 0.50 | 0.42 | 80.5~83.1 | 1.0 |
| 1.0 | 0.96 | 93.9~97.9 | 1.9 | 1.0 | 0.83 | 82.9~84.9 | 0.9 | ||
| 4.0 | 3.8 | 88.5~96.2 | 3.0 | 5.0 | 4.9 | 94.3~102 | 2.8 | ||
| 1, 1, 1, 2, 3-五氯丙烷 | 未检出 | 0.10 | 0.09 | 86.4~92.2 | 2.6 | 0.50 | 0.51 | 100~108 | 2.7 |
| 1.0 | 0.94 | 90.7~98.8 | 3.6 | 1.0 | 1.0 | 99.0~107 | 2.6 | ||
| 4.0 | 3.8 | 91.0~101 | 3.8 | 5.0 | 5.3 | 102~112 | 3.8 | ||
| 1, 1, 2, 3, 3-五氯丙烷 | 未检出 | 0.50 | 0.58 | 108~118 | 3.4 | 0.50 | 0.51 | 97.3~107 | 3.0 |
| 5.0 | 4.8 | 87.8~103 | 6.5 | 1.0 | 0.99 | 95.0~106 | 4.5 | ||
| 20 | 19 | 90.0~105 | 5.6 | 5.0 | 5.2 | 97.0~111 | 5.6 | ||
2.6 实际样品的测定
采用HS-GC和吹扫捕集-GC-MS两种方法同时对研究地区的出厂水和管网末梢水共计21份样品进行测定分析,3种五氯丙烷均为未检出,提示五氯丙烷对研究地区的饮用水造成的影响较小。
3 结论本试验通过优化顶空进样器条件、吹扫捕集进样器条件以及色谱条件,建立了顶空—气相色谱法和吹扫捕集—气相色谱质谱联用法测定饮用水中3种五氯丙烷,并对两种方法的线性范围、检出限、精密度以及准确度进行评价,两种方法均具有检出限低、准确度高、精密度好等特点;使用吹扫捕集-GC-MS法可同时达到定性和定量的目的,可靠性好,而HS-GC法灵敏度高,定量效果也好,且成本低,易于普及;在实际样品检测过程中,可根据实验室的配置来选择合适的分析方法。
| [1] |
余国军, 王爱国, 龚海涛. 1, 1, 1, 3, 3-五氟丙烷的合成技术研究[J]. 有机氟工业, 2011(4): 34-37, 47. (In English: Yu GJ, Wang AG, Gong HT. Study on synthesis of 1, 1, 1, 3, 3-pentafluoropropane[J]. Organo-Fluorine Ind, 2011(4): 34-37, 47.) |
| [2] |
徐桂花, 张彦, 贺辉龙, 等. 1, 1, 1, 3, 3-五氟丙烷的合成研究[J]. 有机氟工业, 2013(2): 1-3. |
| [3] |
穆润敏, 唐平, 熊显云. 一种环保型制冷剂HFO-1234yf生产原料1, 1, 2, 3-四氯丙烯的制备方法[J]. 有机氟工业, 2015(5): 25-28. (In English: Mu RM, Tang P, Xiong XY. Preparation method of 1, 1, 2, 3-tetrachloropropene used as production material of environmentally friendly refrigerant HFO-1234yf[J]. Organo-Fluorine Ind, 2015(5): 25-28.) |
| [4] |
陆明, 汪水旺, 李剑. 1, 1, 1, 3, 3-五氯丙烷的合成工艺[J]. 南京理工大学学报, 2007, 31(3): 385-389. (In English: Lu M, Wang SW, Li J. Synthesis of 1, 1, 1, 3, 3-pentachloropropane[J]. J Nanjing Univ Sci Technol, 2007, 31(3): 385-389. DOI:10.3969/j.issn.1005-9830.2007.03.027) |
| [5] |
刘毓林, 徐卫国, 张勇耀, 等. 1, 1, 1, 3, 3-五氯丙烷的连续制备[J]. 有机氟工业, 2012(4): 26-28. (In English: Liu YL, Xu WG, Zhang YY, et al. Continuous telomerization preparation methods of 1, 1, 1, 3, 3-pentachloropripane[J]. Organo-Fluorine Ind, 2012(4): 26-28.) |
| [6] |
许晓涛, 张未星. 1, 1, 1, 3, 3-五氯丙烷合成的反应动力学[J]. 化工学报, 2014, 65(1): 176-181. (In English: Xu XT, Zhang WX. Kinetics of synthesis of 1, 1, 1, 3, 3-pentachloropropane[J]. CIESC J, 2014, 65(1): 176-181. DOI:10.3969/j.issn.0438-1157.2014.01.022) |
| [7] |
朱宏宇, 周强, 王树华, 等. 氯乙烯与四氯化碳调聚反应生成1, 1, 1, 3, 3-五氯丙烷研究进展[J]. 化工生产与技术, 2013, 20(5): 42-44, 49. (In English: Zhu HY, Zhou Q, Wang SH, et al. Research progress of 1, 1, 1, 3, 3-pentachloropripane telomerization generated by vinyl chloride and carbon tetrachloride[J]. Chem Prod Technol, 2013, 20(5): 42-44, 49. DOI:10.3969/j.issn.1006-6829.2013.05.012) |
| [8] |
杨波, 方敏, 何林, 等. 一种1, 1, 1, 3, 3-五氯丙烷的制备方法研究[J]. 有机氟工业, 2019(2): 11-13. (In English: Yang B, Fang M, He L, et al. A methods of preparing 1, 1, 1, 3, 3-pentachloropripane[J]. Organo-Fluorine Ind, 2019(2): 11-13.) |
| [9] |
中华人民共和国卫生部, 中国国家标准化管理委员会. GB 5749-2006生活饮用水卫生标准[S].北京: 中国标准出版社, 2007.
|
| [10] |
中华人民共和国卫生部, 中国国家标准化管理委员会. GB 5750-2006生活饮用水标准检验方法[S].北京: 中国标准出版社, 2007.
|
| [11] |
魏立菲, 李逸, 刘胜玉. 吹扫捕集-气相色谱-质谱联用法测定饮用水中痕量1, 2-二溴乙烯与五氯丙烷[J]. 水资源保护, 2014(5): 73-76. (In English: Wei LF, Li Y, Liu SY. Determination of trace amount of 1, 2-dibromoethylene and pentachloropropane in drinking water by GC-MS with purge and trap concentrator[J]. Water Resour Prot, 2014(5): 73-76.) |
| [12] |
甘平胜, 黄聪, 于鸿, 等. 顶空毛细管柱气相色谱法测定饮用水中12种挥发性卤代有机物[J]. 中国卫生检验杂志, 2008, 18(10): 2009-2011. (In English: Gan PS, Huang C, Yu H, et al. Determination of twelve volatile halogenated hydrocarbons in drinking water by headspace capillary gas chromatography[J]. Chin J Health Lab Technol, 2008, 18(10): 2009-2011. DOI:10.3969/j.issn.1004-8685.2008.10.026) |
| [13] |
张静芸, 孙仕萍, 杨利军, 等. 顶空气相色谱法测定生活饮用水中的18种挥发性有机物[J]. 中国卫生检验杂志, 2017, 27(4): 477-480, 483. (In English: Zhang JY, Sun SP, Yang LJ, et al. Determination of 18 volatile organic compounds in drinking water by headspace gas chromatography[J]. Chin J Health Lab Technol, 2017, 27(4): 477-480, 483.) |
| [14] |
李琰, 丁克颖, 宁文吉. 吹扫捕集-气质联用法同时测定生活饮用水中86种挥发性有机物[J]. 环境与职业医学, 2017, 34(4): 341-349. (In English: Li Y, Ding KY, Ning WJ. Determination of 86 volatile organic compounds in drinking water using purge and trap in combination with gas chromatography-mass spectrometry[J]. J Labour Med, 2017, 34(4): 341-349.) |
| [15] |
U.S. EPA. EPA Method 524.2: Measurement of Purgeable Organic Compounds in Water by Capillary Column Gas Chromatography/Mass Spectrometry[Z]. U.S. EPA, 1992. https://www.epa.gov/esam/epa-method-5242-measurement-purgeable-organic-compounds-water-capillary-column-gas
|

