尿铅是反映人体内铅负荷及近期铅接触水平的监测重要指标。《职业性慢性铅中毒的诊断》(GBZ 37-2015)[1]将尿铅水平达到或超过70 μg/L、有密切铅接触史者列为铅中毒观察对象,尿铅水平达到或超过120 μg/L是轻度铅中毒的诊断指标之一。
国内现有测定标准方法最常用的是《尿中铅的石墨炉原子吸收光谱测定方法》(WS/T 18-1996)[2],该法通过加入基体改进剂等方式来消除基体干扰,测定结果的准确性受到基改剂浓度、测定条件等多种因素影响。文献报道常用的基体改进剂有磷酸二氢铵及氯化钯[3-5],本文对此两种不同的基体改进剂的浓度,仪器测定条件,样品稀释倍数,定量方式等多方面进行比对并依据《职业卫生标准制定指南第5部分:生物材料中化学物质的测定方法》(GBZ/T 210.5-2008)[5]进行了方法学的规范研究。
1 材料与方法 1.1 仪器PE-800原子吸收分光光度计(美国Perkin Elmer公司);具盖聚乙烯塑料瓶,容量瓶;铅空心阴极灯(北京有色金属研究总院)。仪器工作条件:干燥温度90℃~120℃,灰化温度800℃,原子化温度1 900℃,清除温度2 100℃。
1.2 试剂铅单元素标准溶液1 000 μg/mL(国家标准物质研究中心,GBW 090169);硝酸(高纯,国药集团化学试剂公司);基体改进剂:①氯化钯(国药集团化学试剂公司优级纯,称取0.33g氯化钯加热微溶于10 mL硝酸中,摇匀,用水稀释至500 mL。贮存于棕色试剂瓶中;②磷酸二氢铵,称取4.0 g磷酸二氢铵(国药集团化学试剂公司)溶于20 mL水中,加入6.0 g抗坏血酸(国药集团化学试剂公司)用水稀释至100 mL摇匀;实验用水为去离子水。
1.3 样品的采集用具盖聚乙烯塑料瓶收集1次尿样约20 mL[7]。尽快测量比重后,按照1%的比例加入硝酸,混匀。于冰箱内-18℃冷冻保存。
1.4 标准曲线的制备用1%硝酸将铅标准溶液稀释成1.0 μg/mL的铅标准应用溶液。取7只10 mL容量瓶分别加入0.0、0.200、0.400、0.800、1.20、1.60、2.00 mL铅标准应用液,各加基体改进剂至10 mL,配置成0、20.0、40.0、80.0、120.0、160.0、200.0 μg/L铅标准系列。进样前将铅标准系列与正常人尿样按照1 :1比例进行处理, 制备成铅工作曲线标准系列。
1.5 样品预处理方法将酸化的尿样从冰箱中取出,恢复到室温后,充分摇匀。吸取0.2 mL于具塞聚乙烯离心管中加入0.2mL基体改进剂, 混匀后供测定。
1.6 计算按式计算尿样的铅浓度:
| $ C = c \times k $ |
式中:C—尿中铅的浓度,μg/L;
c—由工作曲线或回归方程得的尿样中扣除空白后铅的浓度,μg /L;
k—尿样换算成标准比重(1.020)下的浓度校正系数。
2 结果与讨论 2.1 基体改进剂浓度及比例的比对样品与基体改进剂体积比例的对比。分别选用两种不同基体改进剂,用冻干人尿铅标准物质(GBW 09104)范围值为(101±11) μg/L作为样品,按照尿样与基体改进剂不同的比例混匀处理后进样。结果显示,尿分别与两种基体改进剂按照1+1的比例处理样品时,测定结果均在参考值范围内;但氯化钯作为基体改进剂时结果RSD值小于10%,效果优于磷酸二氢铵(表 1)。
| 磷酸二氢铵基体改进剂 | 氯化钯基体改进剂 | ||||
| 测定结果均值/(μg/L) | RSD/ % | 测定结果均值/(μg/L) | RSD/ % | ||
| 尿+基改剂(1+1) | 112 | 13.0 | 90.2 | 2.7 | |
| 尿+基改剂(1+2) | 119 | 5.4 | 101 | 5.1 | |
| 尿+基改剂(1+3) | 123 | 18.0 | 115 | 5.2 | |
2.2 基体改进剂浓度的比对
选用两种不同的基体改进剂,配制不同浓度,按照1 :1的比例处理标准点样品,测定结果显示采用磷酸二氢铵作为基体改进剂时随浓度降低吸光度值降低,而采用氯化钯作为基体改进剂时浓度变化对吸光度值无影响(表 2)。
| 磷酸二氢铵(g)+抗坏血酸(g) | 吸光度值 | |
| 磷酸二氢铵基改剂 | 4.00+6.00 | 1.59 |
| 2.00+3.00 | 1.44 | |
| 1.30+2.00 | 1.26 | |
| 1.00+1.50 | 1.25 | |
| 氯化钯基改剂(g/L) | 0.60 | 0.100 |
| 0.40 | 0.100 | |
| 0.30 | 0.100 | |
| 0.20 | 0.100 |
2.3 仪器测定条件的比对 2.3.1 灰化温度的比对
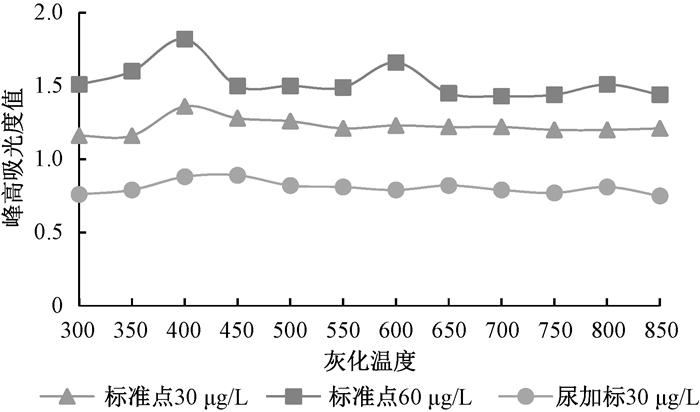
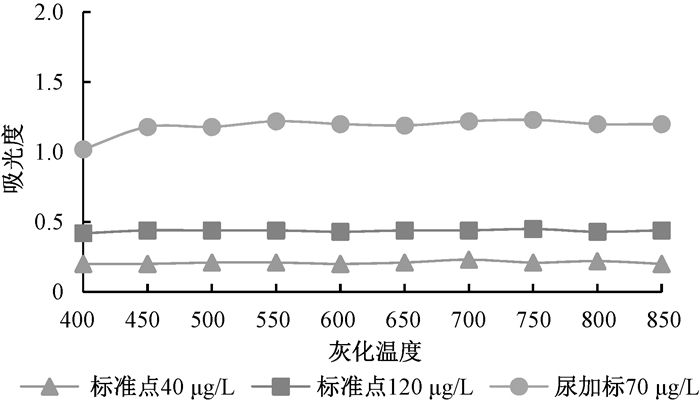
采用磷酸二氢铵及氯化钯基体改进剂处理样品,选用不同的标准点及尿加标的样品,在350℃~850℃灰化温度范围内,测定各点的吸光度值,按照吸光度值与灰化温度绘制图 1,图 2:由图 1,图 2可知,当灰化温度为400℃~450℃时,标准及尿样测定吸光度值响应较大。氯化钯作为基体改进剂测定标准及尿样时,不同的灰化温度对测定影响不大,氯化钯与铅形成稳定的络合物使得铅不易在灰化过程中损失,因此灰化温度可以提高到800℃,在此温度下,尿样中的大部分干扰成份被清除。因此采用氯化钯作为基体改进剂时可选用700℃~900℃的灰化温度。
|
| 图 1 磷酸二氢铵基体改进剂灰化温度选择 |
|
| 图 2 氯化钯基体改进剂灰化温度选择 |
2.3.2 原子化温度的比对
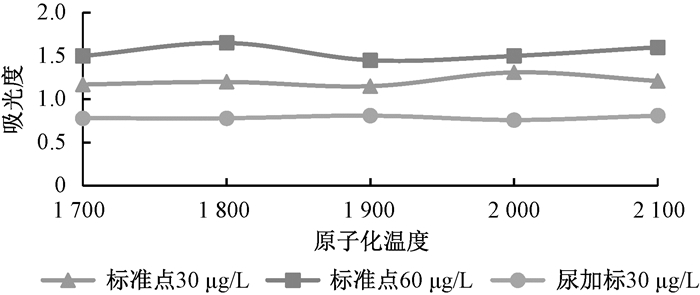
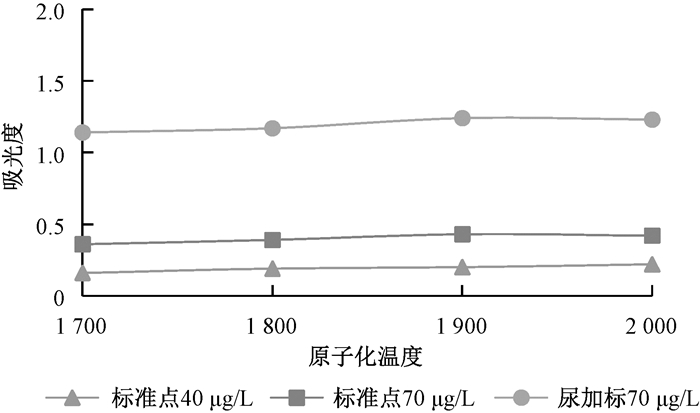
固定灰化温度,分别选用磷酸二氢铵及氯化钯作为基体改进剂处理样品,选取不同的标准点及尿加标样品,在原子化温度1 700℃~2 100℃时测定各点标准浓度及尿加标样品的吸光度值。由图 3,图 4可看出,两种基体改进剂的原子化温度均在1 800℃~2 000℃时有较好的响应,因此原子化温度选用1 900℃。
|
| 图 3 磷酸二氢铵基体改进剂原子化温度的选择 |
|
| 图 4 氯化钯基体改进剂原子化温度的选择 |
2.3.3 基体改进剂对石墨管影响
使用两种不同的基体改进剂处理样品后,进样观察峰形及石墨管的使用情况。由于磷酸二氢铵基体改进剂中含有抗坏血酸,使得石墨管的使用寿命缩短,峰形较差,定量方式受到限制(峰高定量优于峰面积定量),不适合进行大量样品的测定,背景干扰多,基体改进剂在4℃中只能保存1个月。而氯化钯作为基体改进剂基质简单,石墨管的使用寿命周期长,定量方式不受限制,同时可在4℃中保存1 a。从使用效果及经济方面考虑均显示氯化钯基体改进剂较磷酸二氢铵基体改进剂更优。
2.4 方法测定性能指标的比对采用两种基体改进剂,对方法测定性能指标进行比较。
2.4.1 方法线性范围及定量方式采用不同的基体改进剂配制成铅浓度范围为(0~400) μg/L的标准系列,测定时按照1 :1的比例将空白尿样(正常人尿)与标准混匀制备成工作曲线。分别以峰高,峰面积进行定量,测定标准系列并计算相关性。测定结果磷酸二氢铵作为基体改进剂峰面积定量r=0.998 5,峰高定量r=0.999 2,氯化钯作为基体改进剂峰面积定量r=0.999 3,峰高定量r=0.999 3。结果显示氯化钯作为基体改进剂比磷酸二氢铵基体改进剂相关性更优。方法线性范围在(0~400) μg/L相关性均可达到标准但在日常检测及一般人群筛查时可以配置(0~200) μg/L的线性范围即可,如果是驱铅治疗的病人为了减少基质效应则可以将线性范围扩大到400 μg/L,此时也可以达到线性测定范围要求。
依据《职业性慢性铅中毒的诊断》(GBZ 37—2015)[1]采用正常人尿配制成30,70,120 μg/L尿加标样品,使用两种基体改进剂以峰高,峰面积定量计算加标回收及变异。磷酸二氢铵基体改进剂处理样品测定结果显示无论峰高定量还是峰面积定量随着浓度越低回收率越低,变异越大;氯化钯基体改进剂处理的样品结果不受定量方式的影响,峰形及背景均优于磷酸二氢铵基体改进剂(表 3)。
| 标准加入浓度 | 磷酸二氢铵基改剂 | 氯化钯基改剂 | |||||
| 30 | 70 | 120 | 30 | 70 | 120 | ||
| 峰面积定量测定值/(μg/L) | 10.7 | 31.5 | 42.3 | 29.5 | 68.9 | 123 | |
| 回收率/% | 35.0 | 44.0 | 35.0 | 98.0 | 98.0 | 103 | |
| RSD/% | 24.0 | 13.0 | 4.0 | 1.60 | 2.60 | 3.00 | |
| 峰高定量测定值/(μg/L) | 21.8 | 54.1 | 75.2 | 31.5 | 68.3 | 120 | |
| 回收率/% | 72.0 | 77.0 | 62.0 | 104 | 97.0 | 100 | |
| RSD/% | 12.0 | 9.00 | 10.0 | 4.10 | 2.50 | 2.30 | |
根据上述实验结果显示磷酸二氢铵作为基体改进剂峰高定量结果优于峰面积的定量结果,而氯化钯作为基体改进剂,峰高及峰面积定量均可达到要求,因此从定量方式看氯化钯作为基体改进剂时优于磷酸二氢铵。
2.4.2 方法的准确度采用加标回收法进行准确度的实验。取正常人尿液配置成不同浓度的尿加标样品,分别为30、70、120 μg/L,样品经两种基体改进剂按照等体积比例处理后进样,分别以峰高及峰面积定量,计算每个浓度的加标回收率。磷酸二氢铵基体改进剂峰高定量加标回收率范围:73%~86%,磷酸二氢铵基体改进剂峰面积定量加标回收率范围:73%~78%。氯化钯基体改进剂峰面积定量加标回收率范围:97%~98%。峰高定量加标回收率范围:97%~103%。从准确度实验数据看出磷酸二氢铵基体改进剂的加标回收率不如氯化钯基体改进剂的结果(表 4和表 5)。
| 标准加入值/(μg/L) | 峰高定量 | 峰面积定量 | |||||
| 30 | 70 | 120 | 30 | 70 | 120 | ||
| 尿空白均值/(μg/L) | 2.02 | 2.02 | 2.02 | 2.02 | 2.02 | 2.02 | |
| 尿加标测定均值/(μg/L) | 23.9 | 60.1 | 105 | 23.7 | 54.7 | 95.8 | |
| 加标回收率/% | 73 | 83 | 86 | 72 | 75 | 78 | |
| 标准加入值/(μg/L) | 峰高定量 | 峰面积定量 | |||||
| 30 | 70 | 120 | 30 | 70 | 120 | ||
| 尿空白均值/(μg/L) | 2.02 | 2.02 | 2.02 | 2.02 | 2.02 | 2.02 | |
| 尿加标测定均值/(μg/L) | 33.5 | 70.3 | 122 | 31.5 | 70.9 | 119 | |
| 加标回收率/% | 104 | 98 | 99.9 | 98 | 98 | 98 | |
2.4.3 方法的精密度
精密度实验,取正常人尿液配制成不同浓度的尿加标样品,采用两种不同的基体改进剂处理样品,磷酸二氢铵基体改进剂以峰高及峰面积定量;氯化钯基体改进剂以峰面积定量(峰高峰面积定量一致),计算每个浓度的RSD值。磷酸二氢铵基体改进剂峰高定量批内精密度的RSD范围为3.60%~6.40%,批间精密度的RSD范围为3.20%~14.0%。磷酸二氢铵基体改进剂峰面积定量批内精密度的RSD范围为4.60%~9.30%,批间精密度的RSD范围为7.50%~18.0%。氯化钯基体改进剂峰面积定量批内精密度的RSD范围为1.00%~2.60%,批间精密度的RSD范围为1.60%~3.90%。实验中观察到磷酸二氢铵作为基体改进剂峰面积定量时的峰形扁宽,定量结果较差。氯化钯作为基体改进剂不受峰高,峰面积定量的影响。批间及批内的RSD值均小于5%。氯化钯作为基体改进剂比磷酸二氢铵作为基体改进剂更理想(表 6和表 7)。
| 批内精密度 | 批间精密度 | |||||
| 标准加入浓度/ (μg/L) | 平均值/ (μg/L) | RSD/ % | 平均值/ (μg/L) | RSD/ % | ||
| 峰高定量 | 30 | 24.4 | 3.60 | 21.9 | 14.0 | |
| 70 | 59.4 | 6.40 | 59.2 | 4.50 | ||
| 120 | 108 | 4.70 | 103 | 3.20 | ||
| 峰面积定量 | 30 | 24.5 | 9.30 | 21.8 | 18.0 | |
| 70 | 58.9 | 4.60 | 52.8 | 7.50 | ||
| 120 | 106 | 6.10 | 93.9 | 13.0 | ||
| 批内精密度 | 批间精密度 | |||||
| 标准加入浓度/ (μg/L) | 平均值/ (μg/L) | RSD/ % | 平均值/ (μg/L) | RSD/ % | ||
| 峰面积定量 | 30 | 29.5 | 1.60 | 29.1 | 3.90 | |
| 70 | 68.9 | 2.60 | 68.4 | 2.00 | ||
| 120 | 117 | 1.00 | 119 | 1.60 | ||
2.4.4 最小检出浓度
采用正常人尿,用基体改进剂按照1 :1的比例处理,进样11次,用3倍的标准差计算出最小检出浓度为1.00 μg/L,10倍标准差计算定量下限为3.0 μg/L(表 8)。
| 测定次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 平均值 | 标准差 |
| 测定结果 | 2.90 | 2.50 | 2.60 | 2.60 | 3.00 | 2.80 | 2.50 | 2.30 | 2.70 | 2.60 | 1.90 | 2.60 | 0.300 |
2.5 稀释倍数
尿铅测定过程中,当出现超标样品时需要进行稀释,由于样品稀释过程中会有基质效应产生,因此本文对超标样品的稀释范围进行了实验。
2.5.1 标准系列及样品处理方法相同将标准系列及样品按照相同的方法及稀释倍数处理, 测定冻干人尿铅标准物质(GBW 09104)及尿加标300 μg/L(表 9)。结果显示冻干人尿铅标准物质(GBW 09104)测定结果均在测定范围内,但尿加标样品的测定结果的回收率及RSD值氯化钯基体改进剂优于磷酸二氢铵基体改进剂。
| 磷酸二氢铵基体改进剂 | 氯化钯基体改进剂 | ||||||||||
| GBW 09104 (101±11 μg/L) | 尿加标(300 μg/L) | GBW 09104 (101±11 μg/L) | 尿加标(300 μg/L) | ||||||||
| 测定值/ (μg/L) | 测定值/ (μg/L) | 回收率/ % | RSD | 测定值/ (μg/L) | 测定值/ (μg/L) | 回收率/ % | RSD | ||||
| 2倍稀释 | 91.8 | 347 | 115 | 6.50 | 94.9 | 296 | 98.9 | 1.80 | |||
| 3倍稀释 | 95.3 | 289 | 96.0 | 2.70 | 94.1 | 310 | 103 | 2.30 | |||
| 4倍稀释 | 98.5 | 292 | 97.0 | 5.80 | 94.6 | 319 | 106 | 0.80 | |||
| 5倍稀释 | 95.0 | 280 | 93.0 | 12.0 | 90.0 | 308 | 102 | 4.80 | |||
2.5.2 标准系列及样品处理方法不同
标准系列采用3倍稀释,氯化钯基体改进剂处理冻干人尿铅标准物质(GBW 09104)及尿加标300 μg/L进行2,4,5和10倍不同的稀释,将结果进行换算计算结果(表 10)。
| GBW 09104(101±11μg/L) | 尿加标(300μg/L) | ||||||||||
| 稀释倍数 | 2倍 | 3倍 | 4倍 | 5倍 | 10倍 | 2倍 | 3倍 | 4倍 | 5倍 | 10倍 | |
| 测定值/(μg/L) | 87.7 | 94.1 | 96.9 | 105 | 119 | 235 | 310 | 345 | 377 | 524 | |
| 回收率/% | - | - | - | - | - | 78.0 | 103 | 115 | 125 | 174 | |
| 注:“-”表示因为冻干人尿铅标准物质(GBW 09104)采用参考值范围进行评估,所以无需计算回收率 | |||||||||||
由于2.5.2中氯化钯基体改进剂优于磷酸二氢铵基体改进剂的测定结果,因此在处理方法不同时只对氯化钯基体改进剂进行评估。根据以上结果显示当样品超过测定范围时需进行样品稀释,但稀释倍数及方法应与标准系列相同,否则测定结果将出现偏离。
3 结论根据以上结果显示两种基体改进剂具有一定的差别,磷酸二氢铵基体改进剂处理的样品峰形差,不稳定,背景高,精密度RSD值大,回收率低, 石墨管使用寿命短。氯化钯基体改进剂处理的样品峰形较好,石墨管使用寿命不受基体改进剂的影响,精密度RSD值理想,加标回收率较高,不受定量方式限制,峰高,峰面积均可作为定量方式进行定量测定。当样品浓度超过线性范围时,在处理样品时标准系列及样品的处理方法应一致,避免出现基体效应造成结果偏离。
| [1] |
中华人民共和国国家卫生和计划生育委员会中华人民共和国卫生部. GBZ 37-2015职业性慢性铅中毒的诊断标准[S].北京: 中国标准出版社人民卫生出版社, 201608. (In English: National Health and Family Planning Commission of the People's Republic of ChinaMinistry of Health of the People's Republic of China. GBZ 37-2015 Diagnosis Diagnostic criteria of occupational chronic lead poisoning[S]. Beijing: Standards Press of ChinaPeople's Medical Publishing House, 20165.)
|
| [2] |
中华人民共和国卫生部. WS/T 18-1996尿中铅的石墨炉原子吸收光谱测定方法[S].北京: 中国标准出版社, 1997. (In English: Ministry of Health of the People's Republic of China. WS/T 18-1996 Urine-determination of lead-graphite furnace atomic absorption spectrometry[S]. Beijing: Standards Press of China, 1997.)
|
| [3] |
汤晓勇, 吴宜群, 李春玲, 等.基体改进剂石墨炉原子吸收光谱法直接测定尿铅[J].卫生研究, 1993, 22(6): 335-338. (In English: Tang Xiaoyong, et al. Direct determination of lead in urine by graphite furnace atomic absorption spectrometry used matrix modifier. Journal of Hygiene Research1993, 22(6): 335-338.) http://www.cnki.com.cn/Article/CJFDTotal-WSYJ199306004.htm
|
| [4] |
赖娟, 刘锦云, 等. 石墨炉原子吸收光谱法直接测定尿中铅浓度研究[J]. 职业卫生与病伤, 2012, 27(5): 290-292. (In English: Lai Juan, Liu JY, et al. With graphite furnace atomic a bsorption spectrometry method to directly determine the lead density in urine[J]. Journal of Occupational Health and Damage, Oct, 2012, 27(5): 290-292. DOI:10.3969/j.issn.1006-172X.2012.05.011) |
| [5] |
潘尚霞, 刘涛, 曲亚斌, 等. 南方某重金属暴露区儿童血和尿中铅、镉水平及影响因素调查[J]. 环境卫生学杂志, 2016, 6(1): 24-27. (In English: Pan SXhangxia, Liu T, Qu YB, et al. Levels of lead and cadmium in Children' blood and urine exposed to heavy metal pollution in industrial district of South China[J]. J Environ Hyg, 2016, 6(1): 24-27.) |
| [6] |
中华人民共和国卫生部. GBZ/T 210. 5-2008.职业卫生标准制定指南第5部分: 生物材料中化学物质的测定方法[S].北京: 人民卫生出版社, 2008. (In English: The Ministry of Health of the People's Republic of China. GBZ/T 210. 5-2008 Guide for establishing occupational health standards-part 5: determination methods of chemicals in biological materials[S]. Beijing: People's Medical Publishing House, 2008.)
|
| [7] |
胡运清, 陈海鸥, 彭柳明, 等. 蓄电池企业铅污染现状调查及尿铅影响因素分析[J]. 环境卫生学杂志, 2012, 2(5): 204-207. (In English: Hu YQunqing, Chen HO, Peng LM, et al. Status of lead pollution in battery factories and influencing factors for the levels of urine lead[J]. J Environ Hyg, 2012, 2(5): 204-207.) |



