麻痹性贝类毒素(paralytic shellfish poisoning,PSP)是由有毒赤潮的藻类生物产生的一类四氢嘌呤的三环化合物,是世界范围内分布最广、危害最大的一种赤潮生物毒素,常见有石房蛤毒素(STX)、新石房蛤毒素(neoSTX)、脱氨基甲酸石房蛤毒素(dcSTX、dcneoSTX)[1]。贝类水产品通过摄食有毒藻,其藻毒素在体内不断累积,人类误食含有该毒素的贝类可导致人体神经系统麻痹。随着现代化工、农业生产以及沿海养殖业的快速发展,海洋环境遭到污染,有毒有害赤潮频繁发生[2]。在我国沿海地区已有多起因进食海产品而引起贝类毒素中毒事件的案例时有报道[3-5]。国外许多国家及有关国际组织已对贝类水产品进行严格管制,并制定了相关贝类水产品的PSP限量标准,WHO允许的PSP的公共卫生限值为80 μg STX eq/100 g贝肉[6]。
目前PSP的检测方法主要有小鼠生物法[7-8]、酶联免疫法[9]、液相色谱—荧光法[10-11]和液相色谱—串联质谱法(LC-MS/MS)法[12-16]等。小鼠生物法是美国分析化学家协会推荐使用的测定方法,该法对小白鼠和实验环境要求较高,重现性差,且不能对具体毒素进行准确定量。酶联免疫法容易受贝类基质干扰,难以判断样品中潜在总毒素。液相色谱—荧光法,操作繁琐,不稳定,基体杂质复杂,对测定结果造成干扰,容易出现假阳性结果,影响了该法的推广应用。选择灵敏度高,可以同时准确定性定量的测定方法,已逐渐成为检测贝类毒素的研究热点。目前采用液质联用法检测麻痹性贝类毒素的研究陆续有报道。文献[16]采用乙腈甲酸水溶液提取,冰冻后分层除脂净化,Monica[15]采用的0.1%甲酸溶液提取,甲醇除脂后QuEChERS净化管净化,经实际应用发现,所采用处理方法操作繁琐,难以保证测定的准确性。本研究采用的0.1 mol/L乙酸提取,HLB固相萃取柱净化,ZIC-cHILIC色谱柱分析,运用UPLC-MS/MS技术,串联四极杆的扫描方式和线性离子阱的扫描方式相结合,二级质谱MRM模式(多反应监测)进行定性分析,具有实用性更强、操作简便、准确度更高的优点。建立的超高效液相色谱—串联质谱法(UPLC-MS/MS)检测贝类中常见的4种麻痹性贝类毒素(STX、dcSTX、neoSTX、dcneoSTX),将为公共卫生突发事件防控、食品安全风险监测与评估等提供方法依据和技术支撑。
1 材料与方法 1.1 仪器与试剂 1.1.1 主要仪器4 000 QTRAP超高效液相色谱串联质谱仪(美国AB SCIEX公司),配有电喷雾离子源;超高效液相色谱系统,配有输液单元,自动进样器,柱温箱(日本SHIMADZU公司),T25匀浆机(德国IKA公司);涡旋振荡器(德国Heidolph公司);3-30K台式低温高速离心机(美国SIGMA公司);氮吹仪(N-EVAP-112,Organomation公司);固相萃取装置(美国Agilent公司);Milli-Q超纯水系统(法国Millipore公司)。色谱柱:SeQuant ZIC-cHILIC:3 μm,2.1 mm×150 mm(Merck KGaA公司。;固相萃取柱(OASIS HLB 3 mL,60 mg,美国Waters公司)。
1.1.2 试剂甲醇、乙腈(色谱纯,Merk公司);甲酸(色谱纯,CNW公司);乙酸铵(优级纯,ROE SCIENTIFICINC公司)。麻痹性贝类毒素标准溶液:STX、dcSTX、neoSTX和dcneoSTX购于加拿大海洋生物科学研究所,质量浓度分别为STX 24.68 μg/mL、dcSTX 21.40 μg/mL、neoSTX 20.67 μg/mL和dcneoSTX 8.03 μg/mL。
1.2 实验方法 1.2.1 工作曲线的制备将4种麻痹性贝类毒素的标准溶液用0.1 mol/L乙酸稀释成混合标准溶液,分别为STX 246.8 μg/L、dcSTX 214.0 μg/L、neoSTX 206.7 μg/L和dcneoSTX 80.3 μg/L。临用前再用空白基质液配制成混合标准溶液系列。
1.2.2 色谱条件流动相A:10 mmol/L乙酸铵(含0.1%甲酸),流动相B:乙腈(含0.1%甲酸)。梯度洗脱:0 min~2 min,30%B;2 min~3 min,30%~20% B;3 min~7 min,20% B;7 min~7.1 min,20%~30% B;7.1 min~10 min,30%。进样量:10 μL;流速:300 μL/min;柱温:40℃;
1.2.3 质谱条件电喷雾三重四级杆串联质谱,正离子ESI模式,气帘气压力CUR:240×103 Pa;喷雾电压IS:5 500 V;离子源温度:500℃;雾化气压力GS1:345×103 Pa;辅助加热气压力GS2:345×103 Pa。MRM参数见表 1。
| 化合物 | 母离子/(m/z) | 子离子/(m/z) | 锥孔电压/V | 碰撞能/eV |
| STX | 300.2 | 204.2*,179.0 | 110.0 | 35.0 |
| dcSTX | 257.1 | 126.0*,138.0 | 80.0 | 33.0 |
| neoSTX | 316.1 | 220.0*,298.1 | 60.0 | 35.0 |
| dcneoSTX | 273.1 | 225.1*,180.0 | 75.0 | 33.0 |
| 注:*为定量离子 | ||||
1.2.4 样品制备
从原始贝类水产品中取可食用部分,用清水冲去泥污,用滤纸或干净纱布吸去多余的水分,置于匀浆机中匀浆。放置-20℃以下冰箱冷冻储存,测定前解冻至室温。
1.2.5 样品处理提取:称取5.00 g匀浆后的贝类样品至50 mL具塞离心管中,加入20 mL 0.1 mol/L乙酸,涡旋均匀5 min,然后8 000 r/min离心5 min,待净化。
净化:取固相萃取柱(HLB 3mL,60 mg)依次用6 mL甲醇,6 mL 30 mmol/L乙酸溶液活化,取2.00 mL样品提取后的上清液过净化柱,收集流出液,过0.22 μm滤膜,滤液上UPLC-MS/MS分析。
1.2.6 空白基质液的制备称取经检测不含4种PSP扇贝样品,按1.2.5样品处理进行操作,净化后的流出液作为空白基质液,备用。
2 结果与分析 2.1 质谱条件优化离子源的选择,对于极性化合物使用ESI源离子化,对于非极性化合物使用APCI方式,4种PSP均为强极性化合物,故选择ESI离子源。将各标准原液(质量浓度分别为STX 24.68 μg/mL、dcSTX 21.40 μg/mL、neoSTX 20.67 μg/mL、dcneoSTX 8.03 μg/mL)分别用0.1 mol/L乙酸配成质量浓度为1.0 mg/L的4种单个PSP毒素标准储备液,以10 μL/min流动注射的方式分别在正离子(ESI+)、负离子(ESI-)模式下进行一级质谱扫描。进一步比较不同电离模式下检测的灵敏度,结果发现在正离子模式下,4种PSP毒素在正离子扫描下响应值较高,并在找到PSP毒素各自的分子离子峰[M+H]+后,以其作为母离子分别优化其质谱参数,确定最佳质谱参数。然后再进行二级质谱分析(子离子扫描),确定各自得主要碎片离子,从中选取丰度最强的碎片离子作为各自的定量离子,以次强的碎片离子作为定性离子,优化质谱参数见表 1。
2.2 色谱条件优化 2.2.1 色谱柱的选择亲水作用液相色谱(HILIC)是一种采用强极性固定相(如硅胶或衍生硅胶),以高比例极性有机相/低比例水相为流动相的色谱模式[13]。而ZIC-cHILIC色谱柱的固定相表面键合有磷酰胆碱两性离子,适合用于分析极性和亲水性化合物。本实验尝试ZIC-cHILIC和BEH C18色谱柱进行PSP混合标准溶液分析比较,实验结果表明:在选择同一合适流动相条件下,C18柱对PSP无保留,而 ZIC-cHILIC色谱柱能将4种PSP完全保留在色谱柱上,且峰形对称性好、分离较高。所以最终选用 ZIC-cHILIC色谱柱为测定PSP的最佳色谱柱。
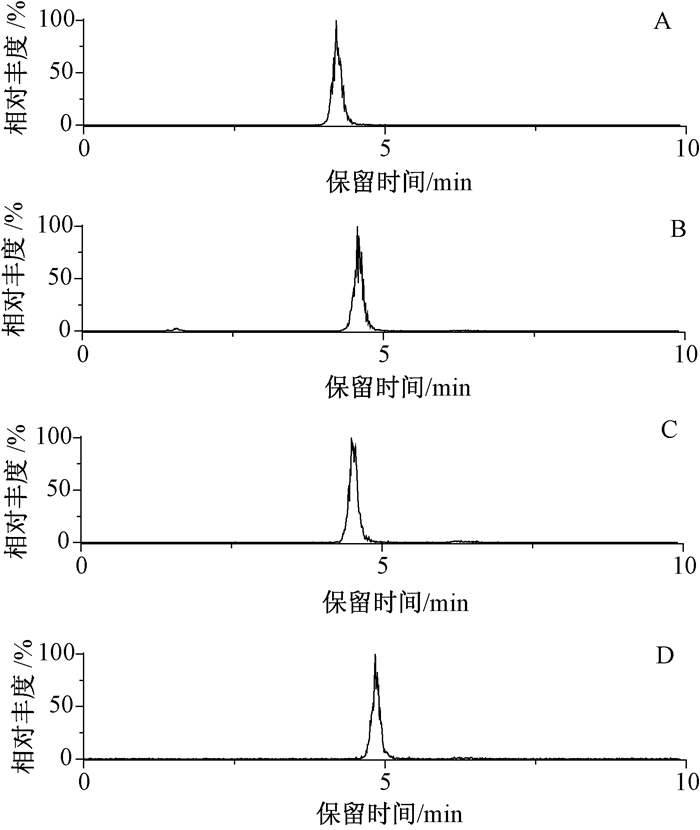
2.2.2 流动相的选择电喷雾质谱的电离是在溶液状态下进行的,流动相的pH值和在纯溶剂中添加的物质不仅会影响目标化合物的保留时间和峰形,还会影响离子化效率,最终影响灵敏度。本研究分别考察了乙腈—水、乙腈—乙酸铵(添加0.1%甲酸)作为流动相的色谱行为发现乙腈—水作为流动相时峰型较宽,响应值较低,不适合定量,而乙腈—乙酸铵流动相中添加0.1%甲酸作为流动相4种PSP的峰型较好,灵敏度提高。继而在选择乙腈—乙酸铵(添加0.1%甲酸)作为流动相基础上,分别考察了2 mmol/L乙酸铵与10 mmol/L乙酸铵两种浓度以及等度洗脱与梯度洗脱的分离效果,结果发现10 mmol/L乙酸铵的流动相梯度洗脱测定4种PSP毒素的灵敏度最高,峰形和分离效果较好。因此,本研究最终选择以含10 mmol/L乙酸铵和0.1%甲酸的水溶液作为流动相A,含0.1%甲酸的乙腈溶液作为流动相B。在质谱、色谱条件优化下,STX、dcSTX、neoSTX、dcneoSTX标准色谱图如图 1所示。
|
| 注:标准色谱图 图 1 4种麻痹性贝类毒素标准色谱图 |
2.3 样品前处理方法优化
PSP为一类强极性、易溶于稀酸的水溶性化合物,不溶于有机试剂。贝类样品基质较复杂,含有丰富的蛋白质、脂肪等杂质,这些杂质不但会干扰测定结果,而且还会对色谱柱、离子源造成污染,导致响应值下降。样品前处理目的是去除杂质、消除干扰,提高方法灵敏度。据相关文献报道,甲酸、乙酸、盐酸、乙腈-酸性水溶液均可作为贝类产品中PSP的提取溶液,参照文献的方法[15-16],分别比较几种样品净化方法,A方法:0.1 mol/L乙酸溶液提取,HLB固相萃取小柱净化;B方法:0.1%甲酸的80%乙腈溶液提取,HLB固相萃取小柱净化;C:方法0.1%甲酸溶液提取,QuEChERS净化管净化。结果发现采用B方法和C方法处理的回收率均低于50%,而采用0.1 mol/L乙酸超声提取,HLB固相萃取净化,4种PSP各目标组分回收率均能达到80%以上。因此,本研究最终选择A方法:0.1 mol/L乙酸溶液提取,HLB固相萃取小柱净化为样品前处理方法。
2.4 基质影响进行UPLC-MS/MS检测时,基质效应会直接影响目标物的测定结果。为了考察基质对4种PSP测定结果的影响,用扇贝空白样品提取液和提取溶剂(0.1 mol/L乙酸)分别配制同一浓度的标准溶液,上机分析比较响应值。发现用空白基质提取液配制PSP标准溶液的响应值明显偏低,表明基质对PSP的响应值有抑制作用,因此确定采用空白基质液配制PSP系列标准工作液,以提高PSP定量的准确性。
2.5 工作曲线线性范围和检出限分别在贝类样品空白提取液中准确添加适量的标准溶液,配制成质量浓度分为STX(6.17 μg/L、12.3 μg/L、24.7 μg/L、30.8 μg/L、61.7 μg/L和74.0 μg/L),dcSTX(5.35 μg/L、10.7 μg/L、21.4 μg/L、26.8 μg/L、53.5 μg/L和64.2 μg/L),neoSTX(5.17 μg/L、10.3 μg/L、20.7 μg/L、25.8 μg/L、51.7 μg/L和62.0 μg/L),dcneoSTX(2.01 μg/L、4.01 μg/L、8.03 μg/L、10.0 μg/L、20.1 μg/L和24.1 μg/L)混合标准溶液系列,按已优化的仪器条件测定。以峰面积(y)对质量浓度(x)作校正曲线,以取样量5g,信噪比为3时对应的待测物的质量浓度计算方法检出限,信噪比为10时对应的待测物的质量浓度计算方法检测(表 2)。
| 化合物 | 线性范围μg/L | 线性方程 | 相关系数(r) | 检出限μg/kg | 定量限μg/kg |
| STX | 6.17~74.0 | y=3.62×103x+2.40×103 | 0.9995 | 9.39 | 31.0 |
| dcSTX | 5.35~64.2 | y=3.86×103x-82.0 | 0.9991 | 8.12 | 26.8 |
| neoSTX | 5.17~62.0 | y=3.06×105x+4.82×104 | 0.9997 | 7.88 | 26.0 |
| dcneoSTX | 2.01~24.1 | y=2.02×103x+919 | 0.9997 | 3.03 | 10.0 |
2.6 方法的准确度和精密度
分别在已经检测不含4种PSP扇贝样品中添加3个质量浓度水平的标准,考察方法的回收率。按1.2的实验方法各平行检测6次,考察方法的精密度(表 3)。
| 化合物 | 添加量/(μg/kg) | 平均测定值/(μg/kg) | 平均回收率/% | RSD/% |
| STX | 61.7 | 50.0 | 81.0 | 6.1 |
| 123 | 113 | 91.9 | 3.1 | |
| 247 | 214 | 86.6 | 6.9 | |
| dcSTX | 53.5 | 46.4 | 86.7 | 5.7 |
| 107 | 98.0 | 91.6 | 3.4 | |
| 214 | 199 | 93.0 | 4.2 | |
| neoSTX | 51.7 | 46.9 | 90.7 | 2.1 |
| 103 | 101 | 98.1 | 1.7 | |
| 206 | 188 | 91.3 | 4.0 | |
| dcneoSTX | 20.1 | 19.0 | 94.5 | 3.4 |
| 40.2 | 40.8 | 101 | 0.47 | |
| 80.4 | 83.6 | 104 | 3.0 |
2.7 实际样品检测
应用建立的方法,对市场采集的20份牡蛎、扇贝、花蛤等贝类水产品中4种麻痹性贝类毒素进行检测,4种麻痹性贝类毒素均未检出。
3 结论本研究通过色谱、质谱条件的优化、样品前处理方法优化等方法学考察,建立超高效液相色谱-串联质谱检测水产品中的4种麻痹性贝类毒素(STX、neoSTX、dcSTX、dcneoSTX)的分析方法。本方法具有较高的灵敏度、精密度;适合水产品中4种麻痹性贝类毒素的确证和定量分析。
| [1] | 张小军, 陈雪昌, 郭远明, 等. 超高效液相色谱-串联质谱法测定4种麻痹性贝类毒素[J]. 浙江海洋学院学报(自然科学版),2011, 30 (2) : 95 –98. |
| Click to display the text | |
| [2] | 杜克梅, 雷芳, 吴霓, 等. 我国东海和南海近岸海域麻痹性贝类毒素污染状况[J]. 暨南大学学报(自然科学版),2013, 34 (3) : 343 –346. |
| Click to display the text | |
| [3] | 林祥田, 张明生, 王志坚, 等. 连云港海州湾麻痹性贝类毒素中毒分析[J]. 中国食品卫生杂志,2005, 17 (3) : 243 –246. |
| Click to display the text | |
| [4] | 刘用锦, 林旭. 一起麻痹性贝类毒素中毒的调查[J]. 海峡预防医学杂志,2001, 7 (3) : 35 . |
| Click to display the text | |
| [5] | 吴蕙岭, 章荣华, 宋燕华, 等. 两起疑似织纹螺中毒事件的实验室调查[J]. 中国卫生检验杂志,2010, 20 (12) : 3455 –3456. |
| Click to display the text | |
| [6] | 刘智勇, 计融. 各国贝类水产品中麻痹性贝类毒素限量标准的比对[J]. 中国热带医学,2006, 6 (1) : 176 –178. |
| Click to display the text | |
| [7] | 中华人民共和国农业部. SC/T 3023-2004无公害食品麻痹性贝类毒素的测定生物法[S]. 北京:中国农业出版社, 2004. |
| Click to display the text | |
| [8] | 中华人民共和国卫生部, 中国标准化管理委员会.GB/T 5009.213-2008贝类中麻痹性贝类毒素的测定[S]. 北京: 中国标准出版社, 2009. |
| Click to display the text | |
| [9] | 吴蓓莉, 钟惠英, 邱结琼, 等. 麻痹性贝类毒素的生物法与酶联免疫法测定比较[J]. 宁波农业科技,2014 (3) : 14 –17. |
| Click to display the text | |
| [10] | 中华人民共和国国家进出口商品检验局. SN/T1735-2006进出口贝类产品中麻痹性贝类毒素检验方法高效液相色谱法[S].北京:中国标准化管理委员会, 2006. |
| Click to display the text | |
| [11] | 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. GB/T 23215-2008贝类中多种麻痹性贝类毒素含量的测定液相色谱-荧光检测法[S].北京: 中国标准化管理委员会, 2008. |
| Click to display the text | |
| [12] | 刘红河, 刘桂华, 毛丽莎. 麻痹性贝类毒素的高效液相色谱-串联质谱测定方法研究[J]. 实用预防医学,2008, 15 (4) : 1024 –1027. |
| Click to display the text | |
| [13] | 刘红河, 杨俊, 陈裕华, 等. 亲水作用液相色谱/串联质谱联用法测定海产品中麻痹性贝类毒素[J]. 现代预防医学,2010, 37 (7) : 1328 –1332. |
| Click to display the text | |
| [14] | 于慧娟, 蔡友琼, 黄宣运, 等. 10种麻痹性贝类毒素的固相萃取及液相色谱-串联质谱测定法[J]. 海洋渔业,2015, 37 (4) : 364 –371. |
| Click to display the text | |
| [15] | 母清林, 方杰, 王晓华, 等. 液相色谱-串联质谱法检测贝类产品中麻痹性贝类毒素[J]. 中国环境监测,2013, 29 (2) : 58 –61. |
| Click to display the text | |
| [16] | Mattarozzi M, Milioli M, Bianchi F, et al. Optimization of a rapid QuEChERS sample treatment method for HILIC-MS2 analysis of paralytic shellfish poisoning (PSP) toxins in mussels[J]. Food Control,2016, 60 : 138 –145. |
| Click to display the text |


