2. 华南师范大学, 广东省化学品污染与环境安全重点实验室, 广州 510006;
3. 华南师范大学, 教育部环境理论化学重点实验室, 广州 510006
2. Guangdong Provincial Key Laboratory of Chemical Pollution and Environmental Safety, South China Normal University, Guangzhou 510006;
3. MOE Key Laboratory of Theoretical Chemistry of Environment, South China Normal University, Guangzhou 510006
目前, 许多行业(如冶金、采矿、化工、制造业等)废水中含有多种有毒有害重金属离子, 其中, 以镉(Cd)污染危害最为严重(Sun et al., 2020).由于Cd极易在生物体内富集, 且难以降解, 如果长期接触过量的Cd, 则会引起人体肾脏和肝脏损害, 甚至可能出现致癌致畸的病变(Wang et al., 2019).为此, 一些高效的水处理技术, 如化学沉淀、离子交换法、浮选法、膜过滤法、电化学处理法、混凝-絮凝法及吸附法等被用于去除水体中的Cd(Ⅱ)(Ali et al., 2019).相较于其他方法, 吸附法具有效率高、性能优、易操作、低成本和环境友好等优点(Hassan et al., 2020).
在吸附法中, 吸附剂的选择尤为重要.作为一种储量丰富、成本低廉的矿物材料, 海泡石(Sepiolite)是一种链层状多孔富镁硅酸盐黏土矿物, 化学通式为Mg4Si6O15(OH)26H2O(Kara et al., 2003).其内部结构呈现出管状贯穿通道(0.36 nm×10.6 nm), 并具有较高的比表面积(800~900 m2·g-1)(李婷婷等, 2021).然而, 海泡石的孔隙容易发生阻塞, 实际的比表面积很难达到理论值(谢婧如等, 2016), 因此, 需要通过适当的改性处理才能够获得更好的吸附性能.目前, 常用的改性方法有水热活化、酸修饰、离子交换、磁化处理和有机改性等, 这些方法各有优缺点(方佳浚等, 2021).其中, 酸修饰是通过氢离子取代海泡石结构八面体层中的镁离子, 可使内部通道更加顺畅, 并增大吸附接触面积.研究表明, 随着海泡石脱镁程度的增加, 其微孔变大和大孔扩展, 而晶体结构也变为硅氧四面体结构(He et al., 2020).同时, 为了满足吸附后固液分离的要求, 需对吸附材料进行磁化处理, 从而实现材料的回收利用(Zhou et al., 2018).
本研究主要采用酸修饰和磁化处理相结合的改性方法, 旨在制备出一种吸附效率高、性能好、易于回收的环保型海泡石材料.然而, 酸的种类很多, 如有机酸和无机酸、含氧酸和无氧酸、一元酸和多元酸、强酸和弱酸、氧化性酸和非氧化性酸等.这些酸对海泡石脱镁的效果具有差异性, 而且可能会影响到海泡石的磁化程度.因此, 本研究通过盐酸、硝酸、磷酸和醋酸等类型的酸改性, 再经过不同比例的混铁磁化处理海泡石, 考察其吸附性能变化并探讨其吸附行为机制, 以期为海泡石材料的高值化利用提供科学的理论依据和技术支持.
2 材料与方法(Materials and methods) 2.1 化学药品与仪器天然海泡石(R-Sep)购于广州某化工公司;盐酸(HCl)、硝酸(HNO3)、磷酸(H3PO4)、醋酸(CH3COOH)、硝酸镉(Cd(NO3)2·4H2O)、六水合三氯化铁(FeCl3·6H2O)和四水合氯化亚铁(FeCl2·4H2O) 均为分析纯, 铅标液和锌标液为优级纯, 以上药品均购于上海阿拉丁生化科技股份有限公司.
2.2 材料制备根据前期的正交实验进行优化, 海泡石吸附材料的制备方法分别为:①盐酸修饰-磁改性海泡石(H-Sep):将40 mL 1.5 mol·L-1的HCl溶液与10 g的R-Sep混合后, 在30 ℃条件下搅拌3 h;抽滤后, 加入100 mL以1 ∶ 3比例配制的Fe(Ⅱ)/Fe(Ⅲ)混铁溶液, 充分搅拌1 h;调节混合液pH至9后, 置于40 ℃条件下再搅拌0.5 h.②硝酸修饰-磁改性海泡石(N-Sep):将40 mL 3.0 mol·L-1的HNO3溶液与10 g的R-Sep混合后, 在30 ℃条件下搅拌6 h;抽滤后, 加入100 mL以4 ∶ 3比例配制的Fe(Ⅱ)/Fe(Ⅲ)混铁溶液, 充分搅拌1 h;调节混合液pH至12后, 置于60 ℃条件下搅拌1.5 h.③磷酸修饰-磁改性海泡石(P-Sep):将140 mL 4.5 mol·L-1的H3PO4溶液与10 g的R-Sep混合后, 在30 ℃条件下搅拌3 h;抽滤后, 加入100 mL以4 ∶ 3比例配制的Fe(Ⅱ)/Fe(Ⅲ)混铁溶液, 充分搅拌1 h;调节混合液pH至10后, 置于40 ℃条件下搅拌2 h.④醋酸修饰-磁改性海泡石(A-Sep):将140 mL 6.0 mol·L-1的醋酸溶液与10 g的R-Sep混合后, 在30 ℃条件下搅拌6 h;抽滤后, 加入100 mL以1 ∶ 3比例配制的Fe(Ⅱ)/Fe(Ⅲ)混铁溶液, 充分搅拌1 h;调节混合液的pH至11后, 置于40 ℃条件下搅拌0.5 h.以上材料均陈化2 h后, 抽滤、烘干、研磨过筛, 在密闭干燥条件下保存以备用.
2.3 表征分析采用扫描电子显微镜(SEM, Hitachis-3400N, 日本)和透射电子显微镜(TEM, FEI Tecnai G2 f20 s-twin, 美国)观察海泡石材料的微观表面形貌, 同时采用能量色散光谱仪(EDS, INCA ENERGY 350, 英国)确定材料的O、Mg、Si等元素含量;利用Brunauer-Emmett-Teller (BET, Micromeritics TriStar Ⅱ, Norcross, 美国)方法计算改性材料的比表面积、平均孔径及孔容;利用傅里叶变换红外光谱(FTIR, Thermo, Nicolet 6700, 美国)分析材料的功能基团;使用VSM-100振动样品磁力计(VSM, Quantum Design SQUID, 美国)测量材料的磁滞回线;通过X射线光电子能谱(XPS, Thermo SCIENTIFIC ESCALAB 250Xi, 美国)测定样品表面元素组成及峰位价态等信息.
2.4 吸附实验在H-Sep、N-Sep、P-Sep和A-Sep投加量分别为0.05、0.10、0.15、0.20 g的10 mL锥形瓶中加入Cd(Ⅱ)溶液(初始浓度为100 mg·L-1, pH为6.5), 然后在25 ℃下恒温振荡(180 r·min-1)3 h, 取样测试;在确定最佳投加量后, 其他条件不变, 将pH分别调至2.0、3.5、5.0、6.5和8.0进行测试, 确定最佳pH值;在上述最佳条件下, 选取在10、25和40 ℃温度条件下进行吸附操作.对于其他阴阳离子的影响, 分别在Cd(Ⅱ)溶液中加入0、50、100、150 mg·L-1的Na+和Cl-干扰离子, 其他反应条件同上.竞争吸附实验则是在100 mg·L-1的Cd(Ⅱ)溶液中分别配置0、50、100、200 mg·L-1的Zn(Ⅱ)溶液, 其他反应条件同离子干扰实验;然后, 利用原子吸收光谱(AA7000型, 日本岛津)测定吸附平衡后溶液中重金属离子浓度;每个样品均设置3个平行样.吸附率(R)和吸附量(qt)计算公式分别见式(1)~(2).

|
(1) |
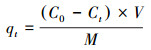
|
(2) |
式中, C0为初始时溶液中重金属离子的浓度(mg·L-1), Ct为吸附一定时间后滤液中重金属离子的浓度(mg·L-1), V为溶液体积(L), M为吸附剂的用量(g).
在上述最佳条件下, 配置50 mL 100 mg·L-1的Cd(Ⅱ)溶液, 分别称取0.25 g 4种改性材料至50 mL离心管中, 振荡3 h取样;然后配置200 mg·L-1的EDTA溶液用于解吸, 振荡1 h取样, 用去离子水洗涤解吸后的材料3~5遍, 烘干, 如此循环5次, 取样测定.
在上述最佳条件下, 分别配置250 mL 100 mg·L-1的Cd(Ⅱ)溶液, 分别称取1.25 g 4种改性材料至250 mL锥形瓶中, 在温度为10、25、40 ℃及振荡速度为180 r·min-1的条件下处理3 h, 在不同时间点取样测定, 根据式(2)计算重金属吸附量.对实验结果采用准一级动力学模型(式(3))、准二级动力学模型(式(4))和颗粒内扩散吸附模型(式(5))进行拟合.其中, 准一级动力学模型是基于吸附过程主要受扩散步骤影响速率的假设(Tan et al., 2017), 准二级动力学模型是假设吸附剂表面未被吸附质占据的空位数目的平方决定了吸附速率(Ho et al., 1999), 颗粒内扩散吸附模型的假设是基于粒子间的扩散(Tan et al., 2017).
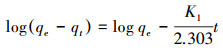
|
(3) |
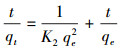
|
(4) |
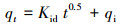
|
(5) |
式中, qe为吸附平衡时的吸附量(mg·g-1), qt为t时刻的吸附量(mg·g-1), K1为准一级速率常数(min-1), K2为准二级速率常数(g·mg-1·min-1), Kid为颗粒内扩散速率常数(mg·g-1·min-0.5), qi为初始吸附量(mg·g-1).
配置浓度分别为10、50、100、200、300、500 mg·L-1的Cd(Ⅱ)溶液, 称取0.05 g H-Sep、N-Sep、P-Sep和A-Sep于锥形瓶中, 分别加入不同浓度的Cd2+溶液, 其他反应条件与2.4.1节相同.根据式(1)计算吸附量, 对实验结果进行Langmuir、Freundlich和Temkin吸附等温线模型拟合, 分别见式(6)~(8)(Wang et al., 2020).
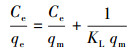
|
(6) |
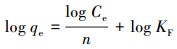
|
(7) |
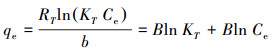
|
(8) |
式中, Ce为吸附平衡时溶液中金属离子浓度(mg·L-1), qe为吸附平衡时的吸附量(mg·g-1), KL为Langmuir常数(L·mg-1), qm为饱和吸附量(mg·g-1), 1/n用于表征吸附强度, KF为Freundlich常数((L·mg-1)1/n), RT为理想气体常数(8.314 J·mol-1·K-1), T为开尔文温度(K), b为吸附能变量(kJ·mol-1), KT为吸附过程中与结合能有关的常数(L·mg-1), 常数B=RT/b.
3 结果与讨论(Results and discussion) 3.1 表征分析H-Sep、N-Sep、P-Sep、A-Sep和R-Sep的SEM和TEM形貌如图 1所示.在SEM图像中, R-Sep的表面光滑, 并呈杂乱状态堆叠, 显然, 这些堆叠结构覆盖了海泡石的表面, 导致其部分孔道可能被堵塞.而所有的酸修饰-磁化海泡石材料表面蓬松稀疏, 且能看到明显的颗粒负载, 这说明其孔隙通道被打开, 从而极大地增加了吸附接触面积.TEM图像结果与SEM结果一致, 与天然海泡石相比, 改性海泡石的纤维束上出现了明显的颗粒状物质, 证实了Fe元素颗粒成功负载在改性海泡石上.这种结构会使得吸附材料与吸附剂接触面积增大, 从而更有利于对污染物的吸附.材料表面元素含量如表 1所示, R-Sep中主要元素是O和Si;与R-Sep相比, H-Sep、N-Sep、P-Sep和A-Sep中Fe元素含量增加较为明显, 确定Fe(Ⅱ)、Fe(Ⅲ)微粒成功大量负载在海泡石表面, 从而使材料更好地具有磁性功能;但与其他改性的海泡石相比, P-Sep的Fe元素含量最少.吸附后, H-Sep、N-Sep、P-Sep和A-Sep中均出现Cd元素信号峰.海泡石改性前后的比表面积及孔容孔径如表 2所示, 从表中数据可以看出, 经过4种酸修饰的海泡石的比表面积和孔容孔径均增大, 从而使重金属离子能够更好地负载在改性海泡石的表面.这可能是由于沸石通道中的杂质经酸修饰后被溶蚀去除, 从而在海泡石中留下了大量的孔道, 因此, 极大地提升了海泡石的比表面积和孔容, 从而增大了其吸附容量(龙来寿等, 2021).
 |
| 图 1 天然海泡石与改性海泡石扫描电镜图(a.H-Sep, b.N-Sep, c.P-Sep, d.A-Sep, e.R-Sep)和透射电镜图(f.H-Sep, g.N-Sep, h.P-Sep, i.A-Sep, j.R-Sep) Fig. 1 Scanning electron micrograph of natural sepiolite and modified sepiolite(a.H-Sep, b.N-Sep, c.P-Sep, d.A-Sep, e.R-Sep) and TEM images(f.H-Sep, g.N-Sep, h.P-Sep, i.A-Sep, j.R-Sep) |
| 表 1 天然与改性海泡石材料的元素组成 Table 1 Elemental composition of natural sepiolite and modified sepiolite |
| 表 2 海泡石改性前后BET表征数据 Table 2 BET characterization data of sepiolite before and after modification |
由FTIR图谱(图 2)可知, 所有材料均具有海泡石特征峰, 例如, 3440 cm-1处的吸收峰为—OH基团伸缩振动峰, 1641 cm-1处的伸缩振动峰是—OH基团的特征峰(Zhang et al., 2018), 1032 cm-1和470 cm-1处的吸收峰属于Si—O—Si和O—Si—O拉伸振动峰, 799 cm-1和780 cm-1处的伸缩振动峰则属于Si—O和Si—Si, 在3687 cm-1处则出现Mg—OH的伸缩振动峰(Zhou et al., 2018).对于改性海泡石, 它们却具有各自明显的特征峰, 例如, N-Sep在1380 cm-1处存在硝酸根的伸缩振动峰(Liatsou et al., 2016);P-Sep在1160 cm-1处和981 cm-1处分别为P—O—P的反对称和对称伸缩振动峰(Kinfack Leoga et al., 2018);A-Sep在1036 cm-1处为C—H反对称和对称的伸缩振动峰, 在1400 cm-1处出现的是羧基的C O伸缩振动峰(Li et al., 2018).同时, 这些改性海泡石的Si—O特征峰强度相对减弱, 而Fe—O的吸收峰(635 cm-1)出现, 而且3440 cm-1处出现的Fe3O4中—OH的伸缩振动峰比R-Sep更强(Chang et al., 2010), 这些变化表明这些材料具有一定的磁化特征.但P-Sep的Fe—O特征峰发生了更为明显的移动, 说明P-Sep的Fe—O成键强度发生了改变, 并可能会对其磁化效果产生影响.同时, VSM结果显示(图 3), H-Sep、N-Sep、A-Sep这3种材料具有超顺磁性(李靖等, 2019), 可通过永磁体作用获得较高的分离效率(Okunev et al., 2010).但P-Sep的磁分离效率不高, 这与EDS和FT-IR分析的结果相符合.
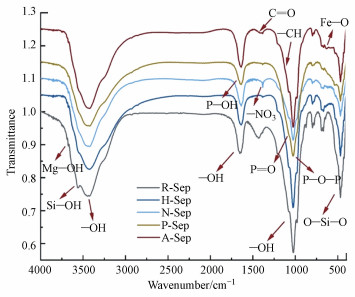 |
| 图 2 天然海泡石与改性海泡石的傅里叶红外变换光谱图 Fig. 2 FTIR pattern of natural sepiolite and modified sepiolite |
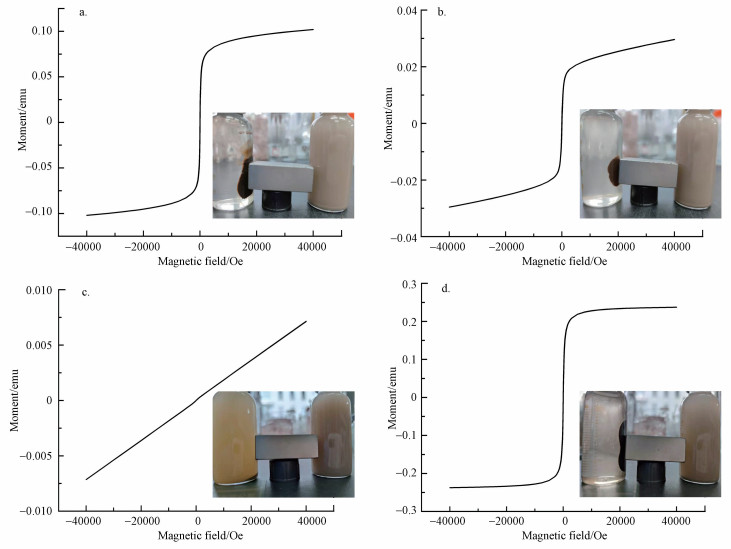 |
| 图 3 改性海泡石的磁化曲线和磁化效果图 (a.H-Sep, b.N-Sep, c.P-Sep, d.A-Sep) Fig. 3 Magnetization curve and effect of the modified sepiolite (a.H-Sep, b.N-Sep, c.P-Sep, d.A-Sep) |
从图 4a看出, 改性海泡石材料在投加量为0.05 g时吸附效果最好, 其中以P-Sep样品最为显著.随着投加量的继续增加, 单位质量吸附剂的可吸附量减少.综合对比后, 选择0.05 g作为后续实验的投加量.溶液pH值会影响材料表面官能团电荷和稳定性, 进而影响其吸附性能(Zhang et al., 2021).如图 4b所示, 当pH值为2.0时, 仅P-Sep具有吸附效果, 但吸附性能较差, 其他改性海泡石材料几乎不能产生吸附作用.这是因为在pH较低时, 大量H+会生成H3O+并结合在吸附剂表面, 导致吸附位点质子化, 表面带正电荷, 使得Cd(Ⅱ)由于静电斥力而无法靠近吸附位点.随着pH值的增加, 改性海泡石材料的吸附量先增大后减小, 在pH值为6.5时, 其吸附量达到最大值.其中, P-Sep的吸附量最大, 可达到23.2 mg·g-1.这是由于pH升高而H+浓度下降, 使得Cd(Ⅱ)与H+之间的竞争吸附影响减弱.同时, pH升高时, 部分Cd(Ⅱ)与OH-结合形成Cd(OH)+, 一方面会降低材料表面的电荷, 减弱静电斥力;另一方面有助于提高吸附位点与Cd(Ⅱ)之间的结合能力(Yu et al., 2021), 从而有利于Cd(Ⅱ)占据更多的吸附位点.但当pH值为8.0时, 改性海泡石的吸附量出现明显下降, 这是由于大量的Cd(OH)+的产生, 并继续与OH-结合生成Cd(OH)2沉淀.因此, 后续吸附实验选择pH值为6.0.
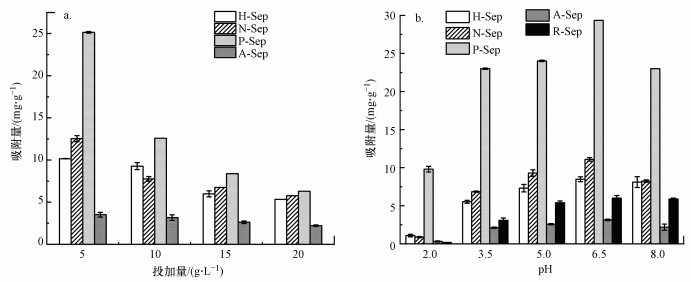 |
| 图 4 投加量(a)和pH值(b) 对改性海泡石材料去除Cd(Ⅱ)的影响 Fig. 4 Effect of dosage (a) and pH values (b) for the removal of Cd (Ⅱ) onto modified sepiolite |
通过Freundlich、Langmuir和Temkin吸附等温模型拟合H-Sep、N-Sep、P-Sep和A-Sep对Cd(Ⅱ)的吸附行为, 结果如图 5所示.相比于Freundlich和Temkin吸附等温模型, 数据拟合结果更符合Langmuir等温模型(R12>0.97), 说明改性海泡石吸附Cd(Ⅱ)的行为是典型的单分子层吸附(Zheng et al., 2018).根据拟合结果可知, P-Sep的最大拟合吸附量可达到59.2 mg·g-1, 远高于H-Sep、N-Sep和A-Sep的最大拟合吸附量, 这可能是因为磷酸属于三元酸, 可电离出的H+量要多于其他3种酸, 其可置换海泡石结构中的Mg(Ⅱ)也更多, 且内部孔径通道打开程度更大.而且, P-Sep的吸附容量也明显高于现有的一些海泡石材料, 如磁性海泡石(16.10 mg·g-1)(余铁萍等, 2013)、预处理海泡石(27.78 mg·g-1)(Huang et al., 2015)、巯基海泡石(34.72 mg·g-1)(Liang et al., 2011)、铁改性海泡石(8.07 mg·g-1)(马烁等, 2019)、酸热处理海泡石(12.31 mg·g-1)(徐应明等, 2010)和酸热处理海泡石(22.147 mg·g-1)(张悦等, 2019)等.
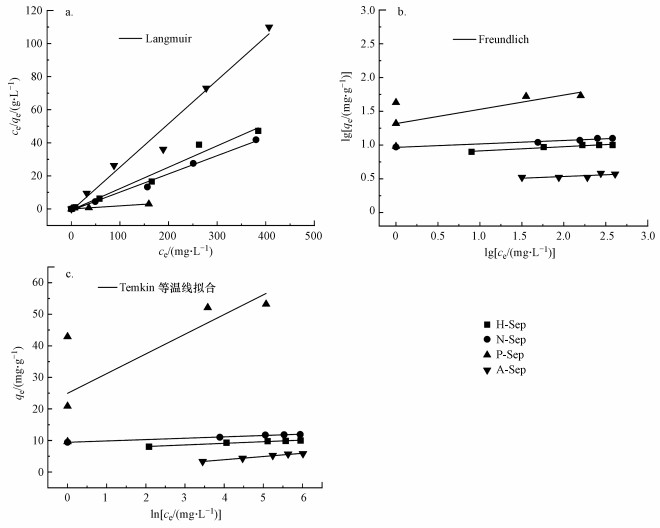 |
| 图 5 吸附等温模型拟合图 (a.Langmuir, b.Freundlich, c.Temkin) Fig. 5 Fitting diagram of adsorption isotherm models (a.Langmuir, b.Freundlich, c.Temkin) |
H-Sep、N-Sep、P-Sep和A-Sep的准一级吸附动力学、准二级吸附动力学和颗粒内扩散方程拟合曲线如图 6所示.从图 6a~6c中可以看出, 在10、25、40 ℃下这些改性海泡石的吸附量稍有差别, 随着温度的增加吸附量增大, 表明在一定温度下其吸附行为会受到温度的影响, 相对较高的温度有利于吸附过程的进行.与准一级吸附动力学模型相比, 准二级动力学模型的拟合效果更好(R22较高, 表 3), 说明化学吸附是Cd(Ⅱ) 吸附的主要速率控制步骤(Zheng et al., 2018).对于颗粒内扩散方程(图 6d~6f), 改性海泡石吸附Cd(Ⅱ)过程包括3个阶段:第1阶段对应图中第一截线段, 斜率较大、坡度较陡, 这是海泡石外表面吸附, 或称大孔扩散阶段;第2阶段的坡度较缓, 属于内扩散阶段;第3阶段斜率趋于平缓, 吸附基本达到饱和状态.这两个阶段(第2和第3阶段)是Cd(Ⅱ)进入改性海泡石内部的过程, 也称为微孔扩散(Song et al., 2015;Wang et al., 2017).其中, K1值大于K2和K3值, 这说明第1阶段的吸附速度最快, 不能视为整个吸附过程的控制速度;而第2阶段和第3阶段属于吸附速度的控制步骤, 即微孔扩散的过程是改性海泡石吸附过程的关键控制因素.
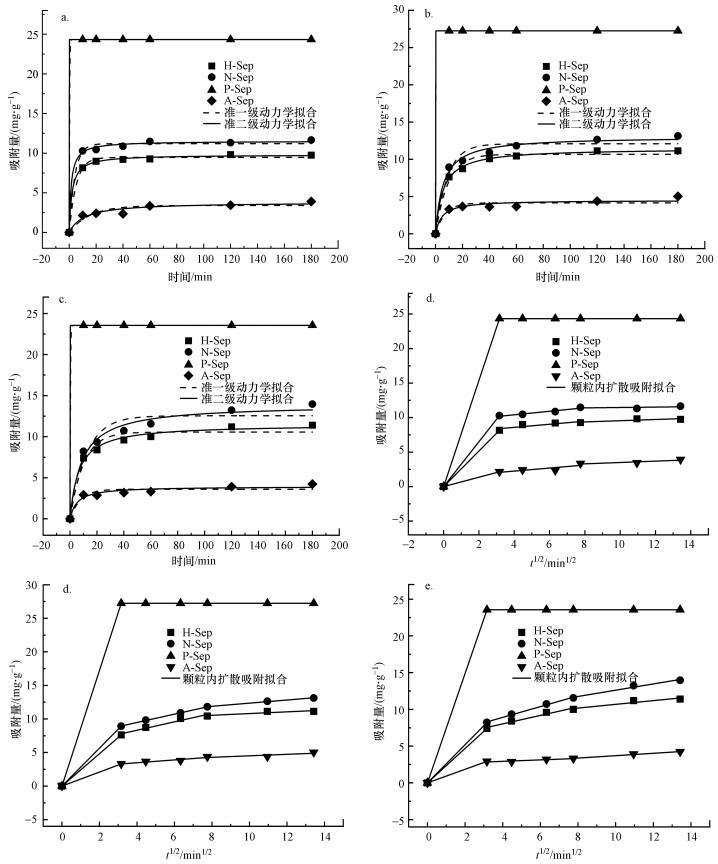 |
| 图 6 在10 ℃ (a)、25 ℃ (b)、40 ℃ (c) 下的准一级和准二级动力学模型拟合结果及在10 ℃ (e)、25 ℃ (d)、40 ℃ (f) 下的颗粒内扩散模型拟合结果 Fig. 6 Pseudo-first-order and pseudo-second-order kinetics at 10 ℃(a), 25 ℃(b), 40 ℃(c), and intra-particle diffusion models at 10 ℃(e), 25 ℃(d), 40 ℃(f) |
| 表 3 不同温度下H-Sep、N-Sep、P-Sep和A-Sep的动力学参数 Table 3 Kinetic parameters of H-Sep, N-Sep, P-Sep and A-Sep at different temperatures |
水体中常见离子, 如Na+、Cl-等对H-Sep、N-Sep、P-Sep、A-Sep和R-Sep吸附性能的影响如图 7a所示.由图可知, Cl-和Na+浓度的增加对天然海泡石与4种酸修饰磁改性海泡石的吸附效果没有太大影响, 这表明这些海泡石材料可以用于天然水体中Cd(Ⅱ)的吸附去除.可再生性能是影响吸附剂是否能够可持续应用的重要影响因素, 如图 7b所示, 经过5次连续吸附脱附后, 4种改性海泡石的吸附量只是略微下降, 说明改性海泡石具有良好的可重复使用性能, 是一种稳定、高效且可循环利用的吸附材料.一些重金属离子如Zn(Ⅱ)、Pb(Ⅱ)的吸附测试结果如图 7c~7i所示, 随着Zn(Ⅱ)、Pb(Ⅱ)浓度的增加, 海泡石材料对Cd(Ⅱ)的吸附性能逐渐降低;反之, 随着Zn(Ⅱ)、Pb(Ⅱ)浓度的增加, 其对Zn(Ⅱ)、Pb(Ⅱ)的吸附量逐渐升高(图 7c、7e).这说明重金属Zn(Ⅱ)、Pb(Ⅱ)会占据海泡石吸附材料中对重金属Cd(Ⅱ)的吸附位点, 且浓度越高, 占据的越多.
 |
| 图 7 Na+、Cl- (a)、再生性(b)、Zn(Ⅱ) (c、d)、Pb(Ⅱ) (e、f)和共吸附(g、h、i) 对海泡石吸附Cd(Ⅱ)的影响 Fig. 7 The influence of Na+, Cl- (a), regeneration property(b), Zn(Ⅱ) (c, d), Pb(Ⅱ) (e, f) and co-adsorption (g, h, i) on the adsorption of Cd(Ⅱ) on sepiolite |
富集系数(E)能够很好地表达改性海泡石对重金属离子的吸附选择性, 计算公式见式(9)(杨秀敏, 2020).如表 4所示, Zn(Ⅱ)与Cd(Ⅱ)的富集系数关系为E(Pb2+)>E(Zn2+)>E(Cd2+), 吸附材料对Pb(Ⅱ)、Zn(Ⅱ)的富集能力要大于对Cd(Ⅱ)的富集能力.而且研究表明, 对同价离子而言, 重金属离子半径越小, 越容易发生交换反应, 吸附能力就越强(李计元等, 2008).对于二价金属离子的有效水合离子半径可由经验公式(10)获取(Shirvani et al., 2006).Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)的离子半径、有效水合离子半径和水合热见表 5.由于离子半径为Cd(Ⅱ)> Zn(Ⅱ), 且Cd(Ⅱ)的有效水合离子半径大于Zn(Ⅱ), 所以Zn(Ⅱ)更易被吸附.然而, 具有低水合热的金属离子易被吸附(陈德翼等, 2009), Cd(Ⅱ)的水合热要小于Zn(Ⅱ), 从这个角度来看, Zn(Ⅱ)对Cd(Ⅱ)的竞争吸附作用十分有限.虽然Pb(Ⅱ)的离子半径最大, 但其水合热却最小, 所以最容易脱失配位体水而成为裸露的Pb2+, 且Pb(Ⅱ)对Cd(Ⅱ)的富集系数最大, 因此, 海泡石对其吸附选择性大于其他两个金属离子(孙亚杰等, 2017).
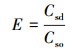
|
(9) |
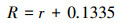
|
(10) |
| 表 4 海泡石材料对Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)的富集系数 Table 4 Enrichment coefficient of sepiolite for Zn(Ⅱ), Pb(Ⅱ) and Cd(Ⅱ) |
| 表 5 Zn(Ⅱ)、Pb(Ⅱ)和Cd(Ⅱ)的离子半径、有效水合离子半径及水化热 Table 5 Ionic radius, effective hydrated ion radius and heat of hydration of Zn(Ⅱ), Pb(Ⅱ) and Cd(Ⅱ) |
式中, Csd为溶液中被吸附重金属离子的含量(mg·g-1), Cso为吸附前溶液中重金属离子的含量(mg·g-1), R为重金属有效水合离子半径(nm), r为重金属离子半径(pm).
3.3 吸附机理通过XPS分析对H-Sep、N-Sep、P-Sep和A-Sep的吸附行为进行研究, 发现这些改性海泡石材料均出现Cd的特征峰(图 8a~8d), 例如, H-Sep的Cd位于412.24 eV(Cd3d3/2)和405.37 eV(Cd3d5/2)处;N-Sep则的Cd位于412.32 eV(Cd3d3/2)和405.51 eV(Cd3d5/2)处;P-Sep的Cd位于412.28 eV(Cd3d3/2)和405.56 eV(Cd3d5/2)处;A-Sep的Cd位于412.64 eV(Cd3d3/2)和405.72 eV(Cd3d5/2)处.经过磁化处理后, 改性海泡石的Fe2p谱主要由Fe 2p3/2和Fe 2p1/2组成.其中, Fe 2p3/2中711 eV附近的峰属于Fe—OH或Fe—O类型(图 8e~8h), 这对于Cd(Ⅱ)产生吸附行为起到关键作用, 如图 8i~8l所示, 吸附后的改性海泡石Fe—OH或Fe—O的峰均发生了变化(Habish et al., 2016).除此之外, N-Sep的O峰从531.26 eV处偏移至531.12 eV处(图 8m, 8p), 结合FT-IR中—OH基团的出现, 可推断吸附过程主要是Cd(Ⅱ)与羟基发生络合反应, 生成CO-Cd+络合物.吸附后P-Sep的P 2p2/3和P 2p1/2峰位置和峰面积都发生了相应的变化(图 8n, 8q), 这表明磷酸基团有利于对Cd(Ⅱ)的络合(Zhuang et al., 2019).A-Sep的羧基则因吸附而出现较明显的位移变化, O—C O峰从287.86 eV位移至287.91 eV处(图 8o, 8r), 这说明羰基与Cd(Ⅱ)之间存在络合行为(Zheng et al., 2018).结合以上分析, P-Sep的磁化程度最差, 但吸附容量最大, 这说明P-Sep的磷酸基团络合作用最大;而A-Sep的吸附性能最差, 这意味着有机酸的修饰效果比无机酸差, 而羧基中O元素的络合行为弱于N-Sep的羟基中的O元素.另外, 含氧酸修饰效果比无氧酸修饰效果好, 这是因为N-Sep吸附Cd(Ⅱ)途径来源于Fe和O元素的作用.
 |
| 图 8 改性海泡石吸附前后的XPS谱图 (a~d.4种改性海泡石的Cd元素;e~l.4种改性海泡石吸附前后的Fe元素;m, p.N-Sep吸附前后的O元素;n, q.P-Sep吸附前后的P元素;o~r.A-Sep吸附前后的C元素) Fig. 8 XPS pattern of modified sepiolite before and after adsorption (a~d. Cd of modified sepiolite after adsorption; e~l. Fe of modified sepiolite before and after adsorption; m, p. O of N-Sep before after adsorption; n, q. P of P-Sep before after adsorption; o~r. C of A-Sep before after adsorption) |
1) 通过酸修饰-磁化的方法, 不但可以显著提升海泡石材料对水体中Cd(Ⅱ)的吸附性能, 而且其他阴阳离子对其吸附行为的干扰影响有限, 可作为一种高效环保的可再生材料.
2) 4种改性海泡石材料的吸附行为符合Langmuir吸附等温模型, 其中, P-Sep的最大吸附量达到52.6 mg·g-1.吸附动力学实验结果最符合准二级动力学发成, 说明改性海泡石对重金属Cd(Ⅱ)的吸附是化学吸附.
3) 结合吸附性能测试结果和XPS机理分析发现, 酸修饰效果顺序为:多元酸修饰(P-Sep)>一元酸修饰(H-Sep和N-Sep);含氧酸修饰(N-Sep)>无氧酸修饰(H-Sep);无机酸修饰(H-Sep、N-Sep和P-Sep)>有机酸修饰(A-Sep);强酸(H-Sep和N-Sep)或中强酸修饰(P-Sep)>弱酸修饰(A-Sep).但磷酸修饰海泡石(P-Sep)的磁化程度最差.
Alia I, Basheer A A, Mbianda X Y, et al. 2019. Graphene based adsorbents for remediation of noxious pollutants from wastewater[J]. Environment International, 127: 160-180. |
Chang C W, Huang Y S, Huang B Y, et al. 2010. Green fabrication of agar-conjugated Fe3O4 magnetic nanoparticles[J]. Nanotechnology, 21(44): 445601. DOI:10.1088/0957-4484/21/44/445601 |
陈德翼, 郑刘春, 党志, 等. 2009. Cu2+和Pb2+存在下改性玉米秸秆对Cd2+的吸附[J]. 环境化学, 28(3): 379-382. DOI:10.3321/j.issn:0254-6108.2009.03.012 |
方佳浚, 任子杰, 高惠民, 等. 2021. 无机有机联合改性海泡石对苯的吸附特性研究[J]. 硅酸盐通报, 40(1): 172-179. |
Habish A J, Lazarević S, Janković-Častvan I, et al. 2016. Nanoscale zerovalent iron (nZVI) supported by natural and acid-activated sepiolites: the effect of the nZVI/support ratio on the composite properties and Cd2+ adsorption[J]. Environmental Science and Pollution Research, 24(1): 628-643. |
Hassan M, Naidu R, Du J, et al. 2020. Critical review of magnetic biosorbents: Their preparation, application, and regeneration for wastewater treatment[J]. Science of the Total Environment, 702: 134893. DOI:10.1016/j.scitotenv.2019.134893 |
He Z, Ren B, Hursthouse A, et al. 2020. Efficient Removal of Cd(Ⅱ) Using SiO2-Mg(OH)2 Nanocomposites Derived from Sepiolite[J]. International Journal of Environmental Research and Public Health, 17(7): 2223. DOI:10.3390/ijerph17072223 |
Ho Y, McKay G. 1999. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 34(5): 451-465. DOI:10.1016/S0032-9592(98)00112-5 |
Huang J, Wu Z, Chen L, et al. 2013. The sorption of Cd(Ⅱ) and U(Ⅵ) on sepiolite: A combined experimental and modeling studies[J]. Journal of Molecular Liquids, 209: 706-712. |
Kara M, Yuzer H, Sabah E, Celik M S. 2003. Adsorption of cobalt from aqueous solutions onto sepiolite[J]. Water Research, 37(1): 224-232. DOI:10.1016/S0043-1354(02)00265-8 |
Kinfack Leoga A J, Youssef L, Roualdès S, et al. 2018. Phosphonic acid-based membranes as proton conductors prepared by a pulsed plasma enhanced chemical vapor deposition technique[J]. Thin Solid Films, 660: 506-515. DOI:10.1016/j.tsf.2018.06.059 |
Li B L, Zhu L, Wang L S, et al. 2018. Sorption of U(Ⅵ) on amidoxime-functionalized mesoporous silica[J]. Journal of Nuclear and Radiochemistry, 40(3): 166-174. |
李计元, 周彩楼, 马玉书, 等. 2008. 酸活化和热活化对海泡石显微结构的影响[J]. 非金属矿, 31(6): 13-15. |
李靖, 范明杰, 刘翔, 等. 2019. 双表面活性剂修饰下纳米零价铁对水中Cr(Ⅵ)污染去除研究[J]. 环境科学学报, 39(10): 3402-3409. |
龙来寿, 周悦, 郭会时, 等. 2021. 功能化磁性海泡石修复重金属污染土壤的研究[J]. 韶关学院学报, 42(3): 48-52. DOI:10.3969/j.issn.1007-5348.2021.03.010 |
李婷婷, 李瑞雪, 马政, 等. 2021. 纤维素-海藻酸钠-海泡石多孔微球的制备及其对亚甲基蓝吸附性能[J]. 复合材料学报, 38(12): 4295-4303. |
Liang X, Xu Y, Sun G, et al. 2013. Preparation and characterization of mercapto functionalized sepiolite and their application for sorption of lead and cadmium[J]. Chemical Engineering Journal, 174(1): 436-444. |
Liatsou I, Michail G, Demetriou M, et al. 2016. Uranium binding by biochar fibres derived from luffa cylindrica after controlled surface oxidation[J]. Journal of Radioanalytical & Nuclear Chemistry, 311(1): 871-875. |
马烁, 熊双莲, 熊力, 等. 2019. 铁改性海泡石吸附镉和砷效果及其影响因素[J]. 水处理技术, 45(10): 73-77. |
Okunev B N, Gromov A P, Zelenko V L, et al. 2009. Effect of residual gas on the dynamics of water adsorption under isobaric stages of adsorption heat pumps: Mathematical modelling[J]. International Journal of Heat and Mass Transfer, 53(7/8): 1283-1289. |
Shirvani M, Shariatmadari H, Kalbasi M, et al. 2006. Sorption of cadmium on palygorskite, sepiolite and calcite: equilibria and organic ligand affected kinetics[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 287(1): 182-190. |
Song W, Gao B, Zhang T, et al. 2015. High-capacity adsorption of dissolved hexavalent chromium using amine-functionalized magnetic corn stalk composites[J]. Bioresource Technology, 190: 550-557. DOI:10.1016/j.biortech.2015.01.103 |
Sun Z, Liu Y, Srinivasakannan C. 2020. One-pot fabrication of rod-like magnesium silicate and its adsorption for Cd2+[J]. Journal of Environmental Chemical Engineering, 8(5): 104380. DOI:10.1016/j.jece.2020.104380 |
孙亚杰, 赵天琪, 张春雷, 等. 2017. 糠醛渣木质素接枝聚丙烯酸水凝胶对Pb2+、Cu2+、Cd2+吸附性能研究[J]. 北京林业大学学报, 39(12): 102-111. |
Tan K, Hameed B H. 2017. Insight into the adsorption kinetics models for the removal of contaminants from aqueous solutions[J]. Journal of the Taiwan Institute of Chemical Engineers, 74: 25-48. DOI:10.1016/j.jtice.2017.01.024 |
Wang F, Hao M, Liang J, et al. 2019. A facile fabrication of sepiolite mineral nanofibers with excellent adsorption performance for Cd2+ ions[J]. RSC Advances, 9(69): 40184-40189. DOI:10.1039/C9RA07836C |
Wang J, Guo X. 2020. Adsorption kinetic models: Physical meanings, applications, and solving methods[J]. Journal of Hazardous Materials, 390: 122156. DOI:10.1016/j.jhazmat.2020.122156 |
Wang Z, Shen D, Shen F, et al. 2017. Ginkgo biloba L.shells-based adsorbent for the removal of Cu2+ and Cd2+ from aqueous solution: Kinetics, isotherm, thermodynamics and mechanisms[J]. Journal of Molecular Liquids, 241: 603-611. DOI:10.1016/j.molliq.2017.05.102 |
谢婧如, 陈本寿, 张进忠, 等. 2016. 巯基改性海泡石吸附水中的Hg(Ⅱ)[J]. 环境科学, 36(6): 2187-2194. |
徐应明, 梁学峰, 孙红国, 等. 2010. 酸和热处理对海泡石结构及吸附Pb2+、Cd2+性能的影响[J]. 环境科学, 31(6): 1560-1567. |
杨秀敏. 2020. 凹凸棒石对Zn2+、Cu2+、Cd2+的等温吸附实验研究[J]. 中国矿业, 29(11): 94-99. |
Yu H, Zheng L, Zhang T, et al. 2021. Adsorption behavior of Cd(Ⅱ) on TEMPO-oxidized cellulose in inorganic/organic complex systems[J]. Environmental Research, 195: 110848. DOI:10.1016/j.envres.2021.110848 |
余铁萍, 戴友芝, 王未平, 等. 2013. 磁性海泡石吸附水中重金属离子的特性及机理[J]. 环境化学, 32(8): 1566-1570. |
Zhang J, Yan Z, Fu L, et al. 2018. Silver nanoparticles assembled on modified sepiolite nanofibers for enhanced catalytic reduction of 4-nitrophenol[J]. Applied Clay Science, 166: 166-173. DOI:10.1016/j.clay.2018.09.026 |
Zhang T, Zheng L, Yu H, et al. 2021. Solution pH affects single, sequential and binary systems of sulfamethoxazole and cadmium adsorption by self-assembled cellulose: Promotion or inhibition?[J]. Journal of Hazardous Materials, 402: 124084. DOI:10.1016/j.jhazmat.2020.124084 |
Zheng L, Peng D, Meng P. 2018. Promotion effects of nitrogenous and oxygenic functional groups on cadmium(Ⅱ) removal by carboxylated corn stalk[J]. Journal of Cleaner Production, 201: 609-623. DOI:10.1016/j.jclepro.2018.08.070 |
Zhou Q, Huang J, Zhang X, et al. 2018. Assembling polypyrrole coated sepiolite fiber as efficient particle adsorbent for chromium (Ⅵ) removal with the feature of convenient recycling[J]. Applied Clay Science, 166: 307-317. DOI:10.1016/j.clay.2018.09.031 |
Zhuang S, Wang J. 2019. Removal of U(Ⅵ) from aqueous solution using phosphate functionalized bacterial cellulose as efficient adsorbent[J]. Radiochimica Acta, 107(6): 459-467. DOI:10.1515/ract-2018-3077 |
 2021, Vol. 41
2021, Vol. 41


