2. 北京建工环境修复股份有限公司, 污染场地安全修复国家工程实验室, 北京 100015
2. National Engineering Laboratory for Site Remediation Technologies, Beijing Construction Engineering Group Environmental Remediation Co., Ltd, Beijing 100015
砷(As)是一种类金属元素, 广泛用于生产半导体、杀虫剂、除草剂、木材防腐剂、农药、颜料等工业和日常用品.据统计, 2017年中国砷化学品生产量为2.5万t, 占全球砷产量的67.57%(3.7万t).由于含砷化学品的广泛使用, 导致每年有大量含砷废气、废渣、废水进入环境中.砷具有很强的毒性, 美国疾病控制中心(CDC)和国际癌症研究机构(LARC)将砷定为第一类致癌物质(刘辉利等, 2009).研究表明, 当人体摄入过量砷就会引起急性或慢性中毒, 还可诱发皮肤癌、肺癌和膀胱癌(Chatterjee et al., 1995).水体中砷以无机三价砷(As(Ⅲ))和五价砷(As(Ⅴ))为主(Rahman et al., 2005), 其中, As(Ⅲ)的毒性比As(Ⅴ)高25~60倍, 且迁移性更强(He et al., 2019).
目前废水中砷的去除方法主要有吸附法、混凝法、离子交换法、膜法及电化学等, 其中, 吸附法因具有操作简便、经济可行、可再生等特点而被广泛应用(Tsegaye et al., 2019).李荣辉等(2019)合成的活性氧化铝纳米材料能够有效吸附去除水中As(Ⅴ), 较商业活性氧化铝具有更好的除砷性能;孙媛媛等(2011)研究发现, Mg/Al双金属氧化物对溶液中的As(Ⅴ)有良好的吸附性能, 最高吸附效率可达到95%;黄博等(2019)研究了铝代水铁矿对As(Ⅴ)和Cd(Ⅱ)的协同作用, 发现其对As(Ⅴ)的去除效率为96%.此外, 环境中普遍存在的铁、锰氧化物也可用于含砷废水的处理.铁氧化物是环境中砷最重要的稳定剂之一, 可以通过表面吸附及共沉淀的方式固定砷, 其中, 弱晶型的水铁矿物因比表面积大和活性高等特性, 除砷效果最为显著(Lee et al., 2003).Dixit等(2003)研究发现, 非晶态氧化铁和针铁矿在pH小于6时, 对As(Ⅴ)的吸附效率更高;当pH大于7时, 对As(Ⅲ)的吸附效率更高.但铁氧化物不能将As(Ⅲ)氧化为As(Ⅴ), 其吸附的As(Ⅲ)易发生解吸而二次释放到环境中.相较而言, 锰氧化物(MnO2)是一种氧化能力仅次于O2且最具反应活性的矿物.Wang等(2015a; 2017)研究表明, 合成的δ-MnO2能够快速氧化As(Ⅲ)为As(Ⅴ), 从而降低砷的毒性, 但同时也发现As(Ⅴ)在锰氧化物表面的吸附能力有限.可见, 铁氧化物或锰氧化物对水中砷的去除均存在一定的弊端.近年来, 诸多学者尝试制备铁锰复合氧化物, 以提高废水中As(Ⅲ)和As(Ⅴ)的去除效率(叶树芯, 2016;周海燕等, 2019).黄永炳(2018)的研究表明, 采用化学法制备的铁锰复合矿物对As(Ⅲ)和As(Ⅴ)具有良好的去除效果, 去除率分别为95.86%和85.27%.Boland等(2014)研究发现, 化学合成的铁锰复合氧化物在As(Ⅲ)氧化过程中会释放Mn(Ⅱ)和Fe(Ⅱ), 其会参与催化铁锰氧化物中晶体结构的转变, 影响砷的吸附效果.
环境中存在多种铁锰氧化微生物能够快速催化氧化Mn(Ⅱ)和Fe(Ⅱ)进而诱导形成生物铁锰氧化物(Biogenic Fe-Mn oxides, BFMO).与化学合成的铁锰氧化物矿物相比, 原位生产BFMO的结晶弱、Mn价态高, 结构中八面体空穴多, 具有更大的比表面积, 从而对砷有更强的吸附、氧化能力(Tebo et al., 2004;Wang et al., 2020).Bai等(2016)研究发现, 原位形成的BFMO矿物表面含有大量铁锰氧化细菌, 可以重新氧化释放的Mn(Ⅱ)和Fe(Ⅱ), 不仅减少了Mn(Ⅱ)和Fe(Ⅱ)的释放, 还可为As(Ⅲ)和As(Ⅴ)提供新的吸附点位.因此, 原位形成的BFMO在含砷废水处理方面具有巨大的应用潜力, 但其除砷效果是否受pH、BFMO浓度、细菌密度、砷价态等因素的影响目前尚不明晰.
基于此, 本文通过改变砷的初始浓度、砷价态、细菌接种比、铁和锰浓度等因素来研究不同条件下细菌原位诱导形成BFMO对砷(As(Ⅲ)和As(Ⅴ))的去除效果.同时, 利用扫描电镜-能谱分析(SEM-EDS)、透射电镜(TEM)及X射线光电子能谱仪(XPS)等仪器分析表征BFMO吸附砷前后的矿物特性, 探讨BFMO对砷的去除机制.以期为BFMO原位修复砷污染环境提供科学指导.
2 材料与方法(Materials and methods) 2.1 锰氧化菌菌株锰氧化菌菌株(Pseudomonas putida strain MnB1, 23483)购于美国模式培养物集存库(ATCC).实验所用培养基为ATCC#279, 含有0.15 g·L-1硫酸亚铁铵、0.15 g·L-1柠檬酸钠、0.075 g·L-1酵母浸粉、0.05 g·L-1焦磷酸钠, 调节pH至7.0.
2.2 实验设计首先进行预实验, 以确定实验反应时间.向200 mL的ATCC#279培养基中加入0.16 g MnCO3后于115 ℃灭菌30 min, 冷却到室温后加入4-羟乙基哌嗪乙磺酸(HEPES), 维持反应体系pH在7.0±0.1(50 mmol·L-1), 再加入4 mL P. putida strain MnB1菌液、4 mL Fe(Ⅱ)储备液(500 mg·L-1).将反应瓶置于振荡培养箱并在180 r·min-1(30 ℃)条件下振荡培养培养7 d, 每天监测溶液中OD600、Mn(Ⅱ)和Fe(Ⅱ)浓度.根据此反应中OD600、Mn(Ⅱ)和Fe(Ⅱ)浓度的变化关系以确定后续反应时间.进一步研究砷浓度、砷价态、细菌接种比、初始铁和锰浓度等因素对原位生产BFMO对废水中砷去除效果的影响.在上述批量实验的基础上, 继续调节As(Ⅲ)或As(Ⅴ)浓度分别为0.5、1、2和5 mg·L-1, 细菌接种比分别为0.1%、0.25%、0.5%、1%和2%, MnCO3浓度分别为0.2、0.5、0.8、1.5和2 g·L-1, Fe(Ⅱ)浓度分别为2.5、5、10、25和50 mg·L-1.将上述各实验组培养瓶置于水平振荡器, 于180 r·min-1(30 ℃)下振荡培养5 d, 用0.22 μm滤头过滤, 测定滤液中残留As(Ⅲ)或As(Ⅴ)浓度, 计算砷的去除效率η(式(1)).
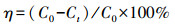
|
(1) |
式中, C0为水溶液中初始砷浓度(mg·L-1);Ct为实验后上清液中砷浓度(mg·L-1).
批量实验结束后, 收集反应后固体残余物, 在冷冻干燥机(FD-2B型, 上海比朗)中于-60 ℃条件下冻干6 h, 对铁锰复合氧化物的矿物特性进行表征分析.此外, 为了获取砷在铁锰氧化物表面的存在形式, 利用0.05 mol·L-1磷酸氢二铵抽提5 h, 测定抽提液中砷的浓度, 即为吸附态的砷;固相中总砷含量减去吸附态的砷, 即为共沉淀形式的砷(Watanabe et al., 2020).
2.3 分析方法OD600采用紫外分光光度计(UVmini-1240)测定, Mn(Ⅱ)和Fe(Ⅱ)浓度采用ICP-MS测定(ELAN DRC Ⅱ, 美国PE).水溶液中砷浓度采用原子荧光光度计(AFS-830, 北京吉天)测定, 仪器条件为:负高压280 V, 灯电流70 mA, 原子化器预热温度200 ℃, 载气流量600 mL·min-1, 屏蔽气流量800 mL·min-1, As(Ⅲ)和As(Ⅴ)的标准曲线浓度为1~20 μg·L-1.此外, 采用Zeiss Super 55 VP扫描电镜(SEM)对矿物样品进行表面结构分析, 同时结合Bruker XFlash 5010能谱分析仪(EDS)对矿物样品进行半定量分析.使用Tecnai G2 F20透射电子显微镜(TEM)观察小于0.2 μm的超微结构, 并用TEM-mapping分析BFMO表面Fe、Mn、As和O元素的分布.Thermo Fisher Scientific ESCALAB 250Xi X射线光电子能谱仪(XPS)用于确定As(Ⅲ)和As(Ⅴ)反应后BFMO表面元素组成和价态.在进行XPS测量时, 结合能扫描范围为0~1200 eV, 以100 ms的停留时间和150 eV进行广谱扫描;以20 eV通能获得As 3d、Mn 2p和Fe 2p的高分辨率光谱;使用Casa XPS进行数据分析、曲线拟合和定量分析, 以284.6 eV下的C 1s结合能作为参考.
3 结果与讨论(Results and discussion) 3.1 P. putida strain MnB1诱导BFMO微生物诱导产生BFMO过程中OD600、Mn(Ⅱ)和Fe(Ⅱ)浓度变化曲线如图 1所示.由图可知, 随着时间的增加, 溶液中的Mn(Ⅱ)浓度呈先升高后下降的趋势, 这是由于锰氧化菌诱导产生BFMO时, P. putida strain MnB1胞外聚合物率先溶解碳酸锰同时释放Mn(Ⅱ), 然后其被氧化成为高价态的MnO2(王华伟, 2015).Fe(Ⅱ)浓度先显著减小(p<0.05), 随后趋于平缓, 说明绝大部分的Fe(Ⅱ)在5 d之内被氧化成为铁氧化物, 与锰氧化物复合最终形成BFMO颗粒.OD600能间接反映BFMO浓度变化, 其数值在3 d时达到最大值, 之后趋于平缓, 这也表明5 d时, Mn(Ⅱ)和Fe(Ⅱ)的氧化作用基本完成.此外, 前期研究也表明, 不添加P. putida strain MnB1或菌株经钝化处理(60 ℃灭活30 min)诱导产生的BFMO含量很低, 说明BFMO的产生以P. putida strain MnB1的生物氧化作用为主, 而不是化学氧化作用(Tebo et al., 2005; 王华伟, 2015).
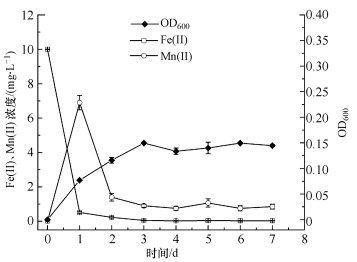 |
| 图 1 OD600和Mn(Ⅱ)、Fe(Ⅱ)浓度随时间的变化曲线 Fig. 1 Curve of OD600 and Mn(Ⅱ), Fe(Ⅱ) concentrations with reaction time |
地表水或地下水环境复杂, 砷污染程度也不同.周鑫(2013)在调查中发现, 矿区废水中砷浓度可达到5 mg·L-1, 因此, 本实验设置0.5~5 mg·L-1的浓度梯度来探究不同砷初始浓度下BFMO对其去除效果的影响.由图 2a可知, 当As(Ⅲ)浓度为0.5、1、2 mg·L-1时, 砷的去除效率随着As(Ⅲ)初始浓度的升高而降低, 分别为72.46%、66.08%、62.05%;当As(Ⅲ)浓度升高至5 mg·L-1时, 砷的去除效率为74.51%.同时, 由图 2b可以看出, As(Ⅴ)去除率的变化规律与As(Ⅲ)相一致, 当As(Ⅴ)浓度为0.5、1、2 mg·L-1时, 砷的去除效率分别为83.92%、66.64%、65.21%.整体而言, 原位形成的BFMO对As(Ⅲ)和As(Ⅴ)有良好的去除效果, 其中, As(Ⅴ)的去除效率略高于As(Ⅲ).然而, 当As(Ⅲ)或As(Ⅴ)浓度为5 mg·L-1时, 砷的去除效率有所提高(p<0.05), 可能是由于砷浓度升高时As(Ⅲ)或As(Ⅴ)与三价铁发生共沉淀反应生成砷酸铁矿物(FeAsO4·H2O、FeAsO4·2H2O或Fe3(AsO4)2)(Kumpiene et al., 2008).Porter等(2004)研究发现, 在近中性的氧化条件下可能生成溶解性更低的Fe3(AsO4)2.
 |
| 图 2 不同砷浓度时As(Ⅲ)(a)和As(Ⅴ) (b)的去除效率 (pH=7.0, As(Ⅲ/Ⅴ)浓度为0.5~5 mg·L-1, 细菌接种比为2%, MnCO3浓度为0.8 g·L-1, Fe(Ⅱ)浓度为10 mg·L-1) Fig. 2 The removal efficiency of As(Ⅲ) (a) and As(Ⅴ) (b) with different As concentrations |
不同细菌接种比对BFMO去除As(Ⅲ)和As(Ⅴ)效率的影响见图 3.由图 3可知, 随着细菌接种比的增高, As(Ⅲ)和As(Ⅴ)的去除效率呈先增加后逐渐稳定的趋势.当细菌接种比为0.1%~0.5%时, 砷的去除效率随着细菌接种比的增大而增大, 这是由于细菌密度越大, 其诱导生成的BFMO浓度越高, 对砷的去除效率也相应地提高(Wang et al., 2019).当细菌接种比为0.5%时, As(Ⅲ)和As(Ⅴ)的去除效率分别为88.90%和85.71%;当细菌接种比提高至1%时, As(Ⅲ)和As(Ⅴ)的去除效率分别为90.99%和89.06%, 较细菌接种比为0.5%时仅分别提升了2.09%和3.35%.可以看出, 随着细菌密度的增加, As(Ⅲ)或As(Ⅴ)的去除效率没有发生明显变化, 说明细菌接种比在1%和2%时, 细菌诱导产生BFMO的能力已经达到极限, 对砷的去除能力不再升高.
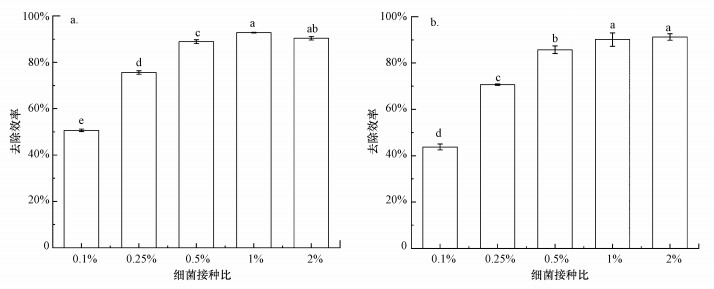 |
| 图 3 不同细菌接种比下As(Ⅲ) (a)和As(Ⅴ) (b)的去除效率 (pH=7.0, As(Ⅲ/Ⅴ)浓度为1 mg·L-1, 细菌接种比为0.1%~2%, MnCO3浓度为0.8 g·L-1, Fe(Ⅱ)浓度为10 mg·L-1) Fig. 3 The removal efficiency of As(Ⅲ) (a) and As(Ⅴ) (b) with different bacterial inoculation ratios |
图 4为不同MnCO3浓度对As(Ⅲ)和As(Ⅴ)去除效率的影响.由图 4可知, 当MnCO3浓度为0.2、0.5、0.8 g·L-1时, As(Ⅲ)和As(Ⅴ)的去除率随MnCO3浓度的升高而显著增加(p<0.05), 其中, As(Ⅲ)的去除效率分别为35.58%、57.68%、67.85%, As(Ⅴ)的去除效率分别为22.74%、51.97%、71.27%.当MnCO3浓度大于0.8 g·L-1时, As(Ⅲ)和As(Ⅴ)的去除效率并未出现显著增加(p>0.05), As(Ⅲ)的去除效率基本维持在68%左右, 而As(Ⅴ)的去除效率维持在71%左右.MnCO3是锰氧化菌P. putida strain MnB1诱导形成生物铁锰氧化物的锰源之一, 但MnCO3的氧化需要经历胞外溶解和催化氧化两个步骤(Wang et al., 2015b), 随着MnCO3浓度的增加, 锰氧化菌会溶解释放更多的Mn(Ⅱ), 进而催化氧化诱导锰氧化物的产生, 进而使As(Ⅲ)和As(Ⅴ)的去除效率增加(Wang et al., 2014);但当MnCO3浓度达到一定程度时, MnCO3的溶解成为生物铁锰氧化物形成的限速步骤, Mn(Ⅱ)释放速率达到最大, 催化氧化诱导锰氧化物的量不能显著增加, 进而表现出As(Ⅲ)和As(Ⅴ)的去除效率缓慢增加或维持不变.Bai等(2016)研究也发现, 反应后BFMO沉淀物表面的砷主要以As(Ⅴ)形式存在, 也证实了BFMO中锰氧化物能够快速氧化As(Ⅲ)为As(Ⅴ).
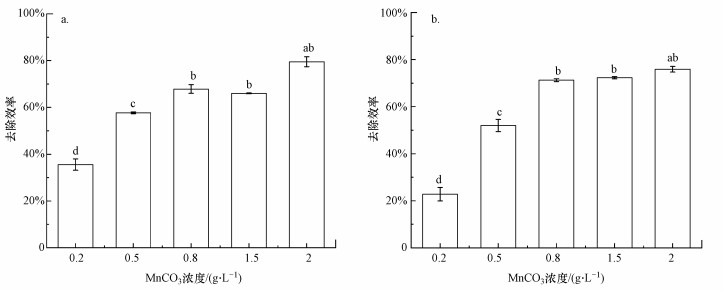 |
| 图 4 不同MnCO3浓度时As(Ⅲ) (a)和As(Ⅴ) (b)的去除效率 (pH=7.0, As(Ⅲ/Ⅴ)浓度为1 mg·L-1, 细菌接种比2%, MnCO3浓度为0.2~2 g·L-1, Fe(Ⅱ)浓度为10 mg·L-1) Fig. 4 The removal efficiency of As(Ⅲ) (a) and As(Ⅴ) (b) with different MnCO3 concentrations |
图 5为不同Fe(Ⅱ)浓度对As(Ⅲ)和As(Ⅴ)去除效率的影响.由图 5可知, 随着Fe(Ⅱ)初始浓度的增加, As(Ⅲ)和As(Ⅴ)的去除效率呈逐渐递增趋势.当Fe(Ⅱ)浓度为2.5、5、10、25、50 mg·L-1时, As(Ⅲ)的去除效率分别为67.51%、70.39%、77.05%、91.22%、95.60%, As(Ⅴ)的去除效率分别为60.49%、64.33%、74.94%、91.83%、93.93%.总体而言, Fe(Ⅱ)浓度的增加对As(Ⅲ)和As(Ⅴ)的去除效果显著增加(p<0.05).当Fe(Ⅱ)浓度升高时, 细菌会诱导形成更多的生物铁氧化物, 为砷吸附提供更多的结合点位.Bai等(2016)研究也表明, 地下水中Fe(Ⅱ)浓度越高, 砷的去除量也越高.此外, 有研究证明, 铁锰氧化物复合矿中, 铁元素的相对含量越高, As(Ⅲ)的去除率越高(杜晓丽, 2017).
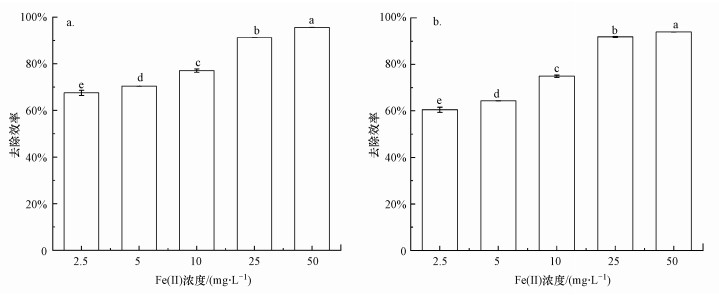 |
| 图 5 不同Fe(Ⅱ)浓度时As(Ⅲ) (a)和As(Ⅴ) (b)的去除效率 (pH=7.0, As(Ⅲ/Ⅴ)浓度为1 mg·L-1, 细菌接种比为2%, MnCO3浓度为0.8 g·L-1, Fe(Ⅱ)浓度为2.5~50 mg·L-1) Fig. 5 The removal efficiency of As(Ⅲ) (a) and As(Ⅴ) (b) with different Fe(Ⅱ) concentrations |
利用SEM和TEM对BFMO吸附As(Ⅲ)和As(Ⅴ)前后矿物特性进行表征.由SEM分析可知(图 6), 原位形成的BFMO主要由不规则的团状和层状矿物聚合体组成, 伴有网状结构的团聚体.通过EDS对元素半定量分析可知, BFMO的元素组成主要为C、O、Fe、Mn.当BFMO与As(Ⅲ)和As(Ⅴ)反应后, BFMO的矿物结构未发现显著变化, 但由EDS分析可知, BFMO表面吸附大量的砷, 其中, As(Ⅲ)和As(Ⅴ)反应后砷的含量分别为0.270%和0.405%.采用TEM对BFMO结构分析发现(图 7), BFMO中矿物结构存在明显界面关系, 其中, 椭圆和类球状的矿物(黑色箭头)位于内核中心, 其表面附着大量无定型和弱晶形的纳米矿物结构(白色箭头).采用TEM Mapping进一步分析发现(图 8), BFMO颗粒物质内核区域中锰元素分布较多, 推测其主要为锰氧化物结构, 而边缘的纳米级微粒中铁元素分布较多, 推测其主要为铁氧化物结构(Tebo et al., 2004).此外, TEM Mapping分析也证实了砷被截留在铁锰复合氧化物表面.这些结果表明, 原位形成的BFMO能够有效吸附水中的As(Ⅲ)和As(Ⅴ).
 |
| 图 6 BFMO的SEM图 (a, b.BFMO, c, d.BFMO+As(Ⅲ), e, f.BFMO+As(Ⅴ)) Fig. 6 SEM images of BFMO (a, b.BFMO, c, d.BFMO+As(Ⅲ), e, f.BFMO+As(Ⅴ)) |
 |
| 图 7 BFMO的TEM图 (a.BFMO, b.BFMO+As(Ⅲ), c.BFMO+As(Ⅴ)) Fig. 7 TEM images of BFMO (a.BFMO, b. BFMO+As(Ⅲ), c.BFMO+As(Ⅴ)) |
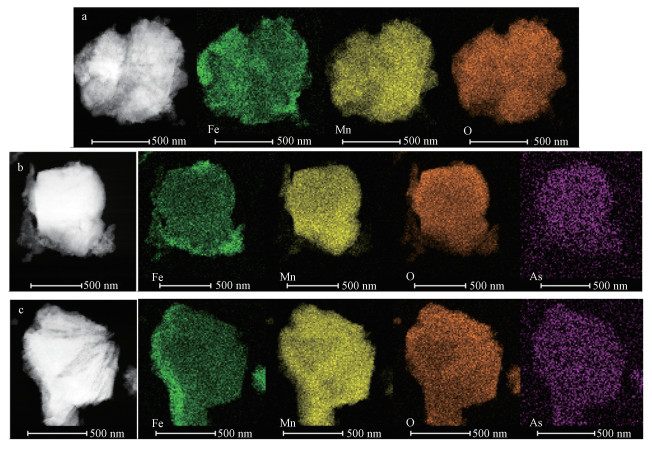 |
| 图 8 BFMO的TEM Mapping图 (a.BFMO, b.BFMO+As(Ⅲ), c.BFMO+As(Ⅴ)) Fig. 8 TEM mapping image of BFMO (a.BFMO, b.BFMO+As(Ⅲ), c.BFMO+As(Ⅴ)) |
进一步利用XPS对BFMO吸附As(Ⅲ)和As(Ⅴ)后砷的价态进行拟合分析.由图 9可知, As(Ⅲ)和As(Ⅴ)与BFMO反应后, 在50.54 eV和48.39 eV处有两个拟合峰, 均为As(Ⅴ)的拟合峰(Wang et al., 2017).在BFMO原位形成过程中As(Ⅴ)直接被吸附固定于BFMO表面, 而大部分As(Ⅲ)则先被氧化为As(Ⅴ)后被吸附固定, 少部分As(Ⅲ)则是先被吸附到铁氧化物表面, 再被锰氧化物氧化, 这与Bai等(2016)的研究结果相一致, 其利用锰氧化菌Pseudomonas sp. QJX-1研究原位形成BFMO对As(Ⅲ)的去除机制时, 发现锰氧化物能够快速氧化As(Ⅲ)为As(Ⅴ).Wang等(2020)研究表明, P. putida strain MnB1诱导产生的生物锰氧化物能够快速氧化As(Ⅲ)为As(Ⅴ), 从而提高了砷的吸附固定效率.宋宜等(2020)也发现, Fe(Ⅲ)水解产生的铁氧化物能提高生物锰氧化物对砷的去除效率.此外, 本文进一步分析了As(Ⅲ)和As(Ⅴ)在BFMO表面的结合形态, 从图 10可以看出, BFMO对砷的去除方式主要为吸附作用, 其次为共沉淀反应, 这与张明月等(2017)和Ouzounis等(2015)的研究结果相一致.结合砷的存在形态判断出XPS拟合图中48.39 eV处的拟合峰应为共沉淀形态的As(Ⅴ), 50.54 eV的处拟合峰应为吸附形态的As(Ⅴ).
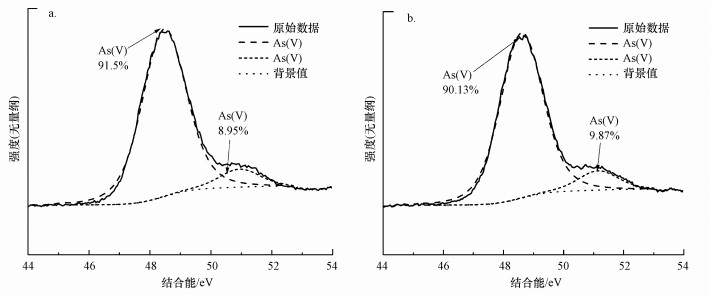 |
| 图 9 BFMO吸附As(Ⅲ) (a)和As(Ⅴ) (b)后As 3d XPS拟合图 Fig. 9 As 3d XPS spectra of As(Ⅲ) (a) and As(Ⅴ) (b) adsorbed by BFMO |
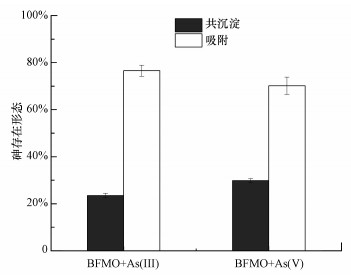 |
| 图 10 砷在BFMO中的存在形态 Fig. 10 Speciation of arsenic in BFMO |
基于上述研究, 结合相关的文献报道(Bai et al., 2016;Wei et al., 2018;王建燕等, 2019), 推测原位形成BFMO对As(Ⅲ)和As(Ⅴ)的吸附去除机制(图 11).P. putida strain MnB1诱导产生胞外聚合物加速MnCO3的溶解产生游离的Mn(Ⅱ), 然后P. putida strain MnB1通过酶促反应产生超氧自由基将Mn(Ⅱ)氧化为生物锰氧化物(Learman et al., 2013;王华伟, 2015), 同时, Fe(Ⅱ)发生生物氧化和化学氧化作用, 转变为铁(氢)氧化物(Fe(OH)3)于锰氧化物表面;由于Fe(Ⅱ)和Mn(Ⅱ)的氧化速率不一致, 锰氧化物和铁氧化物依次生成, 形成BFMO混合物, 内核区域为锰氧化物, 边缘附着大量铁氧化物.BFMO中的锰氧化物主要将As(Ⅲ)有效地氧化成As(Ⅴ), 改变砷的价态和毒性;铁氧化物主要吸附As(Ⅴ).在BFMO形成过程中, As(Ⅴ)与铁锰氧化物形成以单/多齿配体吸附于BFMO表面, 或As(Ⅴ)与Fe3+形成共沉淀的方式吸附去除(Bai et al., 2016).此外, BFMO氧化As(Ⅲ)时可能会释放Mn(Ⅱ)和Fe(Ⅱ), 这些二次产生的Mn(Ⅱ)和Fe(Ⅱ)能够被P. putida strain MnB1重新氧化或吸附于BFMO表面, 为As(Ⅴ)的吸附提供新的活性点位(Wang et al., 2019).总体而言, BFMO吸附固定As(Ⅲ)时会形成一个循环系统, 在去除As(Ⅲ)和As(Ⅴ)的同时降低了Fe(Ⅱ)和Mn(Ⅱ)的释放.
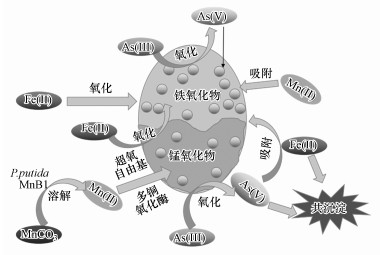 |
| 图 11 原位形成BFMO对As(Ⅲ)和As(Ⅴ)的吸附去除机制示意图 Fig. 11 Schematic diagram of As(Ⅲ) and As(Ⅴ) removal mechanism by in-situ formed BFMO |
1) 原位形成的BFMO对As(Ⅲ)和As(Ⅴ)有良好的去除效率.当砷浓度为0.5~5 mg·L-1时, As(Ⅲ)和As(Ⅴ)的去除效率均在62%以上.
2) 当细菌接种比为0.1%~0.5%时, As(Ⅲ)和As(Ⅴ)的去除效率与细菌接种比成正比, 当细菌接种比大于0.5%时, As(Ⅲ)和As(Ⅴ)的去除效率都在85%以上, 且不发生明显变化(p>0.05).
3) 当MnCO3浓度为0.2~0.8 g·L-1时, BFMO对As(Ⅲ)和As(Ⅴ)的去除效率随MnCO3浓度的增加而增大, 当Fe(Ⅱ)浓度为2.5~25 mg·L-1时, BFMO对As(Ⅲ)和As(Ⅴ)的去除效率也随Fe(Ⅱ)浓度的增加而增大;当MnCO3或Fe(Ⅱ)浓度再升高时, As(Ⅲ)和As(Ⅴ)的去除效率基本保持不变.
4) SEM、TEM及XPS等表征分析表明, 原位形成的BFMO对As(Ⅲ)和As(Ⅴ)的去除主要通过氧化吸附、共沉淀等多种方式起作用.
Bai Y H, Yang T T, Liang J S, et al. 2016. The role of biogenic Fe-Mn oxides formed in situ for arsenic oxidation and adsorption in aquatic ecosystems[J]. Water Research, 98(7): 119-127. DOI:10.1016/j.watres.2016.03.068 |
Boland D D, Collins R N, Miller C J, et al. 2014. Effect of solution and solid-phase conditions on the Fe(Ⅱ)-accelerated transformation of ferrihydrite to lepidocrocite and goethite[J]. Environmental Science & Technology, 48(10): 5477-5485. |
Chatterjee A, Das D, Mandal B K, et al. 1995. Arsenic in ground water in six districts of West Bengal, India:the biggest arsenic calamity in the world.Part Ⅰ.Arsenic species in drinking water and urine of the affected people[J]. The Analyst, 120(3): 643-650. DOI:10.1039/an9952000643 |
Dixit S, Hering J G. 2003. Comparison of arsenic(Ⅴ) and arsenic(Ⅲ) sorption onto iron oxide minerals:implications for arsenic mobility[J]. Environmental Science & Technology, 37(18): 4182-4189. |
杜晓丽.2017.典型含铁锰矿矿物学和表面化学及对砷的吸附研究[D].武汉: 华中农业大学
|
He Z F, Li Z Y, Zhang Q Y, et al. 2019. Simultaneous remediation of As(Ⅲ) and dibutyl phthalate (DBP) in soil by a manganese-oxidizing bacterium and its mechanisms[J]. Chemosphere, 220(4): 837-844. DOI:10.1016/j.chemosphere.2018.12.213 |
黄博, 郭朝晖, 肖细元, 等. 2019. 铝代水铁矿协同吸附砷镉的机制[J]. 环境科学, 40(5): 2287-2294. |
黄永炳.2018.锰矿修复砷污染地下水及其PRB工程技术研究[D].武汉: 华中农业大学
|
Kumpiene J, Lagerkvist A, Maurice C. 2008. Stabilization of As, Cr, Cu, Pb and Zn in soil using amendments-a review[J]. Waste Management, 28(1): 215-225. DOI:10.1016/j.wasman.2006.12.012 |
Learman D R, Voelker B M, Madden A S, et al. 2013. Constraints on superoxide mediated formation of manganese oxides[J]. Frontiers in Microbiology, 4: 262. DOI:10.3389/fmicb.2013.00262 |
Lee Y H, Um I H, Yoon J Y. 2003. Arsenic(Ⅲ) oxidation by iron(Ⅵ) (ferrate) and subsequent removal of arsenic(Ⅴ) by iron(Ⅲ) coagulation[J]. Environmental Science & Technology, 37(24): 5770-5756. DOI:10.1021/es034203+ |
李荣辉, 郏义征, 胡楠楠. 2019. 三维层级花状活性氧化铝纳米材料的制备及其除砷性能研究[J]. 无机材料学报, 34(5): 553-559. |
刘辉利, 梁美娜, 朱义年, 等. 2009. 氢氧化铁对砷的吸附与沉淀机理[J]. 环境科学学报, 29(5): 1011-1020. DOI:10.3321/j.issn:0253-2468.2009.05.019 |
Ouzounis K, Katsoyiannis I, Zouboulis A. 2015. Is the coagulation-filtration process with Fe(Ⅲ) efficient for As(Ⅲ) removal from groundwaters?[J]. Separation Science and Technology, 50(10): 1587-1592. DOI:10.1080/01496395.2014.978470 |
Porter S K, Scheckel K G, Impellitteri C A, et al. 2004. Toxic metals in the environment:thermodynamic considerations for possible immobilization strategies for Pb, Cd, As, and Hg[J]. Critical Reviews in Environmental Science and Technology, 34(6): 495-604. DOI:10.1080/10643380490492412 |
Rahman M M, Sengupta M K, Ahamed S, et al. 2005. The magnitude of arsenic contamination in groundwater and its health effects to the inhabitants of the Jalangi-one of the 85 arsenic affected blocks in West Bengal, India[J]. The Science of the Total Environment, 338(3): 189-200. DOI:10.1016/j.scitotenv.2004.06.022 |
宋宜, 王华伟, 吴雅静, 等. 2020. 三价铁促进生物氧化锰稳定土壤砷的效果和机制[J]. 环境科学学报, 40(4): 1460-1466. |
孙媛媛, 曾希柏, 白玲玉. 2011. Mg/Al双金属氧化物对As(Ⅴ)吸附性能的研究[J]. 环境科学学报, 31(7): 1377-1385. |
Tebo B M, Bargar J R, Clement B G, et al. 2004. Biogenic manganese oxides:Properties and mechanisms of formation[J]. Annual Review of Earth and Planetary Sciences, 32(1): 287-328. DOI:10.1146/annurev.earth.32.101802.120213 |
Tebo B M, Johnson H A, Mccarthy J K, et al. 2005. Geomicrobiology of manganese(Ⅱ) oxidation[J]. Trends in Microbiology, 13(9): 421-428. DOI:10.1016/j.tim.2005.07.009 |
Tsegaye G A, Christain V S, Laing G D. 2019. Use of (modified) natural adsorbents for arsenic remediation:A review[J]. Science of the Total Environment, 676: 706-720. DOI:10.1016/j.scitotenv.2019.04.237 |
王华伟.2015.应用锰氧化菌修复环境中砷、锑和有机复合污染物[D].北京: 中国科学院
|
Wang H W, Zhang D Y, Mou S Y, et al. 2015a. Simultaneous removal of tetracycline hydrochloride and As(Ⅲ) using poorly-crystalline manganese dioxide[J]. Chemosphere, 136(10): 102-110. |
Wang H W, Zhang D, Song W, et al. 2015b. Effect of exopolymers on oxidative dissolution of natural rhodochrosite by Pseudomonas putida strain MnB1:an electrochemical study[J]. Applied Geochemistry, 59: 95-103. DOI:10.1016/j.apgeochem.2015.04.015 |
Wang H W, Lv Z J, Song Y, et al. 2019. Adsorptive removal of Sb(Ⅲ) from wastewater by environmentally-friendly biogenic manganese oxide (BMO) materials:Efficiency and mechanisms[J]. Process Safety and Environmental Protection, 124: 223-230. DOI:10.1016/j.psep.2019.02.022 |
Wang H W, Wang Y N, Sun Y J, et al. 2017. A microscopic and spectroscopic study of rapid antimonite sequestration by a poorly crystalline phyllomanganate:differences from passivated arsenite oxidation[J]. RSC Advances, 7(61): 38377-38386. DOI:10.1039/C7RA05939F |
Wang H W, Pan X L. 2014. Role of extracellular polymeric substances (EPS) from Pseudomonas putida strain MnB1 in dissolution of natural rhodochrosite[J]. Biogeosciences Discussions, 11(5): 7273-7290. |
Wang Y N, Tsang Y F, Wang H W, et al. 2020. Effective stabilization of arsenic in contaminated soils with biogenic manganese oxide (BMO) materials[J]. Environmental Pollution, 258: 113481. DOI:10.1016/j.envpol.2019.113481 |
王建燕, 张传巧, 陈静, 等. 2019. 新型铁铜锰复合氧化物颗粒吸附剂As(Ⅲ)吸附行为与机制研究[J]. 环境科学学报, 39(8): 2575-2585. |
Watanabe J, Tani Y, Miyata N, et al. 2012. Concurrent sorption of As(Ⅴ) and Mn(Ⅱ) during biogenic manganese oxide formation[J]. Chemical Geology, 306: 123-128. DOI:10.1016/j.chemgeo.2012.03.004 |
Wei Z, Zhang G S, Liu C, et al. 2018. Enhanced removal of arsenite and arsenate by a multifunctional Fe-Ti-Mn composite oxide:photooxidation, oxidation and adsorption[J]. Water Research, 147: 264-275. DOI:10.1016/j.watres.2018.10.001 |
叶树芯.2016.铁锰复合氧化物新型固定化及其除砷特性研究[D].武汉: 华中农业大学
|
张明月, 曾辉平, 吕育锋, 等. 2017. 高铁盐与亚铁盐混凝除As(Ⅲ)性能的对比研究[J]. 中国环境科学, 37(5): 1798-1804. DOI:10.3969/j.issn.1000-6923.2017.05.024 |
周海燕, 邓一荣, 林龙勇, 等. 2019. 铁锰氧化物在不同水分条件下对土壤As的稳定化作用[J]. 环境科学, 40(8): 3792-3798. |
周鑫.2013.内蒙古某矿区水环境砷污染特征研究[D].阜新: 辽宁工程技术大学
|
 2021, Vol. 41
2021, Vol. 41


