2. 嘉兴市水务投资集团有限公司, 嘉兴 314000
2. Jiaxing Water Investment Group Co., Ltd., Jiaxing 314000
采矿、冶金、化工、电镀、印刷和制革等一系列人类生产活动是导致我国水体重金属严重超标的重要原因.水体中的重金属有镉、铬、铅、铜、汞、镍等, 其具有不可降解性、隐蔽性和长期性(唐利萍, 2015;陈能场等, 2017).重金属元素镉是一种人体非必需元素.水体中镉主要来源于金属电镀、电池、塑料、颜料、有色金属开采、冶炼等行业(Purkayastha et al., 2014).镉离子具有生物累积性、毒性和不可逆性.同时, 镉的高流动性使其很容易迁移到水源和农田土壤中, 并通过食物链在人体内富集, 对植物、动物甚至人类造成严重的损害(Mulligan et al., 2001;He et al., 2017;Yu et al., 2018;Zhu et al., 2018).人体长期暴露于镉污染的环境中, 会导致骨质疏松症, 还会造成肝脏和肾脏损伤.水体中重金属镉的去除已引起学者的广泛关注(Zhu et al., 2017).因此, 寻找一种绿色、经济、有效的处理方法来去除水中镉离子及其他重金属离子, 防止重金属污染已成为当务之急.常见的去除水体中重金属的工艺主要包括化学沉淀法(Feng et al., 2010;刘羽等, 2001;杨龑等, 2012)、吸附法(Demirbas, 2004;Afkhami et al., 2010;左卫元等, 2015)、生物法(Gao et al., 2012;Hamidian et al., 2014)、电解法(袁绍军等, 2003)和膜分离法(邓娟利等, 2005).
近来有研究表明(Huang et al., 2011), 磷酸盐沉淀法能有效处理水体中重金属污染(Park et al., 2011;Huang et al., 2011), 因大多数重金属离子能与水中的磷酸根离子结合从而形成难溶于水的稳定化合物, 而鸟粪石作为一种磷酸盐类物质, 其通过沉淀溶解平衡释放的磷酸根离子可在一定条件下与水体中的重金属离子反应生成稳定的沉淀, 具有很大的稳定污水中重金属的潜力.鸟粪石(MgNH4PO4·6H2O) (Doyle et al., 2002)是从污水中进行磷元素回收的有价值产物, 将其用作处理污水中重金属污染的材料, 可以实现对回收产物的二次利用, 提升了该水处理工艺的实用价值.目前, 用鸟粪法去除重金属的研究较少(Wang et al., 2016;Zhang et al., 2016;王健等, 2018;邓曼君等, 2019).其中王健等(2018)将鸟粪石负载于硅藻土上制得复合MAP-D材料, 用于土壤中金属元素锌的稳定, 并将土壤中锌的可交换态降低了56.9%, 残余态提高了50.5%, 并增强了被锌抑制的过氧化氢酶和尿素酶的活性.邓曼君等(2019)生产的NZ-MAP材料的主要成分是负载有鸟粪石的天然沸石, 当在水中的投加量为0.4 g·L-1时, 重金属铅的最大吸附量为749. 74 mg·g-1.然而, 鸟粪石-沸石复合材料对Cd的吸附作用尚未见相关研究报道.由于污水中重金属的分离和回收难度大, 溶解度较低, 限制了鸟粪石在去除水中重金属离子方面进一步的应用(Wang et al., 2016).
本研究使用的鸟粪石-沸石复合材料(STR-NZ)是氧化镁负载沸石(MgO-NZ)通过鸟粪石结晶反应固定化回收模拟污水中的氮和磷制备的.相关研究表明, 该制备工艺可以充分回收污水中的氮磷资源, 具有一定的经济和环境效益(Feng et al., 2010;Huang et al., 2014).使用这种材料处理重金属污染水体可能具有以下优点:①MgO-NZ材料为污水中鸟粪石的形成提供了载体, 使其吸附污水中重金属后易于从污水中分离和回收(张志昊等, 2016);②沸石本身具有吸附污水中重金属的能力(Oste et al., 2002), 当其改性后又吸附污水中过量的氨氮时, 将使其具有更大的阳离子交换能力(Hu et al., 2007), 从而提高了污水中重金属的去除能力;③研究表明(张亚雷等, 2012), 铵饱和沸石使难溶性磷酸盐更易于释放磷, 与水中镉离子共沉淀从而去除镉.该实验以镉离子为特征性重金属污染物, 研究了投加量、初始pH、反应时间对STR-NZ吸附溶液中重金属镉的影响, 探讨了重金属在溶液中的吸附机理, 旨在为合理利用氮磷污水回收产品修复重金属污染水提供依据.
2 材料与方法(Materials and methods) 2.1 实验材料天然沸石购自河南省洛阳选矿厂, 其化学组成示于表 1.沸石过60目筛筛分后, 用去离子水洗涤, 在105 ℃下干燥, 密封待用.氯化镁(MgCl2· 6H2O)、氢氧化钠(NaOH)、磷酸二氢钾(KH2PO4)、氯化铵(NH4Cl)和硝酸镉(Cd(NO3)2·4H2O)等试剂购于国药集团, 均为分析纯.
| 表 1 天然沸石成分表 Table 1 Components of natural zeolite |
称取10 g天然沸石加入100 mL 1 mol·L-1的MgCl2溶液, 搅拌1 h后, 缓慢滴加NaOH溶液, 使OH-/Mg2+摩尔比为2.继续振荡浸渍3 h, 静置12 h, 取洗涤后的沉淀, 于105 ℃烘干, 再用马弗炉于400 ℃焙烧5 h, 即制得氧化镁负载沸石材料(记为MgO-NZ).向100 mL氮磷混合模拟废水(NH4+-N=60 mg·L-1, PO43--P=60 mg·L-1, pH=7.0)中投加0.04 g MgO-NZ材料, 于25 ℃以180 r·min-1转速振荡12 h.抽滤得固体物质, 于40 ℃烘干, 避免60 ℃以上高温使其脱水(Ando et al., 1968), 得鸟粪石-沸石复合材料(STR-NZ).
2.2 试验方法 2.2.1 STR-NZ投加量优化准确称取0.01、0.02、0.04、0.06、0.08和0.10 g STR-NZ材料, 并将其分别投加到100 mL重金属Cd2+溶液中, Cd2+的初始浓度为50 mg·L-1.将溶液的初始pH调节至5.0, 然后将其置于25 ℃的恒温振荡器中, 以180 r·min-1的转速振荡1 h, 最后将溶液的上清液通过0.22 μm滤膜, 测量反应前后溶液中Cd2+的浓度, 并计算吸附量.
2.2.2 初始pH影响准确称取0.02 g STR-NZ材料, 并将其投加到一批100 mL重金属Cd2+溶液中, 其中Cd2+的初始浓度为50 mg·L-1.将溶液初始pH依次调节至2.0、3.0、4.0、5.0、6.0, 然后将其置于25 ℃的恒温振荡器中, 以180 r·min-1的转速振荡1 h, 最后将溶液的上清液通过0.22 μm滤膜, 测量反应前后溶液中Cd2+的浓度, 并计算吸附量.
2.2.3 吸附动力学与热力学实验准确称取0.02 g STR-NZ材料, 并将其投加到一批100 mL重金属Cd2+溶液中, 其中Cd2+的初始浓度为50 mg·L-1.将溶液的初始pH调节至5.0, 然后将其置于25 ℃的恒温振荡器中, 以180 r·min-1的转速振荡反应, 间隔取样.将溶液的上清液通过0.22 μm滤膜, 测量反应前后溶液中Cd2+的浓度, 并计算吸附量.
配置一系列体积为100 mL、初始浓度分别为5、10、20、30、40、50、60、75、90 mg·L-1的Cd2+溶液, 并加入0.02 g STR-NZ材料.将溶液的初始pH调节至5.0, 然后将其置于25 ℃的恒温振荡器中, 以180 r·min-1的转速振荡1 h, 最后将溶液的上清液通过0.22 μm滤膜, 测量反应前后溶液中Cd2+的浓度, 并计算吸附量.
2.3 分析方法表面形貌分析(SEM)采用Ultra 55场发射扫描电子显微镜, 表面成分和含量分析(EDS)采用Oxford InstrumnetX-MAX50能谱仪, 物象检索分析(XRD)采用Bruker X′pert Pro型射线衍射仪, 官能团分析(FTIR)采用Nicolet 5700智能傅立叶红外光谱仪.溶液pH测定用FE20pH计.
Cd2+的测定采用HJ 776-2015电热耦合等离子体发射光谱法, 溶解性磷酸盐(PO43--P)测定采用GB11893-89钼酸铵分光光度法.测定PO43--P和Cd2+浓度时, 水样需通过微孔滤膜(φ50 cm、0.22 μm)过滤.
3 结果与讨论(Results and discussion) 3.1 STR-NZ的回收及表征图 1为天然沸石NZ、MgO-NZ和STR-NZ材料的扫描电镜图谱, 由图 1a和图 1b可以看出, 天然沸石表面较为光滑, 而MgO-NZ材料表面较为粗糙, 出现了类似絮状的纳米MgO覆层, 分散较为均匀, 这为MgO-NZ材料同步回收污水中的磷酸盐和氨氮提供了良好的条件.从图 1c中可以看出STR-NZ材料表面存在较为粗壮的棒状晶体, 表面存在明显的刻痕.表 2为STR-NZ材料EDS图谱元素质量比, 由表 2可知, 图中扫描点的鸟粪石晶体构成元素Mg、O、N和P的质量比均较高, 说明图 1c中棒状晶体可能主要为氮磷回收产物.
 |
| 图 1 天然沸石、MgO-NZ和STR-NZ材料的SEM图谱 Fig. 1 SEM spectra of natural zeolite, MgO-NZ and STR-NZ |
| 表 2 STR-NZ材料EDS图谱元素质量比 Table 2 STR-NZ material EDS map element mass ratio |
图 2为MgO-NZ和STR-NZ材料的XRD图谱, 由图 2可知, 回收产物STR-NZ材料中MgO的特征峰(42.82°和62.28°)消失, 在15.81°、20.86°、21.45°和31.93°处出现了高强度衍射峰, 将其与鸟粪石的标准谱图(PDF#15-0762)对比, 可发现两者所在强度峰的位置基本一致, 由此可基本确定图 1c中棒状晶体为鸟粪石.图 3为STR-NZ材料的FTIR图谱, 由图 3可知, 谱图在波数为1007.8、571.2和471.6 cm-1处存在明显的PO43-特征吸收峰(Ohlinger et al., 1998), 在波数为1438.55 cm-1处对应的是NH4+的变形振动, 这说明磷酸盐和铵盐的组分均存在于STR-NZ材料中.根据上述分析, 在氮磷污水中加入MgO-NZ材料后, 负载的镁盐与污水中的氮磷发生鸟粪石结晶反应, 在沸石表面形成大量的鸟粪石, 并可提供磷酸根离子, 对水中镉离子进行吸附及去除.
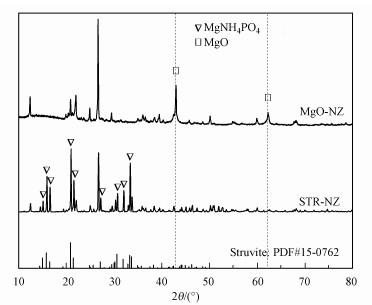 |
| 图 2 MgO-NZ和STR-NZ材料的XRD图谱 Fig. 2 XRD pattern of MgO-NZ and STR-NZ |
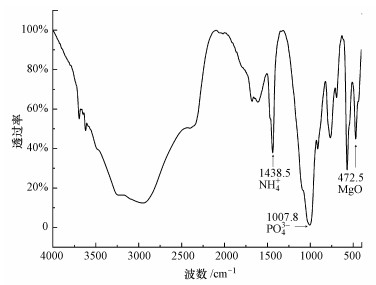 |
| 图 3 STR-NZ材料的FTIR图谱 Fig. 3 FTIR spectrum of STR-NZ |
综合以上分析结果, 可确定MgO-NZ对溶液中磷酸盐和氨氮的回收主要通过鸟粪石沉淀的方式实现的.磷酸盐和铵盐的组分均存在于STR-NZ材料中, 且质量比较高, 这为STR-NZ吸附溶液中重金属Cd2+提供了众多的表面活性基团(Ronteltap et al., 2007), STR-NZ中磷酸盐的释放量的增大, 也能因Cd2+与磷酸盐发生共沉淀从而去除更多的Cd2+.
3.2 STR-NZ投加量优化吸附剂的投加量将影响其对重金属的吸附量(施红, 2006).图 4为天然沸石NZ和STR-NZ材料投加量对溶液中重金属Cd2+吸附效果的影响.Cd2+的初始浓度为50 mg·L-1.由图 4可以看出, 当NZ投加量在0.05~0.2 g·L-1时, NZ对溶液中Cd2+的单位吸附量基本在8.2 mg·g-1左右, 在吸附剂投加量相同的条件下, STR-NZ对溶液中Cd2+的吸附效果要明显强于NZ.随着投加量的增加, STR-NZ对Cd2+的吸附量呈先快速上升后下降的趋势.刘国等(2019)在利用羟基磷灰石/凹凸棒土复合材料去除水中Cd2+时, 控制吸附质浓度一定, 随着吸附剂投加量的增加, 单位质量吸附剂的吸附量降低.而本研究在投加量小于<0.2 g·L-1时, 随投加量增加, 单位吸附量却在增加, 总体上, 单位吸附量呈先增加后降低的趋势, 可能的原因是, STR-NZ材料呈碱性, 在材料投加量较低时, 溶液pH受材料影响低, 低pH使得Cd2+不易生成沉淀从而去除Cd2+.具体来讲, 当STR-NZ投加量为0.2 g·L-1时, STR-NZ对Cd2+的吸附量达到最大, 为249.35 mg·g-1.投加量超过0.2 g·L-1时, STR-NZ对Cd2+的吸附量开始下降.这可能是由于此时溶液体系中没有足量的Cd2+与吸附剂STR-NZ表面众多活性基团结合, 导致产生过多空余的吸附点位, 吸附剂STR-NZ无法得到高效利用.因此, 在初始浓度为50 mg·L-1的Cd2+溶液中, STR-NZ材料的最佳投加量为0.2 g·L-1.
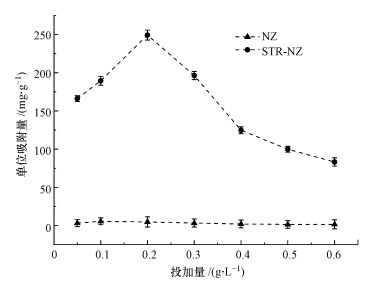 |
| 图 4 NZ-MAP材料投加量对溶液中Cd2+吸附的影响 Fig. 4 Effect of NZ-MAP dosage on Cd2+ adsorption in aqueous solution |
溶液pH是影响吸附剂吸附效果的重要因素, 溶液初始pH会影响吸附剂表面的性质和重金属在溶液中存在形式, 过低或过高的pH皆不利于吸附剂对溶液中重金属的吸附(周莹等, 2011).图 5a为溶液初始pH对STR-NZ材料吸附溶液中重金属Cd2+的影响, Cd2+溶液初始pH范围设定在2.0~6.0之间.由图 5a可知, 当溶液pH为2.0时, STR-NZ对溶液中Cd2+的吸附量为11.26 mg·g-1;当溶液pH增至4.0时, 吸附量可高达244.64 mg·g-1;当溶液pH继续增加时, STR-NZ对溶液中Cd2+的吸附量略有增加, 吸附量变化不甚明显, 最终趋于平衡.当溶液pH较低时, 溶液中存在大量的H+和Cd2+争夺吸附剂STR-NZ表面带有负电荷的吸附点位, 形成有效竞争关系, 不利于STR-NZ对溶液中Cd2+的吸附.随着溶液pH的升高, H+与Cd2+的竞争减弱, 有利于Cd2+和STR-NZ表面发生络合反应, 促进了Cd2+与STR-NZ释放的H2PO4-和HPO42-形成沉淀, 从而表现出较好的吸附能力.反应方程式如(1)和(2)所示.
 |
| 图 5 初始pH对STR-NZ吸附Cd2+(a和释放磷酸盐(b的影响 Fig. 5 Effect of initial pH on adsorption of Cd2+(a) and phosphate release (b) from STR-NZ |
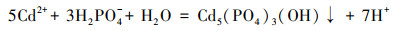
|
(1) |
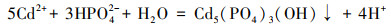
|
(2) |
图 5b为在不同初始pH条件下, 吸附剂STR-NZ在重金属Cd2+溶液中的释放情况.由图 5b可知, 无论是在去离子水中还是在Cd2+溶液中, 磷酸盐浓度皆随着溶液初始pH值的增大而减少, 这说明低pH条件有利于STR-NZ材料中磷酸盐的释放.此外, 可以发现Cd2+溶液中磷酸盐浓度要明显低于去离子水中磷酸盐的浓度, 这一定程度上说明了STR-NZ所释放的磷酸盐和Cd2+发生了化学反应生成重金属沉淀.
为进一步探讨在不同初始pH条件下STR-NZ材料对溶液中重金属的吸附机理, 将最终沉淀产物进行XRD表征分析.图 6为Cd2+溶液于不同初始pH下沉淀产物的XRD图谱.由图 6可知, 沉淀产物在22.03°、26.60°、32.20°和33.00°等处出现了较强的衍射峰, 26.60°处的强衍射峰为SiO2的特征峰, 其余3处的衍射峰和Cd5(PO4)3(OH)的特征峰相重合, 可判定沉淀产物中含有Cd5(PO4)3(OH)晶体, 且Cd5(PO4)3(OH)的特征峰强度随pH的增大而增强.图 7为Cd2+溶液于不同初始pH条件下沉淀产物的SEM图谱, 由图 7可知, Cd5(PO4)3(OH)晶体沉淀呈球状或类球状结构, 当溶液初始pH为2时, 未出现明显的球状颗粒, 随着溶液pH的升高, Cd5(PO4)3(OH)晶体开始出现并相互堆砌, 存在明显的团聚现象.如图 8所示, 用Visual MINTEQ软件模拟在该实验条件下, 溶液中磷酸盐的形态随pH变化的形态分布模型及Cd2+与磷酸盐共存时主要含Cd物质形态分布模型.由图 8a可知, 在初始pH=2~6的范围内, 随着pH的增大, 溶液中H2PO4-和H2PO4-浓度上升, 使Cd2+更容易生成沉淀从而被去除.由图 8b可知, 在初始pH=2~6的范围内, 随着pH的增大, Cd2+开始生成更多的Cd5(PO4)3(OH)沉淀.图 8从理论上验证了图 6和图 7的结论.
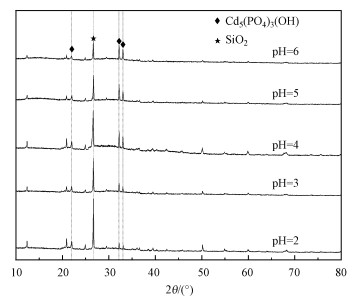 |
| 图 6 不同初始pH下Cd2+溶液沉淀产物XRD图谱 Fig. 6 XRD pattern of precipitated product in Cd2+ solution at different initial pH |
 |
| 图 7 不同初始pH下Cd2+溶液沉淀产物SEM图谱 Fig. 7 SEM spectrum of precipitated product of Cd2+ solution at different initial pH |
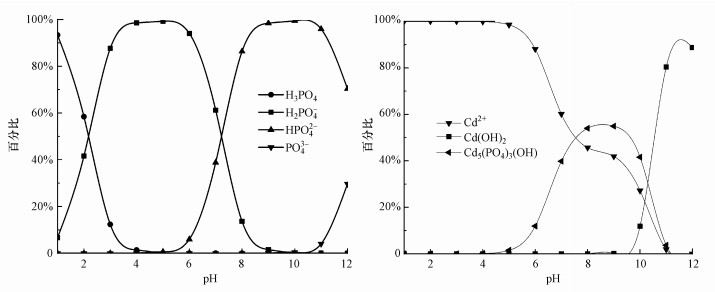 |
| 图 8 不同pH条件下的磷酸盐(a)和主要含Cd物质(b形态分布 Fig. 8 Morphological distribution of phosphates(a) and main Cd-containing substances(b) under different pH conditions |
图 9为不同反应时间对STR-NZ材料吸附溶液中重金属Cd2+的影响.由图 9可知, 在反应时间20 min内, STR-NZ对溶液中Cd2+的吸附量迅速增加, 这可能是由于STR-NZ可在酸性条件下快速释放磷酸盐, 促进重金属沉淀的生成.在反应时间为20 min时, Cd2+吸附量可达239.60 mg·g-1, 20 min以后STR-NZ对溶液中Cd2+的吸附量变化不大, 基本达到平衡.STR-NZ对溶液中Cd2+的吸附量可高达252.3 mg·g-1.
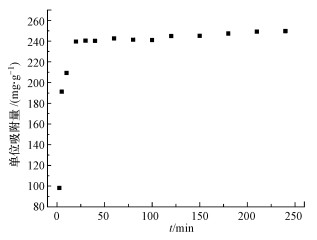 |
| 图 9 反应时间对STR-NZ吸附Cd2+的影响 Fig. 9 Effect of reaction time on the adsorption of Cd2+ by STR-NZ |
为了进一步理解STR-NZ材料对溶液中Cd2+的吸附过程, 采用准一级动力学模型和准二级动力学模型对STR-NZ吸附Cd2+的时间动态数据进行拟合, 图 10为STR-NZ吸附Cd2+的准一级反应动力学和准二级反应动力学方程线性回归直线拟合的拟合结果, 其动力学参数如表 3所示.由图 10和表 3可以发现, 准一级动力学反应方程拟合的qe与实测值相差较大, 而准二级动力学反应方程拟合的qe与实测值更为接近, 这说明准二级动力学对实际应用具有一定的指导意义.此外, 准二级动力学模型的可决系数R2接近1, 准一级动力学的R2仅为0.8210, 因此, 准二级动力学模型更适合STR-NZ对溶液中Cd2+的吸附过程.
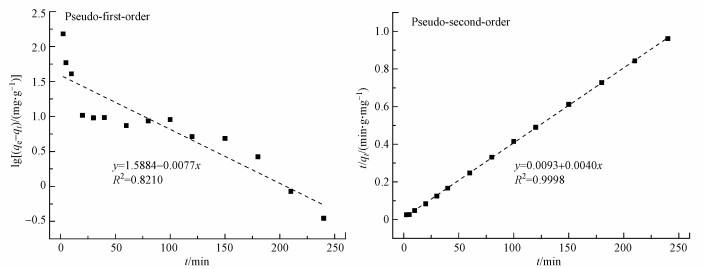 |
| 图 10 STR-NZ吸附Cd2+的准一级反应动力学和准二级反应动力学方程拟合结果 Fig. 10 Quasi-first-order reaction kinetics and quasi-secondary reaction kinetic equation fitting results of STR-NZ adsorption of Cd2+ |
| 表 3 STR-NZ吸附Cd2+的动力学参数 Table 3 Kinetic parameters of STR-NZ adsorption of Cd2+ |
图 11为STR-NZ材料对溶液中Cd2+的吸附量随平衡浓度的变化曲线, 由图 11可知, NZ-MAP对溶液中Cd2+的吸附量随平衡浓度的增加先急剧上升后趋于饱和.采用Langmuir和Freundlich等温吸附模型对试验数据进行拟合, 图 12为NZ-MAP吸附Cd2+的Langmuir和Freundlich等温吸附模型线性拟合结果, 其拟合参数如表 4所示.由图 12和表 4可知, Langmuir吸附等温方程拟合的R2(0.9984)要明显高于Freundlich吸附等温方程拟合的R2(0.7431), 且Langmuir吸附等温方程拟合的最大吸附量为294.12 mg·g-1, 接近实测值, 这说明STR-NZ对Cd2+的吸附过程更符合Langmuir等温吸附方程, 该吸附过程属于单层吸附(Jeppu et al., 2012).
 |
| 图 11 STR-NZ吸附Cd2+的吸附等温线 Fig. 11 STR-NZ adsorption Cd2+ adsorption isotherm |
 |
| 图 12 STR-NZ吸附Cd2+的Langmuir和Freundlich等温吸附模型线性拟合结果 Fig. 12 Linear fitting results of Langmuir and Freundlich isotherm adsorption models for STR-NZ adsorption of Cd2+ |
| 表 4 STR-NZ对Cd2+的等温吸附模型拟合参数 Table 4 STR-NZ isothermal adsorption model fitting parameters for Cd2+ |
1) MgO负载天然沸石回收污水中磷酸盐和氨氮制得STR-NZ材料主要生成鸟粪石沉淀.当Cd2+初始浓度为50 mg·L-1时, STR-NZ的最优投加量为0.2 g·L-1, 相对应的吸附量为249.35 mg·g-1.STR-NZ对Cd2+的吸附量随pH的增大呈先增加后趋于平衡的趋势, 在不同pH条件下的沉淀产物的组分和形貌有一定的差异.
2) 通过对沉淀产物进行XRD和SEM分析, STR-NZ对溶液Cd2+的去除主要通过生成Cd5(PO4)3(OH)沉淀的方式.
3) 采用准一级动力学模型和准二级动力学模型对STR-NZ吸附Cd2+的过程进行拟合, 结果表明STR-NZ对Cd2+的吸附过程符合准二级动力学模型.采用Langmuir和Freundlich等温吸附模型对STR-NZ吸附Cd2+的过程进行拟合, 结果表明Langmuir等温吸附模型更符合STR-NZ对溶液中Cd2+的等温吸附行为.
Afkhami A, Saber-Tehrani M, Bagheri H. 2010. Simultaneous removal of heavy-metal ions in wastewater samples using nano-alumina modified with 2, 4-dinitrophenylhydrazine[J]. Journal of Hazardous Materials, 181(1/3): 836–844.
DOI:10.1016/j.jhazmat.2010.05.089
|
Ando J, Akiyama T, Morita M. 1968. Magnesium ammonium phosphates, related salts and their behavior in compound fertilizers[J]. Bulletin of the Chemical Society of Japan, 41(7): 1716–1723.
DOI:10.1246/bcsj.41.1716
|
陈能场, 郑煜基, 何晓峰, 等. 2017. 《全国土壤污染状况调查公报》探析[J]. 农业环境科学学报, 2017, 36(9): 1689–1692.
|
Demirbas A. 2004. Adsorption of lead and cadmium ions in aqueous solutions onto modified lignin from alkali glycerol delignication[J]. Journal of Hazardous Materials, 109(13): 221–226.
|
邓曼君, 王学江, 成雪君, 等. 2019. 鸟粪石天然沸石复合材料对水中铅离子的去除[J]. 环境科学, 2019, 40(3): 1310–1317.
|
Doyle J D, Parsons S A. 2002. Struvite formation, control and recovery[J]. Water Research, 36(16): 3925–3940.
DOI:10.1016/S0043-1354(02)00126-4
|
邓娟利, 胡小玲, 管萍, 等. 2005. 膜分离技术及其在重金属废水处理中的应用[J]. 材料导报, 2005, 19(2): 23–26.
DOI:10.3321/j.issn:1005-023X.2005.02.007 |
Feng Y, Gong J L, Zeng G M, et al. 2010. Adsorption of Cd (Ⅱ) and Zn (Ⅱ) from aqueous solutions using magnetic hydroxyapatite nanoparticles as adsorbents[J]. Chemical Engineering Journal, 162(2): 487–494.
DOI:10.1016/j.cej.2010.05.049
|
Gao Y, Miao C, Wang Y, et al. 2012. Metal-resistant microorganisms and metal chelators synergistically enhance the phytoremediation efficiency of Solanum nigrum L. in Cd- and Pb-contaminated soil[J]. Environmental Technology, 33(12): 1383–1389.
DOI:10.1080/09593330.2011.629006
|
Hamidian A H, Atashgahi M, Khorasani N. 2014. Phytoremediation of heavy metals (Cd, Pb and V) in gas refinery wastewater using common reed (Phragmitis australis)[J]. Journal of Materials Chemistry, 20(15): 3079–3083.
|
He H, Tam N F Y, Yao A, et al. 2017. Growth and Cd uptake by rice (Oryza sativa) in acidic and Cd-contaminated paddy soils amended with steel slag[J]. Chemosphere, 189: 247–254.
DOI:10.1016/j.chemosphere.2017.09.069
|
Hu K W, Lou Y L, Guan L Z. 2007. Adsorption and desorption of heavy metal ions by ammonium saturated zeolite[J]. Chinese Journal of Soil Science, 38(2): 325–328.
|
Huang H, Xu C, Zhang W. 2011. Removal of nutrients from piggery wastewater using struvite precipitation and pyrogenation technology[J]. Bioresource Technology, 102(3): 2523–2528.
DOI:10.1016/j.biortech.2010.11.054
|
Huang H, Xiao D, Pang R, et al. 2014. Simultaneous removal of nutrients from simulated swine wastewater by adsorption of modified zeolite combined with struvite crystallization[J]. Chemical Engineering Journal, 256(6): 431–438.
|
Jeppu G P, Clement T P. 2012. A modified Langmuir-Freundlich isotherm model for simulating pH-dependent adsorption effects[J]. Journal of Contaminant Hydrology, 129-130(3): 46–53.
|
刘国, 李知可, 徐丽莎, 等. 2019. 羟基磷灰石/凹凸棒土复合材料制备及其对水中镉的去除[J]. 环境化学, 2019, 38(4): 850–861.
|
刘羽, 彭明生. 2001. 磷灰石在废水治理中的应用[J]. 安全与环境学报, 2001, 1(1): 9–12.
DOI:10.3969/j.issn.1009-6094.2001.01.002 |
Mulligan C N, Yong R N, Gibbs B F. 2001. Remediation technologies for metal-contaminated soils and groundwater:an evaluation[J]. Engineering Geology, 60: 193–207.
DOI:10.1016/S0013-7952(00)00101-0
|
Ohlinger K N, Young T M, Schroeder E D. 1998. Predicting struvite formation in digestion[J]. Water Research, 32(12): 3607–3614.
DOI:10.1016/S0043-1354(98)00123-7
|
Oste L A, Lexmond T M, Van Riemsdijk W H. 2002. Metal immobilization in soils using synthetic zeolites[J]. Journal of Environmental Quality, 31(3): 813–821.
DOI:10.2134/jeq2002.8130
|
Park J H, Bolan N, Megharaj M, et al. 2011. Comparative value of phosphate sources on the immobilization of lead, and leaching of lead and phosphorus in lead contaminated soils[J]. Science of the Total Environment, 409(4): 853–860.
DOI:10.1016/j.scitotenv.2010.11.003
|
Ronteltap M, Maurer M, Gujer W. 2007. The behaviour of pharmaceuticals and heavy metals during struvite precipitation in urine[J]. Water Research, 41(9): 1859–1868.
DOI:10.1016/j.watres.2007.01.026
|
Purkayastha D, Mishra U, Biswas S. 2014. A comprehensive review on Cd(Ⅱ) removal from aqueous solution[J]. Journal of Water Process Engineering, 2: 105–128.
DOI:10.1016/j.jwpe.2014.05.009
|
施红. 2006.生物吸附法处理废水中重金属离子的研究[D].南京: 河海大学
|
唐利萍, 方扬, 靳艳玲, 等. 2015. 重金属镉超富集浮萍品种筛选及其对水体中镉的去除效果[J]. 应用与环境生物学报, 2015, 21(5): 830–836.
|
Wang H, Wang X J, Chen J, et al. 2016. Recovery of nutrients from wastewater by a MgClr2r modified zeolite and their reuse as an amendment for Cu and Pb immobilization in soil[J]. RSC Advances, 6(61): 55809–55818.
DOI:10.1039/C6RA12169A
|
Wang H, Wang X J, Wang W S, et al. 2016. Modeling and optimization of struvite recovery from wastewater and reusing for heavy metals immobilization in contaminated soil[J]. Journal of Chemical Technology & Biotechnology, 91(12): 3045–3052.
DOI:10.1002/jctb.4931
|
王健, 夏鹏, 张志昊, 等. 2018. 鸟粪石负载硅藻土复合材料对土壤中锌的稳定化作用[J]. 环境工程学报, 2018, 12(4): 1164–1170.
|
杨龑, 陈进一, 王鑫, 等. 2012. 硫化钠-重金属捕集剂组合处理酸性含镍废水[J]. 电镀与环保, 2012, 32(5): 35–38.
DOI:10.3969/j.issn.1000-4742.2012.05.012 |
Yu Y, Wan Y N, Camara A Y, et al. 2018. Effects of the addition and aging of humic acid-based amendments on the solubility of Cd in soil solution and its accumulation in rice[J]. Chemosphere, 196: 303–310.
DOI:10.1016/j.chemosphere.2018.01.002
|
袁绍军, 姜斌, 李天成, 等. 2003. 电解法净化含重金属离子废水的试验研究[J]. 化学工业与工程, 2003, 20(1): 7–10,58.
|
张亚雷, 杨鸿瑞, 周雪飞, 等. 2012. 鸟粪石-絮凝强化工艺处理鸡粪发酵废水[J]. 同济大学学报(自然科学版), 2012, 40(2): 256–261.
DOI:10.3969/j.issn.0253-374x.2012.02.017 |
Zhang Z H, Chen J, Xia P, et al. 2016. Stabilization of Pb in contaminated soil using zeolite-struvite composites[J]. Journal of Agro-Environment Science, 35(11): 2101–2106.
|
张志昊, 陈杰, 夏鹏, 等. 2016. 沸石-鸟粪石复合材料对土壤中铅的稳定化作用[J]. 农业环境科学学报, 2016, 35(11): 2101–2106.
DOI:10.11654/jaes.2016-0760 |
周莹, 潘纲, 陈灏. 2011. 土壤原位覆盖对底泥的修复作用研究[J]. 环境工程学报, 2011, 5(11): 2459–2463.
|
Zhu C, Wen H, Zhang Y, et al. 2018. Cd isotope fractionation duringsulfide mineral weathering in the Fule Zn-Pb-Cd deposit, Yunnan Province, Southwest China[J]. Science of the Total Environment, 616-617: 64–72.
DOI:10.1016/j.scitotenv.2017.10.293
|
Zhu X H, Li J, Luo J H, et al. 2017. Removal of cadmium (Ⅱ) from aqueous solution by a new adsorbent of fluor-hydroxyapatite composites[J]. Journal of the Taiwan Institute of Chemical Engineers, 70: 200–208.
DOI:10.1016/j.jtice.2016.10.049
|
左卫元, 仝海娟, 史兵方. 2015. 改性活性炭对废水中铬离子的吸附[J]. 环境工程学报, 2015, 9(1): 45–50.
|
 2019, Vol. 39
2019, Vol. 39


