2. 合肥工业大学化学与化工学院, 合肥 230009
2. School of Chemistry and Chemical Engineering, Hefei University of Technology, Hefei 230009
煤在燃烧过程中释放的汞大部分随着烟气排入大气, 成为环境汞污染的主要来源.燃煤电站排放的汞是我国汞污染的最主要来源, 约占全国汞排放总量的40%.根据联合国环境规划署的预测报告, 2020年我国燃煤电站汞排放量约500 t, 将占同期全球化石燃料燃烧排放汞总量的40%以上, 因此, 燃煤汞污染问题不容忽视(孙阳昭等, 2013;Wang et al., 2014;Zhu et al., 2015).我国政府高度重视燃煤污染问题, 新修订的《火电厂大气污染物排放标准》(GB13223-2011)首次对火电厂汞的排放做出了明确规定, 限定汞的排放值在0.03 mg · m-3以下.
燃煤烟气中的汞主要存在3种形态:气态单质汞(Hg0)、气态氧化态汞(Hg2+)和吸附在飞灰上的汞(Hgp).其中, Hg2+和Hgp可以通过电厂现有的污染物控制装置脱除.Hg0由于其化学惰性、挥发性较高及水溶性低的特点, 难以被电厂现有的污染物控制装置有效脱除, 因而成为燃煤电厂烟气汞污染控制的难点和研究的热点(Wang et al., 2011;王钧伟等, 2012;Zhou et al., 2015).
目前研究最多的燃煤烟气汞污染控制技术是向烟道中喷入吸附剂来吸附烟气中的气态Hg0和Hg2+, 其中, 研究和使用最广泛的吸附剂是活性炭及化学改性后的活性炭(Zhou et al., 2010;Hu et al., 2011; Colin et al., 2012;Zhang et al., 2015;Li et al., 2017;Chen et al., 2018).活性炭在低温条件下展现了良好的吸附烟气中Hg的活性, 但在烟气温度下对Hg的吸附能力较低, 而且受烟气成分的影响很大, 消耗量大, 运行成本很高(Jones et al., 2007), 使得活性炭喷射技术在燃煤电厂的推广应用受到限制.因此, 开发经济有效的燃煤烟气汞污染控制技术受到人们的重视.
近年来, 对Hg0同时具有氧化和吸附作用的催化/吸附剂的研究受到科研人员的广泛重视, 该类催化/吸附剂可将Hg0氧化为Hg2+并将其吸附在催化/吸附剂上(Wang et al., 2010;王钧伟等, 2012;2014;Zhao et al., 2016;He et al., 2016;Yang et al., 2016;Wang et al., 2016).凹凸棒石(PG)是一种天然多孔型链层状含水富镁铝硅酸盐类粘土矿物, 孔隙发达, 比表面积大, 吸附性和热稳定性好, 成本低廉, 既是金属氧化物催化剂的优良载体, 又是金属离子较好的吸附介质.已有文献报道采用凹凸棒石负载Mn、Co、Mo等金属氧化物制备催化剂用于脱除烟气中的NOx和Hg0(李金虎等, 2010;Ding et al., 2012;Liu et al., 2014;Luo et al., 2016;王钧伟等, 2017).实验室的研究和燃煤电厂的现场测试结果均表明, V2O5对燃煤烟气中的Hg0具有较高的氧化活性, 活性组分主要为V2O5的SCR催化剂可将Hg0氧化为Hgg2+(He et al., 2009;Zhao et al., 2015;Zhang et al., 2015;Li et al., 2017;Chi et al., 2017).
基于此, 本文通过负载V2O5到凹凸棒石制备V2O5/PG催化剂用于脱除燃煤烟气中的气态Hg0, 研究反应温度、Hg0浓度、空速、烟气成分等对V2O5/PG脱除Hg0的影响, 并利用傅里叶红外光谱、逐级化学提取和程序升温脱附实验分析V2O5/PG上吸附Hg的形态.
2 材料与方法(Materials and methods) 2.1 实验原料与试剂凹凸棒石购自安徽省明光市官山凹凸棒石黏土矿;偏钒酸铵(NH4VO3)购自上海晶纯生化科技有限公司;草酸(C2H2O4 · 2H2O)购自国药集团化学试剂有限公司;五氧化二钒(V2O5)、硼氢化钾(K2BH4)购自天津市晶科精细化工研究所;氮气(N2)、氧气(O2)由安庆市气体责任有限公司提供;二氧化硫(SO2)由大连大特气体有限责任公司提供;蒸馏水为自制.
2.2 主要仪器RA-915M测汞仪(俄罗斯Lumix公司), Nicolet iS 50ATR傅里叶变换红外光谱仪(美国Thermo Fisher Scientific公司).
2.3 研究方法 2.3.1 V2O5/PG催化剂的制备按照质量与体积比为1 g : (4~8) mL的比例将凹凸棒石与蒸馏水混合, 搅拌, 静置, 干燥即可得到凹凸棒石样品.将该样品研磨至30~60目颗粒, 再在300 ℃下的氮气气氛中热处理2 h, 即得到实验所需的凹凸棒石载体.
称取11.27 g偏钒酸铵(NH4VO3)和22 g草酸(C2H2O4 · 2H2O)置于锥形瓶中, 加入70 mL蒸馏水混合均匀, 配置成棕黄色的混合水溶液.缓慢加热该溶液同时快速搅拌, 当溶液颜色逐渐由棕黄色变为深蓝色时停止加热.自然冷却后加蒸馏水定容至100 mL, 得到V2O5前驱体溶液.移取一定量上述前驱体溶液稀释至所需浓度, 将凹凸棒石载体等体积浸渍到前驱体溶液中, 静置24 h, 先后在50 ℃和110 ℃下干燥5 h和10 h, 最后在空气气氛下于300 ℃煅烧2 h, 制得V2O5负载量为1%~5%的V2O5/PG催化剂(Wang et al., 2010).
2.3.2 V2O5/PG催化剂脱除Hg0的实验图 1为V2O5/PG催化剂脱除Hg0的固定床实验反应装置, 主要由模拟烟气配制装置、Hg0蒸气发生装置、催化反应装置和Hg0检测装置组成.
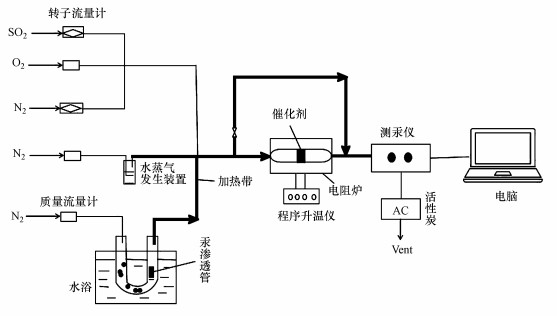 |
| 图 1 V2O5/PG催化剂脱除Hg0的实验装置 Fig. 1 Schematic diagram of Hg0 removal over V2O5/PG catalyst |
模拟烟气由O2、SO2、H2O、Hg0、N2(作为平衡气体使用)组成.气态Hg0由汞渗透管(美国VICI公司)产生, 通过控制一定的水槽温度和载气N2的流量, 可以产生一定浓度的气态Hg0.装有0.5 g V2O5/PG催化剂的石英管放入电阻炉中, 通过程序控温仪和热电偶可自动控制电炉的温度从而对催化剂进行恒温加热.Hg0检测装置由测汞仪(俄罗斯Lumix公司, RA-915M)和电脑组成, 可在线连续监测反应器进口、出口气体中的Hg0.为了防止Hg0在管路内冷凝, 管路采用加热带保温至120 ℃.烟气成分的浓度和实验条件见表 1.
| 表 1 V2O5/PG催化剂脱除Hg0的实验条件 Table 1 Experimental conditions of Hg0 removal over V2O5/PG catalyst |
采用脱除效率(E)表示V2O5/PG催化剂对Hg0的脱除效果, 定义为一定时间内V2O5/PG吸附汞的量与进入反应器的Hg0量的百分比, 即:
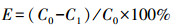
|
(1) |
式中, C0表示反应器进口处测得的模拟烟气中Hg0浓度, C1表示反应器出口气体经KBH4溶液还原后测得的总Hg浓度.
2.3.3 程序升温脱附实验(TPD)程序升温脱附实验也在图 1所示的装置上进行.样品为在N2+O2+SO2+H2O气氛中于150 ℃下脱除Hg0后的V2O5/PG样品, 加入量约5 mg.反应前整个系统先在常温下经200 mL · min-1的高纯氮气吹扫30 min, 然后以10 ℃ · min-1的升温速率由室温升至650 ℃.反应器出口气体先通过KBH4溶液将其中可能存在的Hg2+还原为Hg0后, 再经测汞仪在线连续监测.
2.4 分析表征 2.4.1 傅里叶红外光谱样品经美国Thermo Fisher Scientific公司Nicolet iS 50ATR型傅里叶变换红外光谱仪测定, 测量条件:室温, 分辨率4 cm-1, 波数范围4000~400 cm-1, KBr压片.
2.4.2 逐级化学提取实验逐级化学提取实验用于测定脱除Hg0后的PG和V2O5/PG上吸附Hg的形态及其含量, 具体的实验步骤参见文献(Bloom et al., 2003).将样品依次采用二次去离子水、0.1 mol · L-1 CH3COOH+0.01 mol · L-1 HCl溶液、1 mol · L-1 KOH溶液、12 mol · L-1 HNO3溶液、王水5种溶液提取不同形态的汞.提取溶液与固体样品按照100/1比例混合, 然后在25 ℃下不断搅拌提取20 h.每个样品经同一提取溶液依次提取2次, 所得提取液中的汞含量采用原子荧光光谱仪测定.
3 结果与讨论(Results and discussion) 3.1 温度对V2O5/PG脱除Hg0的影响图 2为在N2+O2+SO2+H2O气氛中, PG在150 ℃和5%V2O5/PG催化剂在不同温度(120、150、180、210 ℃)下脱除Hg0的结果.可以看出, 单纯PG载体对Hg0的脱除能力很低, 开始时的Hg0脱除效率只有50%, 且随着时间的延长迅速下降到10%左右.V2O5/PG催化剂在120~210 ℃范围内展现出良好的脱除Hg0性能.120 ℃时, V2O5/PG催化剂对Hg0的初始脱除效率达到95%以上, 150~180 ℃范围内达到80%以上, 而且随着时间的延长脱除Hg0的性能保持稳定, 400 min后仍达到80%以上.温度为210 ℃时, Hg0的脱除效率有所降低, 保持在60%左右.这可能是由于V2O5的氧化活性随着温度的上升而增强, 但载体的吸附作用会减弱, 两者的共同作用在150~180 ℃温度范围内形成了较高的脱除Hg0性能(Wang et al., 2016;王钧伟等, 2017).温度升高, 吸附(可能包含部分V2O5/PG上吸附Hg的脱附)成为影响V2O5/PG催化剂脱除Hg0能力的主要因素.可见, V2O5/PG催化剂在120~210 ℃温度范围内具有良好的脱除Hg0的能力, 可将Hg0氧化并吸附在催化剂上.V2O5/TiO2类SCR催化剂主要用于烟气脱硝, 操作温度较高, 实验室的研究和燃煤电厂现场测试的结果均表明, V2O5/TiO2虽可将Hg0氧化生成Hg2+, 但其自身对汞的吸附能力很小(Cao et al., 2007;He et al., 2009;Zhang et al., 2015;Zhao et al., 2015).与V2O5/TiO2类SCR催化剂相比, V2O5/PG催化剂脱除Hg0具有更低的使用温度和更高的吸附能力.
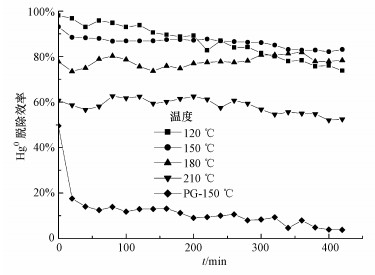 |
| 图 2 温度对V2O5/PG脱除Hg0的影响 Fig. 2 Effect of temperature on Hg0 removal by V2O5/PG |
图 3为在N2+O2+SO2+H2O气氛中, 5%V2O5/PG催化剂在150 ℃和不同Hg0浓度(80、125、240 μg · m-3)下脱除Hg0的结果.可以看出, 在80~240 μg · m-3的Hg0浓度范围内, V2O5/PG催化剂都具有良好的脱除Hg0的能力, Hg0的初始脱除效率均在90%以上.随着反应时间的延长, Hg0的脱除效率基本保持不变, 400 min后仍维持在90%左右.为考察V2O5/PG催化剂对Hg0的吸附容量, 本文进行了5%V2O5/PG催化剂在240 μg · m-3的Hg0浓度条件下脱除Hg0 10 d的实验, 结果表明, Hg0的脱除效率仍保持在65%左右, 远未达到吸附饱和.这表明V2O5/PG催化剂在较宽的Hg0浓度范围内具有良好的脱除Hg0的能力, 而且具有较高的脱除Hg0的容量, 在实际燃煤烟气所含的Hg0浓度范围内(1~35 μg · m-3)可较长时间使用.对脱除Hg0后的V2O5/PG催化剂的再生实验结果表明, 再生后V2O5/PG仍具有良好的再次脱除Hg0的能力, Hg0的脱除效率仍保持在70%以上, 表明该催化剂具有良好的再生循环使用性能, 吸附汞饱和后可再生循环使用.
 |
| 图 3 Hg0浓度对V2O5/PG脱除Hg0的影响 Fig. 3 Effect of mercury concentration on Hg0 removal by V2O5/PG |
图 4为在N2+O2+SO2+H2O气氛中, 5%V2O5/PG催化剂在150 ℃和不同空速(6000、10000、15000 h-1)条件下脱除Hg0的结果.可以看出, 在6000~15000 h-1的空速范围内, V2O5/PG催化剂具有较高的脱除Hg0的能力.空速为15000 h-1时, Hg0的脱除效率在60%左右, 当空速降低为6000 h-1时, Hg0的脱除效率达到90%, 而且随着时间的延长Hg0的脱除效率基本保持不变.这主要是由于空速降低, 增加了气体与催化剂的接触时间, 即增加了气流中Hg0与催化剂上活性位的接触几率, 从而提高了Hg0的脱除效率.图 4中的实验数据表明, V2O5/PG催化剂在较低空速下具有更高的脱除Hg0的能力, 能够与燃煤电厂目前实际运行的烟气净化空速匹配.
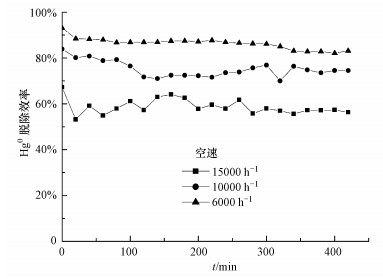 |
| 图 4 空速对V2O5/PG脱除Hg0的影响 Fig. 4 Effect of space velocity on Hg0 removal by V2O5/PG |
图 5为V2O5/PG催化剂在150 ℃和不同烟气成分(N2、N2+8%O2、N2+5%H2O、N2+0.15%SO2、N2+0.05%NO、N2+10%CO2)条件下脱除Hg0的结果.可以看出, N2气氛中, V2O5/PG催化剂具有良好的脱除Hg0的能力, 400 min时Hg0的脱除效率仍保持在90%以上, 这表明V2O5/PG催化剂对Hg0具有良好的氧化吸附能力, Hg在其上的吸附未对V2O5/PG的氧化活性产生明显影响.N2+O2气氛中, Hg0的脱除效率有所上升, 这表明O2对V2O5/PG催化剂脱除Hg0具有促进作用, 这与文献(Wang et al., 2010)中报道的O2对V2O5基催化剂氧化Hg0的促进作用是一致的, 主要是由于O2可向反应后的晶格氧提供O从而恢复其氧化活性.N2+H2O和N2+SO2气氛中, V2O5/PG催化剂对Hg0的脱除效率分别只有55%和40%左右, 远低于N2气氛中的90%, 表明H2O和SO2对V2O5/PG脱除Hg0的抑制作用明显, 主要是由于H2O和SO2可在V2O5/PG催化剂上吸附, 与Hg0在V2O5/PG催化剂的活性位上存在竞争吸附, 从而导致V2O5/PG催化剂对Hg0的脱除效率降低.N2+NO和N2+CO2气氛中, V2O5/PG催化剂对Hg0的脱除效率与N2气氛中相比没有明显变化, NO具有轻微的促进作用, CO2的作用不明显.
 |
| 图 5 烟气成分对V2O5/PG脱除Hg0的影响 Fig. 5 Effect of flue gas components on Hg0 removal by V2O5/PG |
图 6为V2O5/PG催化剂在150 ℃和多种烟气成分共存(N2、N2 +8%O2+0.15%SO2、N2+8%O2+5%H2O、N2+0.15%SO2+5%H2O、N2+8%O2+0.15%SO2+5%H2O)条件下脱除Hg0的结果.可以看出, V2O5/PG催化剂在N2+O2+SO2气氛中对Hg0的脱除效率低于在N2气氛中, 但与N2+SO2气氛中的脱除效率相比明显升高, 反应400 min后Hg0的脱除效率仍维持在70%以上.N2+O2+H2O气氛中, V2O5/PG对Hg0的脱除效率稍低于N2气氛中, 但明显高于N2+H2O气氛中的脱除效率, 400 min后Hg0的脱除效率仍维持在80%左右.N2+SO2+H2O气氛中, Hg0的脱除效率较N2+SO2和N2+H2O气氛中均有所降低, 远低于N2气氛, 400 min后Hg0的脱除效率只有30%左右.N2+O2+SO2+H2O气氛中, V2O5/PG对Hg0的脱除效率与N2气氛中相当, 但明显高于N2+O2+SO2、N2+O2+H2O、N2+SO2+H2O这3种气氛中的脱除效率, 主要是由于SO2在O2和H2O存在条件下可被V2O5催化氧化生成H2SO4, 从而促进了Hg0在V2O5/PG上的氧化脱除.
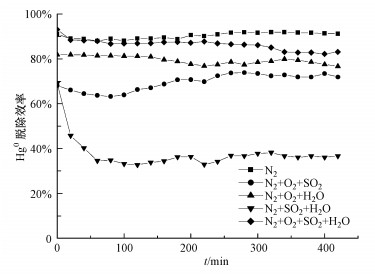 |
| 图 6 多烟气成分对V2O5/PG脱除Hg0的影响 Fig. 6 Effect of multi-components in flue gas on Hg0 removal by V2O5/PG |
采用傅里叶红外光谱、逐级化学提取和程序升温脱附实验等对新鲜的V2O5/PG催化剂和吸附Hg0后的V2O5/PG催化剂(V2O5/PG-Hg)进行分析表征, 以确定V2O5/PG-Hg上吸附汞的形态及含量, 判明V2O5/PG催化剂在Hg0脱除过程中的氧化、吸附作用.图 7为PG、V2O5/PG和V2O5/PG-Hg的傅里叶红外光谱图.可以看出, 3个样品的傅里叶红外光谱图的峰型和峰位置基本上没有区别, 在500、1000、1650、3500 cm-1处均出现一个强的谱带, 这些都是凹凸棒石的特征峰.500 cm-1处的峰可归结为Si—O—Si对称伸缩振动带, 1000 cm-1处的双峰为凹凸棒石的Si—O伸缩带, 1650 cm-1处的峰为凹凸棒石上的吸附水或者为结晶水的伸缩带, 3500 cm-1处的峰是凹凸棒石的Al—Al—OH伸缩振动(Suárez et al., 2006;高翔云等, 2016).但红外谱图中并没有找到明显的Hg的特征峰, 没有给出V2O5/PG催化剂上吸附Hg形态的信息.这主要是由于凹凸棒石载体是一种成分复杂的混合物, 其中一些成分的红外光谱可能存在相互叠加、掩盖等情况.
 |
| 图 7 PG、V2O5/PG和V2O5/PG-Hg的傅里叶红外光谱 Fig. 7 FT-IR analysis of PG, V2O5/PG and V2O5/PG-Hg |
图 8为V2O5/PG和V2O5/PG-Hg的TPD实验结果.可以看出, 温度从室温升高到600 ℃的过程中, V2O5/PG样品没有出现明显的汞的释放峰, 而V2O5/PG-Hg样品出现了两个汞的释放峰, 分别在250 ℃和490 ℃左右.两个汞的释放峰表明V2O5/PG催化剂上吸附的汞存在两种不同的形态, 根据文献报道, 应该与HgO和HgSO4的释放有关(Guo et al., 2009;Rumayor et al., 2015), 表明Hg0在V2O5/PG催化剂上被氧化并发生了化学反应.值得注意的是, 汞的初始释放温度大约在150 ℃左右, 这表明温度高于150 ℃时, V2O5/PG-Hg上吸附的部分汞已经开始脱附, 尽管V2O5对Hg0的氧化作用随温度的升高而增强, 但温度升高会同时导致部分汞的脱附, 从而使得V2O5/PG对Hg0的脱除效率下降, 这解释了图 2中V2O5/PG对Hg0的脱除能力随温度升高而先上升后下降的结果.
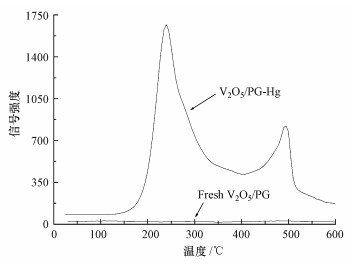 |
| 图 8 V2O5/PG和V2O5/PG-Hg的TPD Fig. 8 TPD profiles of V2O5/PG and V2O5/PG-Hg |
图 9为脱除Hg0后的PG(PG-Hg)和V2O5/PG(V2O5/PG-Hg)样品的逐级化学提取实验结果.可以看出, 两个样品上的汞被不同的提取液所提取出来, PG-Hg上的汞主要被HNO3提取出来(约占其上总汞量的82%), 而V2O5/PG-Hg上的汞主要被CH3COOH+HCl和二次去离子水提取出来(约占其上总汞量的75%), 被HNO3提取出来的汞只占约17%.根据文献报道(Bloom et al., 2003), HNO3提取的主要是Hg0而CH3COOH+HCl和二次去离子水提取的主要是Hg2+, 这表明PG-Hg上的汞主要是Hg0而V2O5/PG-Hg上的汞主要是Hg2+的化合物, 这与图 8中的结果是一致的.综合TPD和逐级化学提取实验的结果, 可以判明V2O5/PG催化剂对Hg0的脱除过程包含了V2O5对Hg0的氧化和PG对Hg2+与Hg0的吸附两种作用, 其中, V2O5对Hg0的催化氧化作用是V2O5/PG具有较高的脱除Hg0能力的主要原因.
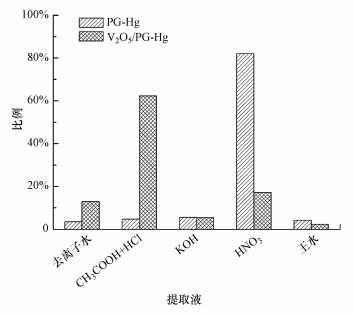 |
| 图 9 PG-Hg和V2O5/PG-Hg样品的逐级化学提取 Fig. 9 Sequential chemical extraction of PG-Hg and V2O5/PG-Hg samples |
1) V2O5/PG催化剂在120~210 ℃温度范围内具有良好的脱除Hg0的能力.温度升高, Hg0的脱除效率有所降低, 主要是由于V2O5/PG对Hg0的脱除是V2O5对Hg0的氧化作用和PG对Hg的吸附作用的共同结果, 两者在不同温度下的作用程度不同.
2) V2O5/PG催化剂在燃煤烟气所含的汞浓度和电厂烟气净化的空速条件下具有良好的脱除Hg0的能力.
3) O2对V2O5/PG脱除Hg0具有促进作用, 而H2O和SO2具有抑制作用, NO和CO2的作用不明显.O2+SO2、O2+H2O气氛中, Hg0的脱除效率明显提高.O2、SO2和H2O共同存在时, 可促进Hg0的脱除.
4) 程序升温脱附和逐级化学提取实验的结果证实, V2O5/PG催化剂上吸附汞的形态主要是Hg2+的化合物HgO和HgSO4.Hg0在V2O5/PG上的脱除包含氧化、反应、吸附等过程.
Bloom N, Preus E, Katon J. 2003. Selective extractions to assess the biogeochemically relevant fractionation of inorganic mercury in sediments and soils[J]. Analytica Chimica Acta, 479: 233–248.
DOI:10.1016/S0003-2670(02)01550-7
|
Cao Y, Chen B, Wu J, et al. 2007. Study of mercury oxidation by a selective catalytic reduction catalyst in a pilot-scale slipstream reactor at a utility boiler burning bituminous coal[J]. Energy Fuels, 21: 145–156.
DOI:10.1021/ef0602426
|
Chen Y, Guo X, Wu F, et al. 2018. Experimental and theoretical studies for the mechanism of mercury oxidation over chlorine and cupric impregnated activated carbon[J]. Applied Surface Science, 458: 790–799.
DOI:10.1016/j.apsusc.2018.07.167
|
Chi G L, Shen B X, Yu R R, et al. 2017. Simultaneous removal of NO and Hg0 over Ce-Cu modified V2O5/TiO2 based commercial SCR catalysts[J]. Journal of Hazardous Materials, 330: 83–92.
DOI:10.1016/j.jhazmat.2017.02.013
|
Colin B W, Chad T, William F, et al. 2012. Preparation and characterization of high efficiency modified activated carbon for the capture of mercury from flue gas in coal-fired power plants[J]. Fuel Processing Technology, 97: 107–117.
DOI:10.1016/j.fuproc.2012.01.017
|
Ding F, Zhao Y C, Mi L L, et al. 2012. Removal of gas-phase elemental mercury in flue gas by inorganic chemically promoted natural mineral sorbents[J]. Industrial & Engineering Chemistry Research, 51(2): 3039–3047.
|
高翔云, 高孝礼, 汪建明. 2016. 盱眙凹凸棒石黏土的中红外和近红外光谱特征研究与应用[J]. 江苏科技信息, 2016, 3(9): 51–54.
DOI:10.3969/j.issn.1004-7530.2016.09.022 |
Guo S Q, Yang J L, Liu Z Y, et al. 2009. Behavior of mercury release during thermal decomposition of coals[J]. Korean Journal of Chemical Engineering, 26(2): 560–563.
DOI:10.1007/s11814-009-0095-9
|
He C, Shen B X, Li F K. 2016. Effects of flue gas components on removal of elemental mercury over Ce-MnOx/Ti-PILCs[J]. Journal of Hazardous Materials, 304: 10–17.
DOI:10.1016/j.jhazmat.2015.10.044
|
He S, Zhou J, Zhu Y, et al. 2009. Mercury oxidation over a vanadia-based selective catalytic reduction catalyst[J]. Energy Fuels, 23: 253–259.
DOI:10.1021/ef800730f
|
Hu C X, Zhou J S, Luo Z Y, et al. 2011. Oxidative adsorption of elemental mercury by activated carbon in simulated coal-fired flue gas[J]. Energy Fuels, 25: 154–158.
DOI:10.1021/ef101100y
|
Jones A, Hoffmann J, Smith D, et al. 2007. DOE/NETL's phase Ⅱ mercury control technology field testing program:Preliminary economic analysis of activated carbon injection[J]. Environmental Science & Technology, 41: 1365–1371.
|
Li B, Wang H L, Xu Y Y, et al. 2017. Study on mercury oxidation by SCR catalyst in coal-fired power plant[J]. Energy Procedia, 141: 339–344.
DOI:10.1016/j.egypro.2017.11.040
|
李金虎, 张先龙, 陈天虎, 等. 2010. 凹凸棒石负载锰氧化物低温选择性催化还原催化剂的表征及对氨的吸脱附[J]. 催化学报, 2010, 31(4): 454–460.
|
Li Y N, Duan Y F, Wang H, et al. 2017. Effects of acidic gases on mercury adsorption by activated carbon in simulated oxy-fuel combustion flue gas[J]. Energy Fuels, 31: 9745–9751.
DOI:10.1021/acs.energyfuels.7b01480
|
Liu F F, Zhang J Y, Zhao Y C, et al. 2014. Mercury removal from flue gas by metal oxide-loaded attapulgite mineral sorbent[J]. Journal of Combustion Science and Technology, 20(6): 553–557.
|
Luo S P, Zhou W T, Xie A J, et al. 2016. Effect of MnO2 polymorphs structure on the selective catalytic reduction of NOx with NH3 over TiO2-Palygorskite[J]. Chemical Engineering Journal, 286: 291–299.
DOI:10.1016/j.cej.2015.10.079
|
Rumayor M, López-Antón M A. 2015. Temperature programmed desorption as a tool for the identification of mercury fate in wet-desulphurization systems[J]. Fuel, 148: 98–103.
DOI:10.1016/j.fuel.2015.01.101
|
Suárez M, García-Romero E. 2016. FTIR spectroscopic study of palygorskite:Influence of the composition of the octahedral sheet[J]. Applied Clay Science, 31: 154–163.
|
孙阳昭, 陈扬, 蓝虹, 等. 2013. 中国汞污染的来源、成因及控制技术路径分析[J]. 环境化学, 2013, 32(6): 937–942.
|
王钧伟, 陈培, 刘瑞卿, 等. 2014. 粉煤灰负载Fe2O3脱除气态单质汞的试验研究[J]. 环境科学学报, 2014, 34(12): 3152–3157.
|
Wang J W, Shen Y Y, Dong Y J, et al. 2016. Oxidation and adsorption of gas-phase Hg0 over a V2O5/AC catalyst[J]. RSC Advances, 6: 77553–77557.
DOI:10.1039/C6RA15455G
|
Wang J, Wang W H, Xu W, et al. 2011. Mercury removals by existing pollutants control devices of four coal-fired power plants in China[J]. Journal of Environmental Sciences, 23(11): 1839–1844.
DOI:10.1016/S1001-0742(10)60584-0
|
Wang J W, Yang J L, Liu Z Y. 2010. Gas-phase elemental mercury capture by a V2O5/AC catalyst[J]. Fuel Processing Technology, 91(6): 676–680.
DOI:10.1016/j.fuproc.2010.01.017
|
王钧伟, 杨建丽, 刘振宇. 2012. 活性焦负载MnO2对气态Hg0的吸附脱除研究[J]. 环境科学学报, 2012, 32(9): 2261–2266.
|
王钧伟, 张庆平, 沈园园, 等. 2017. 凹凸棒石负载CuO催化剂脱除气态Hg0[J]. 环境化学, 2017, 36(5): 1097–1103.
|
Wang S X, Zhang L, Wang L, et al. 2014. A review of atmospheric mercury emissions, pollution and control in China[J]. Frontiers of Environmental Science & Engineering, 8(5): 631–649.
|
Yang J P, Zhao Y C, Ma S M, et al. 2016. Mercury removal by magnetic biochar derived from simultaneous activation and magnetization of sawdust[J]. Environmental Science & Technology, 50: 12040–12047.
|
Zhang B, Xu P, Qiu Y, et al. 2015. Increasing oxygen functional groups of activated carbon with non-thermal plasma to enhance mercury removal efficiency for flue gases[J]. Chemical Engineering Journal, 263: 1–8.
DOI:10.1016/j.cej.2014.10.090
|
Zhang X N, Li C T, Zhao L K, et al. 2015. Simultaneous removal of elemental mercury and NO from flue gas by V2O5-CeO2/TiO2 catalysts[J]. Applied Surface Science, 347: 392–400.
DOI:10.1016/j.apsusc.2015.04.039
|
Zhao B, Liu X W, Zhou Z J, et al. 2015. Mercury oxidized by V2O5-MoO3/TiO2 under multiple components flue gas:An actual coal-fired power plant test and a laboratory experiment[J]. Fuel Processing Technology, 134: 198–204.
DOI:10.1016/j.fuproc.2015.01.034
|
Zhao B, Yi H H, Tang X L, et al. 2016. Copper modified activated coke for mercury removal from coal-fired flue gas[J]. Chemical Engineering Journal, 286: 585–593.
DOI:10.1016/j.cej.2015.10.107
|
Zhou W, Gilles E, Abu R, et al. 2010. Prediction of activated carbon injection performance for mercury capture in a full-scale coal-fired boiler[J]. Industrial & Engineering Chemistry Research, 49: 3603–3610.
|
Zhou Z J, Liu X W, Zhao B, et al. 2015. Effects of existing energy saving and air pollution control devices on mercury removal in coal-fired power plants[J]. Fuel Processing Technology, 131: 99–108.
DOI:10.1016/j.fuproc.2014.11.014
|
Zhu C Y, Tian H Z, Cheng K, et al. 2015. Potentials of whole process control of heavy metals emissions from coal-fired power plants in China[J]. Journal of Cleaner Production, 114: 343–351.
|
 2019, Vol. 39
2019, Vol. 39


