碘甲烷(CH3I)又名甲基碘, 是卤代甲烷的一种, 可为陆地需碘生物提供必须的微量元素(Fuge, 1986), 也是碘在海陆之间循环的重要载体(Singh et al., 1983).CH3I在大气中不仅会与臭氧直接反应生成碘自由基(I ·), 破坏大气中的臭氧(李冠霖等, 2017), 还会通过一系列化学反应对大气中其他气体的浓度产生影响(Von et al., 2007).随着对大气卤代甲烷人为释放源的控制, 其自然释放源的相对重要性日益突出.在大气卤代甲烷自然源研究进程中, 目前的研究证明, 海洋CH3I的释放量占全球释放总量的85%(Youn et al., 2010).
沿海盐沼是海陆相交的过渡带, 初级生产力较高, 且被富含卤素的海水淹没.由于其具有丰富的有机碳、游离卤素和生物活性, 所以将沿海盐沼视为研究CH3I潜在来源的合理场所.国际上关于盐沼卤代甲烷的研究主要集中在美国(Manley et al., 2006; Rhew et al., 2007)、爱尔兰(Dimmer et al., 2001)、澳大利亚(Cox et al., 2004)等地.国内关于卤代甲烷的研究起步较晚, 谢文霞等(2015)对海岸带盐沼生态系统卤代甲烷释放机制进行了阐述, 仅王进欣等(2012;2006)对苏北盐沼、中国东部沿海盐沼海拔梯度上的CH3Cl气体进行了具体测定, 有关其他盐沼对卤代甲烷的研究鲜有报道.Rhew等(2000)等通过研究发现, 不同地域卤代甲烷的释放量有明显的不同.
目前, 全球CH3I预算存在很大的不确定性, 本研究选取胶州湾盐沼互花米草湿地(S区)和光滩(M区)作为研究对象, 通过对两类样地中CH3I排放通量、时空变化及其影响因素等进行探究, 以期科学估量胶州湾盐沼释放CH3I气体的情况.
2 采样与研究方法(Sampling and research methods) 2.1 研究区概况实验样地位于黄海中部、胶东半岛南岸的胶州湾洋河入湾口(图 1, 120°01′~120°20′E, 36°06′~36°13′N).胶州湾盐沼是山东半岛最大的河口海湾型湿地, 属于以潮汐作用为主的海岸, 潮汐为正规半日潮, 平均潮差2.71 m, 最大潮差6.87 m.区内气候为暖温带季风气候, 年均气温在12.2 ℃左右, 降水分布不均匀, 平均降雨量达775.6 mm, 植被以互花米草为主, 覆盖率达95%以上.
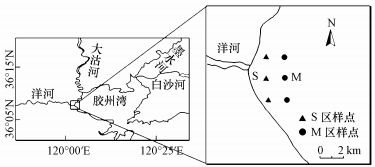 |
| 图 1 胶州湾盐沼采样位置图 Fig. 1 Sampling location of salt marsh in Jiaozhou Bay |
本试验遵循典型性、代表性、可行性和一致性的原则, 在胶州湾洋河入海口依据有无互花米草生长来确定2类样地, 根据距海远近, 依次是互花米草湿地(S区)和光滩(M区).在每类采样区分别设置3个平行采样点(图 1), 最终数据取3个平行样点数据平均值.
选用静态箱法采集气体样品, 具体采样时间分别为2016年的7、9、10、11、12月及2017年的3、5月, 各月均采样一次.每个测点分别于采样当日的10:00、13:00、16:00进行气体采集, 将气样注入到1 L的铝塑复合气袋中, 在每个时间点分别各重复测量3次, 且时间间隔为20 min.待测样品在24 h内带回实验室, 随后用Agilent 6890N气相色谱仪进行分析.在气体样品采集过程中还需对气温、箱温和地温(0~25 cm)进行同步测量.此外, 在每个样点采集0~60 cm的土壤样品, 并测定土样含水量、pH、盐度、总有机碳(TOC)、总氮(TN)和总硫(TS).其中, 土壤含水量采用重量法测定, pH用pH计测定, 盐度采用电导分析法测定, TOC用重铬酸钾氧化分光光度法测定, TN采用凯氏定氮法测定, TS选用硫酸钡浊度法测定.
2.3 数据分析箱内CH3I通量采用以下公式进行计算:
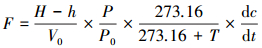
|
(1) |
式中, F为CH3I气体排放通量(nmol · m-2 · d-1); H为采样箱体有效高度(m); h为水位高度(m); V0为标准状态下气体的摩尔体积(22.4 L · mol-1); P为采样时实际大气压(Pa); P0为标准大气压(Pa); T为箱内温度(℃); dc/dt表示单位时间箱体内CH3I气体浓度的变化率, 采用线性拟合气体物质的量浓度随采样时间的变化, R2至少大于0.9.
统计分析采用Microsoft Excel 2016和SPSS 22.0软件, 对同一地带不同季节及同一季节不同地带的CH3I通量进行单因素差异性方差分析(One-Way ANOVA), 气体通量和环境因素间的相关性采用Pearson相关性分析, 最后使用软件Origin 2017进行绘图.
3 结果与分析(Results and analysis) 3.1 CH3I通量变化研究区在整个采样期间的CH3I通量范围为-99.43~76.38 nmol · m-2 · d-1, 年均值为8.06 nmol · m-2 · d-1, 整体表现为排放.其中, S区CH3I的年均排放通量为9.61 nmol · m-2 · d-1, 而M区CH3I的年均排放通量为6.63 nmol · m-2 · d-1, S区的CH3I排放通量高于M区, 但两个样区之间不具显著性差异(p>0.05).S区与M区在不同采样月份中呈现出不同的变化趋势(图 2), S区CH3I通量最大值出现在夏季的7月, M区CH3I通量在冬季的12月最大.
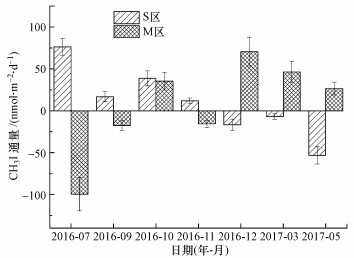 |
| 图 2 S区和M区在不同月份的CH3I通量变化 Fig. 2 CH3I flux changes in different months in area S and M |
此外, 本研究以2017年3、5月代表春季, 2016年7月代表夏季, 2016年9、10、11月代表秋季, 2016年12月代表冬季.CH3I在S区和M区春、夏、秋、冬4个季节的平均通量分别为-29.98、76.38、22.53、-16.73 nmol · m-2 · d-1和36.48、-99.43、0.76和70.62 nmol · m-2 · d-1.S区CH3I通量在夏、秋季节为正值, 表现为排放, 而在冬、春季节为负值, 表现为吸收, 且夏季通量明显高于另外三季, 但季节间的CH3I通量没有显著性差异(p>0.05).而M区CH3I通量除在夏季为负值, 表现为吸收之外, 其他季节均表现排放, 且冬季通量明显高于其他季节, 季节间的CH3I通量不具显著性差异(p>0.05).据图 3可知, S区和M区的CH3I季节通量变化趋势相反, S区CH3I通量在夏、秋季高, 而M区CH3I通量在冬、春季高.
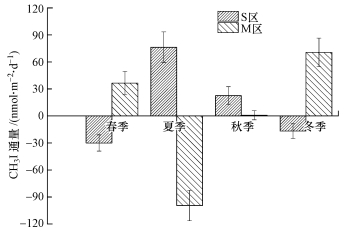 |
| 图 3 S区和M区在不同季节的CH3I通量变化 Fig. 3 CH3I flux changes in different seasons in area S and M |
S区和M区的温度(气温和地温)呈现出相同的季节变化趋势(图 4).S区的pH低于M区(表 1), 不同采样区的pH具有显著性差异(p < 0.05).S区的有机质含量比M区高, 但不同采样区之间不存在显著性差异(p>0.05).此外, 两个采样区间的盐度和含水率无显著性差异(p>0.05), 且S区的盐度和含水率均比M区高.S区与M区TN的季节变化趋势基本一致, 从春季到冬季均呈现先下降后上升的走势, S区在秋季出现最低值(图 5).S区的TN、TS含量均低于M区, 且S区与M区之间的TS和TN均不具显著性差异(p>0.05).
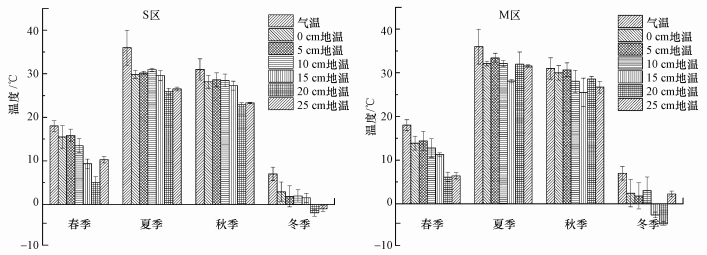 |
| 图 4 S区与M区不同季节环境温度变化 Fig. 4 Changes of environmental temperatures in different seasons between S and M regions |
| 表 1 不同观测点土壤理化性质比较 Table 1 Comparison of environmental conditions of soils at different sampling sites |
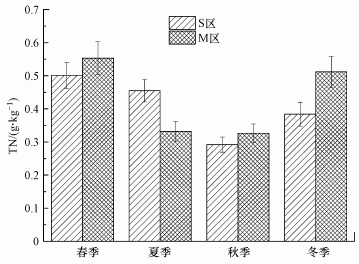 |
| 图 5 S区与M区不同季节TN变化 Fig. 5 TN changes in S and M regions in different seasons |
确定和量化CH3I源汇的平衡机制与排放规律是近年来卤代甲烷研究的主要内容之一.世界各地盐沼CH3I通量数据存在明显的差异(表 2), 尽管同属CH3I排放的排放源, 但不同地区盐沼CH3I对全球的贡献各不相同.
| 表 2 全球不同区域盐沼CH3I的通量 Table 2 Fluxes of CH3I from global salt marshes |
胶州湾盐沼的CH3I通量年均值相当于美国上纽波特湾盐沼CH3I通量的1/10, S区CH3I通量在夏季达到峰值, 与Manley等(2006)的研究结果一致.而阿拉斯加州盐沼与上纽波特湾盐沼同属加利福尼亚南部沿海沼泽, 实验时间虽相同, 所测得的CH3I通量却存在很大区别, 其原因除了不同研究地点土壤性质的差异外, 还与沼泽植物类型、水分条件的不同亦有分不开的关系.
胶州湾盐沼CH3I通量年均值与其他区域比较相对较小, 推测不同研究区CH3I的排放情况可能受区域内植被情况、光照、气温、土壤理化性质、生物量、潮汐作用及大气中甲基卤化物背景浓度等各种因素的共同影响.综合来看, 各地CH3I排放通量大小虽有很大的差异, 但各研究区均表现为CH3I通量的“源”.
4.2 影响因子分析 4.2.1 土壤理化性质对CH3I通量的影响有研究证实, 盐沼卤代甲烷释放通量的时间和空间变化与环境和生物因子有很密切的关系(Rhew et al., 2002).土壤任何理化性质的变化均可能引起微生物活动等发生改变, 从而对CH3I排放通量造成影响(宫健等, 2018).CH3I通量与土壤微生物和酶活性等密切相关, 土壤酶参与土壤生物化学过程, pH通过对微生物和酶活性起作用, 进而影响气体的排放.由CH3I通量与环境因子的相关性分析结果可以看出(表 3), M区CH3I通量与pH之间呈显著负相关(p < 0.05), 说明pH是影响M区CH3I通量重要的影响因子.这与仝川等(2010)得出的以pH=6.8为分界点, 随着pH增大, 痕量气体排放通量会减小的结论一致.
| 表 3 CH3I排放通量与环境因子的相关性分析 Table 3 Pearson correlation analysis between CH3I fluxes and environmental paraments |
土壤TN含量的变化会对痕量气体通量产生明显影响(宋长春等, 2006).在本研究中, CH3I通量与S区土壤TN含量之间呈显著负相关(p < 0.01), 这表明TN是影响S区CH3I通量变化的一个重要因素.土壤TN的分布受植被类型与土壤理化性质的共同影响(陈怀璞, 2016).TN含量的变化会直接影响互花米草的生产力和生物量, 进而影响CH3I的排放.此外, 对所测量的环境因子进行主成分分析(PCA), 通过逐步引入-剔除法得出S区CH3I通量与环境因素的回归方程为:Y=-151.267X+109.068(R2=0.133, p=0.029), 其中, Y为CH3I通量, X为TN含量.发现所选取的环境因素只有TN进入回归方程, 表明TN含量的变化对胶州湾盐沼S区中CH3I的排放具有显著影响, 这与相关性分析中得出的结果一致.
研究发现, CH3I可以在土壤沉积物中的有机质氧化过程中形成(Keppler et al., 2002).再者盐沼土壤有机质含量会直接影响到土壤微生物群落组成及生物量营养元素, 进而影响CH3I排放通量.本研究中S区土壤有机质含量较M区高, CH3I通量也比M区高, 这与王进欣(2009a)得出的有机质含量高的湿地具有更高的气体通量的结论一致.
盐度可以通过影响微生物及植物活动间接影响痕量气体通量变化(王玲玲等, 2011).在本研究中, CH3I通量与盐度之间没有相关性, 可能是由于CH3I气体排放通量的影响因素较为复杂, 某些环境因子的交互效应使得盐度的独立作用被掩盖.此外, 土壤含水率与盐度之间的相互作用会影响TN动态(Zeng et al., 2013), 而TN是影响本研究区CH3I通量的关键因子.
4.2.2 温度对CH3I通量的影响温度是使CH3I通量呈现出明显季节变化规律的重要原因, 其对制约土壤有机质分解、调节参与CH3I形成的微生物活性起着主导作用.研究表明, 温度是痕量气体排放季节变化的主要控制因子(曾从盛等, 2010).据表 3可知, S区CH3I通量与各土层地温(0~25 cm)呈显著正相关(p < 0.05).S区各季节CH3I通量与温度(气温、地温)的变化趋势大体一致(图 3、图 4), 均表现出先上升后下降的情况, 都在夏季达到峰值.S区CH3I在夏、秋季显示为排放(正值), 在冬、春季显示为吸收(负值).夏、秋季温度较高, 微生物活动增强, 大多数酶处在最适温度附近, 气体产生和排放速率相应增加; 当温度较低时, 土壤碳、氮等元素的循环过程及土壤微生物和酶的活性都不能正常发挥作用(伍星等, 2014), 这可能是造成S区CH3I通量在冬、春季比夏、秋季低的一个重要原因.温度增加会影响土壤微生物群落组成结构及养分等因素, 从而对土壤微生物生物量产生间接作用, 且土壤微生物生物量还会受到上述过程的同时作用, 从而改变湿地生态系统的物质循环(高艳娜等, 2018), 最终对CH3I排放产生影响.但温度在冬季达到最低时CH3I通量却未达到最低, 还可能是由在S区温度与其他影响因子产生交互作用引起的, 从而将温度的效应弱化, 没有完全体现出来, 这也说明温度并不是影响CH3I通量季节性变化的唯一因素.
M区的CH3I通量与季节的温度变化趋势呈现相反的规律(图 3、图 4), 夏、秋季CH3I的排放通量反而要低于冬、春季.M区CH3I在冬、春季显示为排放(正值), 在夏、秋季显示为吸收(负值), 这与S区CH3I通量的季节变化趋势相反, 说明M区与S区CH3I通量的影响因素存在较大的区别.研究表明, 在中高纬地区发生的冻融交替是影响湿地痕量气体排放的重要过程(Song et al., 2006).而胶州湾盐沼地处中纬度地区, 在冬、春季节土壤表层很容易发生冻融交替.土壤冻融循环是季节或昼夜气温变化使土温在0 ℃上下波动而出现的冻结-解冻的反复过程(郭冬楠等, 2015).其中, 冻融频次、冻融温度和土壤含水量及它们之间的交互效应都会影响土壤冻融(焦志华等, 2010).冻融过程通过影响土壤的理化性质和微生物活性, 改变土壤的生物地球化学循环过程, 从而对土壤生态系统结构和功能产生影响(伍星等, 2014).冻融作为一种非生物应力对土壤会产生直接或间接影响, 是影响土壤碳、氮生物地球化学循环的因素(郭冬楠等, 2015).M区CH3I通量在冬季达到峰值, 此时气温偏低, 且12月地温常在冰冻零界点上下波动(图 4), 冻融循环过程频繁出现, 猜想出现较高的CH3I通量可能与冻融会抑制气体消耗存在关联.
4.2.3 植物对CH3I通量的影响S区CH3I通量的季节排放规律与M区之所以大相径庭, 除了上述原因外, 还和植物作用有密不可分的关系.有研究表明, 沿海湿地植被是CH3I的重要排放源, 而没有植被的地方排放量比较低(Cox et al., 2004).S区互花米草覆盖率高达95%, 而M区无植被生长, 相比之下S区环境条件更加复杂.研究表明, 互花米草植株具有很强的气体传输机制, 自然湿地卤代烃气体排放的各个过程均受到维管植物形态的影响(段晓男等, 2005).互花米草能为土壤中已经产生的CH3I提供运输通道, 使CH3I在土壤中不经氧化而直接进入大气, 为传输气体提供了保证.研究发现(Wuosmaa et al., 1990), 卤代甲烷的产生是通过甲基转移酶酶促催化的.Saini等(2010)在碘化钾溶液中用漂浮的叶盘对118种草本植物的甲基转移酶活性进行了测试, 得出盐生植物本身会产生一定量的CH3I.推测互花米草甲基转移酶会促进CH3I产生, 从而提高S区CH3I通量.土壤中CH3I的产生还可能来自根部和与根际相关的有机体(Manley et al., 2006), 其中, 外生菌根真菌是已知的CH3I生产者, 有助于CH3I的排放(Redeker et al., 2004).所以互花米草也可以通过根系的作用来分泌有机物质到根系土壤中促进CH3I的产生.互花米草在生长过程中, 其根系为土壤提供的分泌物和死亡残体又很容易被土壤中的发酵型细菌分解生成产CH3I基质, 也可促进S区CH3I排放.相关研究发现, 卤代烃排放的季节变化与地上植物生物量相关, 卤代烃气体排放表现出强烈的季节性, 在生长季节的气体通量比非生长季节大(Rhew et al., 2000; 颜文等, 2017).本研究结果与之相似, S区的CH3I通量在非生长季(冬、春)明显比生长季(夏、秋)低, 这表明S区CH3I的排放通量会受互花米草的生长期与季节变化之间所存在的对应关系影响, S区CH3I通量在7月要明显高于12月.在互花米草生长旺盛的7月, S区表现为CH3I的强源, 无植被覆盖的M区表现为强汇; 在植物干枯且土壤间歇封冻的12月, S区表现为CH3I的汇, 而M区则表现为CH3I的源.研究表明, 处于生长季的植被具有更高的生物生产力和更大的地上生物量(王进欣等, 2009b), 与生长季相比, 冬季互花米草已经枯萎, 微生物活性降低, 通过植被进行气体传输的能力随之减弱.CH3I气体的产生基质和排放途径均受限, 因此可以推断, 互花米草在一定程度上可以促进CH3I的排放.此外, 互花米草的生理活动(如光合作用等)也会对底物质量和氧化剂数量等调控CH3I氧化的因素造成影响, 从而控制CH3I的排放(胡敏杰等, 2015).正因为互花米草对CH3I的传输过程具有若干不确定性, 所以S区CH3I通量的影响机理更为复杂.
4.2.4 潮汐作用对CH3I通量的影响胶州湾盐沼在周期性的潮汐作用下出现的干湿交替会通过改变土壤的通透性、孔隙度、团聚体结构和可溶性有机碳等理化性质, 使土壤物理聚合状态发生变化, 从而影响土壤通气情况(韩广轩, 2017).已有研究表明, 卤代甲烷最高的释放通量出现在潮汐淹没的时候(Rhew et al., 2002).由于在本次研究中并未在完整的涨落潮周期内采集气样, 故而使得S区和M区受潮汐作用的影响不够明确, CH3I通量可能会受到潮汐水位和温度等其他关键因素的综合作用, 所以潮汐仍是沿海盐沼一个不可忽略的影响因素及今后开展实验的重点研究方向.
5 结论(Conclusions)1) 胶州湾盐沼整体上是CH3I的排放源, 但排放相对较弱.S区CH3I通量大于M区, S区CH3I的年均排放通量为9.61 nmol · m-2 · d-1, 而M区CH3I的年均排放通量为6.63 nmol · m-2 · d-1.
2) 胶州湾盐沼S区与M区CH3I排放通量存在明显的季节差异, 这是由所受的主要影响机理不同造成的.其中, S区的CH3I通量在夏、秋季较高, 主要受温度、植物和TN含量等变化的影响; 而M区CH3I通量在冬、春季较高, 可能受冻融循环过程及潮汐作用的影响较大.
3) CH3I气体各月的排放情况在S区和M区之间具有明显区别, 各月通量总体呈现相反的变化趋势, 且S区与M区CH3I通量的最大值和最小值都出现在夏季7月.
陈怀璞.2016.崇明东滩湿地土壤有机碳及总氮储量研究[D].上海: 华东师范大学
|
Cox M L, Fraser P J, Sturrock G A, et al. 2004. Terrestrial sources and sinks of halomethanes near Cape Grim, Tasmania[J]. Atmospheric Environment, 38(23): 3839–3852.
DOI:10.1016/j.atmosenv.2004.03.050
|
Dimmer C H, Simmonds P G, Nickless G, et al. 2001. Biogenic fluxes of halomethanes from Irish peatland ecosystems[J]. Atmospheric Environment, 35(2): 321–330.
DOI:10.1016/S1352-2310(00)00151-5
|
段晓男, 王效科, 欧阳志云. 2005. 维管植物对自然湿地甲烷排放的影响[J]. 生态学报, 2005, 25(12): 3375–3382.
DOI:10.3321/j.issn:1000-0933.2005.12.037 |
高艳娜, 戚志伟, 仲启铖, 等. 2018. 长期模拟升温对崇明东滩湿地土壤微生物生物量的影响[J]. 生态学报, 2018, 38(2): 711–720.
|
宫健, 谢文霞, 柴娜. 2018. 胶州湾潮滩湿地CHBr3通量特征及影响因素研究[J]. 中国环境科学, 2018, 38(7): 2699–2705.
DOI:10.3969/j.issn.1000-6923.2018.07.041 |
郭冬楠, 臧淑英, 赵光影, 等. 2015. 冻融作用对小兴安岭湿地土壤溶解性有机碳和氮素矿化的影响[J]. 水土保持学报, 2015, 29(5): 260–265.
|
韩广轩. 2017. 潮汐作用和干湿交替对盐沼湿地碳交换的影响机制研究进展[J]. 生态学报, 2017, 37(24): 8170–8178.
|
胡敏杰, 仝川, 邹芳芳. 2015. 氮输入对土壤甲烷产生、氧化和传输过程的影响及其机制[J]. 草业学报, 2015, 24(6): 204–212.
|
焦志华, 黄占斌, 李勇, 等. 2010. 再生水灌溉对土壤性能和土壤微生物的影响研究[J]. 农业环境科学学报, 2010, 29(2): 319–323.
|
Keppler F, Eiden R, Niedan V, et al. 2000. Halocarbons produced by natural oxidation processes during degradation of organic matter[J]. Nature, 403(6767): 298–301.
DOI:10.1038/35002055
|
李冠霖, 何真, 杨桂朋, 等. 2017. 秋季东海挥发性卤代烃的分布和海-气通量研究[J]. 中国环境科学, 2017, 37(5): 1724–1734.
DOI:10.3969/j.issn.1000-6923.2017.05.015 |
Manley S L, Wang N, Walser M L, et al. 2006. Coastal salt marshes as global methyl halide sources from determinations of intrinsic production by marsh plants[J]. Global Biogeochemical Cycles, 20(3).
DOI:10.1029/2005GB002578
|
Redeker K R, Treseder K K, Allen M F. 2004. Ectomycorrhizal fungi:A new source of atmospheric methyl halides?[J]. Global Change Biology, 10(6): 1009–1016.
DOI:10.1111/gcb.2004.10.issue-6
|
Rhew R C, Miller B R, Weiss R F. 2000. Natural methyl bromide and methyl chloride emissions from coastal salt marshes[J]. Nature, 403(6767): 292–295.
DOI:10.1038/35002043
|
Rhew R C, Miller B R, Bill M, et al. 2002. Environmental and biological controls on methyl halide emissions from southern California coastal salt marshes[J]. Biogeochemistry (Dordrecht), 60(2): 141–161.
DOI:10.1023/A:1019812006560
|
Rhew R C, Teh Y A, Abel T. 2007. Methyl halide and methane fluxes in the northern Alaskan coastal tundra[J]. Journal of Geophysical Research Biogeosciences, 112(G2): 1169–1172.
|
Richter U, Wallace D W R. 2004. Production of methyl iodide in the tropical Atlantic Ocean[J]. Geophysical Research Letters, 31(23).
DOI:10.1029/2004gl020779
|
Fuge R. 1986. The geochemistry of iodine-a review[J]. Environmental Geochemistry and Health, 8(2): 31–54.
DOI:10.1007/BF02311063
|
Saini H S, Attieh J M, Hanson A D. 1995. Biosynthesis of halomethanes and methanethiol by higher plants via a novel methyltransferase reaction[J]. Plant Cell and Environment, 18(9): 1027–1033.
DOI:10.1111/pce.1995.18.issue-9
|
Singh H B, Salas L J, Stiles R E. 1983. Methyl halides in and over the eastern Pacific (40°N~32°S)[J]. Journal of Geophysical Research Oceans, 88(C6): 3684–3690.
DOI:10.1029/JC088iC06p03684
|
宋长春, 张丽华, 王毅勇, 等. 2006. 淡水沼泽湿地CO2、CH4和N2O排放通量年际变化及其对氮输入的响应[J]. 环境科学, 2006, 27(12): 2369–2375.
DOI:10.3321/j.issn:0250-3301.2006.12.001 |
Song C, Zhang J, Wang Y, et al. 2006. Emission of CO2, CH4 and N2O from freshwater marsh in northeast of China[J]. Atmospheric Environment, 88(3): 428–436.
|
仝川, 王维奇, 雷波, 等. 2010. 闽江河口潮汐湿地甲烷排放通量温度敏感性特征[J]. 湿地科学, 2010, 8(3): 240–248.
|
Von Glasow R, Crutzen P J. 2007. Tropospheric halogen chemistry[J]. Treatise on Geochemistry, 4: 1–67.
|
Wang J, Li R, Guo Y, et al. 2006. The flux of methyl chloride along an elevational gradient of a coastal salt marsh, Eastern China[J]. Atmospheric Environment, 40(34): 6592–6605.
DOI:10.1016/j.atmosenv.2006.05.065
|
王进. 2009. 苏北海岸带盐沼二氯甲烷和1, 2-二氯乙烷通量沿高程梯度的变化特征[J]. 生态学报, 2009, 29(8): 4026–4034.
DOI:10.3321/j.issn:1000-0933.2009.08.002 |
王进欣, 孙书存, 王今殊, 等. 2009. 苏北盐沼DMS、CS2和CH4排放通量沿高程梯度的变化[J]. 地理科学, 2009, 29(4): 535–539.
DOI:10.3969/j.issn.1000-0690.2009.04.011 |
王进欣, 王今殊, 钦佩, 等. 2012. 海岸带盐沼挥发性氯代烷烃单体成分通量的相互关系[J]. 地理科学, 2012, 32(2): 213–218.
|
王玲玲, 孙志高, 牟晓杰, 等. 2011. 黄河口滨岸潮滩湿地CO2、CH4和N2O通量特征初步研究[J]. 草业学报, 2011, 20(3): 51–61.
|
伍星, 刘慧峰, 张令能, 等. 2014. 雪被和土壤水分对典型半干旱草原土壤冻融过程中CO2和N2O排放的影响[J]. 生态学报, 2014, 34(19): 5484–5493.
|
Wuosmaa A M, Hager L P. 1990. Methyl chloride transferase:a carbocation route for biosynthesis of halometabolites[J]. Science, 249(4965): 160–162.
DOI:10.1126/science.2371563
|
谢文霞, 赵全升, 崔育倩, 等. 2015. 海岸带盐沼生态系统卤代甲烷释放研究进展[J]. 应用生态学报, 2015, 26(11): 3554–3560.
|
颜文, 王进欣, 赵赟昊, 等. 2017. 潮水作用下苏北海岸带盐沼甲烷通量时空特征研究[J]. 海洋湖沼通报, 2017(3): 7–14.
|
Youn D, Patten K O, Wuebbles D J, et al. 2010. Potential impact of iodinated replacement compounds CF3I and CH3I on atmospheric ozone:a three-dimensional modeling study[J]. Atmospheric Chemistry and Physics, 10(20): 10129–10144.
DOI:10.5194/acp-10-10129-2010
|
曾从盛, 王维奇, 张林海, 等. 2010. 闽江河口短叶茳芏潮汐湿地甲烷排放通量[J]. 应用生态学报, 2010, 21(2): 500–504.
|
Zeng W Z, Xu C, Wu J W, et al. 2013. Effect of salinity on soil respiration and nitrogen dynamics[J]. Ecological Chemistry & Engineering, 20(3): 519–530.
|
 2019, Vol. 39
2019, Vol. 39


