2. 安徽工业大学材料科学与工程学院, 马鞍山 243032
2. School of Materials Science and Engineering, Anhui University of Technology, Ma'anshan 243032
银作为一种性质优良的贵金属, 已被广泛应用于电子、医药、电镀、感光材料和化工等领域(Hui et al., 2009).但涉及到银制品相关的行业, 几乎都会产生工业含银废液, 而超标的含银废液会严重危害人类健康、恶化水质、危害水产资源及影响动植物生存等.随着银制品相关领域的高速发展, 所带来的含银工业废物也越来越多, 更进一步加剧了水体污染.因此, 开展从含银废液中高效回收银的研究, 对于解决含银废液对环境的污染和银资源的浪费问题具有重要的现实意义.
目前, 国内外治理含银废液的技术主要有沉淀法(刘芳, 2000)、电解法(Condomitti et al., 2014)、还原取代(Han et al., 2008)、离子交换(Virolainen et al., 2015)、吸附法(Lu et al., 2010)和萃取法(Celik et al., 2010)等, 以上方法在处理回收银方面均取得了较好的效果, 但依然存在选择性差、杂质离子干扰等问题.冠醚是一类含有[—O—CH2—CH2—O—]基元的环状化合物, 因其对金属离子具有优异的选择性配位能力, 近30年来, 众多的冠醚化合物被不断设计合成(Nagai et al., 2015; Zheng et al., 2016; 方秋生等, 2017).研究表明, 冠醚对金属离子的配位作用主要利用孔径效应, 即冠醚氧环形成的腔穴尺寸与金属离子直径相当时, 会以离子-偶极静电作用形成稳定配合物(韩建荣等, 2005).基于此, 本研究通过分子结构设计的方法设计了一种对银预期选择性萃取能力较强的冠醚化合物—7, 10-二硫杂苯并18-冠-6(Thia18C6), 设计理念如下:①银离子直径为0.23 nm, 冠醚中尤以18冠6(腔穴尺寸0.26~0.32 nm)的孔径大小与银离子较匹配, 符合孔径效应;②在冠醚氧环中引入硫原子, 根据软硬酸碱理论, 含硫配体为软碱, 对软酸类银离子具有强烈的配位能力, 引入硫原子可大大增强其选择性络合能力(田欢等, 2018).
本文根据Ag+的特性, 通过上述分子结构设计的方法设计了一种冠醚衍生物7, 10-二硫杂苯并-18-冠-6(Thia18C6), 并对其合成路线进行设计优化, 产物通过核磁共振氢谱(1H NMR)、X-射线衍射等技术进行结构表征, 最后采用溶剂萃取的方法考察其对银离子的选择性萃取能力.
2 7, 10-二硫杂苯并-18-冠-6的合成路线设计(Synthetic route of Thia18C6)硫杂冠醚在络合金属离子方面有着重要的应用, 但由于某些原因(如所用巯基化合物气味极臭及碱性环境下易氧化等)导致合成难、产率极低等问题, 因此, 目前对硫杂冠醚的研究深度和广度都不及相应的氧杂、氮杂冠醚.常见的硫杂18冠6合成方法是在碱性条件下, 二卤化物与硫化钠或巯基化合物缩合成环, 但其产率普遍很低.Pedersen等(1971)报道的硫杂18冠6产率还不到1%;在Dann等(1961)的研究中, 采用1, 2-二(2-氯乙氧基)乙烷和硫化钠反应88 h合成1, 10-二硫杂-18-冠-6, 产率也仅有22.6%;Oue等(1985)采用苯环带硝基的二氯化物与巯基化合物反应合成硫杂冠醚, 产率有所提升;陈立钦等(1990)在NaOH-叔丁醇-二氧六环体系中合成了苯并硫杂冠醚, 产率突破40%.近年来, 有研究人员提出利用铸型剂的模板效应(Template effect)来提高冠醚产率, 由此掀起了一股研究热潮.常见的铸型模板为碱金属和碱土金属化合物, 其离子直径大小与相应的冠醚环穴尺寸相当, 在闭环过程中, 由于铸型离子的正电荷与氧环上未用电子对之间存在较强的相互作用力, 从而促进了环化反应的顺利进行(秦圣英等, 1981).由此可认为, 采用钾离子作铸型(模板)来提高Thia18C6的产率是有可能的.主要原因在于:Li+(0.12 nm)、Na+(0.19 nm)、K+(0.266 nm)和Cs+(0.34 nm)中尤以K+与18冠6(0.26~0.32 nm)的尺寸最为匹配.结果表明, 经亲核取代、酰氯酰化、环化反应合成Thia18C6, 路线更为简短, 单步冠醚产率更高, 环化反应采用邻苯二酚为原料, K2CO3为铸型剂, 在水-乙醇-甲苯体系中反应合成Thia18C6, 化学物合成路线如图 1所示.
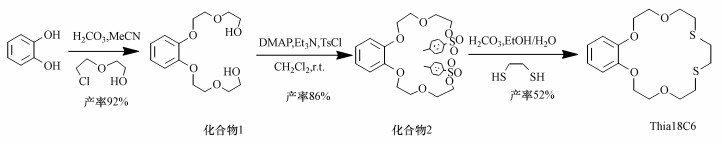 |
| 图 1 Thia18C6的合成路线图 Fig. 1 Synthetic route of Thia18C6 |
试剂:邻苯二酚、碳酸钾、乙腈(MeCN)、对甲苯磺酰氯(TsCl)、1, 2-乙二硫醇、三乙胺、浓盐酸、4-二甲氨基嘧啶、甲苯、二氯甲烷(CH2Cl2)、N, N-二甲基甲酰胺(DMF)、乙酸乙酯、石油醚、氘代氯仿(CDCl3)、4-二甲氨基吡啶(DMAP)、无水乙醇均购自上海泰坦科技股份有限公司, 为Adamas-beta品牌的分析纯试剂, 必要时均经干燥和纯化处理.
仪器:Bruker-AVANCE400(400 MHz)核磁共振仪、SMART APEXⅡX-射线单晶衍射仪, 购自瑞士Bruker公司;CL4A磁力加热搅拌器、SHZ-D(III)循环水式真空泵, 购自巩义市予华仪器有限责任公司;RE52-2旋转蒸发仪、WFH-204B手提式紫外分析仪, 购自上海泰坦科技股份有限公司.
3.2 合成步骤 3.2.1 1, 2 -双(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)苯(化合物1)的合成取干燥的500 mL三口圆底烧瓶, 将10.3 g邻苯二酚(0.093 mol)和40.4 g碳酸钾(0.29 mol)加入到400 mL无水乙腈溶液中, 加热回流45 min后加入5.2 g KI(0.031 mol), 将反应混合物加热回流10 min, 使用滴液漏斗在2 h内滴加入34.87 g 2-氯乙氧基乙醇(0.28 mol), 将反应混合物在回流下搅拌19 h.待反应结束冷却至室温, 将反应混合物过滤并真空浓缩.将所得残余物溶于250 mL二氯甲烷中, 经HCl水溶液洗涤后用MgSO4干燥, 以展开剂V(二氯甲烷):V(甲醇)=20:1洗脱, 旋干得到橙黄色化合物1, 产率为92%(图 1).
3.2.2 1, 2-双(2-(2-(2-对甲苯磺酰氧基)乙氧基)乙氧基)苯(化合物2)的合成将10 g化合物1(35 mmol)、0.793 g DMAP(7 mmol)和60 mL Et3N溶于120 mL CH2Cl2中并冷却至0 ℃.含33.37 g TsCl(175 mmol)的250 mL CH2Cl2溶液在3 h内滴加到冷却的反应混合物中, 使反应混合物达到室温并搅拌19 h.待反应冷却至室温, 将反应混合物过滤并真空浓缩, 倒入4 mol·L-1 HCl水溶液中.有机相用1 mol·L-1 HCl水溶液洗涤, 无水Na2SO4干燥.蒸发溶剂后, 用展开剂V(二氯甲烷):V(甲醇)=30:1洗脱, 旋干得到化合物2, 为黄色油状物, 产率为86%(图 1).
3.2.3 7, 10-二硫杂苯并-18-冠-6的合成取干燥的500 mL三口圆底烧瓶, 将1.58 g 1, 2-乙二硫醇(16.8 mmol)加入到10 mL乙醇和75 mL甲苯的混合溶液中, 再将此溶液缓慢滴入混有90 mL乙醇、80 mL水和10 g化合物2(16.8 mmol)的沸腾Na2CO3(88.98 g, 0.89 mol)混合液中, 待反应结束, 冷却至室温, 用二氯甲烷和水多次萃取, 取有机相用无水硫酸钠干燥后旋蒸, 以展开剂V(石油醚):V(乙酸乙酯)=5:1洗脱, 得到Thia18C6, 产率为52%.
3.3 合成产物表征 3.3.1 核磁共振取色柱法纯化后的产物约8 mg溶于适量CDCl3中, 振荡使其完全溶解.中间产物数据均采用Bruker-AVANCE400(400 MHz)核磁共振仪检测而得.
3.3.2 X-射线单晶衍射将合成的高纯度白色针状固体7, 10-二硫杂苯并-18-冠-6(0.5 g)溶于15 mL的CH2Cl2溶液中, 并用滴管在该溶液表面铺一层正己烷, 将带有一个小孔的保鲜膜密封住, 约5~7 d后, 长出针状透明的晶体, 取适量晶体用于X-射线单晶衍射.X-射线单晶衍射采用SMART APEXⅡX-射线单晶衍射仪.
3.4 络合常数测定称取12.5 mg硝酸银配制成250 mL的溶液备用, 分别称取不同质量的Thia18C6溶于50 mL CH2Cl2中, 配制成不同浓度的冠醚有机相, 取25 mL水相和50 mL有机相振荡10 min, 静置一段时间后取水相经电感耦合等离子发射光谱仪(ICP)检测, 由式(1)和式(2)计算络合常数(Roper et al., 2008).
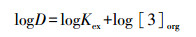
|
(1) |

|
(2) |
式中, Kex表示稳定常数, 下标org表示有机相, aq表示水相, [3]org表示有机相中Thia18C6的浓度, [Ag+3NO3-]org表示在有机相中Thia18C6与Ag+形成的配合物浓度.
3.5 萃取实验分别配制含0.5 g·L-1 Ag+的硝酸盐溶液及Cu2+、Pb2+、Zn2+、Ni2+、Ag+均为0.5 g·L-1的硝酸盐混合溶液备用, 再称取与Ag+等物质的量的Thia18C6溶于CH2Cl2中制成萃取有机相.取一定量有机相与50 mL AgNO3溶液或其它硝酸盐溶液一同加入到分液漏斗, 在25 ℃下振荡15 min, 然后静置30 min, 分相后取水相中样品采用ICP法测定金属离子浓度.由式(3)计算萃取率E(李洲等, 2008).
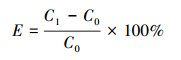
|
(3) |
式中, C0为初始水相中离子浓度, C1萃取时间t后水相中的离子浓度.
4 结果与讨论(Results and discussion) 4.1 核磁H谱产物在氘代氯仿(CDCl3)中溶解后经核磁H谱表征, 结果如图 2所示.由图 2可知, 化合物中H的数量及化学位移均与目标产物一致并且产物纯度均较高.
 |
| 图 2 中间体1(a)、中间体2(b)及Thia18C6(c)的核磁H谱(CDCl3, 400 MHz) Fig. 2 1H HMR spectrum of compound 1(a), compound 2(b), and Thia18C6(c) (CDCl3, 400 MHz) |
由图 3的晶体结构及表 1的单晶数据可知, 7, 10-二硫杂苯并-18-冠-6的分子式为C16H24O4S2, 分子量为344.47, 所得的结构为大环分子, 以一个苯环为一端, 另一端为醚与硫醚连成的一个大环, 且该大环分子的构象不在同一平面内, 冠醚环中的氧原子及硫原子平面性较差, C—S—C、C—O—C及O—C—C、S—C—C呈锯齿状, 在该结构中键角数据分别为:C(29)—S(1)—C(28)为100.02°, C(30)—C(29)—S(1)为113.9°, C(26)—S(2)—C(33)为102.1°, C(25)—C(26)—S(2)为115.1°, O(6)—C(21)—C(20)为124.4°, O(6)—C(21)—C(22)为115.9°, O(5)—C(22)—C(17)为125.1°, O(5)—C(22)—C(21)为115.3°, 可知合成的冠醚环不在同一个平面内.硫原子和氧原子共同构成高电子云密度环境并提供未共用电子对, 使金属阳离子与冠醚环中带孤对电子的负电性原子键合, 并通过离子-偶极相互静电作用发生配位反应, 为生成稳定的络合物提供了可能, 这也就很好地说明冠醚与碱金属或碱土金属离子能够络合的部分原因.
 |
| 图 3 Thia18C6的单晶结构 Fig. 3 Single crystal figure of Thia18C6 |
| 表 1 Thia18C6的单晶结构数据 Table 1 The crystal structure parameter of Thia18C6 |
由图 4可知, 该冠醚氧环中相对原子间距分别为:O(7)—O(8)为0.570 nm, S(1)—O(6)为0.586 nm, S(2)—O(5)为0.728 nm, 而腔体大小是两个相对供体原子间最小距离(Zhang et al., 2011), 因此, 该冠醚实际腔穴尺寸为0.570 nm.
 |
| 图 4 Thia18C6的腔穴尺寸测定 Fig. 4 The cavity diameters calculation of Thia18C6 |
不同浓度的Thia18C6对银离子的萃取能力及logD和log[3]org的线型关系如图 7所示, 通过ICP检测确定水相中金属离子浓度, 经线性拟合计算出冠醚对Ag+的lgKex为22.177.
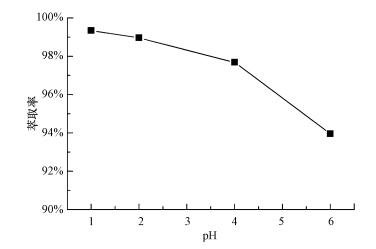 |
| 图 7 萃取率随pH的变化 Fig. 7 Influence of pH on extraction rate |
在溶剂萃取实验中, 水相中的金属离子被硫杂冠醚萃取至有机相中.金属离子选取工业废水中常见的Ag+、Cu2+、Pb2+、Zn2+、Ni2+, 分别考察了pH、温度、单一及多元体系下, Thia18C6对金属离子的萃取能力.
4.4.1 温度对萃取效果的影响萃取过程中, 控制时间为30 min, 有机相为CH2Cl2, V(二氯甲烷):V(水相)=2:1, pH=3~4, 由图 5可知, 随温度的升高, 冠醚的萃取率呈下降趋势, 但仍在90%以上.说明温度对萃取效果的影响总体不大, 但低温时更有利于Thia18C6萃取过程.张志远等(2017)研究报道的冠醚络合金属离子过程为放热反应, 因此, 升温不利于萃取, 本研究结果与之较为一致.
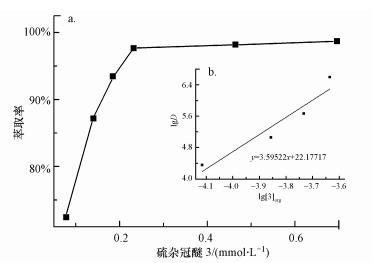 |
| 图 5 不同浓度Thia18C6对水相中银离子(0.05 g·L-1)的萃取率(a)及lgD-lg[3]org关系图(b) Fig. 5 Extraction of Ag+ from 0.05 g·L-1 aqueous solutions into choroform by Thia18C6 (a.Change in the percent extraction of Ag+ with varying concentrations of the ligand in the organic phase, b.the plot of logD vs log[3]org) |
实验设置时间为30 min, V(二氯甲烷):V(水相)=2:1, 温度为25 ℃, 由图 6可知, Thia18C6对银的萃取率随pH的增大而呈现下降的趋势.在pH为5之前, 随着pH的增大, 萃取效率慢慢降低, 当pH大于5时, 萃取率急剧下降, 可能是AgNO3水溶液发生水解平衡所致.
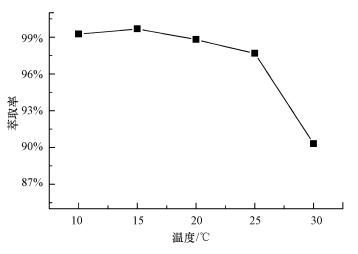 |
| 图 6 萃取率随温度的变化 Fig. 6 Influence of temperature on extraction rate |
由表 2可知, 在单一体系中, Thia18C6对银离子表现出极高的萃取能力, 萃取率高达97.68%.这主要是由于冠醚氧环中处于邻位的两硫原子产生协同效应, 以致对金属离子的亲和力大大增强, 软硬酸碱理论起主导作用, 硫原子为软碱, 对软酸类银离子产生强烈的配位能力, 因此, 在单一体系中对银离子表现出高的萃取能力;而在多元体系中, Thia18C6对银离子的萃取率略有下降, 选择性萃取率只有70.15%, 但也远高于其他杂质离子, 与田欢等(2018)研究中采用4, 13-二硫杂苯并18冠6(DSB18C6)萃取银离子的结果相比, DSB18C6在多元体系中对银的选择性优于Thia18C6, 其选择性萃取率可达93.4%.导致这一现象的原因可能为:两硫原子处于对位的冠醚(DSB18C6)更符合分子结构预期设计理念, 萃取过程中孔径效应和软硬酸碱理论起协同作用, 对银离子表现出较高的选择性萃取能力;而两硫原子处于邻位的冠醚(Thia18C6), 其空腔尺寸有所增大, 虽不影响银离子的进入, 但孔径效应作用略有减弱, 因此, 在复杂体系中对银的萃取率略低于DSB18C6.
| 表 2 Thia18C6对金属离子萃取率 Table 2 The extractability of Thia18C6 towards various ions |
本文基于硫杂冠醚对金属离子的选择性络合能力, 设计合成了一种全新结构硫杂冠醚—7, 10-二硫杂苯并-18-冠-6(Thia18C6), 单步冠醚产率高达52%.采用核磁共振氢谱(1H NMR)及X-射线衍射单晶对其进行了结构表征, 并测定了其实际腔穴尺寸, 进而采用溶剂萃取的方法计算了对银离子的络合常数, 系统考察了温度、pH对萃银率的影响, 以及对部分软酸及交界酸离子的选择性萃取性能.结果表明, 设计合成的Thia18C6对Ag+表现出了较强的萃取能力, 萃取率高达97.68%, 同时在复杂体系中对Ag+也表现出了较高的选择性.
陈立钦, 汪玉庭. 1990. 硫杂冠醚的合成[J]. 有机化学, 1990, 10(6): 546–549.
|
Celik Z, Gülfen M, Aydin A O. 2010. Synthesis of a novel dithiooxamide-formaldehyde resin and its application to the adsorption and separation of silver ions[J]. Journal of Hazardous Materials, 174(1/3): 556–562.
|
Condomitti U, Silveira A T, Condomitti G W, et al. 2014. Silver recovery using electrochemically active magnetite coated carbon particles[J]. Hydrometallurgy, 147(8): 241–245.
|
Dann J R, Chiesa P P, Jr J W G. 1961. Sulfur-containing large-ring compounds.The preparation of 4, 7, 13, 16-Tetraoxa-1, 10-dithiacyclooctadecane and related compounds[J]. Journal of Organic Chemistry, 26(6): 1991–1995.
DOI:10.1021/jo01065a075
|
方秋生, 李艳红, 陈岭. 2017. 新型蒽并冠醚的合成及主客体键合行为[J]. 高等学校化学学报, 2017, 38(9): 1563–1567.
|
韩建荣, 张衡益, 刘育. 2005. 双臂式苯并-15-冠-5的合成及其对金属离子的选择键合[J]. 高等学校化学学报, 2005, 26(7): 1273–1276.
DOI:10.3321/j.issn:0251-0790.2005.07.016 |
Han Z, Wei J, Zhao M, et al. 2008. A method to recover silver from waste X-ray films with spent fixing bath[J]. Hydrometallurgy, 92(3/4): 148–151.
|
Hui M A, Yang T, Liu W, et al. 2009. Study on reduction of silver with sodium sulfite from silver-containing liquid waste[J]. Precious Metals, 30(1): 6–10.
|
刘芳. 2000. 废液中银的回收[J]. 安阳师范学院学报, 2000(4): 38–39.
|
李洲, 朱屯. 2008. 溶剂萃取(现代分离科学与技术丛书)[M]. 北京: 化学工业出版社: 5–160.
|
Lu X, Yin Q, Xin Z, et al. 2010. Powerful adsorption of silver(I) onto thiol-functionalized polysilsesquioxane microspheres[J]. Chemical Engineering Science, 65(24): 6471–6477.
DOI:10.1016/j.ces.2010.10.001
|
Nagai H, Suzaki Y, Osakada K. 2015. Thiacrown ethers with oxygen and sulfur for coordination:formation of the Pd and Pt complexes and pseudorotaxane with dialkylammonium[J]. European Journal of Inorganic Chemistry, 2014(26): 4376–4384.
|
Oue M, Ishigaki A, Kimura K, et al. 1985. Synthesis and cation-binding properties of poly-and bis(thiacrown ether)s[J]. Journal of Polymer Science Polymer Chemistry Edition, 23(7): 2033–2042.
DOI:10.1002/pol.1985.170230718
|
Pedersen C J. 1971. Crystalline complexes of macrocyclic polyethers with thiourea and related compounds[J]. Journal of Organic Chemistry, 36(12): 254–257.
|
秦圣英, 金荣久, 刘义远. 1981. 苯并-12-冠-4与二苯并-24-冠-8的"铸型"(模板)合成[J]. .化学试剂, 1981(5): 31–33.
|
Roper E D, Talanov V S, Butcher R J. 2008. Selective recognition of thallium (I) by calix[4]arene-bis (crown-6 Ether):A new talent of the known ionophore[J]. Supramolecular Chemistry, 20(1/2): 217–229.
|
田欢, 张梦龙, 王莉莎, 等. 2018. 4, 13-二硫杂苯并-18-冠-6的合成及对Ag+的选择性萃取[J]. 高等学校化学学报, 2018, 39(6): 1191–1196.
|
Virolainen S, Tyster M, Haapalainen M, et al. 2015. Ion exchange recovery of silver from concentrated base metal-chloride solutions[J]. Hydrometallurgy, 152: 100–106.
DOI:10.1016/j.hydromet.2014.12.011
|
张志远, 陈鸿伟, 于海龙, 等. 2017. 冠醚对准东煤水洗液中碱-碱土金属离子萃取动力学[J]. 煤炭学报, 2017, 42(3): 768–774.
|
Zhang S, Lu W, Liu X, et al. 2011. Fast and effective identification of the bioactive compounds and their targets from medicinal plants via computational chemical biology approach[J]. Med Chem Commun, 2(6): 471–477.
DOI:10.1039/c0md00245c
|
Zheng T X, Yide N N. 2016. A cobalt supramolecular compound constructed from 4, 6-Di(1-imidazolyl)-1, 3, 5-triazine-2-one:Synthesis, characterization and magnetic property[J]. Chemical Research in Chinese Universities, 32(2): 184–187.
DOI:10.1007/s40242-016-5456-4
|
 2019, Vol. 39
2019, Vol. 39


