2. 环境水质学国家重点实验室, 中国科学院生态环境研究中心, 北京 100085;
3. 中国科学院大学, 北京 100049;
4. 膜材料与膜应用国家重点实验室, 天津膜天膜科技股份有限公司, 天津 300457
2. State key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085;
3. University of Chinese Academy of Sciences, Beijing 100049;
4. State Key Laboratory of Membrane Materials and Membrane Applications, Tianjin Motimo Membrane Technology Co., Ltd., Tianjin 300457
近年来, 炼油、冶钢采矿、煤化工、印染、焦化(杜永家, 1993; Namasivayam et al., 2007; Kononova et al., 2007)等行业快速发展, 产生了大量的高浓度含硫工业废水, 水体污染情况恶化, 含硫污染废水的治理是废水处理行业面临的又一挑战.硫代硫酸盐(S2O32-)作为主要的含硫阴离子, 可引起水体富营养化(叶正平等, 2011), 对生态环境产生重要危害.如在焦化脱硫废水中, S2O32-含量可高达100 g·L-1 (Stott et al., 2001), 而工业废水硫化物最高允许排放标准为1 mg·L-1.目前常见的硫代硫酸盐的处理方法有:沉淀法、碱性吸收法(杜永家, 1993)、氧化法(洪冰等, 2004)和吸附法(杨国华等, 2009; 匡晔, 2011).沉淀法操作简单, 条件温和, 但处理效果不佳, 且产生大量污泥; 碱性吸收法可适用于浓度高的废液, 但去除率低, 产生二次污染; 氧化法无二次污染, 但对设备要求高, 成本大; 吸附法操作简单, 效果显著, 但传统吸附剂以粉体为主, 选择性差、难以回收.
电容去离子技术(也称电吸附, 简写CDI), 是利用静电作用力使水中的荷电离子向具有相反电性电极方向移动, 在电极表面形成电层, 使离子吸附富集在电极表面, 达到脱盐目的.通过断路或电位反接就能使被吸附的离子脱附下来, 同时电极材料得以再生(García-Quismondo et al., 2013).CDI具有能耗低、无二次污染、操作及维护简单等优点, 成为水处理研究和应用的热点.CDI的核心是电极材料, 要求具有较大的比表面积和稳定的电化学性能.目前国内外研究较多的CDI电极材料是多孔炭材料, 如活性炭纤维、碳纳米管、炭气凝胶、石墨烯等(Kim et al., 2012; 李娜等, 2013).层状双金属氢氧化物(又称类水滑石, 简写LDHs)具有大的比表面积、良好的化学稳定性和高的比电容, 成为一种极具应用潜力的CDI电极材料(Yan et al., 2013; Lin et al., 2014).LDHs的化学组成式为[M1-x2+M3+x(OH)2]x+(An-)x/n·mH2O, 其中, M2+、M3+代表金属阳离子; An-代表层间阴离子; x代表三价阳离子占所有阳离子的摩尔比; m代表层间的水分子数(Wu et al., 2013; Lu et al., 2015).将LDHs在一定温度下煅烧, 可形成稳定的层状复合金属氧化物(LMO), LMO与客体阴离子反应, 可恢复成有序层状结构的LDHs, 此现象称为水滑石的“结构记忆”效应, 这也是LMO可用于吸附去除阴离子的重要原因(姚铭等, 2005; Mascolo et al., 2015).
本研究采用共沉淀法, 在泡沫镍基体上合成了NiAl-LDHs, 并将其煅烧后成功转化为NiAl-LMO电极, 此方法与溶胶凝胶法制备过程相比, 操作步骤更为简便.通过SEM、XRD、FT-IR对NiAl-LDHs、NiAl-LMO电极进行基本表征, 并利用电化学工作站对NiAl-LMO电极进行电化学性能测试, 最后探究了NiAl-LMO电极电吸附去除S2O32-的性能和最佳吸附条件, 并对吸附曲线进行吸附动力学模型拟合.
2 材料与方法(Materials and methods) 2.1 实验材料和仪器材料:泡沫镍(纯度大于99%); 碳纸; 盐酸(HCl)、无水乙醇(CH3CH2OH)、六水合氯化镍(NiCl2·6H2O)、六水合氯化铝(AlCl3·6H2O)、碳酸钠(Na2CO3)、氢氧化钠(NaOH)等均为分析纯(AR), 购于国药集团化学试剂有限公司.
仪器:扫描电子显微镜(SEM)(SU8020, 日立公司), X射线粉末衍射(XRD)仪(X′Pert pro, 北京明卓仪器有限公司), 傅里叶红外光谱(FT-IR)仪(TENSON27, BRUKER Germany), 电化学工作站(CHI660, 上海辰华仪器公司), 离子色谱(IC)仪(ICS-2000, Thermo U.S.A).
2.2 电极的制备方法取厚为1 mm的泡沫镍剪切成2 cm×3 cm的片, 随后用1%的稀盐酸超声清洗5 min, 然后用去离子水超声清洗3次, 每次5 min, 再用无水乙醇清洗5 min, 最后放入60 ℃的烘箱中烘2 h备用.
将28.52 g六水合氯化镍、9.65 g六水合氯化铝溶于100 mL去离子水中, 记为a溶液; 将12.8 g NaOH和8.48 g Na2CO3溶于100 mL去离子水中, 记为b溶液.在60 ℃强烈搅拌下, 将b溶液逐滴滴入a溶液, pH调至9.5~10.5, 将混合液转入100 mL高压反应釜中, 放入处理好的泡沫镍, 在100 ℃鼓风干燥箱干燥10 h, 待反应釜冷却至室温, 取出泡沫镍样品, 用去离子水反复冲洗, 干燥, 即获得了NiAl-LDHs.将制备好的NiAl-LDHs电极置于马弗炉中, 500 ℃下煅烧4 h, 得到最终产物NiAl-LMO电极.
2.3 电吸附除盐实验(1) 以3 cm×2 cm的NiAl-LMO电极做正极, 面积相同的碳纸做负极, 并联两组放入盛有100 mL浓度为1 mmol·L-1的Na2S2O3的反应器中, 打开直流电源, 于电压1.0 V、pH为7的条件下, 电吸附90 min, 电吸附达到平衡, 分别在0、5、10、20、40、60、90 min各取样1 mL; 再将电极反接, 电脱附60 min, 分别在0、10、20、40、60 min各取样1 mL, 稀释后用IC测S2O32-含量.
离子的去除率、脱附率计算公式分别为:
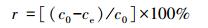
|
(1) |
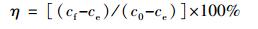
|
(2) |
式中, c0、ce、cf分别为离子的初始浓度、吸附平衡浓度、脱附平衡浓度(mmol·L-1); r为离子的去除率; η为脱附率.
(2) 对吸附结果进行吸附动力学模型拟合, 吸附动力学是用于研究电吸附过程和时间关系的曲线.准一级模型基于假定吸附受扩散步骤控制, 吸附速率和平衡吸附量与t时吸附量的差值成正比, 公式为:
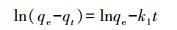
|
(3) |
准二级模型基于假定吸附速率受化学吸附机理控制, 这种化学吸附涉及到吸附剂与吸附质之间的电子公用和电子转移, 公式为:
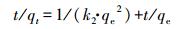
|
(4) |
式中, qe和qt分别是平衡吸附量(mg·g-1)和t时间吸附量(mg·g-1), k1是准一级吸附速率常数(min-1), k2是准二级吸附速率常数(g·mg-1·min-1) (Kim et al., 2012; 蔡苏彦等, 2012).
2.4 表征方法采用SEM对电极的形貌结构进行分析; 采用电感耦合等离子体扫描仪(ICP-OES)分析样品组成元素含量及比例; 采用XRD(铜靶, Kα射线, λ = 0.15406 nm, 管电压为40 kV, 扫描速率是5 °·min-1, 扫描范围为10°~90°)表征NiAl-LDHs, 以及其煅烧后的NiAl-LMO的晶相结构; 将1 mg从NiAl-LDHs上刮下来的粉末样品及其煅烧后的NiAl-LMO粉末样品分别与100 mg的KBr粉末充分混合后压片, 采用FT-IR在400~4000 cm-1波数范围进行定性分析; 配制1 mol·L-1的KOH溶液100 mL, 以NiAl-LMO电极为工作电极, Pt为标准电极, 饱和甘汞电极为参比电极, 用电化学工作站进行循环伏安和恒电流充放电性能测试; 采用IC测量电吸附过程中的离子浓度变化情况.
3 结果与讨论(Results and discussion) 3.1 NiAl-LMO电极的形貌结构图 1为泡沫镍、NiAl-LDHs、NiAl-LMO电极的扫描电子显微镜(SEM)图片.图 1a为空白泡沫镍基体, 表面为光滑网孔状结构; 图 1b为NiAl-LDHs电极, 可清晰看出非常规则的片状六边形结构LDHs; 图 1c为煅烧后的NiAl-LMO电极, 通过对比可以看出和煅烧前的NiAl-LDHs结构相比无明显变化, 是由于水滑石脱出层间阴离子的反应主要在层板间进行(Chen et al., 2015).为了确定镍铝的含量比, 从NiAl-LDHs上刮下少许粉末溶于王水中, 利用ICP-OES测定镍铝的含量比为2.8:1, 根据LDHs晶体的金属离子摩尔比的限定原则, 含量比在2~4时才有纯的LDHs晶体形成(Wan et al., 2011), 与前人实验结果相一致(王婷等, 2016).
 |
| 图 1 泡沫镍(a)、NiAl-LDHs(b)、NiAl-LMO(c)电极的SEM图 Fig. 1 SEM image of nickel foam, NiAl-LDHs films electrode and NiAl-LMO films electrode |
图 2a为泡沫镍、NiAl-LDHs、NiAl-LMO电极的XRD图谱, 扫描范围为10°~90°.图 2a中Ni的XRD图谱显示, 在45.1°、52.5°、77.1°处出现了泡沫镍单质的特征衍射峰(110)、(200)、(220);NiAl-LDHs的XRD图谱显示, 在11.2°、22.4°、33.6°处出现了LDHs的特征衍射峰(003)、(006)、(012), 说明在泡沫镍基底上成功合成了LDHs; NiAl-LMO的XRD图谱显示, LDHs的特征衍射峰消失, 在63.09°出现了NiAl-LMO的特征衍射峰(220), 在56.9°、76.0°处出现了氧化铝的特征衍射峰(422)、(620), 由此可推测出, 经煅烧后, NiAl-LDHs成功转化为NiAl-LMO.
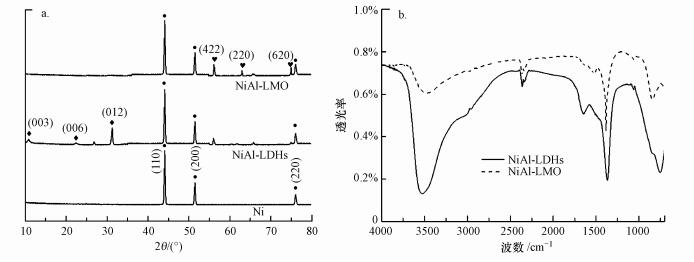 |
| 图 2 泡沫镍、NiAl-LDHs及NiAl-LMO的XRD图谱(a)及NiAl-LDHs及NiAl-LMO的FT-IR图谱(b) Fig. 2 XRD patterns of nickel foam, NiAl-LDHs and NiAl-MMO(a) and FT-IR spectra of NiAl-LDHs and NiAl-LMO(b) |
图 2b显示, NiAl-LDHs的红外光谱在3500 cm-1附近出现明显吸收峰, 峰型较宽, 是由于LDHs层间水分子与层板上羟基伸缩振动而产生; 1350 cm-1附近处有明显的特征吸收峰, 是由于阴离子碳酸根的(C=O)伸缩振动引起, 且750 cm-1附近处出现碳酸根的弯曲振动吸收峰, 说明NiAl-LDHs层间插层阴离子为CO32-(王婷等, 2016).经煅烧后, NiAl-LMO的红外光谱在3500 cm-1附近的吸收峰明显减弱, 1350 cm-1和750 cm-1附近处由碳酸根离子而产生的振动峰均明显减弱, 说明经煅烧层间的阴离子和层板的羟基大部分已经脱出(王秀娟等, 2012), NiAl-LDHs成功转化为NiAl-LMO.
3.2 NiAl-LMO电极电化学性能图 3a为NiAl-LMO电极在不同扫描速率下的循环伏安测试曲线, 扫描电压范围为0~0.45 V, 扫描速率分别为1、5、10、50 mV·s-1.图中可看出明显的氧化还原峰, 这证明了法拉第电容的存在.图中的氧化还原峰是由于Ni(Ⅱ)/(Ⅲ)氧化还原反应引起的, 反应如下:Ni(OH)2+OH-=NiOOH+H2O+e-, 即Ni(Ⅱ)和Ni(Ⅲ)的价态相互转化的过程(Lu et al., 2015).氧化峰和还原峰峰电位的差值可用来表征电极材料的可逆性, 差值越小, 可逆性越好.由图可看出, 氧化峰峰电位为0.355 V, 还原峰峰电位为-0.256 V, 电位差值为0.099 V, 和ΔEP较接近, 因此此电极可逆性良好.
 |
| 图 3 NiAl-LMO电极循环伏安曲线(a)及NiAl-LMO电极恒电流充放电曲线(b) Fig. 3 CV curves of NiAl-LMO films electrode(a) and Galvanostatic charge-discharge curves of NiAl-LMO films electrode(b) |
图 3b为NiAl-LMO电极在不同电流密度下进行的恒电流充放电测试曲线, 充放电电压范围为0~0.3 V, 电流密度分别为0.5、1.0、2.0、3.0 A·g-1.由充放电曲线可计算出电极材料的比电容值.相关研究表明法拉第电容值远远大于LDHs双电层电容值(王婷等, 2016).
比电容计算公式为:
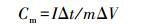
|
(5) |
式中, Cm表示电容, I表示充放电电流, Δt代表充放电时间, m代表活性组分的量(Wei et al., 2014), ΔV代表电压.
比电容计算结果见图 4.结合图 3b和图 4可以看出, 随着电流密度的增大, 充放电时间逐渐减小, 这是因为电解液在较高的电流密度下, 不能够与电极充分的润湿, 从而减少了参与氧化还原反应的活性位点(王婷等, 2016).NiAl-LMO电极比电容可达577 F·g-1, 高于已报道的活性炭(360 F·g-1)和活性炭纤维(425 F·g-1).
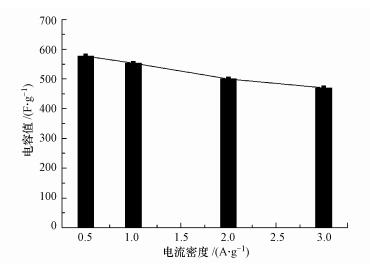 |
| 图 4 不同电流密度下的电容值 Fig. 4 Capacitance values at different current densities |
图 5为NiAl-LMO电极在1 mmol·L-1的Na2S2O3溶液中进行的电吸附-脱附的实验结果.由图可清晰看出, 在电吸附初始阶段, 吸附速率较快, 20 min时, 去除率为37.7%, 60 min时, 去除率为54.2%, 90 min时基本达到吸附平衡, 此时S2O32-的去除率为60.9%.将正负电极反接, 进入电脱附过程, 脱附进行到60 min左右, S2O32-浓度基本不再明显变化, 达到电脱附平衡状态, S2O32-脱附率达84.9%.NiAl-LMO电极对于S2O32-具有良好的电吸附去除能力, 通过施加反向电位被吸附的S2O32-可以迅速释放, 电极材料本身得到再生.
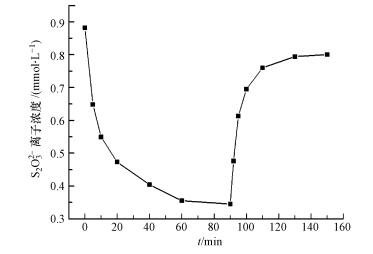 |
| 图 5 NiAl-LMO电极的电吸附/脱附曲线 Fig. 5 Electrosorption and desorption equilibrium curve of the NiAl-LMO films electrode |
图 6a显示, 在未施加电压时, NiAl-LMO电极对S2O32-吸附去除率达25.7%, 因为NiAl-LMO自身是一种阴离子插层的吸附材料, 对阴离子具有一定的吸附效果; 随着电压的增加, 离子去除效果明显提高, 电压为1.0 V时, 达到最大的吸附率60.9%;当电压继续增加到1.2 V时, 吸附效果并没有提高, 可能是由于电压的增大导致了水的电解, 降低了电流效率.NiAl-LMO电极电吸附去除S2O32-的最佳工作电压为1.0 V.
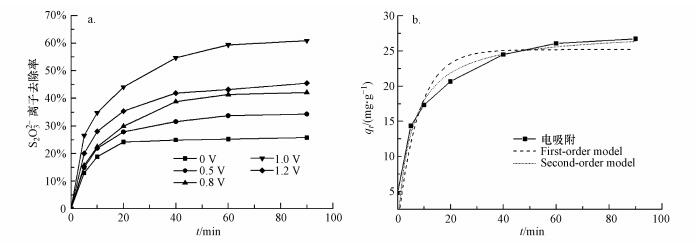 |
| 图 6 不同电压下NiAl-LMO电极电吸附S2O32-(a)及NiAl-LMO电极对S2O32-的吸附动力学拟合(b) Fig. 6 Effect of different voltage conditions on electrosorption of S2O32- on NiAl-LMO electrode(a) andAdsorption Kinetics fitting of S2O32- on NiAl-LMO electrode(b) |
图 6b为电压为1.0 V下, 电吸附S2O32-曲线的吸附动力学模型拟合结果.
结合图 6b和表 1可知, 一级动力学可决系数大于二级动力学可决系数, 平衡吸附量为25.57 mg·g-1, 所以此电吸附过程倾向于物理吸附.
| 表 1 吸附动力学参数 Table 1 Adsorption kinetic parameters |
图 7a为NiAl-LMO电极在不同pH环境进行的电吸附实验结果.由图可看出, 在pH为中性(pH= 7)时, 电极对S2O32-的吸附率最高, pH=5时次之, pH为9时最低.当水溶液呈酸性(pH=5)时, 溶液中氢离子浓度相对较高, 而LDHs结构本身呈碱性, 在酸性条件下容易使双羟基结构遭到破坏, 从而降低吸附效率(刘晓华, 2016); 而当溶液呈碱性(pH=9)时, 溶液中氢氧根离子浓度相对较高, 与S2O32-产生竞争吸附, 导致电极对S2O32-的吸附效率降低.NiAl-LMO电极电吸附去除S2O32-的最佳吸附pH为7.
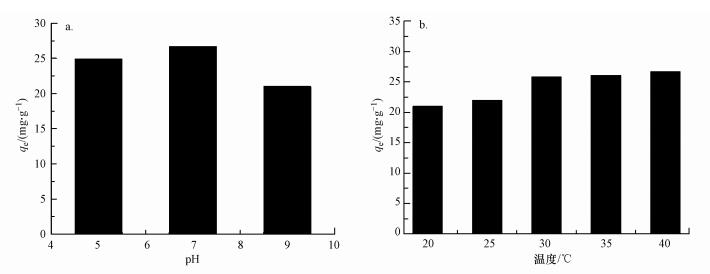 |
| 图 7 pH(a)和温度(b)对NiAl-LMO电极电吸附S2O32-的影响 Fig. 7 Effect of pH(a) and temperatures(b)on electrosorption of S2O32- on NiAl-LMO electrode |
图 7b为NiAl-LMO电极在不同温度下的电吸附实验结果.随着温度的升高, 电极的电吸附容量得到提高, 根据界面效应, 温度越高, 界面上的热扰动引起的离子扩散就越明显, 可以推断电吸附过程是吸热过程.所以本实验中, NiAl-LMO电极电吸附去除S2O32-的最佳反应温度为40 ℃.
4 结论(Conclusions)利用共沉淀法, 在泡沫镍基体上合成了NiAl-LDHs, 并经煅烧成功转化成NiAl-LMO电极.NiAl-LMO电极电化学性能稳定, 可逆性好、比电容值高, 比电容可达577 F·g-1.NiAl-LMO电极在外加电压1.0 V、pH为7、温度40 ℃时, 对S2O32-电吸附效率达60.9%, 电极反接S2O32-的脱附率达84.9%.NiAl-LMO电极可用于工业废水中S2O32-的去除.
Chen Z, Zhang H, Wu C, et al. 2015. A study of electrosorption selectivity of anions by activated carbon electrodes in capacitive deionization[J]. Desalination, 369: 46–50.
DOI:10.1016/j.desal.2015.04.022
|
蔡苏彦, 孙琼, 许宜铭. 2012. 锌铝水滑石负载羧酸基酞菁锌可见光降解水中氯苯酚[J]. 环境科学学报, 2012, 32(11): 2725–2731.
|
杜永家. 1993. 含硫废水处理综述[J]. 染料与染色, 1993, 30(1): 54–56.
|
García-Quismondo E, Santos C, Lado J, et al. 2013. Optimizing the energy efficiency of capacitive deionization reactors working under real-world conditions[J]. Environmental Science & Technology, 47(20): 11866–11872.
|
洪冰, 王铁汉. 2004. 空气氧化法在治理炼油厂低含硫污水中的应用[J]. 辽宁城乡环境科技, 2004, 24(6): 20–21.
|
匡晔. 2011.基于水滑石的复合功能材料制备及性能研究[D].北京: 北京化工大学
http://cdmd.cnki.com.cn/Article/CDMD-10010-1012216870.htm |
Kim Y J, Choi J H. 2012. Selective removal of nitrate ion using a novel composite carbon electrode in capacitive deionization[J]. Water Research, 46(18): 6033–6039.
DOI:10.1016/j.watres.2012.08.031
|
Kononova O N, Kholmogorov A G, Danilenko N V, et al. 2007. Recovery of silver from thiosulfate and thiocyanate leach solutions by adsorption on anion exchange resins and activated carbon[J]. Hydrometallurgy, 88(1/4): 189–195.
|
李娜, 张国珍, 杨仕超, 等. 2013. 活性炭纤维电吸附处理含盐溶液吸附特性研究[J]. 工业水处理, 2013, 33(8): 48–51.
DOI:10.3969/j.issn.1005-829X.2013.08.013 |
刘晓华. 2016.结构化镍铝复合氧化物选择性吸附材料的制备及性能研究[D].北京: 北京化工大学
|
Lin W, Yu W, Hu Z, et al. 2014. Superior performance asymmetric supercapacitors based on flake-like Co/Al hydrotalcite and graphene[J]. Electrochimica Acta, 143: 331–339.
DOI:10.1016/j.electacta.2014.08.024
|
Lu H, Zhu Z, Zhang H, et al. 2015. Simultaneous removal of arsenate and antimonate in simulated and practical water samples by adsorption onto Zn/Fe layered double hydroxide[J]. Chemical Engineering Journal, 276: 365–375.
DOI:10.1016/j.cej.2015.04.095
|
Lu X F, Li G R, Tong Y X. 2015. A review of negative electrode materials for electrochemical supercapacitors[J]. Science China, 58(11): 1799–1808.
DOI:10.1007/s11431-015-5931-z
|
Mascolo G, Mascolo M C. 2015. ChemInform abstract:On the synthesis of layered double hydroxides (LDHs) by reconstruction method based on the "Memory Effect"[J]. Microporous & Mesoporous Materials, 214(34): 246–248.
|
Namasivayam C, Sureshkumar M V. 2007. Modelling thiocyanate adsorption onto surfactant-modified coir pith, an agricultural solid 'waste'[J]. Process Safety & Environmental Protection, 85(6): 521–525.
|
Stott M B, Franzmann P D, Zappia L R, et al. 2001. Thiocyanate removal from saline CIP process water by a rotating biological contactor, with reuse of the water for bioleaching[J]. Hydrometallurgy, 62(2): 93–105.
DOI:10.1016/S0304-386X(01)00185-2
|
Wan D J, Qu D, Xiao H, et al. 2011. Adsorption of chloride anion from aqueous solution by calcined (Mg-Al) hydrotalcites of different Mg/Al Ratio[J]. Advanced Materials Research, 233-235: 420–426.
DOI:10.4028/www.scientific.net/AMR.233-235
|
Wei H, Wang J, Niu L, et al. 2014. Controllable synthesis of CoAl LDH@Ni(OH)2 nanosheet arrays as binder-free electrode for supercapacitor applications[J]. Journal of Alloys & Compounds, 608(4): 297–303.
|
Wu X, Tan X, Yang S, et al. 2013. Coexistence of adsorption and coagulation processes of both arsenate and NOM from contaminated groundwater by nanocrystallined Mg/Al layered double hydroxides[J]. Water Research, 47(12): 4159–4168.
DOI:10.1016/j.watres.2012.11.056
|
王婷, 朱春山, 胡承志. 2016. 镍铝层状氧化物薄膜电极的制备及其除盐性能[J]. 环境科学, 2016, 37(2): 602–608.
|
王秀娟, 王海增, 孙宝维, 等. 2012. 硫氰酸根在粒状镁铝复合氧化物上的吸附性能[J]. 环境科学, 2012, 33(9): 3182–3188.
|
Yan T, Zhu H, Li R, et al. 2013. Microwave synthesis of nickel/cobalt double hydroxide ultrathin flowerclusters with three-dimensional structures for high-performance supercapacitors[J]. Electrochimica Acta, 111(6): 71–79.
|
杨国华, 黄统琳, 姚忠亮, 等. 2009. 吸附剂的应用研究现状和进展[J]. 化学工程与装备, 2009(6): 84–88.
|
姚铭, 杜莉珍, 王凯雄, 等. 2005. 合成水滑石治理水体阴离子染料污染研究[J]. 环境科学学报, 2005, 25(8): 1034–1040.
DOI:10.3321/j.issn:0253-2468.2005.08.007 |
叶正平, 常铮, 雷晓东, 等. 2011. 镍铝混合氧化物薄膜的制备及其对水中S2O32-的电吸附脱除性能[J]. 化工进展, 2011(s1): 881–886.
|
 2018, Vol. 38
2018, Vol. 38


