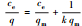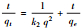腐植酸(Humic Acid, HA)是自然界动植物残体经腐烂分解后的产物, 是一种复杂的天然高分子有机质(郑平, 1991;Kishi et al., 1990), 广泛存在于土壤、河泥、海洋、泥炭、褐煤和风化煤中, 占土壤和水圈生态体系总有机质50%~80%(Li et al., 2004), 其中泥炭、褐煤和风化煤中的腐植酸含量较高, 是提取腐植酸的主要来源.
腐植酸的组成元素极其复杂, 分子组成和明确分子量尚不确定.研究表明(马明广等, 2006), 腐植酸主要含有C、H、O、N、S、P等元素, 化学结构复杂多样, 含有羧基、醇羟基、酚羟基、醌型羰基和酮型羰基等多种活性官能团(Uyguner et al., 2005;Yip et al., 2010).腐植酸具有很高的反应活性, 能与环境中的金属离子、矿物质、有机质、氧化物、氢氧化物和有毒活性污染物等发生吸附、络合和氧化还原作用.
土壤重金属污染来源有工矿企业的生产、化肥和农药的使用、机动车辆尾气的排放等各种人类活动.重金属是土体污染中最主要的污染物质之一, 大多数重金属危害性大且难治理, 随着生态系统中重金属元素的不断累积, 其毒性不断增强, 导致粮食、蔬菜和水果等农产品污染超标, 大气、水和土壤环境被污染, 生态系统退化, 最终直接或间接地危害人体健康.重金属在人体内蓄积, 产生急性和慢性毒性反应, 甚至“三致”(致畸、致癌和致突变)效应.对土壤重金属污染修复途径主要采用活化作用和钝化作用, 其中活化作用是通过淋洗、萃取和热解等方式使土壤中重金属溶解和迁移, 降低土壤重金属含量;固化作用则是通过钝化和固化稳定化等化学技术, 改变土壤中重金属的赋存形态, 弱化其迁移转化性和生物有效性(Arias et al., 2005).土壤中重金属的危害程度取决于重金属的性质和浓度, 其中重金属浓度受土壤对重金属的吸附和解吸能力影响.在土壤生态系统中土壤对重金属的吸附-解吸是重金属迁移和转化过程中的重要影响因子, 影响重金属的生物有效性(Arias et al., 2011).
目前, 国内外关于环境材料对重金属的吸附-解吸效果及影响颇多(Bhattacharyya et al., 2008;Šćiban et al., 2007), 也有很多文献探究了腐植酸在各种因素影响下对水和土壤中重金属的吸附-解吸特性(Komy et al., 2014), 但大多数研究对象偏向于单一重金属.然而实际中大多数土壤污染为多重金属的复合, 农田中主要存在铜、锌重金属复合和铅、镉重金属复合, 多种重金属之间会相互影响(Covelo et al., 2004), 产生与单一重金属不同的污染后果.因此, 研究环境材料对单一和多重金属复合污染的吸附特征很有必要.本文以腐植酸为吸附剂, 研究腐植酸对土壤中常见的铅镉复合重金属污染物的吸附效果, 比较腐植酸对单一Pb、单一Cd和Pb、Cd复合污染物的吸附特性, 为土壤重金属复合污染的防治和修复提供科学依据.
2 材料与方法(Materials and methods) 2.1 材料选用风化煤腐植酸, 黑色粉末状, 颗粒大小为80~100目, pH值为7.58.购于北京澳佳肥业有限公司, 其理化性质见表 1.目标铅镉化合物采用分析纯的Pb(NO3)2和CdCl2, 分别购于西陇化工股份有限公司和天津市津科精细化工研究所.
| 表 1 风化煤腐植酸基本组成和含量 Table 1 Basic composition and content of humic acid |
 |
| 图 1 腐植酸电镜扫描图 Fig. 1 The SEM of humic acid |
实验采用吸附模拟实验:风化煤腐植酸对Pb2+、Cd2+吸附实验以批量式进行.称取0.5 g腐植酸于50 mL离心管中, 分别加入600 mg·L-1 Pb2+、10 mg·L-1 Cd2+的单一或等离子浓度的复合溶液30 mL到离心管中.25 ℃下, 在恒温振荡器上以180 r·min-1转速振荡24 h, 进行吸附实验.吸附结束后, 以8000 r·min-1转速离心10 min, 上清液经0.45 μm滤膜过滤后, 加入2滴HNO3摇匀, 使用ICP-OES测定滤液Pb2+、Cd2+浓度.
用0.5 mol·L-1HCl和0.5 mol·L-1 NaOH调节pH值分别为3、4、5、6、7、8、9, 研究溶液pH值对腐植酸吸附重金属的影响;在15、25、35和45 ℃等4个设定温度下进行恒温振荡, 研究温度对腐植酸吸附重金属的影响;分别配置Pb2+浓度为100、200、400、600、800、1000和1200 mg·L-1, Cd2+浓度为1、2、5、10、20、50和100 mg·L-1的溶液, 研究初始浓度对腐植酸吸附重金属的影响;分别振荡5 min、10 min、20 min、40 min、80 min、2 h、4 h、6 h、8 h和24 h, 研究吸附时间对腐植酸吸附重金属的影响.另外, 配置Pb2+浓度为600 mg·L-1, Cd2+浓度分别为1、2、5、10、20 mg·L-1和Cd2+浓度为10 mg·L-1, Pb2+浓度分别为100、200、400、600、800 mg·L-1的复合重金属溶液, 研究复合重金属溶液中的Pb2+和Cd2+的竞争吸附.
2.3 测定指标与方法溶液重金属铅、镉含量采用ICP-OES仪(美国LEEMANS公司)测定.腐植酸重金属吸附量, 表示腐植酸吸附重金属离子的绝对量, 无法表示吸附的相对量, 而吸附率是被吸附的金属离子浓度与金属离子总浓度的比值, 能够反映腐植酸对重金属离子吸附的相对值, 所以需要比较吸附率.
吸附量计算公式:

|
(1) |
吸附率计算公式:

|
(2) |
式中, c0为溶液初始Pb2+、Cd2+的浓度(mg·L-1);ce为吸附平衡时溶液Pb2+、Cd2+的浓度(mg·L-1);V为溶液体积(L);M为腐植酸用量(g).
3 结果(Results) 3.1 pH对腐植酸Pb、Cd吸附效果影响溶液pH对材料吸附离子过程具有重要影响, pH值影响重金属在溶液中的水解、存在形态和表面电荷等(袁方, 2016), 这些性质又影响着腐植酸对重金属的吸附过程.金属阳离子在碱性条件下产生水解, 见式(3)(Naiya et al., 2000).

|
(3) |
吸附剂对金属离子吸附量通常随pH值的升高而增加(刘云等, 2005;陈海珊等, 2014), 但吸附量与pH并不是简单的线性关系, 线性关系只发生在特定pH区间范围内.确定腐植酸吸附重金属的最佳pH范围, 具有重要的应用价值.
3.1.1 pH对腐植酸吸附Pb2+量和吸附率的影响图 2为pH对腐植酸吸附铅镉复合和单一Pb2+效果的影响.比较发现, 腐植酸对铅镉复合和单一Pb2+的吸附效果类似, 吸附率在85.8%左右, pH值对腐植酸吸附Pb2+几乎无影响.可能是腐植酸含有多种含氧官能团, pH值较低时, Pb2+主要为游离态, Pb2+进入腐植酸分子内表面, 腐植酸与Pb2+通过离子键和配位键与羧基、酚羟基和羰基发生配位、络合和螯合反应, 产生沉淀(陈盈等, 2010);pH升高时, 部分Pb2+与OH-作用发生水解产生沉淀, 部分与腐植酸络合.另外腐植酸吸附Pb2+也可能不是简单的化学作用过程, 而是物理吸附和化学作用综合的结果(Wu et al., 2003).
 |
| 图 2 pH对腐植酸吸附铅镉复合Pb2+效果的影响(a)及单一Pb2+效果的影响(b) Fig. 2 Effect of pH on the adsorption of Pb2+ (Cd2+)(a) and Pb2+ (b)by humic acid |
图 3为pH对腐植酸吸附铅镉复合和单一Cd2+效果的影响.结果表明, 腐植酸对铅镉复合和单一Cd2+的吸附效果类似, 吸附量均随pH增加而增加, 但单一Cd2+受pH影响程度更大;Cd2+吸附量与吸附率变化趋势一致.pH较低时由于H+的竞争作用, H+与Cd2+形成竞争吸附.腐植酸表面的活性位点被H+占据, Cd2+由于静电斥力无法靠近吸附位点, 抑制了腐植酸对Cd2+的吸附作用.当pH值升高, 溶液中H+减少, 腐植酸表面吸附位点上负电荷增加, 对Cd2+产生引力作用, 腐植酸与Cd2+之间的结合能力增强, 吸附量增大.同时随着pH值升高, 部分Cd2+与OH-结合形成Cd(OH)+形态, 表面电荷降低, 专性吸附和静电吸附作用加强(Meine et al., 1997), 腐植酸吸附更多的Cd(OH)+, Cd2+的吸附量增加.但pH值越高不一定越利于Cd的吸附, 因为碱性条件下Cd会以Cd(OH)2沉淀形式析出, 水解和吸附作用同时进行, 很难判断Cd是被腐植酸吸附还是Cd本身生成沉淀(朱先芳, 2013).
 |
| 图 3 pH对腐植酸吸附铅镉复合Cd2+效果的影响(a)及单一Cd2+效果的影响(b) Fig. 3 Effect of pH on Cd2+ (Pb2+)(a) and Cd2+ (b) adsorption by humic acid |
吸附时间是影响腐植酸吸附效果的重要因素, 土壤对重金属吸附-解吸的速率大小, 直接反映重金属在一定环境条件下的迁移性能.了解重金属达到吸附-解吸平衡所需的时间, 有助于深化认识重金属在土壤中的动态转化规律.
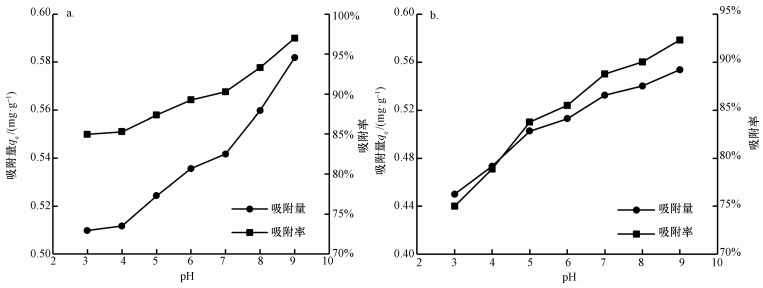
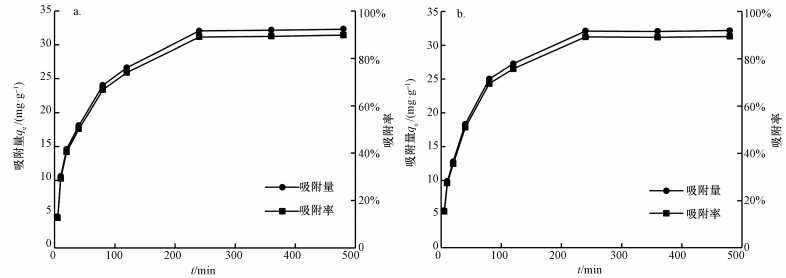
图 4、图 5表明, 腐植酸对铅镉复合和单一Pb2+和Cd2+吸附过程整体相似, 表现为先快后慢, 最后趋于平衡.吸附量与吸附率变化趋势一致.吸附过程主要有快速吸附、慢速吸附和吸附平衡3个阶段, 饱和吸附时间均为240 min.在前120 min腐植酸吸附Pb2+和Cd2+非常迅速, 可能是因为初始阶段腐植酸比表面积较大, 存在大量吸附活性位点, 迅速吸附Pb2+和Cd2+(武瑞平, 2010), 且初始阶段溶液中Pb2+、Cd2+浓度较高, 与腐植酸表面的Pb2+、Cd2+存在明显浓度差, 产生推动力;当吸附位点逐渐被占据后, 吸附饱和在240 min达到平衡.腐植酸对Pb2+的吸附量大于Cd2+, 这与两种金属本身性质和初始浓度有关.Cd2+在腐植酸表面以静电吸附为主, 即非专性吸附, 而腐植酸与Pb2+大部分形成共价键发生专性吸附(朱丽珺等, 2008), 专性吸附比非专性吸附更稳定且不易解吸.所以腐植酸对Pb2+吸附能力及吸附选择都优于Cd2+(Soltan et al., 2001).
 |
| 图 4 吸附时间对腐植酸吸附铅镉复合Pb2+效果的影响(a)及单一Pb2+效果的影响(b) Fig. 4 Effect of time on Pb2+(Cd2+)(a) and Pb2+(b)by humic acid |
 |
| 图 5 吸附时间对腐植酸吸附铅镉复合Cd2+效果的影响(a)及单一Cd2+效果的影响(b) Fig. 5 time profile of the adsorption of Cd2+(Pb2+)(a) and Cd2+(b) by humic acid |
通常吸附材料对Pb2+、Cd2+吸附量随浓度的增加而增加, 但吸附率则随起始浓度的增大而减小(孙朋成, 2016).图 6表明, 腐植酸吸附Pb2+、Cd2+的量随着Pb2+、Cd2+浓度增大而增加, 但吸附率随浓度增大而减少.重金属离子的初始浓度, 在一定程度上反映了环境被污染的程度(张小亮等, 2013).腐植酸投加量一定时, 当Pb2+、Cd2+浓度较低, 腐植酸表面活性位点尚未饱和, 单位质量的腐植酸与Pb2+、Cd2+的碰撞机会多(李静萍等, 2016), 因此低浓度时腐植酸吸附Pb2+、Cd2+效果很好;浓度增大时, 溶液中Pb2+、Cd2+总数增加, 提高了与腐植酸吸附位点接触的概率, 容易被腐植酸内部活性位点吸附;同时削弱了其他离子如H+的竞争作用, 因此Pb2+、Cd2+吸附量随着初始浓度的增加而增加.但随着浓度增大, 溶液中单位数量Pb2+、Cd2+对应的腐植酸数量减少, 碰撞概率降低, 导致吸附率降低.
 |
| 图 6 浓度对腐植酸吸附Pb2+(a)及Cd2+(b)效果的影响 Fig. 6 Effect of concentration on the adsorption of Pb2+(a) and Cd2+(b)by humic acid |
图 7~8表明, 温度对腐植酸吸附Pb2+、Cd2+效果的影响显著, 腐植酸吸附铅镉复合和单一Pb2+和Cd2+均随着温度的增加而增加, 腐植酸对铅镉的吸附量与吸附率变化趋势一致, 腐植酸吸附Pb2+、Cd2+均为吸热反应.这可能是因为温度升高改变了腐植酸的结构(韩雪峰等, 2016), 使腐植酸表面具有更多的吸附位点, 增加了腐植酸吸附Pb2+和Cd2+的机会;也可能是温度升高增强了离子运动, Pb2+、Cd2+扩散速度增加, 离子活度增大, 更多的Pb2+、Cd2+能够进入腐植酸表面和内部结构中(Chowdhury et al., 2011;符娟林等, 2006).
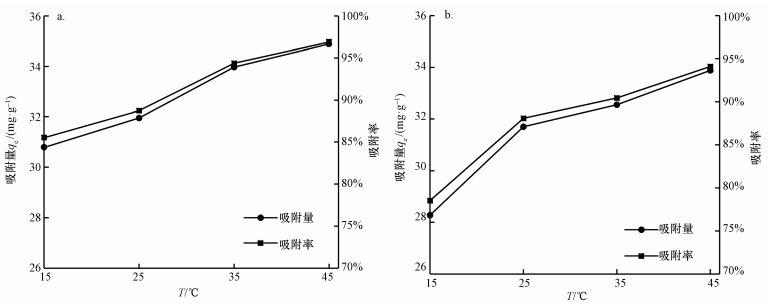 |
| 图 7 温度对腐植酸吸附铅镉复合Pb2+效果的影响(a)及单一Pb2+效果的影响(b) Fig. 7 Effect of temperature on the adsorption of Pb2+(Cd2+)(a) and Pb2+(b)by humic acid |
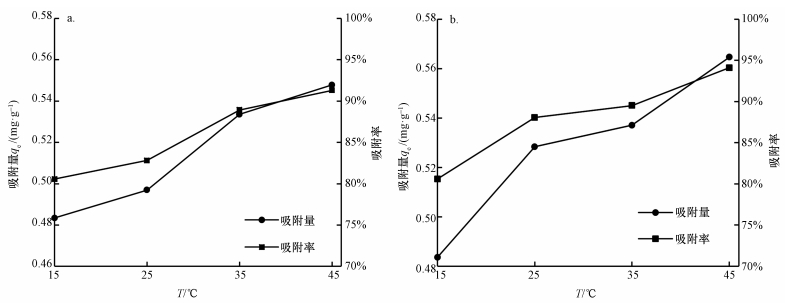 |
| 图 8 温度对腐植酸吸附铅镉复合Cd2+效果的影响(a)及单一Cd2+效果的影响(b) Fig. 8 Effect of temperature on Cd2+(Pb2+)(a) and Cd2+(b)by humic acid |
等温吸附试验是研究吸附剂在不同温度下对不同初始浓度的吸附质的吸附效果.吸附等温线在一定程度上能够反映吸附质和吸附剂相互作用的强度以及吸附质在吸附剂界面的状态和吸附层结构(Yan et al., 2005).通过数据计算与模型拟合, 选择对吸附过程拟合较好的吸附模型.常用模型有Langmuir和Freundlich和Temkin模型.
(1) Langmuir吸附模型等温式:
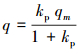
|
(4) |
变形可得:
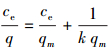
|
(5) |
式中, q为吸附剂吸附量(mg·g-1);qm为最大吸附量, 也称为单层饱和吸附量(mg·g-1);ce为溶液中重金属离子的平衡浓度(mg·L-1);k为吸附平衡常数, 与吸附剂与吸附质的性质和温度有关, k越大, 表示吸附剂的吸附能力越强.
(2) Freundlich吸附模型等温式:
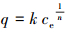
|
(6) |
变形可得:
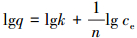
|
(7) |
式中, q为吸附剂吸附量(mg·g-1);ce为溶液中重金属离子的平衡浓度(mg·L-1);n为吸附指数强度.
(3) Temkin吸附模型等温式:

|
(8) |
式中, q为吸附剂吸附量(mg·g-1);ce为溶液中重金属离子的平衡浓度(mg·L-1).
腐植酸吸附铅镉复合和单一Pb2+、单一Cd2+的热力学模型参数见表 2.结果表明, 腐植酸吸附铅镉复合中的Pb2+和单一Pb2+、单一Cd2+的等温吸附模型中, 均为Langmuir等温吸附模型对腐植酸吸附的拟合效果最好, 可决系数R2大于0.99, 其次均是Temkin模型, Freundlich模型的拟合效果均为最差.
| 表 2 腐植酸对Pb2+和Cd2+的等温吸附方程拟合 Table 2 A comparison of isotherm model on Pb2+、Cd2+ by humic acid |
腐植酸对铅镉复合Cd2+的吸附, Freundlich等温吸附模型的拟合效果最好, 可决系数R2大于0.999, 其次是Langmuir模型和Temkin模型.Freundlich方程中KF大致可以表示吸附剂吸附能力的强弱, KF越大吸附能力越强.1/n值可作为腐植酸吸附重金属离子的吸附力强度指标, 1/n越大, 腐植酸对重金属离子的吸附作用越强(Arias et al., 2011).
3.6 吸附动力学研究吸附动力学研究吸附过程中吸附量随时间的变化规律, 反映了吸附速率的大小.常用模型有一级动力学模型、二级动力学模型和内部扩散模型(Yu et al., 2003).
一级动力学模型:

|
(9) |
式中, qe为平衡时吸附量(mg·g-1);qt为t时吸附量(mg·g-1);k1为一级动力学吸附速率常数(min-1).
二级动力学模型:
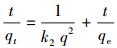
|
(10) |
式中, qe为平衡时吸附量(mg·g-1);qt为t时吸附量(mg·g-1);k2为二级动力学吸附速率常数(min-1).
内部扩散速率模型:

|
(11) |
式中, qe为平衡时吸附量(mg·g-1);qt为t时吸附量(mg·g-1);ki为颗粒内部扩散速率常数(mg·g-1·min-0.5);C为边界层常数.
腐植酸吸附铅镉复合和单一Pb2+、单一Cd2+动力学模型具体参数见表 3.腐植酸吸附铅镉复合和单一Pb2+、单一Cd2+的吸附过程均为准二级动力学模型拟合效果较好, 线性可决系数R2均大于0.99, 其他两种模型的拟线性可决系数相对较低.准二级动力学模型包含了吸附的所有过程, 如外部液膜扩散、表面吸附和颗粒内扩散等, 因此腐植酸吸附Pb2+和Cd2+是一个多步骤反应, 包括物理扩散过程和化学吸附过程, 且化学吸附在吸附过程中占主导地位.
| 表 3 腐植酸对Pb2+、Cd2+的吸附动力学方程拟合 Table 3 A comparison of kinetic model parameters on Pb2+、Cd2+ by Humic Acid |
图 9和10显示, 单一Pb2+溶液中加入Cd2+时, 对腐植酸吸附Pb2+量并没有产生影响.然而, 单一Cd2+溶液中加入Pb2+时, 由于Pb2+存在, 与Cd2+产生竞争吸附, 腐植酸吸附Cd2+量降低, 虽然吸附量降低不显著, 但吸附率降低明显.说明腐植酸在Pb2+、Cd2+复合溶液中, 对金属离子吸附具有一定的选择性, 对不选择性吸附的金属离子比单一溶液中的吸附量要小(Martyniuk et al., 2003).两种离子的电子层分布、水合离子半径、电荷性质及水合能等因素不同, 导致重金属离子在腐植酸表明的吸附能力存在差异(Gomes et al., 2001).Pb外层电子层分布为:6s26p2, Pb2+半径为120 pm, Cd外层电子层分布为:4d105s2;Cd2+半径为97 pm, Pb的原子序数和离子半径均大于Cd, 因此Pb生成的水合离子比较稳定, 使得腐植酸对Pb的络合和螯合能力比Cd强.Covelo等(2004)研究腐殖质对土壤重金属作用时得到Pb2+优于Cd2+.Manunza等(1995)研究腐植酸对同一价态不同金属离子的吸附性能时得到Pb2+>Cd2+, 这可能是Cd2+只与腐植酸的—COOH发生络合作用, 而Pb2+则可以与—COOH和—OH都发生络合作用.
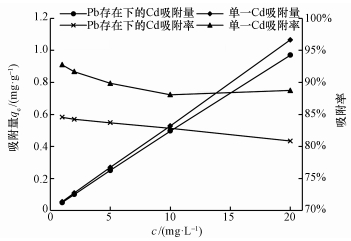 |
| 图 9 浓度对腐植酸吸附Cd2+效果的影响 Fig. 9 Effect of concentration on Cd2+ by humic acid |
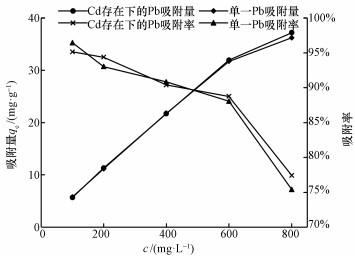 |
| 图 10 浓度对腐植酸吸附Pb2+效果的影响 Fig. 10 Effect of concentration on Pb2+ by humic acid |
1) 风化煤腐植酸对Pb2+吸附率在85.85%左右, 受pH值影响较小.腐植酸吸附Cd2+随着pH增加而增加, 对铅镉复合中Cd2+吸附量从0.50 mg·g-1增加到0.58 mg·g-1, 吸附率从83.11%上升到96.63%, 单一Cd2+吸附量从0.46 mg·g-1增加到0.55 mg·g-1, 吸附率从76.71%上升到91.67%, 说明腐植酸对不同重金属的吸附原理不同.
2) 腐植酸吸附Pb2+和Cd2+过程主要经历快速吸附、慢速吸附和吸附平衡3个阶段, 饱和吸附时间均为240 min.Pb2+、Cd2+吸附量均随温度增加而增加;Langmuir等温吸附模型对腐植酸吸附铅镉复合Pb2+、单一Pb2+、单一Cd2+拟合效果最好, 而Freundlich等温吸附模型对铅镉复合Cd2+拟合效果最好.
3) 腐植酸吸附Pb2+和Cd2+均为二级动力学模型, 拟合效果较好;Pb2+和Cd2+共存时, Pb2+与Cd2+会竞争吸附位点.单一Pb2+溶液加入Cd2+时, 对腐植酸吸附Pb2+几乎不产生影响.但单一Cd2+溶液加入Pb2+时, Pb2+会与Cd2+产生竞争吸附.这是由于腐植酸吸附Pb2+、Cd2+复合溶液中的重金属离子具有一定的选择性, 对Pb2+的吸附优于Cd2+.
Arias M, Pérez-Novo C, Osorio F, et al. 2005. Adsorption and desorption of copper and zinc in the surface layer of acid soils[J]. Journal of Colloid & Interface Science, 288(1): 21–29.
|
Bhattacharyya K G, Gupta S S. 2008. Adsorption of a few heavy metals on natural and modified kaolinite and montmorillonite:a review[J]. Advances in Colloid and Interface Science, 140(2): 114–131.
DOI:10.1016/j.cis.2007.12.008
|
陈海珊, 蔡爱华, 赵志国, 等. 2014. 蔗渣木质素对溶液中重金属离子的吸附性能[J]. 桂林理工大学学报, 2014, 34(2): 301–305.
DOI:10.3969/j.issn.1674-9057.2014.02.015 |
陈盈, 张满利, 关连珠, 等. 2010. pH对不同来源腐殖酸吸附铅和锰的影响[J]. 中国农学通报, 2010, 26(12): 67–69.
|
陈玉娟, 符海文, 温琰茂. 2001. 淋洗法去除土壤重金属研究[J]. 中山大学学报(自然科学版), 2001, 40(s4): 111–113.
|
Chowdhury S, Mishra R, Saha P, et al. 2011. Adsorption thermodynamics, kinetics and isosteric heat of adsorption of malachite green onto chemically modified rice husk[J]. Desalination, 265(1/3): 159–168.
|
Covelo E F, Andrade M L, Vega F A. 2004. Simultaneous adsorption of Cd, Cr, Cu, Ni, Pb and Zn by different soils[J]. International Journal of Food Agriculture & Environment, 2(3): 244–250.
|
Covelo E F, Andrade M L, Vega F A. 2004. Heavy metal adsorption by humic umbrisols:selectivity sequences and competitive sorption kinetics[J]. Journal of Colloid and Interface Science, 280(1): 1–8.
DOI:10.1016/j.jcis.2004.07.024
|
符娟林, 章明奎, 黄昌勇. 2006. 长三角和珠三角农业土壤对Pb、Cu、Cd的吸附解吸特性[J]. 生态与农村环境学报, 2006, 22(2): 59–64.
DOI:10.3969/j.issn.1673-4831.2006.02.013 |
Gomes P C, Fontes M P F, da Silva A G, et al. 2001. Selectivity sequence and competitive adsorption of heavy metals by Brazilian soils[J]. Soil Science Society of America Journal, 65(4): 1115–1121.
DOI:10.2136/sssaj2001.6541115x
|
韩雪峰, 赵宝福, 朱彤. 2016. 腐殖酸对污泥中重金属的稳定化研究[J]. 非金属矿, 2016, 39(4): 35–37.
|
Kishi H, Kogure N, Hashimoto Y. 1990. Contribution of soil constituents in adsorption coefficient of aromatic compounds, halogenated alicyclic and aromatic compounds to soil[J]. Chemosphere, 21(7): 867–876.
DOI:10.1016/0045-6535(90)90167-R
|
Komy Z R, Shaker A M, Heggy S E M, et al. 2014. Kinetic study for copper adsorption onto soil minerals in the absence and presence of humic acid[J]. Chemosphere, 99(3): 117–124.
|
李静萍, 仝云霄, 管振杰, 等. 2016. 腐植酸吸附剂的制备表征及对As(Ⅲ)吸附性能研究[J]. 腐植酸, 2016(4): 1631–1634.
|
Li L, Zhao Z, Huang W, et al. 2004. Characterization of humic acids fractionated by ultrafiltration[J]. Organic Geochemistry, 35(9): 1025–1037.
DOI:10.1016/j.orggeochem.2004.05.002
|
刘云, 吴平霄, 唐剑文, 等. 2005. 聚羟基铝柱撑蒙脱石吸附重金属离子实验研究[J]. 矿物岩石, 2005, 25(3): 122–126.
DOI:10.3969/j.issn.1001-6872.2005.03.027 |
马明广, 周敏, 蒋煜峰, 等. 2006. 不溶性腐殖酸对重金属离子的吸附研究[J]. 安全与环境学报, 2006, 6(3): 68–71.
DOI:10.3969/j.issn.1009-6094.2006.03.021 |
Manunza B, Deiana S, Maddau V, et al. 1995. Stability constants of metal-humate complexes:titration data analyzed by bimodal gaussian distribution[J]. Soil Science Society of America Journal, 59(59): 1570–1574.
|
Martyniuk H, Więckowska J. 2003. Adsorption of metal ions on humic acids extracted from brown coals[J]. Fuel Processing Technology, 84(1/3): 23–36.
|
Naiya T K, Bhattacharya A K, Das S K. 2009. Adsorption of Cd(Ⅱ) and Pb(Ⅱ) from aqueous solutions on activated alumina[J]. Journal of Colloid and Interface Science, 333(1): 14–26.
DOI:10.1016/j.jcis.2009.01.003
|
Noordwijk M V, Cerri C, Woomer P L, et al. 1997. Soil carbon dynamics in the humid tropical forest zone[J]. Geoderma, 79(1/4): 187–225.
|
Šćiban M, Radetić B, Žarko Kevrešan, et al. 2007. Adsorption of heavy metals from electroplating wastewater by wood sawdust[J]. Bioresource Technology, 98(2): 402–409.
DOI:10.1016/j.biortech.2005.12.014
|
Soltan M E, Rashed M N, Taha G M. 2001. Heavy metal levels and adsorption capacity of Nile River Sediments[J]. International Journal of Environmental Analytical Chemistry, 80(3): 167–186.
DOI:10.1080/03067310108044368
|
孙朋成. 2016. 三种环境材料对土壤铅镉固化及氮肥增效机理研究[D]. 北京: 中国矿业大学
|
Uyguner C S, Bekbolet M. 2005. Evaluation of humic acid photocatalytic degradation by UV-vis and fluorescence spectroscopy[J]. Catalysis Today, 101(3): 267–274.
|
Wu C H, Lin C F, Ma H W, et al. 2003. Effect of fulvic acid on the sorption of Cu and Pb onto gamma-Al2O3[J]. Water Research, 37(4): 743.
DOI:10.1016/S0043-1354(02)00391-3
|
武瑞平. 2010. 风化煤腐植酸对重金属铅污染土壤修复作用的研究[D]. 太原: 山西大学
|
王艳. 2012. 黄土对典型重金属离子吸附解吸特性及机理研究[D]. 杭州: 浙江大学
|
袁方. 2016. 不同pH值下重金属的形态及MEUF法对其去除机理的研究[D]. 长沙: 湖南大学
|
Yan W L, Bai R. 2005. Adsorption of lead and humic acid on chitosan hydrogel beads[J]. Water Research, 39(4): 688–698.
DOI:10.1016/j.watres.2004.11.007
|
Yip T C, Yan D Y, Yui M M, et al. 2010. Heavy metal extraction from an artificially contaminated sandy soil under EDDS deficiency:significance of humic acid and chelant mixture[J]. Chemosphere, 80(4): 416–421.
DOI:10.1016/j.chemosphere.2010.03.033
|
Yu Y, Zhou Q. 2003. Effect of methamidophos on sorption-desorption behavior of copper in soils[J]. Bulletin of Environmental Contamination & Toxicology, 71(5): 979–987.
|
张小亮, 何江涛, 石钰婷, 等. 2013. 不同金属离子及三氯乙烯(TCE)初始浓度对有机-矿质复合体的吸附影响研究[J]. 农业环境科学学报, 2013, 32(1): 95–102.
|
郑平. 1991. 煤炭腐植酸的生产和应用[M]. 北京: 化学工业出版社: 35–38.
|
朱丽珺, 张金池, 俞元春, 等. 2008. 胡敏酸吸附重金属Cu2+~Pb2+~Cd2+~的特征及影响因素[J]. 农业环境科学学报, 2008, 27(6): 2240–2245.
DOI:10.3321/j.issn:1672-2043.2008.06.020 |
朱先芳. 2013. 密云水库沉积物中腐殖酸特征及其与重金属吸附作用研究[D]. 北京: 首都师范大学
|
 2018, Vol. 38
2018, Vol. 38