随着城市区域不透水下垫面的增加, 雨水径流产生的面源污染日益严重.道路是不透水下垫面的重要组成部分, 路面径流是城市面源污染的重要来源.邻苯二甲酸酯(PAEs)是一类普遍使用的化学工业产品, 主要作为聚氯乙烯等生产中的改性添加剂使用, 以增大产品的可塑性;同时还用作农药载体、驱虫剂、润滑剂、化妆品等的生产原料.研究表明, PAEs具有抗雄性激素作用, 能够影响动物内分泌系统(Martine et al., 2013; Zhang et al., 2016).一度时间由于PAEs被大量使用, 以致在城市道路径流中发现PAEs化合物的存在.2009年5月美国EPA将邻苯二甲酸(2-乙基已基)酯(DEHP)列入饮用水标准(EPA 816-F-09-004; Polidoro et al., 2017), 我国、欧盟等也将DEHP列入地表水环境质量标准中.研究发现, 澳大利亚不同道路的径流中PAEs的测定浓度为9.47~58.21 μg · L-1(Clara et al., 2010), 瑞典地表径流中PAEs的测定浓度为4.67~100 μg · L-1(Björklund et al., 2009).国内学者对我国广州、西安、天津等城市道路颗粒物中PAEs进行调查发现, 道路颗粒物中存在多种PAEs, DEHP为主要的污染物, 占总PAEs的50%以上, 其中, 广州城市道路颗粒物中PAEs污染最严重, 含量达1463.7 μg · g-1(陈丽旋等, 2005; Wang et al., 2017; Zhao et al., 2017).大气沉降、道路及车辆产生的颗粒物累积在道路表面, 随着降雨的冲刷转移到径流中, 成为道路径流中PAEs污染的主要来源(Nielsen et al., 2000), 直接排放会对受纳水体造成污染, 给水生生物及人体带来危害(Aryal et al., 2009; Teil et al., 2010).目前,我国城市道路存在严重的PAEs污染, 对道路径流中PAEs的去除控制成为亟待解决的问题.
城市低影响开发(LID)设施可以有效地从源头上对径流污染进行控制, 其中, 生物滞留设施(Bioretention system)作为道路及停车场雨水径流控制的主要LID设施得到广泛应用(David et al., 2014;Brown et al., 2009).然而, 已有的采用生物滞留设施控制径流污染效果的研究主要集中于常规污染物及PAHs等持久性有机污染物(Shrestha et al., 2015; Davis et al., 2007; Hunt et al., 2006), 迄今仅有Zhang等(2014)采用人工配水, 探讨了生物滞留设施对邻苯二甲酸二丁酯(DBP)和邻苯二甲酸(2-乙基己基)酯(DEHP)的去除效果, 结果表明, 生物滞留设施可以很好地控制这两种PAEs.但目前研究主要集中在生物滞留设施对PAEs去除效果上, 而在设施对PAEs的去除机理上仍有待进一步研究.
为了考察生物滞留设施对PAEs的去除效果及机理, 本研究在上海市内环高架道路下建造了应用规模的生物滞留设施, 在实际降雨条件下, 监测设施对道路径流中PAEs的控制效果, 并对影响控制效果的因素和机制进行探讨.
2 材料与方法(Materials and methods) 2.1 实验装置在上海市内环高架某路段建造了应用规模的生物滞留设施, 处理高架道路的降雨径流.生物滞留设施由前置沉淀池和生物滞留池组成(图 1).前置沉淀池可以有效地缓冲进水径流流速, 截留部分颗粒物.沉淀池尺寸为1.0 m×1.0 m×0.6 m(长×宽×高), 末端设有90°三角薄壁堰, 结合超声波液位计(SIN-ES)与数据记录仪(RX200D), 每1 min记录一次液位值.
 |
| 图 1 生物滞留设施示意图 Fig. 1 A field scale bioretention facility |
生物滞留池是由植物、覆盖层、种植过滤层和砾石排水层构成, 池子底部铺有防渗膜与穿孔排水管, 为生物滞留设施重要的组成部分.路面径流通过落水管进入前置沉淀池后进入生物滞留池基质, 池尺寸为8 m×2.5 m×1.15 m(长×宽×高), 设施汇水面积为400 m2.植被为黄菖蒲, 不仅耐淹耐旱, 而且耐半阴, 适合高架道路下的生长环境.覆盖层为松树皮, 能缓解径流对土壤的冲刷, 保持土壤湿度, 维持较高的渗透速率, 同时在土壤界面创造适合微生物和有机物降解的环境.种植过滤层由质量比4 : 15 : 1的表层土、黄沙和发酵木屑混合组成, 作为生物滞留池的基本介质, 基质深度为85 cm.流经种植土过滤层的雨水被铺设在砾石层中的穿孔管统一收集, 出水通过计量井排入市政雨水管道.
设施出水计量井上方装有超声波液位计, 结合三角堰监测出水流量及水力负荷.当径流流量超过设施的设计标准(1年一遇1 h)时, 可通过布置在覆盖层上方的溢流管直接排出.在距离设施约100 m的屋顶设置翻斗式自记雨量计(SL3-1)记录降雨量变化过程.
2.2 样品采集与检测使用棕色玻璃瓶在落水管处收集路面径流, 在前置沉淀池出口收集生物滞留池进水样品, 在出水计量井处收集出水样品.所有取样容器在采样之前均用蒸馏水冲洗并烘干.降雨径流产生时, 根据降雨特性, 每隔3~30 min取一次样, 并记录采样的起、止时间.为保证样品的代表性, 每场降雨事件样品采集数量不少于10个.降雨结束后, 参照雨量过程配制考虑水量权重的混合样品, 将混合样品直接作为该场降雨PAEs的事件平均浓度样品(EMC).待测水样立即送回实验室, 在4 ℃冰箱中保存并在24 h内完成萃取处理.
参考《水质邻苯二甲酸二甲(二丁、二辛)酯的测定液相色谱法》(HJT 72—2001)对水样中6种PAEs进行测定.用70 mL正己烷萃取500 mL水样, 萃取液用减压式旋转蒸发仪进行浓缩定容至1.5 mL待测.用高效液相色谱仪(Shimadzu LC-20A)对水样中6种PAEs进行测定, 包括邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二辛酯(DnOP)、邻苯二甲酸丁基苄基酯(BBP)和邻苯二甲酸(2-乙基己基)酯(DEHP).以甲醇与水按比例混合作为流动相, 进行梯度洗脱.
其他水质检测指标包括TSS、COD, 采用国家标准检测方法测定:TSS为重量法, COD为比色法(HACHDRP2010).
2.3 质量控制实验分析过程按方法空白、样品空白、空白加标、样品加标及平行样进行质量控制.在萃取前加入6种PAEs标准溶液(美国o2si公司)进行加标回收率测定, 样品加标回收率为68.5%~101.7%;空白水样加标回收率为63.3%~107.9%, 空白实验未检出目标污染物, 满足环境样品中PAEs的分析要求.同一样品进行3次平行样测定, 相对标准偏差均小于10%, 有较好的重现性, 满足质量控制标准.
2.4 监测降雨事件2017年6—10月间, 采集到完整路面径流过程样品, 同时生物滞留设施产生出流的降雨事件共有8场, 其中, 中雨(10.0~24.9 mm)6场、大雨(25.0~49.9 mm)3场, 监测降雨事件的降雨特性见表 1.本文使用的生物滞留设施, 在降雨量≤10 mm条件下基本不产生出流.
| 表 1 监测降雨事件的降雨特征 Table 1 Characteristics of monitored rainfall evens |
次降雨出水平均水力负荷(qo)可反映生物滞留池进水与基质的接触时间, 计算公式如式(1)所示.
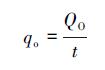
|
(1) |
式中, QO为出水总流量(L), t为出水时间(s).
2.6 数据分析采用IBM SPSS 20进行正态检验, 结果表明, 在0.05水平下, 所有数据均符合正态分布.由于数据方差不齐, 故使用Games-Howell法进行分析, 对不同水样间水质参数差异的显著性进行分析.数据间相关性用Pearson相关系数(r)表示.
3 结果(Results) 3.1 PAEs的去除效果统计8场监测降雨事件路面径流及设施进、出水各种污染物的多次监测EMC的平均浓度(表 2), 道路径流∑6PAEs的均值为171.71 μg · L-1, 其中, DEHP占比最高, 占总PAE的76.4%, 其次为DnOP, 占总PAE的15.9%, DBP、DMP、DEP占比分别为3.0%、2.7%、1.9%, 而BBP含量低于检测限.澳大利亚不同道路径流中PAEs的测定浓度为9.47~58.21 μg · L-1(Clara et al., 2010), 瑞典地表径流中PAEs的测定浓度为4.67~100 μg · L-1(Björklund et al., 2009), 同本实验测得的浓度相比大约低一个数量级.其中, DEHP浓度只有3 μg · L-1, 这主要是因为在欧洲DEHP的使用已受到限制, 其他更高分子量的PAEs使用量逐年增加.
| 表 2 不同监测样品中PAEs的平均浓度及TSS浓度 Table 2 Concentrations of pollutants from different water samples |
监测降雨事件路面径流及设施进、出水PAEs的EMC浓度分布, 结果见图 2.统计显示, 径流与进水PAEs之间无显著性差异(p>0.05), 进水与出水PAEs之间具有显著性差异(p < 0.05).
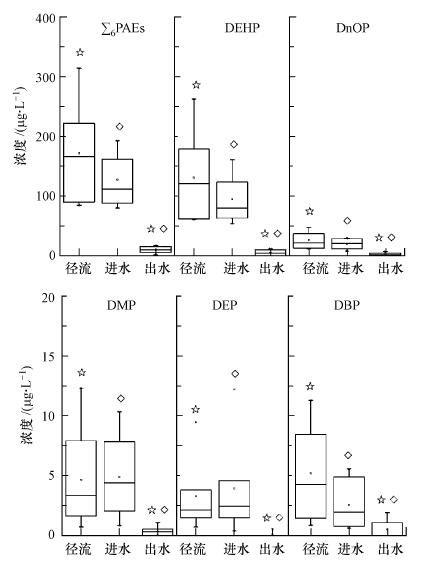 |
| 图 2 生物滞留设施不同样品中PAEs浓度 (☆表示径流与出水之间具有显著性差异(p < 0.05), ◇表示进水与出水之间具有显著性差异(p < 0.05)) Fig. 2 PAEs concentrations in road runoff, influent and effluent samples of thebioretention system |
不同分子量的PAEs在水中的存在形态不同(EU-RAR, 2008), LMW PAEs具有溶解性, 在径流中主要以溶解态的形式存在;DEHP为高分子量(HMW)PAE, 在水中溶解度低, 约为3×10-4 mg · L-1, logKOW>4, 容易吸附在颗粒物表面, 在径流中主要以颗粒态的形式存在(Tang et al., 2015).路面径流中PAEs主要来自街尘, 且随着灰尘粒径的减小, 单位质量吸附的PAEs量增加, 径流中的PAEs主要吸附在小颗粒上(陈丽旋等, 2005).路面径流首先经过前置沉淀池, 其中, 较大的悬浮颗粒经沉淀被去除.经过前置沉淀池后的径流∑6PAEs的平均浓度为127.70 μg · L-1, 与路面径流相比有所下降.沉淀池出水与进水的∑6PAEs浓度不存在显著性差异(p>0.05), 而TSS浓度显著降低(p < 0.05).有报道表明(Kalmykova et al., 2013), 沉淀池对PAEs等有机物的去除效果较差, 与本实验结果相同.前置沉淀池主要去除大颗粒悬浮物, 无法有效去除径流中的PAEs.
3.2 生物滞留池对PAEs去除效果的影响因素为了研究影响PAEs去除效果的因素, 对PAEs的去除率与影响因素之间的相关性进行分析.生物滞留池对DEHP去除率与TSS去除率之间的相关性如图 3所示, 结果表明, DEHP与TSS的去除率之间呈显著正相关(r=0.818, p < 0.05), 生物滞留池对DEHP的去除率随TSS去除率的增大而增大.
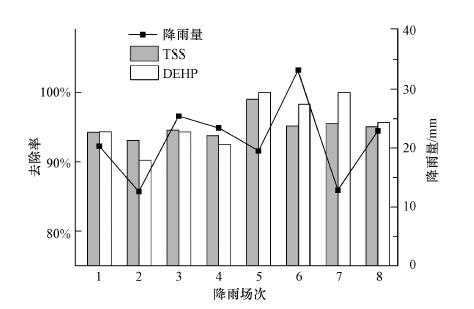 |
| 图 3 DEHP去除率与TSS去除率的比较 Fig. 3 A comparison between DEHP/TSS removal efficiencies |
有研究发现, 生物滞留池基质中PAEs主要分布在表层0~15 cm及进水口处(Sayyad et al., 2017).生物滞留池对TSS的去除主要通过滤饼过滤(Cake Filtration)和深度过滤(Depth Filtration)作用, 大部分TSS被截留在介质表面及0~10 cm处(Li et al., 2008a;2008b).DEHP为HMW PAE, 具有较强的疏水性, KOW较大, 易吸附在颗粒物表面(Diblasi et al., 2009), 随着生物滞留池对TSS的截留而去除.在生物滞留池对径流PAHs的去除研究中发现(Tedoldi et al., 2017;Peijnenburg et al., 2006), 高环PAHs在生物滞留池中随着TSS的截留而去除, 高环PAHs具有较强的疏水性, KOW较大, 与PAEs具有相似的性质.
生物滞留池对LMW PAEs的去除效果与DEHP相比较差, 且不稳定.对LMW PAEs出水浓度与进水浓度进行相关性分析发现(图 4a), LMW PAEs出水浓度与进水浓度呈显著正相关(r=0.769, p<0.05), 出水浓度随着进水浓度的增大而增大.LMW PAEs的lgKOW<4, 具有挥发性且易溶于水(Yang et al., 2013), 其去除机理与DEHP可能不同.对LMW PAEs出水浓度、去除率与次降雨设施出水平均水力负荷进行相关性分析发现(图 4b), 出水浓度随着出水水力负荷的增大而增大(r=0.763, p<0.05), 去除率随着水力负荷的增大而减小(r=-0.716, p<0.05).说明随着径流与基质的接触时间增大, 设施对LMW PAEs的去除效果升高.结果表明, 溶解性LMW PAEs的去除可能是依靠吸附作用.有研究表明, 土壤通过吸附作用去除DMP、DEP, 效果与土壤中的有机颗粒含量有关(Li et al., 2015; Wu et al., 2015).
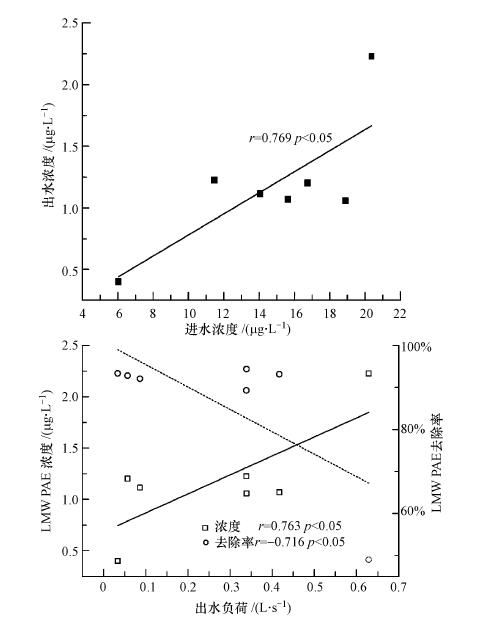 |
| 图 4 LMW PAEs出水浓度与进水浓度的关系(a)及出水浓度、去除率与出水负荷的关系(b) Fig. 4 Relationship between outflow and inflow concentrations of LMW PAEs(a) and relationship between hydraulic loading rates and outflow concentrations, removal efficiency of LMW PAEs(b) |
吸附、截留在设施基质中的PAEs, 在无雨期可以通过生物降解、植物吸收、蒸发等方式去除(Xu et al., 2008).PAEs在土壤中可被生物降解, 随着分子量的增大, 降解周期越长, 其中, DMP、DEP的生物降解速率最快, DEHP、DnOP较慢(Wang et al., 2015).本实验监测期间为生物滞留设施连续运行的第2年, 实验结果表明, 生物滞留设施在连续运行2年后对PAEs仍然具有良好的控制效果.生物滞留设施基质的吸附、截留作用是去除道路径流中PAEs的主要途径, 与基质配比、深度、汇水面积等因素有关, 通过优化设计参数从而提高设施对PAEs的去除效果.
3.3 生物滞留设施出水中PAEs与规范限值的比较路面径流对地表水体中PAEs含量具有显著影响, 是地表水污染的重要来源之一(He et al., 2013), 径流直接流入水体会产生严重的污染(Clara et al., 2010; Aryal et al., 2009; Teil et al., 2010).对于合流制排水系统, 降雨径流中DEHP对CSO排放负荷的贡献率在39%~85%(Launay et al., 2016).《欧洲水框架指令》地表水环境质量标准中DEHP的限定值为1.3 μg · L-1, 这在我国比较难实现, 因为欧洲近年来对DEHP的使用进行了限制, 使得地表径流中DEHP的浓度较小, 与上海地表径流中DEHP的浓度相比小一个数量级.我国《地表水环境质量标准》规定的DEHP、DBP标准值分别为8、3 μg · L-1.对不同类型样品中PAEs浓度与规范限值的比值进行统计(表 3), 可知道路径流中DEHP的浓度可以达到水环境标准的32倍, DBP在多数降雨径流中超过标准的限值.经过生物滞留设施处理后的出水DEHP浓度与标准限值之间的比值最大不超过1.55, 达标率为71.42%;出水DBP浓度与标准限值之间的比值均小于1, 达标率为100%, 说明生物滞留设施可以较好地控制路面径流中PAEs对受纳水体的污染.
| 表 3 不同样品DEHP、DBP浓度与规范的比值 Table 3 Relative DEHP and DBP concentrations referred to the standard values for water samples |
1) 高架道路径流经过生物滞留设施处理后, 出水PAEs浓度显著降低, 设施对∑PAEs去除率的平均值超过90%.
2) 生物滞留池对不同分子量的PAEs的去除机理不同.对DEHP的去除与TSS相关, 主要是通过基质对TSS的截留过滤去除.LMW PAEs主要是通过基质的吸附作用去除.
3) 道路径流经过生物滞留设施处理后, 出水DEHP浓度基本达到地表水环境质量标准, DBP完全达标.生物滞留设施可以有效地控制城市路面径流中PAEs对地表水体的污染.
Aryal R K, Lee B K. 2009. Characteristics of suspended solids and micropollutants in first-flush highway runoff[J]. Water Air & Soil Pollution Focus, 9(5/6): 339–346.
|
Björklund K, Cousins A P, Strömvall A M, et al. 2009. Phthalates and nonylphenols in urban runoff:Occurrence, distribution and area emission factors[J]. Science of the Total Environment, 407(16): 4665–4672.
DOI:10.1016/j.scitotenv.2009.04.040
|
Brown R A, Hunt W F, Davis A P, et al. 2009. Bioretention/Bioinfiltration performance in the Mid-Atlantic[C]. World Environmental and Water Resources Congress, American Society of Civil Engineers. Kansas City, Missouri: 1-10
|
陈丽旋, 曾锋, 罗丹玲, 等. 2005. 城市道路灰尘中邻苯二甲酸酯污染特征研究[J]. 环境科学学报, 2005, 25(3): 409–413.
|
Clara M, Windhofer G, Hartl W, et al. 2010. Occurrence of phthalates in surface runoff, untreated and treated wastewater and fate during wastewater treatment[J]. Chemosphere, 78(9): 1078–1084.
DOI:10.1016/j.chemosphere.2009.12.052
|
Davis A P. 2007. Field performance of bioretention:Water quality[J]. Environmental Engineering Science, 24(8): 1048–1064.
DOI:10.1089/ees.2006.0190
|
David N, Leatherbarrow J E, Yee D, et al. 2014. Removal efficiencies of a bioretention system for trace metals, PCBs, PAHs, and Dioxins in a semiarid environment[J]. Journal of Environmental Engineering, 141(6).
DOI:10.1061/(ASCE)EE.1943-7870.0000921
|
Diblasi C J, Li H, Davis A P, et al. 2009. Removal and fate of polycyclic aromatic hydrocarbon pollutants in an urban stormwater bioretentionfacility[J]. Environmental Science & Technology, 43(2): 494–502.
|
EU-RAR. 2008. European union risk assessment report on bis(2-ethylhexyl) phthalate (DEHP)[S]. Sweden: Swedish Chemicals Agency
|
He W, Qin N, Kong X, et al. 2013. Spatio-temporal distributions and the ecological and health risks of phthalate esters (PAEs) in the surface water of a large, shallow Chinese lake[J]. Science of the Total Environment, 461-462(7): 672–682.
|
Hunt W F, Jarrett A R, Smith J T, et al. 2006. Evaluating bioretention hydrology and nutrient removal at three field sites in North Carolina[J]. Journal of Irrigation & Drainage Engineering, 132(6): 600–608.
|
Kalmykova Y, Björklund K, Strömvall A M, et al. 2013. Partitioning of polycyclic aromatic hydrocarbons, alkylphenols, bisphenol A and phthalates in landfill leachates and stormwater[J]. Water Research, 47(3): 1317–1328.
DOI:10.1016/j.watres.2012.11.054
|
Launay M A, Dittmer U, Steinmetz H. 2016. Organic micropollutants discharged by combined sewer overflows-Characterisation of pollutant sources and stormwater-related processes[J]. Water Research, 104: 82.
DOI:10.1016/j.watres.2016.07.068
|
Li B H, Yuan Q, Bi E P, et al. 2015. Sorption behavior of phthalic acid esters on reference soils evaluated by soil column chromatography[J]. Clean -Soil, Air, Water, 38(5/6): 425–429.
|
Li H, Davis A P. 2008. Urban particle capture in bioretention media Ⅰ:laboratory and field studies[J]. Journal of Environmental Engineering, 134(6): 409–418.
DOI:10.1061/(ASCE)0733-9372(2008)134:6(409)
|
Li H, Davis A P. 2008. Urban particle capture in bioretention media Ⅱ:theory and model development[J]. Journal of Environmental Engineering, 134(6): 419–432.
DOI:10.1061/(ASCE)0733-9372(2008)134:6(419)
|
Martine B, Marie-Jeanne T, Cendrine D, et al. 2013. Assessment of adult human exposure to phthalate esters in the urban center of Paris (France)[J]. Bulletin of Environmental Contamination & Toxicology, 90(1): 91–96.
|
Peijnenburg W J, Struijs J. 2006. Occurrence of phthalate esters in the environment of The Netherlands[J]. Ecotoxicology & Environmental Safety, 63(2): 204–215.
|
Polidoro B A, Comeros-Raynal M T, Cahill T, et al. 2017. Land-based sources of marine pollution:Pesticides, PAHs and phthalates in coastal stream water, and heavy metals in coastal stream sediments in American Samoa[J]. Marine Pollution Bulletin, 116(1/2): 501–507.
|
Sayyad G, Price G W, Sharifi M, et al. 2017. Fate and transport modeling of phthalate esters from biosolid amended soil under corn cultivation[J]. Journal of Hazardous Materials, 323(Pt A): 264–273.
|
Shrestha P, Hurley S, Cording A. 2015. Water quality performance of bioretention systems associated with different hydrologic, vegetation, and soil media treatments[C]. Low Impact Development Conference
|
Tang X, Wang S, Yang Y, et al. 2015. Removal of six phthalic acid esters (PAEs) from domestic sewage by constructed wetlands[J]. Chemical Engineering Journal, 275: 198–205.
DOI:10.1016/j.cej.2015.04.029
|
Tedoldi D, Chebbo G, Pierlot D, et al. 2017. Assessment of metal and PAH profiles in SUDS soil based on an improved experimental procedure[J]. Journal of Environmental Management, 202(Pt 1): 151–166.
|
Teil M, Blanchard M, Dargnat C, et al. 2010. Occurrence of phthalate diesters in rivers of the Paris district (France)[J]. Hydrological Processes, 21(18): 2515–2525.
|
Wang L, Liu M, Tao W, et al. 2017. Pollution characteristics and health risk assessment of phthalate esters in urban soil in the typical semi-arid city of Xi'an, Northwest China[J]. Chemosphere, 191: 467–476.
|
Wang J, Zhao X, Wu W. 2004. Biodegradation of phthalic acid esters (PAEs) in soil bioaugmented with acclimated activated sludge[J]. Process Biochemistry, 39(12): 1837–1841.
DOI:10.1016/j.procbio.2003.08.005
|
Wu Y, Si Y, Zhou D, et al. 2015. Adsorption of diethyl phthalate ester to clay minerals[J]. Chemosphere, 119(119C): 690–696.
|
Xu G, Li F, Wang Q. 2008. Occurrence and degradation characteristics of dibutyl phthalate (DBP) and di-(2-ethylhexyl) phthalate (DEHP) in typical agricultural soils of China[J]. Science of the Total Environment, 393(2/3): 333–340.
|
Yang F, Wang M, Wang Z. 2013. Sorption behavior of 17 phthalic acid esters on three soils:effects of pH and dissolved organic matter, sorption coefficient measurement and QSPR study[J]. Chemosphere, 93(1): 82–89.
DOI:10.1016/j.chemosphere.2013.04.081
|
Zhang L, Liu J, Liu H, et al. 2016. The occurrence and ecological risk assessment of phthalate esters (PAEs) in urban aquatic environments of China[J]. Ecotoxicology, 24(5): 1–18.
|
Zhang K, Randelovic A, Page D, et al. 2014. The validation of stormwater biofilters for micropollutant removal using in situ challenge tests[J]. Ecological Engineering, 67(6): 1–10.
|
Zhao J, Ji Y, Zhu Z, et al. 2017. PAEs occurrence and sources in road dust and soil in/around parks in May in Tianjin, China[J]. Ecotoxicology & Environmental Safety, 147: 238–244.
|
Zhao W Y, Wu Z B, Zhou Q H, et al. 2004. Removal of dibutyl phthalate by a staged, vertical-flow constructedwetland[J]. Wetlands, 24(1): 202–206.
DOI:10.1672/0277-5212(2004)024[0202:RODPBA]2.0.CO;2
|
 2018, Vol. 38
2018, Vol. 38


