2. 中国地质环境监测院, 北京 100081;
3. 美国亚利桑那大学科学学院水文与大气科学系, 图森 85719
2. China Institute of Geo-Environment Monitoring, Beijing 100081;
3. Department of Hydrology and Atmospheric Sciences, School of Science, University of Arizona, Tucson 85719
活性炭(AC)是一种具有发达孔隙结构、巨大比表面积和极强吸附能力的无定型炭, 在很多领域都得到了广泛应用(刘守新等, 2001), 主要涉及环保、化工、食品加工、湿法冶金、药物精制、军事化学防护等行业(戴芳天, 2003).AC可以吸附多种有机物, 其中, 最为常见的是挥发性有机化合物(VOCs)(王宝庆等, 2000;许伟等, 2016).作为一种多孔吸附材料, AC吸附饱和后内部的孔隙结构会被吸附质堵塞从而丧失吸附能力, 如果直接废弃使用后的AC, 会造成二次污染(侯立安等, 2003).因此, 将吸附饱和的AC进行再生实现循环使用具有较高的经济价值和环境价值(李婷等, 2013).
AC再生是指用物理或化学方法将吸附于AC微孔的吸附质予以去除, 恢复其吸附性能, 达到重复使用的目的(翁元声, 2004).再生方法主要取决于AC的类型和吸附物质的性质(吴琪等, 2011).常用的再生方法主要有热再生、微波再生、化学再生及生物再生(周琴等, 2013).其中, 热再生效率高但炭损失较大, 费用高;微波再生能耗低但缺少专业的微波再生加热装置;生物再生操作简单、针对性强, 但再生时间较长(曾雪玲等, 2008;韩庭苇等, 2016);而氧化再生法因氧化效率高、能耗低、再生工艺简单等特点近年来备受关注(刘守新等, 2001;吴琪等, 2011;王福禄, 2011).
三氯乙烯(TCE)是一种常见且具有致癌、致畸、致突变性质的氯代污染物, AC吸附是目前使用较广泛的TCE处理方法(Quinlivan et al., 2005;Su et al., 2013).AC吸附饱和后, 利用氧化剂氧化去除吸附的TCE能够实现AC的再生.王福禄(2011)利用二价铁(Fe2+)催化过氧化氢(H2O2)实现了被苯酚吸附饱和的AC的再生.Liang等(2009a)证明了利用Fe2+催化过硫酸钠(Na2S2O8)(IAP)再生被TCE吸附饱和的AC的可行性.近年来, 利用催化的H2O2-Na2S2O8双氧化体系可以实现TCE的有效去除, 且去除效果优于H2O2及Na2S2O8单氧化体系(Yan et al., 2015).但利用双氧化体系对AC进行再生的效果仍不明确.
基于此, 本文拟采用Fe2+催化条件下H2O2-Na2S2O8双氧化体系(ICHP)对被TCE吸附饱和的AC(AC-TCE)进行再生, 通过研究再生过程、再生效率及对再生前后AC进行表征来探讨ICHP氧化再生AC-TCE的可行性.
2 材料与方法(Materials and methods) 2.1 主要仪器和试剂实验试剂:粒状AC(20~40目)为试剂纯, 购自Sigma-Aldrich;TCE、FeSO4·7H2O、Na2S2O8、H2O2(30%)、NaOH均为分析纯, 购自北京化工厂;甲醇、异丙醇均为色谱纯, 购自DIKMA公司;实验用水均为超纯水.
实验仪器:HZ85-2型磁力搅拌器(北京中兴伟业仪器有限公司);FD5-3T冷冻干燥机(美国金西盟国际集团);电感耦合等离子体发射光谱仪(ICP-OES)(德国斯派克分析仪器公司);PB-10数显pH计(北京赛多利斯仪器系统有限公司);自动电位滴定仪(Metrohm 877 Titrino plus, 配有Metrohm 801 stirrer)(瑞士万通公司);Agilent 6820气相色谱仪(Agilent公司), DB-5毛细柱(30 m×0.53 mm×1.5 μm), FID检测器, HP 7694E顶空自动进样器;Agilent 6890/5973N气相色谱-质谱仪(Agilent公司), DB-VRX毛细管色谱柱(60m×0.25 mm×1.4 μm)(Agilent公司), G1888型顶空自动进样器(Agilent公司);KF-500E型超声波清洗器(昆山禾创超声仪器有限公司);L550型离心机(湘仪离心机仪器有限公司).
2.2 实验方法使用甲醇作为溶剂, 配制浓度为50000 mg·L-1的TCE储备液.实验均在室温条件下进行, 使用磁力搅拌器在转速为300 r·min-1条件下进行搅拌.实验均设置2组平行样品, 吸附实验再设置1组挥发控制, 整个过程中加盖并用封口膜进行密封.反应结束时迅速取5 mL样品于10 mL顶空瓶中, 迅速压盖, 使用Agilent 6820气相色谱仪对TCE进行测定.
2.2.1 吸附动力学实验在2 L三角瓶中加入超纯水2 L、TCE储备液1.2 mL、AC 1 g, 分别在0 min、10 min、0.5 h、1 h、2 h、3 h、4 h、6 h、8 h、12 h、24 h时迅速取样测定TCE.
2.2.2 等温吸附实验在1 L三角瓶中分别加入超纯水1 L, TCE储备液0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8 mL, 配置成初始浓度分别为5、10、15、20、25、30、35、40 mg·L-1的TCE溶液, 分别加入AC 0.5 g, 迅速取初始及反应12 h后的样品测定TCE.
2.2.3 再生实验为了测定再生过程中溶液pH值、总溶解性铁、TCE的变化, 确定再生产物及再生AC吸附容量, 进行以下实验.
在1 L三角瓶中制备吸附饱和的AC, 加入超纯水1 L、TCE储备液0.6 mL、AC 0.5 g, 吸附12 h后迅速取样测定TCE.
再生实验在1 L三角瓶中进行, 加入超纯水1 L、吸附饱和AC 0.5 g, 按顺序加入Na2S2O8 5.35 g、H2O2 (30%) 1.77 mL、FeSO4·7H2O 0.74 g, 即TCE:Fe2+:H2O2:S2O82- = 1:9.20:59.79:77.52(物质的量比), 加入过程始终进行搅拌, 再生12 h后取出进行冷冻干燥得到再生AC.再生实验分别于0 min、5 min、0.5 h、1 h、2 h、4 h、8 h、12 h每个时间点设置样品.每个时间点反应结束后迅速取10 mL样品到20 mL顶空瓶中, 用1 mL异丙醇终止反应, 用以测定再生溶液中的TCE及脱氯产物;使用pH计测定溶液pH值;取80 mL样品到100 mL玻璃瓶中, 用5 mL异丙醇终止反应, 用以测定总溶解性铁及氯离子.
再吸附实验在2 L三角瓶中进行, 加入超纯水2 L、TCE储备液1.2 mL, 分别加入原状AC及再生AC 1 g, 12 h后迅速取样测定TCE.
2.2.4 解吸实验解吸实验在40 mL玻璃瓶中进行, 加入再生AC 0.5 g、甲醇40 mL, 超声20 min后离心20 min, 转速为2500 r·min-1.离心后倒出上清液, 共解吸3次, 后2次加入甲醇的体积均为30 mL, 甲醇加入总体积为100 mL.
2.2.5 脱氯产物研究利用气相色谱-质谱仪(GC-MS)对再生过程溶液及再生AC在甲醇中的解吸溶液进行测试.测试方法包含TCE及其所有脱氯产物, 定量采用内标法, 选择氟苯作为内标.
2.2.6 表征为了验证氧化剂的存在是否对AC产生影响, 从而使其吸附容量发生变化, 分别利用扫描电子显微镜(SEM)、能量散射光谱仪(EDS)、X射线光电子能谱仪(XPS)及氮气吸附-解吸技术对原状AC和再生AC进行表征.
2.3 测试方法TCE利用气相色谱进行测定, 测试条件如下:进样口温度160 ℃, 载气为N2, 分流进样, 分流比为20:1.升温程序:初始100 ℃, 保持2 min, 以65 ℃·min-1升至220 ℃, 保持1 min.
TCE脱氯产物利用气相色谱-质谱进行测定, 其中, 气相条件:进样口温度150 ℃, 载气为He, 流速1 mL·min-1, 分流进样, 分流比为10:1.升温程序:初始40 ℃, 保持5 min, 以6 ℃·min-1升至120 ℃.质谱条件:离子源温度230 ℃, 四级杆温度150 ℃.
总溶解性铁利用电感耦合等离子体发射光谱仪进行测定, 氯离子利用电位滴定仪进行测定.
3 结果与讨论(Results and discussion) 3.1 AC对TCE的吸附特征 3.1.1 动力学特征本研究主要是为了解TCE在AC上的吸附动力学特征, 为后续实验确定吸附平衡时间.吸附动力学实验结果如图 1所示, 由图可知, AC吸附TCE在反应前2 h为快速吸附阶段, 吸附量随时间基本呈线性增加趋势;2~6 h为减速吸附阶段, 吸附速率降低, 吸附量呈缓慢增加趋势;6~12 h为缓慢吸附阶段, 这一阶段吸附过程趋于平衡;在12 h时达到吸附平衡, 12 h后为平衡吸附阶段, 吸附量基本不再增加, 因此, 确定吸附平衡时间为12 h.对实验结果进行动力学方程拟合, 符合准一级动力学方程(式(1)), R2值为0.991, 拟合参数如表 1所示.本实验结果与徐翯等(2006)的研究结果一致.
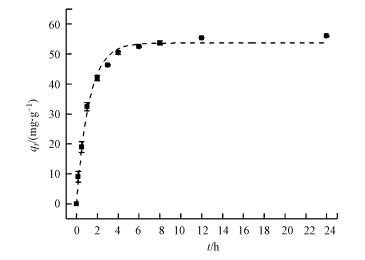 |
| 图 1 AC吸附TCE的动力学拟合结果 Fig. 1 Kinetic of TCE on AC |
| 表 1 AC吸附TCE准一级动力学方程拟合参数 Table 1 Fitting parameters of pseudo \first order kinetics equation for TCE adsorption on AC |
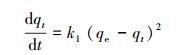
|
(1) |
式中, k1为准一级动力学吸附速率常数(h-1);qe为平衡吸附量(mg·g-1);t为时间(h);qt为t时刻吸附量(mg·g-1).
3.1.2 等温吸附特征等温吸附实验结果如图 2所示, 由于TCE在水中溶解度的限制, 本实验中TCE最高浓度为40 mg·L-1.在0~40 mg·L-1浓度范围内, AC对TCE的吸附量随TCE浓度的增加而增加.对实验结果进行等温吸附模型拟合, 符合Freundlich方程(式(2)), R2值为0.988, 拟合参数如表 2所示.
 |
| 图 2 AC对TCE的等温吸附线 Fig. 2 Isothermal adsorption of TCE on AC(25 ℃) |
| 表 2 AC对TCE吸附的Freundlich方程拟合参数 Table 2 Fitting parameters of Freundlich equation for TCE adsorption on AC |
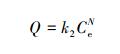
|
(2) |
式中, k2为吸附速率常数(L·mg-1);N为表示非线性吸附强度的参数;Q为平衡时固相吸附量(mg·g-1);Ce为平衡时液相浓度(mg·L-1).
3.2 再生研究 3.2.1 再生过程研究再生过程中pH值变化如图 3a所示, 由图可知, pH值从初始的2.7逐渐减小至1.7, 这是由于再生体系中发生反应(3)~(5), 产生了大量H+(Liang et al., 2008;Liang et al., 2009b).Fe2+催化H2O2体系(芬顿试剂)需要在特定pH值范围(pH=2~4)内才能进行, 因此, 需要加入其它药剂调节pH.而根据式(3)~(5)及图 3a可知, 双氧化体系中的S2O82-不仅能够分解产生SO4-·, 还可以产生大量的H+, 不需要加入其它药剂就能够为体系中的芬顿试剂提供其所需的低pH值环境, 从而促进TCE的氧化去除, 实现AC的再生(Yan et al., 2015).
 |
| 图 3 再生过程中pH值(a)、总溶解性铁浓度(b)及TCE浓度(c)变化 Fig. 3 Changes of solution pH(a), total dissolved iron(b) and TCE(c) in regeneration process |
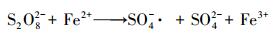
|
(3) |
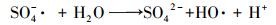
|
(4) |
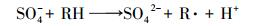
|
(5) |
再生过程中总溶解性铁浓度变化见图 3b, 由图可知, 总溶解性铁浓度随时间逐渐减小, 至反应结束约减少3%.根据公式(3)推测, 总溶解性铁浓度减小的原因是:Fe2+在反应过程中被氧化为Fe3+, 而Fe3+以沉淀的形式附着在AC上, 一方面使溶液中的总溶解性铁浓度减小, 另一方面形成的沉淀堵塞AC吸附孔径, 具体反应过程见式(3).为进一步证实这一结论, 后文中将通过EDS及XPS对AC表面Fe的存在及价态进行分析.
再生过程中, 部分TCE由于解吸作用会重回溶液中.因此, 对再生溶液中的TCE进行测定, 结果如图 3c所示.结果表明, 溶液中TCE的浓度随时间逐渐增大, 12 h后解吸量占总吸附量的5.12%(以氯元素量(mmol)计).
3.2.2 再生产物研究吸附在AC上的TCE被氧化会释放出Cl-(式(6)).对再生过程中的Cl-进行测定, 结果如图 4a所示.由图可知, AC上部分TCE被氧化脱氯生成Cl-, 且浓度逐渐增大, 这与Liang等(2009a)在利用Fe2+催化Na2S2O8再生AC(TCE)的实验中得出的Cl-浓度变化一致.12 h后被氧化为Cl-的TCE占吸附量的63.03%(以氯元素量(mmol)计).为了证明AC是否会吸附氧化生成的Cl-, 从而影响Cl-的测定, 分别配制3个不同Cl-浓度的NaCl溶液进行吸附实验, 结果如图 4b所示.结果表明, 在3个不同浓度条件下, Cl-的浓度在12 h内基本不变.顾广隽等(1985)研究也得出同样结论.因此可以得出, 在此实验条件下, AC对Cl-无吸附作用, 溶液中Cl-的测定不受AC吸附作用的影响.
 |
| 图 4 再生过程中Cl-浓度变化(a)及AC对Cl-的吸附(b) Fig. 4 Changes of Cl- in regeneration process(a) and adsorption of Cl- on AC(b) |
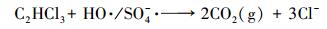
|
(6) |
为了确定再生过程中是否有氧化副产物产生, AC是否会吸附氧化副产物, 以及AC上是否仍吸附有未被氧化的TCE, 分别对再生溶液及再生AC解吸产物进行测定, 结果如图 5a所示.再生溶液中检测到少量1, 1-二氯乙烯(1, 1-DCE), 说明再生过程中发生了如式(7)所示的反应, TCE被不完全氧化为1, 1-DCE.由图可知, 1, 1-DCE浓度较低, 随时间缓慢增加, 最大检出浓度仅占TCE吸附量的0.02%(以氯元素量(mmol)计).再生AC在甲醇中的解吸结果如图 5b所示, 由图可知, 共检测到氯乙烯(VC)及TCE两种物质, 分别占TCE吸附量的0.10%和27.51%(以氯元素量(mmol)计), 这说明再生过程中有少量氧化副产物VC生成(式(8)), 在后续反应中VC又被AC全部吸附.27.51%的TCE从再生AC上解吸, 说明这部分AC上的TCE不能被氧化, 再生过程中始终吸附在AC上占据吸附位点, 阻碍了后续吸附实验中TCE的吸附, 从而降低了AC的再生效率.
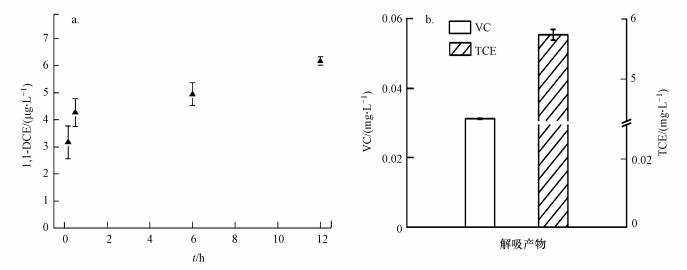 |
| 图 5 再生过程1, 1-二氯乙烯浓度变化(a)及再生AC解吸产物(b) Fig. 5 Changes of 1, 1-DCE in regeneration process(a) and desorption products from regenerated AC(b) |
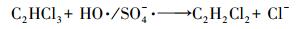
|
(7) |
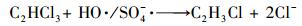
|
(8) |
再生体系氯平衡率等于再生后的氯元素的总量/再生前氯元素的总量.根据所得实验数据及方程式对应关系推导出氯平衡率计算公式, 具体见式(9).利用式(9)对再生前后的体系进行氯平衡率(B)计算, 得出氯平衡率为95.78%, 基本达到平衡.
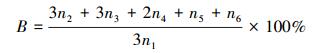
|
(9) |
式中, n1为TCE吸附量(mmol), n2再生溶液中TCE的量(mmol), n3为甲醇中TCE的量(mmol), n4为1, 1-DCE的量(mmol), n5为VC的量(mmol), n6为Cl-的量(mmol), 单位均以氯元素量计.
3.3 吸附容量对比为了计算双氧化体系再生AC的再生效率RE, 将原状AC、再生AC(Re-AC)在同一TCE初始浓度(30 mg·L-1), 同一条件下进行吸附实验.吸附平衡后得到各AC吸附量, 吸附量对比结果如图 6所示.得到两种AC的吸附量后, 通过计算得到AC的再生效率, 计算方法见公式(10)(Narbaitz et al., 1997).
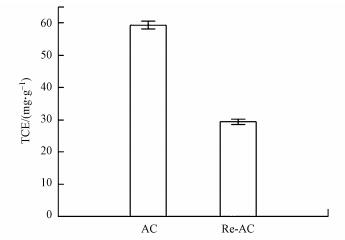 |
| 图 6 原状AC、再生AC吸附量对比 Fig. 6 Adsorption capacities of AC and Re-AC |

|
(10) |
式中, (x/M)R为再生AC吸附量(mg·g-1, 以VOC计), (x/M)V为原状AC吸附量(mg·g-1, 以VOC计).
通过公式(10)计算得出AC再生效率约为50%, 说明在TCE:Fe2+:H2O2:S2O82-=1:9.20:59.79:77.52的条件下再生AC, 再生AC吸附容量约为原状AC的1/2.谭德俊等(2014)在氧化剂质量分数为100%, 活化温度为100 ℃, 再生时间为60 min的条件下利用Na2S2O8对吸附生化废水的AC进行再生, 再生效率为55.98%.再生效率基本相同的前提下, 本研究的再生方法不需要高温活化, 具有耗能低的优点.
3.4 表征 3.4.1 SEM及EDS分析SEM(30万倍)测试结果如图 7所示, 其中, 图 7a为原状AC, 图 7b为再生AC.由图可知, 相比于原状AC, 再生AC表面杂质增多, 孔隙明显减少, 并出现了大的孔洞.EDS测试结果见表 3, 由表可知, C元素含量减小, O元素含量增加, 这说明约有11%的AC在再生过程中会被氧化剂氧化造成炭损失;Cl元素含量增加, 说明再生AC上有含Cl元素的物质, 可能是TCE或其氧化副产物;Fe元素含量增加, 证明了前文对再生溶液中总溶解性铁浓度减少原因的推测, 部分溶液中的溶解性铁附着在AC上.
 |
| 图 7 原状AC(a)和再生AC(b)的SEM图 Fig. 7 SEM images of AC(a) and Re-AC (b) |
| 表 3 原状AC、再生AC EDS分析 Table 3 EDS analysis of AC and Re-AC |
氮气吸附-解吸结果见表 4, 由表可知, 相比于原状AC, 再生AC的比表面积减小了21.70%.由于比表面积是评价AC吸附能力强弱最重要的因素之一, 因此, 比表面积减小会降低再生AC的吸附能力.有研究表明, 吸附孔径也是评价AC吸附能力的重要因素, 适宜的AC孔径(0.5~1.0 nm)有利于TCE在AC上的吸附(Li et al., 2002;Karanfil et al., 2004).从孔径体积及孔径面积的对比结果中可以看出, d < 0.47 nm的孔径体积减少了14.40%, d≤216.63 nm的孔径体积减少了5.17%, d≥0.47 nm的孔径面积减少了26.92%, d>216.63 nm的孔径面积减少了8.96%.因此, 孔径体积及孔径面积的减小是降低再生AC吸附能力的原因之一(Liang et al., 2009a).
| 表 4 原状AC、再生AC氮气吸附-解吸结果分析 Table 4 Nitrogen adsorption-desorption analysis of AC and Re-AC |
通过XPS的2p轨道扫描结果可以判断AC表面是否有Fe及确定Fe存在的价态.若2p1/2轨道上结合能在近725 eV处有特征峰, 可以证明Fe存在, 若2p3/2轨道上结合能在709.3 eV及711.2 eV处有特征峰, 分别可以证明有二价Fe及三价Fe存在(Yamashita et al., 2008;Rey et al., 2009).如图 8a所示, 原状AC在以上3个结合能峰值处均未出峰, 结合表 3中Fe的EDS分析结果, 可知原状AC上有少量Fe, 但由于含量很少, 在XPS谱图上并没有出峰.如图 8b所示, 725 eV及711.2 eV结合能处的特征峰证明了再生AC上三价Fe的存在, 但并未发现二价Fe的特征峰.由此可以得出, 再生AC上的Fe以三价Fe的形式存在.Liang等(2009a)在利用Fe2+催化Na2S2O8再生AC(TCE)的实验中证明了再生AC上存在Fe离子的沉淀.由此可以得出, 再生AC上附着有三价Fe沉淀, 堵塞了AC吸附孔径, 减小了孔径体积及面积, 从而降低了AC再生效率.
 |
| 图 8 原状AC(a)、再生AC(b) XPS Fe 2p分析图 Fig. 8 XPS survey of the Fe 2p regions of AC(a) and RE-AC(b) |
1) AC对TCE的吸附动力学符合准一级动力学模型, 等温吸附符合Freundlich模型.在TCE:Fe2+:H2O2:S2O82-=1:9.20:59.79:77.52(物质的量比)条件下, AC再生效率约为50%.
2) 再生过程中AC吸附的TCE有63.03%被完全氧化为Cl-, 0.02%被氧化为1, 1-DCE, 0.10%被氧化为VC, 5.12%解吸到再生溶液中, AC上仍有27.51%的TCE不能被氧化剂氧化而始终占据着吸附位点, 再生前后氯平衡率为95.78%.
3) 研究表明, ICHP再生AC-TCE可行.AC的炭损失、比表面积、孔隙体积及孔隙面积的减小, 是再生AC吸附能力低于原状AC的主要原因.虽然再生AC吸附效率低于原状AC, 但仍可达到原状AC吸附量的50%, 可以实现TCE的有效吸附并达到AC重复使用的目的.
戴芳天. 2003. 活性炭在环境保护方面的应用[J]. 东北林业大学学报, 2003, 31(2): 48–49.
|
顾广隽, 孙香潭. 1985. 活性炭吸附焦化污水中某些无机离子的行为[J]. 环境化学, 1985, 4(6): 58–62.
|
韩庭苇, 王郑, 朱垠光, 等. 2016. 活性炭的再生方法比较及其发展趋势研究[J]. 化工技术与开发, 2016, 45(10): 44–48.
DOI:10.3969/j.issn.1671-9905.2016.10.014 |
侯立安, 左莉. 2003. 二硫化碳的污染特征与净化材料的筛选试验[J]. 洁净与空调技术, 2003(2): 35–37.
|
Karanfil T, Dastgheib S A. 2004. Trichloroethylene adsorption by fibrous and granular activated carbons: aqueous phase, gas phase, and water vapor adsorption studies[J]. Environmental Science & Technology, 38(22): 5834.
|
Li L, Quinlivan P A, Knappe D R U. 2002. Effects of activated carbon surface chemistry and pore structure on the adsorption of organic contaminants from aqueous solution[J]. Carbon, 40(12): 2085–2100.
DOI:10.1016/S0008-6223(02)00069-6
|
李婷, 王毅霖, 张晓飞, 等. 2013. 浅析活性炭再生技术的发展现状[C]. 中国环境科学学会2013年学术年会. 昆明: 6791-6793
|
Liang C, Bruell C. 2008. Thermally activated persulfate oxidation of trichloroethylene: Experimental investigation of reaction orders[J]. Industrial & Engineering Chemistry Research, 47(9): 2912–2918.
|
Liang C, Lin Y T, Shin W H. 2009a. Persulfate regeneration of trichloroethylene spent activated carbon[J]. Journal of Hazardous Materials, 168(1): 187–192.
DOI:10.1016/j.jhazmat.2009.02.006
|
Liang C, Su H W. 2009b. Identification of sulfate and hydroxyl radicals in thermally activated persulfate[J]. Industrial & Engineering Chemistry Research, 48(11): 472–475.
|
刘守新, 王岩, 郑文超. 2001. 活性炭再生技术研究进展[J]. 东北林业大学学报, 2001, 29(3): 61–63.
|
Narbaitz R M, Cen J. 1997. Alternative methods for determining the percentage regeneration of activated carbon[J]. Water Research, 31(31): 2532–2542.
|
Quinlivan P A, Li L, Knappe D R. 2005. Effects of activated carbon characteristics on the simultaneous adsorption of aqueous organic micropollutants and natural organic matter[J]. Water Research, 39(8): 1663–1673.
DOI:10.1016/j.watres.2005.01.029
|
Rey A, Faraldos M, Casas J A, et al. 2009. Catalytic wet peroxide oxidation of phenol over Fe/AC catalysts: Influence of iron precursor and activated carbon surface[J]. Applied Catalysis B Environmental, 86(1/2): 69–77.
|
Su Y F, Cheng Y L, Shih Y H. 2013. Removal of trichloroethylene by zerovalent iron/activated carbon derived from agricultural wastes[J]. Journal of Environmental Management, 129(129C): 361–366.
|
谭德俊, 赵旭好, 陈泉源. 2014. 基于硫酸根自由基的高级氧化技术原位再生活性炭[J]. 东华大学学报(自然科学版), 2014, 40(5): 633–638.
|
王宝庆, 陈亚雄, 宁平. 2000. 活性炭水处理技术应用[J]. 环境科学导刊, 2000, 19(3): 46–49.
|
王福禄. 2011. Fenton试剂再生活性炭的试验研究[J]. 工业用水与废水, 2011, 42(3): 48–51.
|
翁元声. 2004. 活性炭再生及新技术研究[J]. 给水排水, 2004, 30(1): 86–91.
|
吴琪, 宋乾武, 曾燕艳, 等. 2011. 活性炭再生技术研究进展和发展趋势[J]. 中国环保产业, 2011(10): 14–17.
DOI:10.3969/j.issn.1006-5377.2011.10.004 |
许伟, 刘军利, 孙康. 2016. 活性炭吸附法在挥发性有机物治理中的应用研究进展[J]. 化工进展, 2016, 35(4): 1223–1229.
|
徐翯, 冯流. 2006. 三氯乙烯在天然土壤中的吸附行为及其影响因素[J]. 农业环境科学学报, 2006, 25(s1): 65–68.
|
Yamashita T, Hayes P. 2008. Analysis of XPS spectra of Fe2+, and Fe3+, ions in oxide materials[J]. Applied Surface Science, 254(8): 2441–2449.
DOI:10.1016/j.apsusc.2007.09.063
|
Yan N, Liu F, Xue Q, et al. 2015. Degradation of trichloroethene by siderite-catalyzed hydrogen peroxide and persulfate: Investigation of reaction mechanisms and degradation products[J]. Chemical Engineering Journal, 274: 61–68.
DOI:10.1016/j.cej.2015.03.056
|
曾雪玲, 唐晓东, 卢涛. 2008. 活性炭再生技术的研究进展[J]. 四川化工, 2008, 11(4): 11–15.
|
周琴, 沈健, 黄敏. 2013. 活性炭的制备及再生研究进展[J]. 化学与生物工程, 2013, 30(12): 10–13.
|
 2018, Vol. 38
2018, Vol. 38


