2. 中海油气(泰州)石化有限公司, 泰州 225003
2. Cnooc Oil & Gas(Taizhou) Petrochemical Co. LTD, Taizhou 225003
随着我国化工行业规模的不断扩大, 化工污水的排放量也日益增多, 如何处理大量的化工污水已经成为我国急需解决的水污染问题之一.苯酚及其衍生物由于毒性高、难降解, 并且是化工过程中高分子量的芳香类化合物氧化的中间产物, 因此, 常被用作废水处理的模型化合物(Lin et al., 2003; Santos et al., 2001).湿式氧化技术(WAO)是一种处理高浓度、难降解和高毒性含酚废水的有效方法.然而, WAO的反应条件苛刻、能耗高、对设备材质要求严格, 因此, WAO在实际应用中往往只作预处理技术使用(Debellefontaine et al., 2000; Kim et al., 2011).而利用过渡金属作为催化剂的催化湿式氧化法(CWAO)可以在较低的温度和压力下分解难降解的污染物, 由此降低了反应成本和操作费用(Oliviero et al., 2003; Bhargava et al., 2006).由于固体催化剂容易从被处理污水中分离, 因而受到广泛关注.
目前, 贵金属催化剂(Lousteau et al., 2015; Rocha et al., 2011; Yang et al., 2015; 王建兵等, 2007)和复合金属氧化物催化剂(Chen et al., 2004; 2007)是催化湿式氧化法的主要固体催化剂.由于贵金属催化剂价格昂贵, 并且在含卤素、硫、氮化合物的污水中极容易失活, 因此, 复合金属氧化物催化剂被广泛用作贵金属催化剂的替代品.水滑石是一种层状双金属氢氧化物, 焙烧水滑石后得到的复合金属氧化物催化剂称为水滑石衍生催化剂, 该类催化剂一般具有比表面积大、活性组分分散均匀、稳定性高等优点(Fan et al., 2011; Wang et al., 2012).Vallet等(2012; 2013)利用共沉淀法制备了MgAl水滑石前驱体, 再利用浸渍法将Ni负载于水滑石上, 经焙烧后得到Ni/MgAlO催化剂并将其应用于催化湿式氧化反应过程, 结果表明, 水滑石衍生催化剂表现出良好的催化湿式氧化性能, 连续反应20 h, 催化剂没有明显失活现象, 最高TOC转化率为82%.目前, 利用本体合成的水滑石衍生催化材料应用于催化湿式空气氧化过程的报道较为常见(Ovejero et al., 2013a; 2013b), 但利用原位合成制备的水滑石衍生催化材料应用于催化湿式空气氧化过程的报道较少.鉴于此, 本文采用原位合成的方法在γ-Al2O3的表面合成锌铝水滑石, 再采用浸渍法制备CuO/ZnO-Al2O3水滑石衍生催化材料, 并将其应用于催化湿式空气氧化苯酚过程, 着重探索催化剂的结构和性质对催化氧化苯酚性能的影响, 建立起催化剂的构效关系, 以期为催化湿式空气氧化苯酚废水催化剂的设计提供理论依据.
2 实验部分(Experimental) 2.1 催化剂的制备采用表面原位合成法在γ-Al2O3上制备锌铝水滑石, 具体操作为将10 g γ-Al2O3加入到装有306 mL Zn(NO3)2·6H2O(0.1 mol·L-1)和NH4NO3(0.1 mol·L-1)配成的混合溶液的三口烧瓶中, 在70 ℃下搅拌24 h后, 用氨水(5%)溶液调节pH值至7~8.将氨水和NH4NO3加入去离子水中配置洗涤液, 调节洗涤液的pH值与反应结束后反应体系pH值基本一致.然后用该洗涤液洗涤样品5~7次后在空气中老化1 h, 再用去离子水洗涤到中性, 放入烘箱于70 ℃干燥24 h, 得ZnAl-LDHs/Al2O3, 然后在马弗炉中400 ℃焙烧4 h得到复合金属氧化物, 记为ZnO-Al2O3.
取一定量的ZnO-Al2O3作为载体, 浸渍不同质量分数(5%、10%、20%、30%)的Cu(NO3)2·3H2O(按铜元素计)溶液, 之后放入烘箱中110 ℃干燥12 h, 然后放在马弗炉中500 ℃焙烧3 h得CuO/ZnO-Al2O3.研磨, 压片, 粉碎至80~120目的CuO/ZnO-Al2O3催化剂, 命名为x%CuO/ZnO-Al2O3(x=5、10、20、30).
2.2 催化剂的表征样品的物相组成和结构采用德国Bruker D8型X射线衍射仪测定, 测试条件为:Cu-Kα1靶, 入射波长λ=0.154 nm, 管电压40 kV, 管电流40 mA, 扫描范围2θ=10o~70o;样品的晶粒大小由Scherrer公式计算得到;样品形貌由日本Hitachi公司SU 8010型扫描电子显微镜表征;样品的红外光谱图通过美国赛默飞世尔科技Nicolet 380傅里叶红外光谱仪测得;采用美国Quantachrome公司NOVA 2200E型自动比表面和孔隙度分析仪测定样品的N2吸附脱附等温线, 由BET法计算比表面积, BJH法计算孔容.催化剂的还原性能、铜比表面积(SCu)和铜分散度的测试过程见参考文献(张磊等, 2013; 2015;Zhang et al., 2013a; 2013b).金属溶出采用Agilent 725 ICP-AES分光光度仪测定.
2.3 催化湿式氧化苯酚实验催化湿式空气氧化水中苯酚的实验在带有控温装置的300 mL高压反应釜中进行.将100 mL浓度为500 mg·L-1的苯酚溶液和0.5 g催化剂加入到反应釜中, 并控制温度为30 ℃.通入0.7 MPa空气后, 将反应釜加热到200 ℃, 以此时的温度和压力作为反应温度和压力, 并作为反应的“零点”计时.此后每隔一定时间取1 mL反应液, 将反应液过滤后采用重铬酸钾法分析化学需氧量(COD) (American et al., 2005).COD去除率X采用如下公式计算:
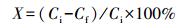
|
(1) |
式中, Ci和Cf分别代表起始和测量样品的COD值(mg·L-1).
3 结果与讨论(Results and discussion) 3.1 形貌和结构分析γ-Al2O3和ZnAl-LDHs/γ-Al2O3的形貌由扫描电子显微镜(SEM)得到, 结果如图 1所示.由图 1a可以看到, γ-Al2O3有均匀的多孔表面.从图 1b可以看出, 一些具有层状结构的不规则的小颗粒均匀地分散在γ-Al2O3的表面, 类似于典型的水滑石的特征形貌, 这与XRD所述的水滑石的特征谱图一致.
 |
| 图 1 γ-Al2O3(a)和ZnAl-LDHs/γ-Al2O3(b)的扫描电镜图 Fig. 1 SEM images of γ-Al2O3 (a) and ZnAl-LDHs/γ-Al2O3 (b) |
图 2a为γ-Al2O3和ZnAl-LDHs/γ-Al2O3的XRD谱图.对比γ-Al2O3载体的特征衍射峰, ZnAl-LDHs/γ-Al2O3在10.3°、20.3°、34.5°和60.3°出现了典型的水滑石晶体(JCPDS 51-0045)结构的(003)、(006)、(012)、(110)特征衍射峰(Cavani et al., 2000), 说明在γ-Al2O3的表面原位合成了锌铝水滑石催化材料.
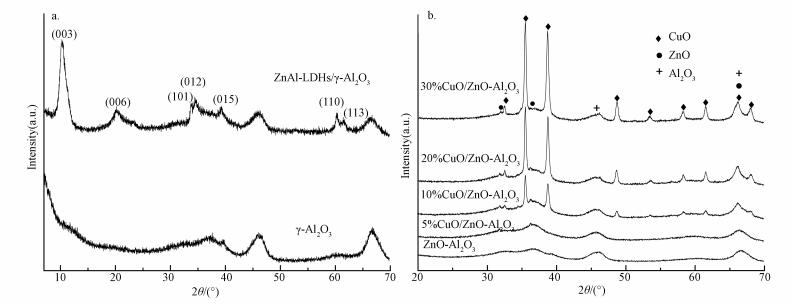 |
| 图 2 γ-Al2O3、ZnAl-LDHs/γ-Al2O3(a)和载体ZnO-Al2O3及不同Cu含量x%CuO/ZnO-Al2O3催化剂(b)的XRD谱图 Fig. 2 XRD patters of γ-Al2O3, ZnAl-LDHs/γ-Al2O3(a) and ZnO-Al2O3 support and prepared x%CuO/ZnO-Al2O3 catalysts with different copper mass fraction(b) |
图 2b为焙烧ZnAl-LDHs/γ-Al2O3后得到的ZnO-Al2O3复合氧化物载体和不同Cu含量x%CuO/ZnO-Al2O3催化剂的XRD谱图.从图中可以看出, 5%CuO/ZnO-Al2O3催化剂和ZnO-Al2O3复合氧化物载体的XRD谱图基本一致, 没有出现CuO的特征衍射峰, 这说明CuO在ZnO-Al2O3复合氧化物载体上高度分散, 这与表 1铜的分散度结果相吻合.当CuO的负载量增加到10%后, 明显出现了CuO的特征衍射峰, 且强度逐渐增加.利用Scherrer公式计算CuO晶粒的大小如表 1所示, 通过计算表明, 负载量从10%到30%, CuO的晶粒大小基本保持不变.
| 表 1 催化剂的物理性质 Table 1 The physical characteristics of the prepared catalyst |
图 3为ZnO-Al2O3载体和不同Cu含量x%CuO/ZnO-Al2O3催化剂的FT-IR谱图.从图 3可以看出, 1635 cm-1的吸收峰归属于载体ZnO-Al2O3层间水分子的震动, 1117 cm-1的吸收峰归属于层间阴离子和邻近原子间的相互作用, 在564 cm-1附近的峰归属于CuO的特征峰, 796 cm-1的峰可能是尖晶石相, 但前面XRD的测试中并没有显示相对应的谱图, 说明样品中尖晶石相结晶度很差或者以无定型存在(Kannan et al., 2004).此外, 在1385 cm-1附近, 仅载体ZnO-Al2O3出现了一个峰, 将其归属为层间少量的硝酸盐的特征峰, 其它4个样品由于焙烧温度相对较高, 硝酸盐已完全转化, 因此, 1385 cm-1附近的峰消失了(Behrens et al., 2009).
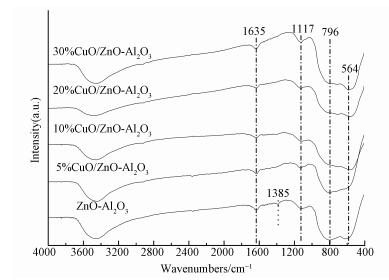 |
| 图 3 载体ZnO-Al2O3和不同Cu含量x%CuO/ZnO-Al2O3催化剂的FT-IR谱图 Fig. 3 FT-IR spectra of ZnO-Al2O3 and prepared x%CuO/ZnO-Al2O3 catalysts with different copper mass fraction |
催化剂的比表面积和孔体积由N2吸附法测定, Cu分散度和Cu比表面积由N2O滴定测定, 结果见表 1.与γ-Al2O3比较, ZnAl-LDHs/γ-Al2O3的比表面积和孔体积都变小, 说明一部分ZnAl-LDHs进入到γ-Al2O3的孔道内部, 这也进一步说明ZnAl-LDHs/γ-Al2O3成功合成.随着Cu含量的增加, 催化剂的比表面积和孔体积也逐渐下降, 这可能是因为载体的部分孔道被催化活性组分占据(Agarwal et al., 2005).从表 1还可以看出, 5%CuO/ZnO-Al2O3催化剂中Cu分散度最大, 为14.16%, 这是因为5%CuO/ZnO-Al2O3催化剂中Cu含量较少, 分散较好, 进而分散度较大.Cu负载量由5%增加到30%时, Cu分散度逐渐降低.另外, 从Cu的比表面积来看, 10%CuO/ZnO-Al2O3催化剂中Cu的比表面积最大, 为5.9 m2·g-1, 5%CuO/ZnO-Al2O3催化剂和30%CuO/ZnO-Al2O3催化剂Cu的比表面最小, 均为4.3 m2·g-1, 这是由铜的负载量和铜的分散度两方面决定的.本课题组前期研究表明(张磊等, 2017), 催化剂中Cu比表面积越大, 活性组分利用率越高, 催化降解苯酚活性越高.
3.3 还原性能分析为了研究催化剂的活性和还原性之间的关系, 给出了不同Cu含量x%CuO/ZnO- Al2O3催化剂的H2-TPR谱图, 结果如图 4所示.在400 ℃之前, 10%CuO/ZnO-Al2O3催化剂出现了2个重叠交错的还原峰, 一个低温还原峰(266 ℃左右, 尖峰)和一个高温还原峰(324 ℃左右, 主峰), 分别对应表相CuO物种的还原和体相CuO物种的还原.其它3组催化剂出现了一个还原峰且还原温度都低于文献报道中CuO的还原温度(340 ℃)(Liu et al., 2002), 对应的都是体相CuO物种的还原.除此之外, 所有催化剂在630~650 ℃出现了一个还原峰, 这可能是一些Cu2+物种进入到ZnO或者Al2O3的晶格当中, 很难被还原出来, 因而表现出的还原峰温度特别高(Hammoud et al., 2015).由于表相铜物种在催化过程中更容易与反应物苯酚接触, 且表相铜物种催化活性更高, 这可能是造成10%CuO/ZnO-Al2O3催化剂催化湿式空气氧化苯酚活性更高的原因之一.
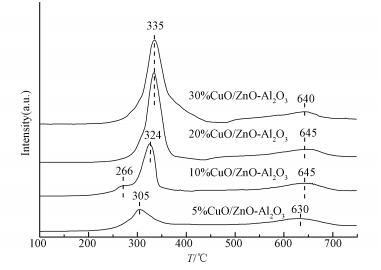 |
| 图 4 不同Cu含量x%CuO/ZnO-Al2O3催化剂的H2-TPR谱图 Fig. 4 H2-TPR profiles of the prepared x%CuO/ZnO-Al2O3 catalysts with different copper mass fraction |
图 5为催化湿式空气氧化水中苯酚的COD去除率.不加入催化剂的空白实验中COD去除率最低, 在反应条件为200 ℃和2 MPa下, 最终(240 min)COD去除率仅为70.6%.Al2O3载体和ZnO-Al2O3复合氧化物的COD去除率略高于空白实验, 说明Al2O3载体和ZnO-Al2O3复合氧化物催化氧化苯酚的活性很低.浸渍CuO后, CuO/ZnO-Al2O3催化剂的催化氧化苯酚活性大幅度提升, 说明CuO为该反应的主要活性物种.其中, 10%CuO/ZnO-Al2O3催化剂的催化性能最佳, 在反应条件为200 ℃和2 MPa下, 最终(240 min)COD去除率可达95.3%, 这是由催化剂的Cu比表面积和还原性质共同决定的.10%CuO/ZnO-Al2O3催化剂的Cu比表面积在所制备的催化剂中最大, Cu比表面积越大, 参与反应的活性位增加, 从而使得催化活性提高.另外, 从H2-TPR中可以看出, 10%CuO/ZnO-Al2O3催化剂明显的出现了表相铜物种, 表相铜物种的出现有利于苯酚氧化反应的进行(张磊等, 2017), 进而使得催化剂活性提高.因此, 10% CuO/ZnO-Al2O3催化剂表现出最佳的催化活性.20%CuO/ZnO-Al2O3和30%CuO/ZnO-Al2O3催化剂的催化活性紧随其后, 相比于5%CuO/ZnO-Al2O3催化剂, 铜含量的增加使得苯酚与活性组分的接触几率增加, 因此, 20%CuO/ZnO-Al2O3和30%CuO/ZnO-Al2O3催化剂的催化活性高于5%CuO/ZnO-Al2O3催化剂.综上所述, 催化剂催化降解苯酚的能力与活性组分的含量和活性组分在载体上的分散情况有关.
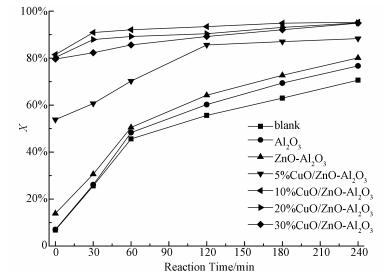 |
| 图 5 催化湿式空气氧化苯酚性能 Fig. 5 CWAO of phenol over the uncatalyst and prepared catalysts |
催化湿式空气氧化催化剂的稳定性和重复利用是催化剂的一项重要指标, 如果催化剂稳定性差, 不仅会造成浪费还会引起二次污染, 因此, 需要对所制备的催化剂进行稳定性和重复性实验.对反应后的10%CuO/ZnO-Al2O3催化剂进行回收, 考查反应次数对COD去除率的影响, 结果如表 2所示.10%CuO/ZnO-Al2O3催化剂在每次使用后的催化活性略有下降, 但重复使用5次后, 仍保持了较高的COD去除率(91.5%), 说明通过该方法所制备的10%CuO/ZnO-Al2O3催化剂具有较好的稳定性, 可多次重复使用.
| 表 2 10%CuO/ZnO-Al2O3催化剂的重复使用性 Table 2 The repetition of the 10% CuO/ZnO-Al2O3 catalyst |
当催化剂在高温条件下催化氧化降解小分子酸时, 金属元素会从固相催化剂中流失到水溶液中.金属元素在溶液中的流失是造成催化剂失活的重要因素之一, 同时金属的溶出也会造成水质的二次污染.因此, 本文采用ICP-AES测定了经10%CuO/ZnO-Al2O3和30%CuO/ZnO-Al2O3催化剂处理苯酚一次后溶液中的金属含量.结果发现, 在用10%CuO/ZnO-Al2O3催化剂催化氧化苯酚后的水样中, 铜、锌和铝的溶出量分别为14.7、5.7和8.7 mg·L-1, 在用30%CuO/ZnO-Al2O3催化剂催化氧化苯酚后的水样中, 铜、锌和铝的溶出量分别为22.2、3.1、1.64 mg·L-1, 两个催化剂铜、锌和铝元素溶出量都保持在了较低的水平.
3.7 反应前后催化剂结构对比图 6为新鲜的10%CuO/ZnO-Al2O3催化剂和反应一次后的10%CuO/ ZnO-Al2O3催化剂的XRD谱图.由Scherrer公式计算得, 新鲜的10%CuO/ZnO-Al2O3催化剂的CuO晶粒大小为34 nm, 反应后的CuO晶粒大小为37 nm, 反应前后CuO晶粒变化不大.
 |
| 图 6 反应前后10%CuO/ZnO-Al2O3催化剂XRD谱图 Fig. 6 XRD patterns of fresh and used 10%CuO/ZnO-Al2O3 catalysts |
采用表面原位合成法成功地在γ-Al2O3的表面合成了锌铝水滑石, 再将焙烧后的锌铝水滑石作为载体采用浸渍法制备了CuO/ZnO-Al2O3水滑石衍生催化剂, 并着重探讨了CuO含量对CuO/ZnO-Al2O3催化剂的结构-性能影响.结果表明, Cu比表面积和催化剂的还原性质是影响催化活性的主要原因, 当CuO负载量为10%时, 催化剂表现出最佳的性能, 在200 ℃、2 MPa空气、苯酚初始浓度500 mg·L-1的条件下, COD去除率为95.3%.重复使用5次后, COD去除率仍能达到91.5%.
Agarwal V, Patel S, Pant K K. 2005. H2 production by steam reforming of methanol over Cu/ZnO/Al2O3 catalysts: transient deactivation kinetics modeling[J]. Applied Catalysis A-General, 279(1): 155–164.
|
American Public Health Association(APHA). 2005. Standard methods for the examination of water and wastewater[S]. Washington, D. C. : American Water Works Association, and Water Environment Federation
|
Behrens M, Kasatkin I, Kühl S, et al. 2009. Phase-pure Cu, Zn, Al hydrotalcite-like materials as precursors for copper rich Cu/ZnO/Al2O3 catalysts[J]. Chemistry of Materials, 22(2): 386–397.
|
Bhargava S K, Tardio J, Prasad J, et al. 2006. Wet oxidation and catalytic wet oxidation[J]. Industrial & Engineering Chemistry Research, 45: 1221–1258.
|
Cavani F, Trifiro F, Vaccari A. 1991. Hydrotalcite-type anionic clays:preparation, properties and applications[J]. Catalysis Today, 11: 173–301.
DOI:10.1016/0920-5861(91)80068-K
|
Chen I P, Lin S S, Wang C H. 2007. CWAO of phenol using CeO2/γ-Al2O3 with promoter- Effectiveness of promoter addition and catalyst regeneration[J]. Chemosphere, 66: 172–178.
DOI:10.1016/j.chemosphere.2006.05.023
|
Chen I P, Lin S S, Wang C H, et al. 2004. Preparing and characterizing an optimal supported ceria catalyst for the catalytic wet air oxidation of phenol[J]. Applied Catalysis B-Environmental, 50: 49–58.
DOI:10.1016/j.apcatb.2003.12.019
|
Debellefontaine H, Foussard J N. 2000. Wet air oxidation for the treatment of industrial wastes chemical aspects, reactor design and industrial applications in Europe[J]. Waste Management, 20: 15–25.
|
Fan G, Sun W, Wang H, et al. 2011. Visible-light-induced heterostructured Zn-Al-In mixed metal oxide nanocomposite photocatalysts derived from a single precursor[J]. Chemical Engineering Journal, 174: 467–474.
DOI:10.1016/j.cej.2011.09.054
|
Hammoud D, Gennequin C, Aboukaïs A, et al. 2015. Steam reforming of methanol over x% Cu/Zn-Al 400 500 based catalysts for production of hydrogen:preparation by adopting memory effect of hydrotalcite and behavior evaluation[J]. International Journal of Hydrogen Energy, 40(2): 1283–1297.
DOI:10.1016/j.ijhydene.2014.09.080
|
Kannan S, Rives V, Knözinger H. 2004. High-temperature transformations of Cu-rich hydrotalcites[J]. Journal of Solid State Chemistry, 177(1): 319–331.
DOI:10.1016/j.jssc.2003.08.023
|
Kim K H, Ihm S K. 2011. Heterogeneous catalytic wet air oxidation of refractory organic pollutant in industrial wastewaters:A review[J]. Journal of Hazardous Materials, 186: 16–34.
DOI:10.1016/j.jhazmat.2010.11.011
|
Lin S S Y, Chang D J, Wang C H, et al. 2003. Catalytic wet oxidation of phenol by CeO2 catalyst-effect of reaction conditions[J]. Water Research, 37: 793–800.
DOI:10.1016/S0043-1354(02)00422-0
|
Liu Y, Hayakawa T, Suzuki K, et al. 2002. Highly active copper/ceria catalysts for steam reforming of methanol[J]. Applied Catalysis A-General, 223(1): 137–145.
|
Lousteau C, Besson M, Descorme C. 2015. Catalytic wet air oxidation of ammonia over supported noble metals[J]. Catalysis Today, 241: 80–85.
DOI:10.1016/j.cattod.2014.03.043
|
Oliviero L, Barbier J, Duprez D. 2003. Wet air oxidation of nitrogen-containing organic compounds and ammonia in aqueous media[J]. Applied Catalysis B-Environmental, 40: 163–184.
DOI:10.1016/S0926-3373(02)00158-3
|
Ovejero G, Rodriguez A, Vallet A, et al. 2013a. Catalytic wet air oxidation of a non-azo dye with Ni/MgAlO catalyst[J]. Chem Eng J, 215-216: 168–173.
DOI:10.1016/j.cej.2012.11.028
|
Ovejero G, Rodriguez A, Vallet A, et al. 2013b. Ni/Fe-supported over hydrotalcites precursors as catalysts for clean and selective oxidation of basic yellow 11:reaction intermediates determination[J]. Chemosphere, 90: 1379–1386.
DOI:10.1016/j.chemosphere.2012.07.067
|
Rocha M A L, Angel G D, Torres-Torres G, et al. 2015. Effect of the Pt oxidation state and Ce3+/Ce4+ ratio on the Pt/TiO2-CeO2 catalysts in the phenol degradation by catalytic wet air oxidation (CWAO)[J]. Catalysis Today, 250: 145–154.
DOI:10.1016/j.cattod.2014.09.016
|
Santos A, Yustos P, Durban B, et al. 2001. Catalytic wet oxidation of phenol:kinetics of the mineralization[J]. Industrial & Engineering Chemistry Research, 40: 2773–2781.
|
王建兵, 祝万鹏, 王伟, 等. 2007. 催化剂Ru/ZrO2-CeO2催化湿式氧化苯酚[J]. 环境科学学报, 2007, 28(7): 1460–1465.
|
Vallet A, Besson M, Ovejero G, et al. 2012. Treatment of a non-azo dye aqueous solution by CWAO in continuous reactor using a Ni catalyst derived from hydrotalcite-like precursor[J]. Journal of Hazardous Materials, 227-228: 410–417.
DOI:10.1016/j.jhazmat.2012.05.081
|
Vallet A, Ovejero G, Rodriguez A, et al. 2013. Ni/MgAlO regeneration for catalytic wet air oxidation of an azo-dye in trickle-bed reation[J]. Journal of Hazardous Materials, 244-245: 46–53.
DOI:10.1016/j.jhazmat.2012.11.019
|
Wang Q, Zhang X, Zhu J, et al. 2012. Preparation of stable dispersions of layered double hydroxides (LDHs) in nonpolar hydrocarbons:new routes to polyolefin/ LDH nanocomposites[J]. Chemical Communications, 48: 7450–7452.
DOI:10.1039/c2cc32708b
|
Yang S X, Besson M, Descorme C. 2015. Catalytic wet air oxidation of succinic acid over Ru and Pt catalysts supported on CexZr1-xO2 mixed oxides[J]. Applied Catalysis B - Environmental, 165: 1–9.
DOI:10.1016/j.apcatb.2014.09.057
|
张磊. 2013. 甲醇水蒸汽重整制氢催化剂的研究[D]. 大连: 大连理工大学. 18-22
|
张磊, 雷俊腾, 田园, 等. 2015. 前驱体和沉淀剂浓度对CuO/ZnO/CeO2-ZrO2甲醇水蒸气重整制氢催化剂性能的影响[J]. 燃料化学学报, 2015, 43: 1366–1374.
DOI:10.3969/j.issn.0253-2409.2015.11.012 |
张磊, 赵吉昊, 许家维, 等. 2017. CeO2-ZrO2固溶体在催化湿式空气氧化苯酚废水中的作用[J]. 环境科学学报, 2017, 37(7): 2642–2648.
|
Zhang L, Pan L W, Ni C J, et al. 2013a. CeO2-ZrO2-promoted CuO/ZnO catalyst for methanol steam reforming[J]. International Journal of Hydrogen Energy, 38: 4397–4406.
DOI:10.1016/j.ijhydene.2013.01.053
|
Zhang L, Pan L W, Ni C J, et al. 2013b. Effect of precipitation aging time on the performance of CuO/ZnO/CeO2-ZrO2 for methanol steam reforming[J]. Journal of Fuel Chemistry and Technology, 41: 883–888.
DOI:10.1016/S1872-5813(13)60038-9
|
 2018, Vol. 38
2018, Vol. 38


