2. 合肥工业大学智能研究院, 合肥 230009;
3. 安徽省环境科学研究院, 合肥 230061
2. Intelligent Manufacturing Institute of Hefei University of Technology, Hefei 230009;
3. Anhui Academy of Environmental Science Research, Hefei 230061
多环芳烃(Polycyclic aromatic hydrocarbons, 简称PAHs)是指有两个至多个苯环通过共价键构成的稠环不饱和芳香烃, 因具有“三致”作用(致癌、致畸和致突变)、生物富集能力和环境持久性而受到科学家的广泛关注(Wang et al., 2013).同时, PAHs来源极为广泛, 因而在环境中大量存在.PAHs的来源通常分为人为和自然来源, 其中, 人为来源包括各种化石燃料、木材等有机质的不完全燃烧或在还原气氛下热解生成, 以及人为造成的各种石油排放或泄漏, 而自然源包括生物合成及火山活动等.尽管自然来源的PAHs对局部地区环境具有重要影响(Lammel et al., 2013), 但现代环境介质主要受到人为来源PAHs的影响(Zhang et al., 2009).不同来源的PAHs进入环境中, 可以在不同介质间迁移.水体是接纳PAHs的重要载体, 可以以自由溶解态、胶体结合态、悬浮颗粒物结合态、沉积物结合态及生物结合态等形式存在(李海燕等, 2014;朱樱等, 2009).由于PAHs溶解度低、正辛醇-水分配系数(Kow)较大, 因此, 易于吸附在悬浮颗粒物、沉积物和生物体中.但悬浮颗粒物和生物体中PAHs最终亦会通过生物沉降过程进入沉积物.
因此, 沉积物成为水体中PAHs重要的汇.但当外界输入通量减少时, 水体中PAHs浓度相应降低, 此时沉积物中PAHs可以通过沉积物再悬浮、分子扩散和生物扰动等过程再次进入水体, 成为水体PAHs的二次污染物源.同时, PAHs在水体-沉积物间的扩散过程亦对其在水生食物链中的迁移具有重要作用, 可以客观评价沉积物生态风险.因此, 明确污染物在水体-沉积物界面扩散的趋势和通量是认识污染物在水生环境归趋的一个重要科学问题, 同时对于认识沉积物中污染物的释放、吸附和迁移等过程具有重要意义, 亦有助于预测沉积物污染自然恢复的时间, 可为进一步制定相应的保护政策和修复方案提供科学依据.尽管该过程在研究污染物的生物地球化学循环和生态风险等方面具有重要意义, 但相对研究却较少.主要原因在于此界面交换过程取决于上层水体和沉积物孔隙水中污染物浓度梯度, 但孔隙水体积相对较小, 在采样过程中容易受到干扰, 再加上孔隙水在沉积物中流动较慢, 一定采样量就可能造成污染物从沉积物中解析出来, 不能真正反映实际状况.近年来, 原位被动采样技术的发展和应用在一定程度上解决了这一采样技术难题.如Liu等(2013)设计了一套利用低密度聚乙烯薄膜为吸附剂的被动采样器, 该装置可同时测定水体和沉积物孔隙水中滴滴涕等疏水性有机污染物, 并结合Fuck扩散定律, 计算了污染物在水体-沉积物界面上的扩散通量.但这一方法对污染物在薄膜吸附及其定量上要求严格, 同时受到成本和野外状况的限制, 难以大范围应用于环境监测和研究中.基于数学方法而发展的各种模型则可以有效地避免这些不足, 尤其基于逸度方法的多介质扩散模型的发展, 有效地模拟了多种污染物在多个界面上的扩散过程, 并且不需要测定沉积物孔隙水中污染物浓度.由于该方法简单可靠, 在国内外得到了广泛应用(Sweetman et al., 2002; Wania et al., 1999).自20世纪70年代, Mackay等(1979)第一次将逸度模型这一概念进行描述以来, 各类模型得到了不断的丰富和发展, 从最初的一级模型(污染物在环境介质内平衡且均匀分布, 没有物质的流入流出, 且不存在降解反应)发展到目前的Ⅳ模型(动态描述污染物在环境介质中的迁移转化和降解反应).基于逸度概念发展的各种模型已被广泛应用到生物累积效应评价、优先污染物筛选、污染物持久性和长距离迁移潜力研究、多介质环境迁移转化和人体暴露风险评价(Bennett et al., 2004; Zhang et al., 2012)等方面.
本课题组先前的研究表明, 巢湖流域沉积物中PAHs存在明显的空间差异性, 主要表现为:南淝河(NFR)及其入湖口处沉积物受到明显的历史工业废水排放影响(Ren et al., 2015b; Zhang et al., 2016), 可能已影响了底栖生物的生存环境(Wang et al., 2011b), 比未受工业废水排放影响区域高1~2个数量级(Ren et al., 2015b; Wang et al., 2011b).但巢湖水体中PAHs污染较其他研究区域相对较轻, 同时未呈明显的空间差异性(Qin et al., 2013; 任琛, 2015).巢湖流域水体和沉积物中PAHs污染的差异性主要在于两种介质中PAHs的来源不同.沉积物曾富集了历史上工业废水排放的PAHs, 但影响范围较小, 而水体接纳了近期排放的废水.随着针对巢湖流域环境保护措施的实施, 各种污水处理厂相继建设和运行, 大大减小了流域PAHs外源污染的输入, 因此, 水体中PAHs污染较轻.同时研究亦表明, 由于巢湖流域长期处于富营养化状态, 大量藻类的生长可以快速吸附污染物, 并最终沉降至底部沉积物中, 因此, 降低了水体中污染物的浓度, 进一步导致污染物在沉积物中富集(Wang et al., 2016; Wu et al., 2015).因此, 随着PAHs外源污染逐渐得到有效控制, 内源污染问题变得日益突出.污染物在水体-沉积物间的分子扩散过程是污染物归趋的重要过程之一, 然而对于这方面的研究至今未见报道.
因此, 本研究基于先前的研究结果, 结合巢湖流域内49个采样点水体和沉积物中17种PAHs的浓度数据, 通过逸度模型构建PAHs在水体-沉积物间的扩散过程, 明确沉积物作为水体二次污染源的可能性, 并判断不同污染物的分子扩散趋势的空间差异性, 明确沉积物有机碳中炭黑的存在对分子扩散过程的影响.
2 研究方法与数据来源(Study methods and data sources) 2.1 沉积物-水体界面扩散过程污染物在环境介质间的扩散可以通过在特定介质中的逃逸趋势来描述, Lewis将其定义为逸度f (Mackay et al., 1990), 单位为Pa.f值可以通过介质中化合物浓度进行换算.当化合物在两相介质中的f值相等时, 则反映了该化合物在这两种介质间达到了平衡, 反之, 则处于不平衡状态, 化合物会从f值较高的介质向f值较低的介质扩散.因此, 可以通过比较某化合物在两相邻介质之间的f比率(fugacity quotient)来判断它的传输方向(Mackay, 1979).一般而言, 化学物质在沉积物与水体中的f值可以通过它的浓度Cs(ng·g-1)、Cw(ng·L-1)、沉积物密度ρs(kg·m-3)和在两种介质中的逸度容量Zs和Zw(mol·m-3·Pa-1)来定义, 即:
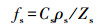
|
(1) |
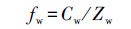
|
(2) |
Zs和Zw则可以根据有机碳归一化分配系数(Koc)、有机碳含量(foc)和亨利常数(H)进行计算:
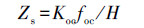
|
(3) |
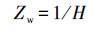
|
(4) |
因此, 化合物在沉积物与水体中的逸度比率可写为:
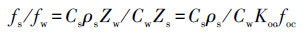
|
(5) |
其中, Koc可以通过Kow进行估算, 即:
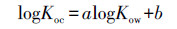
|
(6) |
当fs/fw=1时, 表示化合物在沉积物和水体间处于平衡, 当fs/fw>1时, 表示化合物从沉积物向水体扩散, 反之, 当fs/fw < 1时, 表示化合物从水体向沉积物扩散.式(5)也可转化为式(7):

|
(7) |
式中, ff为逸度分数, 逸度分数与逸度比率无本质区别, 二者都可反映化合物的扩散方向, 但化合物的逸度分数在0~1.0间变化, 更利于细致比较, 而化合物的逸度比率可能跨越几个数量级, 不利于细微比较差别(Wang et al., 2011a).当ff=0.5时, 表示物质在沉积物和水中处于平衡, 当ff>0.5时, 表示物质从沉积物向水体扩散, 而当ff < 0.5时, 则表示物质从水体向沉积物扩散.
由于ff大小由Cs、Cw、Koc、foc、ρs 5个参数决定, 其中, foc、ρs变化较小, 误差可忽略.Cs、Cw和Koc变化范围较大, 因此, 它们的测量误差对ff影响更大.Koc主要由Kow决定, 文献(Wang et al., 2011a)报道了Cs、Cw和Koc的实验再现性(即相对标准偏差, RSD)为60%, 再利用误差传递公式(式(8)), 得到ff的范围为0.2~0.8(ff=0.5±0.3).
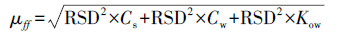
|
(8) |
也有文献(Cui et al., 2016)报道ff的RSD为40%, 即ff的范围为0.3~0.7(ff=0.5±0.2).但二者都认为, 若考虑到其他参数的RSD, ff的RSD会更大, 可达到80%, 即ff范围为0.1~0.9(ff=0.5±0.4).由于本研究并未对污染物浓度的RSD进行定量, 因此, 把前人认为合理的范围作为本实验的RSD, 即本研究认为ff的RSD为80%, 所以当ff=0.1~0.9时, PAHs处于平衡态; 当ff>0.9时, PAHs从沉积物向水体扩散; 当ff < 0.1时, PAHs从水体向沉积物扩散.
炭黑是土壤/沉积物中的重要组成部分(Song et al., 2002; Xiao et al., 2004), 具有芳香化合物结构特性, 可以“锁定”疏水性有机污染物, 因此, 它对PAHs的吸附是非线性的, 具有不可逆性(Ran et al., 2002; Weber et al., 1999).大量的研究均表明, 沉积物有机碳中炭黑的存在, 可以“锁定”沉积物中疏水性有机污染物, 大大降低它们在溶解态中的浓度, 进一步影响污染物的迁移性、生物可利用性和降解速率(Ghosh et al., 2000; Karickhoff et al., 1979), 因此, 研究沉积物有机碳中炭黑对污染物的环境过程影响具有重要意义.考虑到炭黑的存在, 污染物在沉积物-水体间的分配常数(Ksw)可以重新定义为(Bärring et al., 2002):
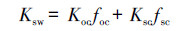
|
(9) |
而fs/fw亦由公式(5)变成公式(10):
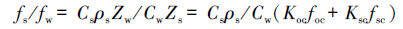
|
(10) |
式中, Ksc表示碳黑标准化分配系数, fsc表示沉积物中碳黑含量.本研究中Ksc值取自文献(Wang et al., 2011a).由于本研究没有实测沉积物中fsc, 而文献中报道沉积物中fsc通常为foc的1%~10%(Gustafsson et al., 1997).因此, 本研究假设碳黑含量分别占有机碳含量的1%和10%两种可能的情况.
2.2 研究区域及样品采集巢湖是我国五大淡水湖之一, 位于淮河和长江流域之间, 紧邻合肥市区, 流域内水系发达, 共有33条支流直接与巢湖湖区相连.湖区水域面积达730 km2, 其中, 西半湖主要通过南淝河(NFR)和十五里河接纳市区污水, 东半湖主要接纳农业区域的地表径流.巢湖流域包括2市8县, 流域总人口877万人, 是安徽省重要的商品粮生产基地、淡水水产基地及旅游观光基地, 经济社会地位突出.本研究中所涉及的支流包括南淝河(NFR)、杭埠河(HBR)、烔炀河(TYR)和裕溪河(YXR).其中, 南淝河是巢湖西北部主要入湖河流, 入湖流量占巢湖总径流量的10.9%, 流经合肥市市区, 是巢湖流域污染物的重要输入途径(Wang et al., 2011b).杭埠河是巢湖西南方向的一条入湖河流, 主要流经农业区域, 入湖流量占巢湖总径流量的65.1%.烔炀河是巢湖东北方向的一条入湖河流, 亦流经农业区域, 而裕溪河位于巢湖东南角, 是巢湖唯一一条出湖河流, 与长江连接.本研究分别在4条支流(NFR、HBR、TYR、YXR)和湖区采集了上层水样和表层沉积物, 4条支流内采样点数分别为16、10、5和9个, 东、西半湖各选择了5和3个采样点, 分别标记为CH1~CH5和CH6、CH8、CH9(图 1).
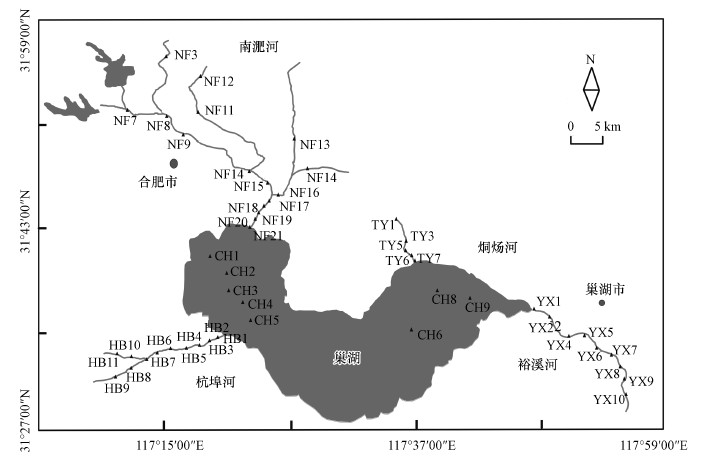 |
| 图 1 采样点分布位置示意图 Fig. 1 Map of sampling location |
采样时间集中于2013年7月和8月, 采用不锈钢抓斗采集表层沉积物样品, 采集过的表层沉积物样品用铝箔纸包装密封放入密封袋中, 编号记录, 置于0 ℃冰盒中冷冻保存.在相同采样点, 分别采集了水体样品.采集前先用采样点的湖水将事先洗净的1 L棕色瓶润洗3遍, 再采集1 L水样.编号记录后置于水样采集箱中避光保存, 于24 h内运回实验室冷冻保存或置于干燥阴暗处, 于72 h内完成水样预处理.沉积物分别经冷冻干燥、磨碎过筛、溶剂萃取、净化分离和仪器分析等处理过程, 而水体样品经过滤后采用二氯甲烷液液萃取, 再经层析柱净化后通过GC-MS定量分析, 详细操作过程描述分别见文献(Ren et al., 2015a; Zhang et al., 2016; 任琛, 2015).本实验分析了16种美国EPA优控的PAHs和苝.利用德国Elementar公司的Vario TOC Cube仪分析了沉积物foc.测定foc前, 样品分别采用HCl和纯净水洗涤数次并烘干, 以此除去样品中的无机碳.
为了评价样品处理的效率和重现性, 所有样品在萃取前均加入5种氘代PAHs(包括Nap-d8、Ace-d10、Phe-d10、Chr-d12和Per-d12)作为回收率指示物, 每分析12个沉积物样品, 加入一组空白样和平行样.空白样品中, 除萘以外的PAHs总浓度均小于样品浓度平均值的10%, 沉积物样品中5种回收率指示物(Nap-d8、Ace-d10、Phe-d10、Chr-d12和Per-d12)的平均回收效率分别为67%±24%、103%±21%、107%±23%、112%±21%和87%±18%, 所有水体样品中5种回收率指示物(Nap-d8、Ace-d10、Phe-d10、Chr-d12和Per-d12)的回收效率分别为54.6%±11.6%、63.1%±13.9%、75.2%±17.2%、115.0%±13.8%和99.6%±16.7%, 最终各化合物的浓度统计数据见表 1.为了叙述简便, 本文将研究的17种PAHs按苯环多寡分为低环(2~3环)、中环(4~5环)和高环(5~6环).各污染物的Kow值从文献(Wang et al., 2011a)中获得, 公式(6)中的a、b值分别采用0.989和-0.346(Karickhoff, 1981).ρs取值为2.0×103 kg·m-3(Kong et al., 2014)
| 表 1 巢湖流域沉积物和水中PAHs浓度 Table 1 PAHs concentrations in sediment and water in Chaohu lake basin |
所有数据分析在Excel 2007中完成, 水体和沉积物中PAHs的正态分布检验采用Kolmogorov-Smirnov检验方法(SPSS 20.0).空间分布图在Golden Surfer 9.0中实现, 不同化合物的ff值及其炭黑影响下的ff值变化分布图在Sigma Plot中完成.
为了明确水体和沉积物中各污染物浓度的空间差异性, 本研究采用变异系数表征指标的离散程度, 因为它消除了测量尺度和量纲的影响, 可以比较两组不同量纲数据, 其定义见公式(11).
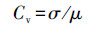
|
(11) |
式中, σ表示沉积物或水体中∑17PAHs浓度的标准偏差, μ表示对应的浓度均值.一般认为:Cv≤ 0.1, 表示弱变异; 0.1 < Cv < 1, 表示中等变异, Cv ≥1, 表示强变异.本研究中, Cvsed(i)和Cvwat(i)分别表示沉积物和水体中PAHs浓度变异系数, i表示某种或某些PAHs.
3 结果与讨论(Results and discussion) 3.1 沉积物与水体PAHs的空间变异水体中17种PAHs浓度(Σ17PAHs)为5.75~276 ng·L-1, 算术均值为98.6 ng·L-1, 所有污染物的浓度均符合正态分布(p值均大于0.05), 变异系数变化范围为0.739~2.040.沉积物中Σ17PAHs含量为10.7~33100 ng·g-1(以干重计), 所有化合物含量和foc值均符合对数正态分布(p>0.05), 变异系数变化范围为1.32~3.46.一般而言, 正态分布反映了数据分布较为均一, 比较集中于整体均值附近, 但对数正态分布则反映大部分样品浓度较低, 但少数样品浓度极高, 只有通过对数转化后, 才能使数据集中于整体几何均值附近(王学松等, 2007).由此可知, 较水体而言, 沉积物中PAHs含量呈较为明显的空间差异.通过变异系数可知, 水体中低环PAHs的变异系数要低于高环PAHs, 但沉积物中则呈相反的规律, 即沉积物中低环PAHs的变异系数大于高环PAHs(表 1).主要原因在于低环PAHs在水体中易于通过水-气、水-沉积物、水-颗粒物交换, 减小它们在水体中的空间差异性.但高环PAHs易于吸附于颗粒物中并进一步沉降至底部沉积物, 导致了底部沉积物高环PAHs不断累积, 因此, 在沉积物中高环PAHs的空间差异性较小.同时, 水体中各污染物和总浓度的空间变异系数小于沉积物, 如水体中∑17PAHs浓度的变异系数Cvwat(∑17PAHs)为0.7, 属于中等变异, 但沉积物中∑17PAHs含量的变异系数Cvsed(∑17PAHs)为2.2, 属于强变异, 表明沉积物中∑17PAHs含量的空间变异较强.主要原因在于, 南淝河沉积物明显受到历史工业排放污染影响, 如南淝河中游附近一家钢铁厂在1956年成立, 截止1999年, 该企业共计排放出3700万t工业废水(《合肥钢铁集团有限公司志》编辑委员会, 2001).而其它采样点主要受农业径流的影响(Zhang et al., 2016).由于污染源的不同, 流域内沉积物中PAHs呈现明显的空间差异性, 南淝河、杭埠河、烔炀河、裕溪河和巢湖沉积物中∑17PAHs含量分别为8861、499、105、305和772 ng·g-1, NFR沉积物中含量高于其它区域几十倍.因此, 南淝河内高残留是巢湖流域沉积物中含量空间变异大的主要原因.南淝河、杭埠河、烔炀河、裕溪河和巢湖水体中∑17PAHs浓度分别为72、47、136、87和219 ng·L-1, 基本处于同一个数量级.水体中PAHs主要反映当前水质特征.随着各种环境保护措施的实施, 环巢湖逐渐建设和运行多座污水处理系统, 大大减少了污染物的直接排放, 水体直接接纳点源污染的可能性减小, 因此, PAHs在水体中的空间变异性较小.同时大气干湿沉降可能是水体中PAHs的一个重要来源(Li et al., 2009), 湖泊上空空气对流通畅, 干湿沉降通量空间差异性较小, 亦可能是导致它们在水体中较为均一分布的另一个原因.另外, 水体易于流动交换, 可减小污染物的空间差异性.由于Per来源于自然成因, 但它在沉积物与水体中的变异系数分别为1.3和1.1, 均大于1.0, 属于强变异, 这表明沉积物与水体中自然来源PAHs浓度的空间变异均较大, 这可能与沉积物中有机碳的组成含量有关.
3.2 逸度分数ff通过式(1)~(7)计算出各采样点各PAHs的ff值, 结果表明(图 2a), 2~3环PAHs的ff均值大于0.9, 其中, 93%采样点处2~3环PAHs的ff值都大于0.9, 表明低环PAHs主要从沉积物向水体扩散, 仅7%采样点处低环PAHs的ff值介于0.1~0.9, 表明少量低环PAHs处于平衡态.4环PAHs的ff均值介于0.1~0.9, 表明整体处于平衡态, 其中, 47%采样点处ff值大于0.9, 反映了从沉积物向水体扩散过程, 53%站点处于平衡状态.57%采样点处5环PAHs(除了Per)的ff值大于0.9, 表示从沉积物向水体扩散过程, 42%采样点的ff值介于0.1~0.9之间, 处于平衡态, 1%的采样点处ff值小于0.1, 揭示了从水体向沉积物扩散过程.Per与其它5环PAHs来源不同, 因此, 扩散方向也可能存在差异, 其中, 88%采样点Per的ff值大于0.9, 反映了其主要从沉积物向水体扩散过程, 而12%采样点的ff值介于0.1~0.9之间, 处于平衡态.6环PAHs的ff值在15%的采样点大于0.9, 反映了从沉积物向水体扩散过程, 但77%的站点处于平衡态, 而8%的采样点处6环PAHs则从水体向沉积物扩散.由以上分析可知, PAHs的ff值随化合物环数增大而减小.其中, 低环PAHs和Per的ff值在较小的范围内波动, 几乎所有站点ff值均大于0.9, 反映了这些污染物在巢湖流域水体-沉积物间交换过程基本相似, 没有明显的空间差异性, 主要从沉积物向水体扩散.中、高环PAHs(Per除外)的ff值波动较大, 说明它们在研究区域内的水体-沉积物间扩散存在明显空间差异性, 其中, 中环PAHs在两种介质间基本处于平衡状态或从沉积物向水体扩散, 而高环PAHs更多的处于平衡态, 说明PAHs环数越多, 越倾向于从水体扩散至沉积物中.随着PAHs环数的增多, 水溶性降低, Kow值增大, 更倾向于吸附在沉积物TOC中(蓝家程等, 2015).结果亦说明了巢湖流域沉积物作为二次污染源是上层水体中PAHs(尤其低环和部分中环PAHs)的一个重要来源.各种污染排放的PAHs进入巢湖水体后通过沉降等过程在沉积物中富集, 通过分子扩散过程再次进入水体, 造成水体的二次污染.
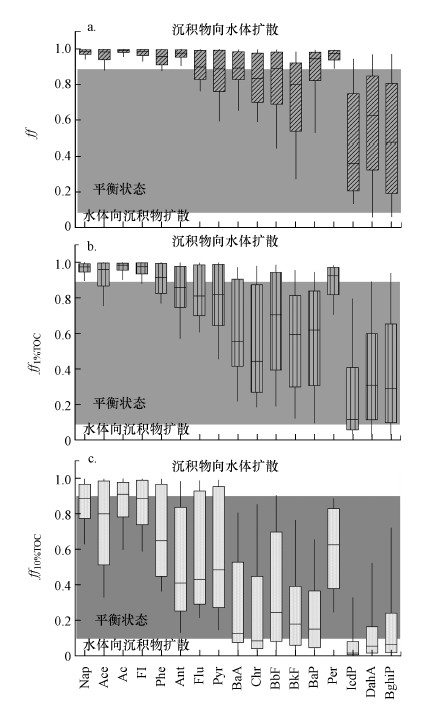 |
| 图 2 不同PAHs在巢湖流域沉积物-水相的逸度分数ff (a.仅考虑TOC影响时ff值, b.假设炭黑含量为TOC1%时ff值; c.假设炭黑含量为TOC10%时ff值) Fig. 2 Fugacity fraction(ff) of individual PAH species between sediment and water in Chaohu lake basin(a.ff values affected by only TOC; b.ff values affected by TOC and black carbon(with 1% of TOC); c.ff values affected by TOC and black carbon(with 10% of TOC)) |
如上所述, 低环PAHs和Per的ff值波动较小, 但高环PAHs的ff值则在较大范围内波动, 反映了低环PAHs和Per在巢湖流域水体-沉积物间的交换过程基本相似, 而高环化合物在水体-沉积物界面上的扩散存在明显的空间差异性.为了更好地阐述不同污染物的扩散差异性, 特以Per和BghiP为例进行详细论述, 因为二者物理化学性质比较接近(高环、较大的logKow值等), 且它们在巢湖流域具有较高的残留浓度, 但它们的来源则明显不同.Per主要指示自然来源(Jiang et al., 2000), 而BghiP则指示人为活动中的热解来源(Yan et al., 2005).
图 3是Per和BghiP的扩散方向空间分布图.结果表明, 43个采样点处Per均从沉积物向水体扩散, 6个采样点处于平衡状态, 因此, 反映了底部沉积物是巢湖流域水体中Per的重要来源.但对BghiP而言, 其在水体-沉积物间扩散存在明显的空间差异性, 对于南淝河而言, 位于工业排放源上游的采样点处BghiP基本处于平衡状态, 但下游其主要从沉积物向水体扩散, 明显地揭示了长期的工业污水排放导致了污染物在下游沉积物中富集, 然而随着排放的减少, 沉积物作为水体二次污染源向水体不断传输污染物.而其它区域采样点处BghiP基本上处于平衡状态, 其中, 有5个采样点(3个位于南淝河中, 2个位于烔炀河中)处BghiP从水体向沉积物扩散, 反映了这些地区沉积物仍然作为PAHs的存储库, 不断积累PAHs.
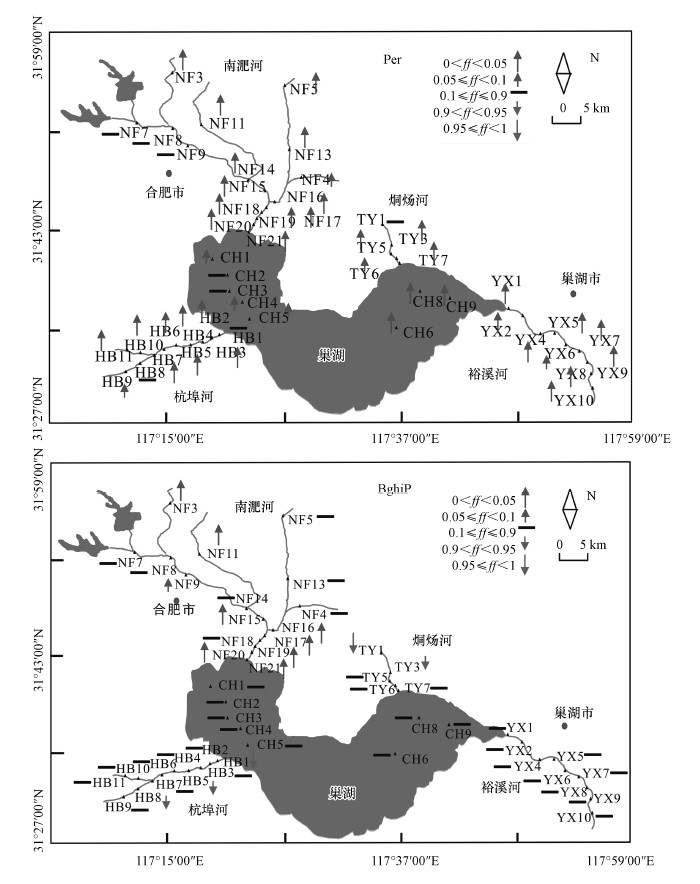 |
| 图 3 巢湖流域Per和BghiP的逸度分数的空间分布 Fig. 3 The spatial distribution offugacity fraction of Perylene and Benzo[g, h, i]perylene in Chaohu lake basin |
结果显示(图 2b和2c), 当改变沉积物有机碳中炭黑含量时, 明显改变了污染物在水体-沉积物间的交换趋势.如当fsc分别为1%foc和10%foc时, 20%和54%采样点2~3环PAHs扩散方向发生了变化, 污染物由从沉积物向水体扩散过程改为平衡状态, 或从水体向沉积物扩散.炭黑对Per的扩散影响与2~3环PAHs类似.而对中高环PAHs的影响更为显著, 如fsc分别为1%foc和10%foc时, 17%和55%采样处4环PAHs扩散方向发生了变化, 污染物在半数以上采样点仍处于平衡态, 但部分采样点PAHs从水体向沉积物汇集.31%和82%采样点处5环(除Per)PAHs扩散方向发生了变化, 污染物主要从沉积物向水体扩散变成了处于平衡状态或向沉积物富集, 34%和73%采样点处6环PAHs扩散方向发生了变化, 且污染物从原先主要处于平衡状态变为主要向沉积物富集.由此可见, 不考虑炭黑存在时, 巢湖流域大部分区域PAHs主要从沉积物向水体扩散或者在两者之间平衡, 当考虑炭黑存在时, 污染物主要处于平衡状态或者从水体向沉积物汇集.多数采样区域低环PAHs在水体-沉积物间达到了平衡状态, 但中环PAHs仍然主要处于平衡状态, 高环PAHs则从平衡状态转为向沉积物富集, 沉积物成为这些污染物的存储库.因此, 沉积物有机碳中炭黑的存在明显地改变着污染物的环境行为和归趋, 炭黑含量越高对污染物的影响越大, 而且随着污染物疏水性的增加, 炭黑的影响效果越明显.主要原因在于炭黑的存在改变了沉积物对疏水性有机污染物的吸附能力, 而且炭黑对这些污染物的吸附是一种“锁定”吸附(不可逆过程), 大大增加了沉积物对污染物的吸附潜力, 减小了污染物在水体中自由溶解态浓度.
4 结论(Conclusions)巢湖流域沉积物中PAHs含量的空间差异性与水体不同, 其中, 沉积物中∑17PAHs含量属于强变异, 而水体属于中等变异.二者之间不同的主要原因在于南淝河富集了历史残留的PAHs, 导致该区域沉积物中PAHs含量远远大于其它采样区域, 但水体接纳近期污染排放, 在巢湖流域未呈现明显的空间差异性.17种PAHs的ff大致随环数增大而减小, 整体上, 低环PAHs和Per的ff均值都大于0.9, 表示其从沉积物向上层水体释放, 中高环PAHs(除了Per)的ff均值介于0.1~0.9, 表示其处于平衡态.自然来源的Per在巢湖流域主要从沉积物向水体扩散, 反映了沉积物是水体中Per的重要来源.BghiP在南淝河下游区域从沉积物向水体扩散, 其它区域主要处于平衡状态或从水体向沉积物聚集, 揭示了历史上残留的PAHs可以通过界面交换成为水体的二次污染源.因此, 为保障南淝河水体环境, 需要对南淝河及其入湖口区域的沉积物采取治理措施.炭黑对PAHs在沉积物-水两相的扩散有重要影响, 能促使其从水体向沉积物富集, 且对高环PAHs的扩散影响更大.当沉积物中fsc为1%foc时, 炭黑对PAHs扩散影响不明显, 当沉积物中fsc为10%foc时, 炭黑对PAHs扩散影响较明显, 巢湖流域一半以上区域的PAHs扩散方向发生了改变.
Bärring H, Bucheli T D, Broman D, et al. 2002. Soot-water distribution coefficients for polychlorinated dibenzo-p-dioxins, polychlorinated dibenzofurans and polybrominated diphenylethers determined with the soot cosolvency-column method[J]. Chemosphere, 49(6): 515–523.
DOI:10.1016/S0045-6535(02)00389-2
|
Bennett D H, Furtaw E J. 2004. Fugacity-based indoor residential pesticide fate model[J]. Environmental Science and Technology, 38(7): 2142–2152.
DOI:10.1021/es034287m
|
Cui S, Fu Q, Li T X, et al. 2016. Sediment-water exchange, spatial variations, and ecological risk assessment of polycyclic aromatic hydrocarbons(PAHs) in the Songhua River, China[J]. Water, 8(8): 334.
|
Ghosh U, Gillette J S, Luthy R G, et al. 2000. Microscale location, characterization, and association of polycyclic aromatic hydrocarbons on harbor sediment particles[J]. Environmental Science and Technology, 34(9): 1729–1736.
DOI:10.1021/es991032t
|
Gustafsson Ö, Haghseta F, Chan C, et al. 1997. Quantification of the dilute sedimentary soot phase:Implications for PAH speciation and bioavailability[J]. Environmental Science and Technology, 31(1): 203–209.
DOI:10.1021/es960317s
|
《合肥钢铁集团有限公司志》编辑委员会. 2001. 合肥钢铁集团有限公司志(1996-2000)[M]. 北京: 冶金工业出版社.
|
Jiang C, Alexander R, Kagi R I, et al. 2000. Origin of perylene in ancient sediments and its geological significance[J]. Organic Geochemistry, 31(12): 1545–1559.
DOI:10.1016/S0146-6380(00)00074-7
|
Karickhoff S W. 1981. Semi-empirical estimation of sorption of hydrophobic pollutants on natural sediments and soils[J]. Environmental Science and Technology, 10(8): 833–846.
|
Karickhoff S W, Brown D S, Scott T A. 1979. Sorption of hydrophobic pollutants on natural sediments[J]. Water Research, 13(3): 241–248.
DOI:10.1016/0043-1354(79)90201-X
|
Kong X Z, He W, Qin N, et al. 2014. Modeling the multimedia fate dynamics of g-hexachlorocyclohexane in a large Chinese lake[J]. Ecological Indicators, 41: 65–74.
DOI:10.1016/j.ecolind.2014.01.024
|
Lammel G, Heil A, Stemmler I, et al. 2013. On the contribution of biomass burning to POPs(PAHs and PCDDs) in air in Africa[J]. Environmental Science and Technology, 47(20): 11616–11624.
DOI:10.1021/es401499q
|
Li J, Cheng H R, Zhang G, et al. 2009. Polycyclic aromatic hydrocarbon(PAH) deposition to and exchange at the air-water interface of Luhu, an urban lake in Guangzhou, China[J]. Environmental Pollution, 157(1): 273–279.
DOI:10.1016/j.envpol.2008.06.039
|
蓝家程, 孙玉川, 肖时珍. 2015. 多环芳烃在岩溶地下河表层沉积物-水相的分配[J]. 环境科学, 2015, 36(11): 4081–4087.
|
李海燕, 段丹丹, 黄文, 等. 2014. 珠江三角洲表层水中多环芳烃的季节分布、来源和原位分配[J]. 环境科学学报, 2014, 34(12): 2963–2972.
|
Liu H H, Bao L J, Zhang K, et al. 2013. Novel passive sampling device for measuring sediment-water diffusion fluxes of hydrophobic organic chemicals[J]. Environmental Science and Technology, 47(17): 9866–9873.
DOI:10.1021/es401180y
|
Mackay D. 1979. Finding fugacity feasible[J]. Environmental Science and Technology, 13(10): 1218–1223.
DOI:10.1021/es60158a003
|
Qin N, He W, Kong X Z, et al. 2013. Ecological risk assessment of polycyclic aromatic hydrocarbons(PAHs) in the water from a large Chinese lake based on multiple indicators[J]. Ecological Indicators, 24: 599–608.
DOI:10.1016/j.ecolind.2012.08.019
|
Ran Y, Huang W, Rao P S C, et al. 2002. The role of condensed organic matter in the nonlinear sorption of hydrophobic organic contaminants by a peat and sediments[J]. Journal of Environmental Quality, 31(6): 1953–1962.
DOI:10.2134/jeq2002.1953
|
任琛. 2015. 巢湖流域多环芳烃的分布、来源与生态风险评价[D]. 合肥: 合肥工业大学
|
Ren C, Wu Y, Zhang S, et al. 2015a. PAHs in sediment cores at main river estuaries of Chaohu Lake:implication for the change of local anthropogenic activities[J]. Environmental Science and Pollution Research, 22(3): 1687–1696.
DOI:10.1007/s11356-014-3141-z
|
Ren C, Wu Y, Zhang S, et al. 2015b. PAHs in sediment cores at main river estuaries of Chaohu Lake:implication for the change of local anthropogenic activities[J]. Environmental Science and Pollution Research, 22(3): 1687–1696.
DOI:10.1007/s11356-014-3141-z
|
Song J Z, Peng P A, Huang W L. 2002. Black carbon and kerogen in soils and sediments1.Quantification and characterization[J]. Environmental Science and Technology, 36(18): 3960–3967.
DOI:10.1021/es025502m
|
Sweetman A J, Cousins I T, Seth R, et al. 2002. A dynamic level Ⅳ multimedia environmental model:application to the fate of polychlorinted biphenyls in the United Kingdom over a 60-year period[J]. Environmental Toxicology and Chemistry, 21(5): 930–940.
DOI:10.1002/etc.v21:5
|
Wang D G, Alaee M, Byer J, et al. 2011a. Fugacity approach to evaluate the sediment-water diffusion of polycyclic aromatic hydrocarbons[J]. Journal of Environmental Monitoring, 13(6): 1589–1596.
DOI:10.1039/c0em00731e
|
Wang J Z, Zhang K, Liang B, et al. 2011b. Occurrence, source apportionment and toxicity assessment of polycyclic aromatic hydrocarbons in surface sediments of Chaohu, one of the most polluted lakes in China[J]. Journal of Environmental Monitoring, 13(12): 3336–3342.
DOI:10.1039/c1em10599j
|
Wang J Z, Bai Y S, Wu Y, et al. 2016. Occurrence, compositional distribution, and toxicity assessment of pyrethroid insecticides in sediments from the fluvial systems of Chaohu Lake, Eastern China[J]. Environmental Science and Pollution Research, 23(11): 10406–10414.
DOI:10.1007/s11356-015-5831-6
|
Wang J Z, Zhu C Z, Chen T H. 2013. PAHs in the Chinese environment:levels, inventory mass, source and toxic potency assessment[J]. Environmental Science-Processes and Impacts, 15(6): 1104–1112.
DOI:10.1039/c3em00070b
|
Wania F, Mackay D, Li Y F, et al. 1999. Global chemical fate of a-hexachlorcyclohexane.1.evaluation of a global distribution model[J]. Environmental Toxicology and Chemistry, 18(7): 1390–1399.
DOI:10.1002/etc.v18:7
|
Weber W J, Huang W L, Le B, et al. 1999. Geosorbent organic matter and its relationship to the binding and sequestration of organic contaminants[J]. Colloids and Surfaces.A:Physicochemical and Engineering Aspects, 151(1): 167–179.
|
Wu Y, Zhang S, Ren C, et al. 2015. Residues of organophosphorus insecticides in sediment around a highly eutrophic lake, Eastern China[J]. Journal of Soils and Sediments, 15(2): 436–444.
DOI:10.1007/s11368-014-1011-4
|
王学松, 秦勇. 2007. 利用对数正态分布图解析徐州城市土壤中重金属元素来源和确定地球化学背景值[J]. 地球化学, 2007, 36(1): 98–102.
|
Xiao B H, Yu Z Q, Huang W L, et al. 2004. Black carbon and kerogen in soils and sediments.2.their roles in equilibrium sorption of less-polar organic pollutants[J]. Environmental Science and Technology, 38: 5842–5852.
DOI:10.1021/es049761i
|
Yan B Z, Abrajano T A, Bopp R F, et al. 2005. Molecular tracers of saturated and polycyclic aromatic hydrocarbon inputs into Central Park Lake, New York City[J]. Environmental Science and Technology, 39(18): 7012–7019.
DOI:10.1021/es0506105
|
Zhang L, Bai Y S, Wang J Z, et al. 2016. Identification and determination of the contribution of iron-steel manufacturing industry to sediment-associated polycyclic aromatic hydrocarbons(PAHs) in a large shallow lake of eastern China[J]. Environmental Science and Pollution Research, 23(21): 22037–22046.
DOI:10.1007/s11356-016-7328-3
|
Zhang R R, Zhan C S, He Z P, et al. 2012. Review of environmental multimedia models[J]. Environmental Forensics, 13(3): 216–224.
DOI:10.1080/15275922.2012.702328
|
Zhang Y X, Tao S. 2009. Global atmospheric emission inventory of polycyclic aromatic hydrocarbons(PAHs) for 2004[J]. Atmospheric Environment, 43(4): 812–819.
DOI:10.1016/j.atmosenv.2008.10.050
|
朱樱, 吴文婧, 王军军, 等. 2009. 小白洋淀水-沉积物系统多环芳烃的分布、来源与生态风险[J]. 湖泊科学, 2009, 21(5): 637–646.
|
 2018, Vol. 38
2018, Vol. 38


