2. 华中师范大学环境生物医学实验室, 武汉 430079
2. Laboratory of Environment Biomedicine, Central China Normal University, Wuhan 430079
作为评价大气污染的重要指示物之一, 可吸入细颗粒物PM2.5(空气动力学直径≤2.5 μm)污染被认为是当前国内最有害的环境暴露问题之一(阚海东, 2012).据2014年发布的2013年城市空气PM2.5年均浓度数据显示, 包括武汉在内的全国32座主要城市的PM2.5年均浓度均不符合国家标准(0.035 mg·m-3), 都达到了0.07 mg·m-3以上.武汉市环保局在2013年发布的空气质量通报称, 该年PM2.5浓度(≥80 μg·m-3)超标天数为177 d, 超标率达48.5%, 为2004年以来该市空气质量最差的一年(蔡翠, 2014).因此, 对2013年武汉中心城区洪山区的家庭住户进行室内PM2.5采集分析研究是很有必要的.
PM2.5污染与潜在的健康风险密切相关, 室内空气PM2.5暴露相比室外(大气)PM2.5污染而言, 更应该受到普遍的关注(Bai et al., 2003).美国的一项权威调查报告显示(Klepeis et al., 2001), 成人日常活动时间中每天约有80%的时间是在室内度过的, 老人和儿童在室内活动的时间甚至更高.事实上, 一些研究也表明(Geller et al., 2002), 室内PM2.5的来源与室外不同, 而且室内PM2.5的浓度或许比室外PM2.5浓度更高.根据Liu等(2004)的研究显示, 调查的北京地区49个室内公共场合中约有20%的区域PM2.5浓度超过65 μg·m-3, 反映出室内PM2.5暴露程度不容忽视.越来越多的研究也表明(Trasande et al., 2005; Liu, 2012), PM2.5的暴露与过敏性疾病有着一定的联系, PM2.5浓度越高, 其所暴露的人群患过敏性疾病的发病率就会升高;然而, 室内PM2.5暴露产生的毒性是否受微观环境的影响目前尚不清楚.
本研究对武汉市洪山区的10户家庭进行环境调查, 分别收集过敏儿童与非过敏儿童的室内PM2.5, 对二者PM2.5成分中含碳组分进行简单分析, 并通过检测PM2.5暴露对小鼠巨噬细胞的形态及吞噬功能的影响, 以细胞活力、乳酸脱氢酶漏出率等指标作为细胞毒性指示, 比较过敏与非过敏儿童室内PM2.5的细胞毒性, 以期为进一步探究室内PM2.5暴露与过敏性疾病的联系提供一定的参考依据.
2 材料与方法(Materials and methods) 2.1 实验动物7周龄SPF级((24±1) g)雌性KM小鼠(实验动物合格证号:SCXK(鄂)2008-0005;实验动物质量合格证:42000600003915、42000600004123), 购买自湖北省疾病预防控制中心实验动物中心.
2.2 主要仪器与试剂仪器:PM2.5环境采样器(AirChek XR5000, 美国SKC Inc.)、QMA石英膜(直径46.2 mm, 美国Whatman)、碳气溶胶分析仪(美国Sunset Laboratory Inc.)、真空离心浓缩仪(Centrivap®, 美国Labconco)、荧光梅标仪(FLX800, 美国Bio-Tek)、超净工作台(SW-CJ-2D, 中国苏州净化)、倒置显微镜(TE2000-S, 日本Nikon).
试剂:RPMI 1640培养基、胎牛血清(Gibco)、噻唑蓝(MTT)购自美国Sigma-Aldrich公司, 小鼠LDH酶联免疫试剂盒购自南京建成生物科技有限公司, 其他化学试剂均为国产分析纯.
2.3 PM2.5采样时间和采样点采样时间为2013年10—12月, 每日采样时长均为8 h, PM2.5采样器设置的空气流量为1.5 L·min-1.采样点为武汉市洪山区的10户家庭室内, 当时监测的室内PM2.5浓度为200~500 μg·m-3, 室内温度变化为17~22 ℃, 相对湿度为55%~70%.本研究先对170户家庭中10~12岁的儿童进行问卷调查, 该问卷调查表参照American Thoracic Society-Division of Lung Disease(ATS-DLD)改进而来, 再实时走访家庭, 筛选出的10户家庭中, 儿童环境居住的时间>3年, 且将其按表 1所示进行分组, 在过敏儿童的室内PM2.5实验组中, 5个家庭的儿童出现一种或一种以上的过敏性症状;而非过敏儿童的室内PM2.5实验组中, 5个家庭的儿童健康, 没有过敏症状.
| 表 1 实验分组信息 Table 1 Experimental grouping information |
采样后的QMA石英滤膜(直径46.2 mm)经干燥处理后, 将滤膜剪成1~2 cm2的小块, 置于容量瓶中用三蒸水浸润;再超声振荡3次, 每次20 min, 以洗脱滤膜表面的大颗粒物.振荡液经4层纱布过滤, 滤液经4 ℃、14000 r·min-1离心30 min, 用已称重且洁净的EP管收集下层滤液, 滤液混匀后, 再经真空离心浓缩仪处理6 h, 残留于EP管底的即为PM2.5.称重后, 用PBS配成所需浓度, 混匀并灭菌, 4 ℃保存.实验前40 kHz、20 ℃超声振荡15 min, 混匀使用.
2.5 PM2.5中含碳组分分析含碳组分(也称碳气溶胶)是PM2.5中主要的化学成分, 据调查显示(Seinfeld et al., 1998), 其在城市空气PM2.5中占比可高达40%, 通常主要分为有机碳(OC)和元素碳(EC).采用碳气溶胶分析仪对PM2.5中含碳组分进行检测, 可区分过敏与非过敏儿童室内PM2.5成分中碳来源的不同, 其检测步骤参照Gao等(2012)的研究.
2.6 PM2.5上菌落数的统计PM2.5上的附着物(如真菌)可影响PM2.5介导的细胞毒性.对PM2.5上菌落数的统计分析, 可区分过敏与非过敏儿童室内PM2.5的生物特性.将分别从过敏与非过敏儿童的起居室、卧室和室外收集2 h的PM2.5置于真菌培养基, 在恒温培养箱中培养观察, 统计第3 d和第5 d的菌落数, 并拍照记录.
2.7 巨噬细胞的分离和培养25只SPF级雌性KM小鼠随机分为3组, 分别记为空白组、过敏儿童室内PM2.5实验组、非过敏儿童室内PM2.5实验组, 两实验组各为5例, 每例的小鼠只数为2只, 实验重复2次.选择雌性实验动物的原因是:雌性小鼠的腹部较雄鼠大, 经腹腔注射1 mL 6%可溶性淀粉后, 可刺激小鼠腹腔产生更多的巨噬细胞.小鼠适应喂养3 d后, 实验按如下步骤进行:①脱颈处死实验小鼠, 然后用75%酒精浸泡1~2 min, 移入超净工作台中, 使小鼠仰卧固定于解剖板上, 用手术直剪充分剪开小鼠腹部皮肤;②用眼科镊稍提起腹腔, 并用眼科剪剪开一个小口, 从腹腔内缓慢注射约3 mL无菌PBS, 重复吹打数次后抽出洗液, 置于离心管内;③250 r·min-1离心10 min后弃上清, 用移液枪加入1~2 mL含10%小牛血清的RPMI-1640培养基, 轻轻吹打混匀, 制成细胞悬液, 同时用台盼蓝染液估计细胞的存活率, 要求细胞存活率在90%以上;④将悬浮细胞先铺板于6孔板2 h后, 用PBS洗去未贴壁细胞, 同时取少许细胞在光镜下观察, 细胞形态多样, 有钝圆形突起, 经HE染色鉴定为巨噬细胞;待巨噬细胞计数后, 调整细胞密度为l × l09个·L-1, 移入96孔板中, 每孔180 μL, 再加入不同浓度的PM2.5染毒液20 μL, 使PM2.5终浓度分别为0、10、200 μg·mL-1, 混匀后置于培养箱中培养.
2.8 PM2.5暴露浓度的选择与分组过敏与非过敏儿童室内收集的PM2.5分别暴露于巨噬细胞24 h和48 h.PM2.5暴露浓度参考贾玉巧等(2011)及郭翔等(2012)的研究, 选择设置为0 μg·mL-1 (空白)、10 μg·mL-1 (低剂量)、200 μg·mL-1(高剂量).以贾玉巧等(2011)研究中的最高浓度200 μg·mL-1作为本研究的高剂量, 以郭翔等(2012)研究中染毒浓度10 μg·mL-1作为本研究的低剂量.24 h的实验分组如下:对照组、非过敏儿童室内10 μg·mL-1 PM2.5、非过敏儿童室内200 μg·mL-1 PM2.5、过敏儿童室内10 μg·mL-1 PM2.5、过敏儿童室内200 μg·mL-1 PM2.5.48 h的实验分组如下:对照组、非过敏儿童室内200 μg·mL-1 PM2.5、过敏儿童室内200 μg·mL-1 PM2.5.
2.9 PM2.5暴露的巨噬细胞的形态观察和吞噬能力检测巨噬细胞经PM2.5暴露24 h后, 用PBS迅速吹洗2~3次, 以消除粒子的影响, 吉姆萨染色剂(1:9)染色固定, 室温干燥15 min, 再使用显微镜观察巨噬细胞形态.
巨噬细胞经PM2.5暴露48 h后, 用PBS洗去粒子后吹至悬浮, 再与鸡红细胞(CRBC)共培养30 min.随后取少许培养液制成装片, 吉姆萨染色剂染色固定.巨噬细胞的吞噬能力通过吞噬鸡红细胞进行检测, 结果用吞噬率(R)和吞噬指数(PI)表示:
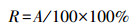
|
(1) |
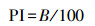
|
(2) |
式中, A表示吞噬CRBC的巨噬细胞数, B表示吞噬细胞吞噬的CRBC总数.
2.10 PM2.5暴露的巨噬细胞的细胞毒性检测巨噬细胞的细胞活力测定:PM2.5诱导的细胞毒性是通过MTT比色法测定的(Li et al., 2010).MTT是一种黄色的噻唑盐, 它在活细胞内能被脱氢酶还原成蓝色沉淀物, 实验方法简言之, 巨噬细胞(37 ℃、5% CO2培养箱中培养)经PM2.5分别暴露24 h和48 h后, 每孔加MTT染液(5 mg·mL-1, 用PBS (pH=7.4)配)20 μL, 孵育4 h后, 终止培养.小心吸弃孔内上清液, 向96孔板中每孔加入150 μL二甲基亚枫(DMSO), 再置于黑暗的培养箱中低速振荡10 min, 使结晶物充分融解.然后选择490 nm波长比色, 测定各孔的OD值.
巨噬细胞释放的乳酸脱氢酶(LDH)测定:PM2.5诱导的细胞损伤是通过乳酸脱氢酶比色法测定的(Bagchi, 1995).经PM2.5分别暴露24 h和48 h后的巨噬细胞, 会释放乳酸脱氢酶, 通过检测LDH活性作为细胞毒性指示, 具体操作根据LDH试剂盒的标准程序进行.
2.11 统计学分析实验数据采用平均值±标准差表示, 采用Origin 6.1软件进行统计分析, 组间的差异分析通过单因素方差分析(ANOVA)结合t检验(Tukey test)确定, p < 0.05为差异显著, p < 0.01为差异极显著, 统计图由GraphPad Prism 5.0软件绘制.
3 结果(Results) 3.1 室内PM2.5成分中含碳组分的分析有机碳和元素碳是PM2.5成分中含碳组分的重要指标, 是区分PM2.5来源与差异的关键指标之一.图 1显示了过敏与非过敏儿童室内PM2.5的有机碳和元素碳数据.PM2.5的来源通常与有机碳和元素碳有关, 而有机碳和元素碳含量分别受季节影响而变化, 二者同一天波动范围分别在0.413~1.087、0.052~0.151 μg·m-3之间.实验数据表明, 过敏儿童室内PM2.5中有机碳和元素碳碳的含量明显高于非过敏儿童的室内PM2.5中有机碳和元素的含量, 通过研究二者PM2.5中有机碳和元素碳含量的变化, 可以区分碳气溶胶粒子的来源, 也可间接反映过敏与非过敏儿童室内PM2.5存在的差异.
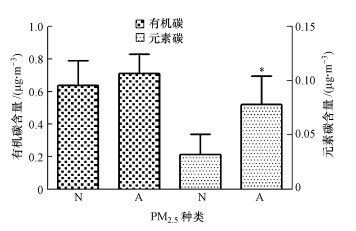 |
| 图 1 室内PM2.5的有机碳和元素碳含量(N:非过敏儿童室内PM2.5;A:过敏儿童室内PM2.5;*p < 0.05) Fig. 1 The organic carbon and elemental carbon concentrations of indoor PM2.5 during 8 h |
PM2.5产生的影响很大程度上与其复杂的成分密切相关.除了分析室内PM2.5化学成分外, 还对其所处环境进行了菌落数统计分析.图 2显示了真菌培养第5 d的外观, 图 3显示了第3 d和第5 d真菌的菌落数统计结果.过敏儿童室内第3 d和第5 d真菌的菌落数平均值分别为16.6和49.0个;相应地, 非过敏儿童室内菌落数平均值分别为14.4和41.9个.图中也显示, 过敏儿童的室内真菌菌落数较多.以上实验结果表明, 随着时间的增加, 过敏儿童的室内PM2.5可能携带更多的真菌.
 |
| 图 2 第5 d的真菌外观图(G1~G5表示非过敏儿童室内实验组, G6~G10表示对应的过敏儿童室内实验组;L、B、O分别表示起居室、卧室和室外) Fig. 2 Fungal appearance of 5th day |
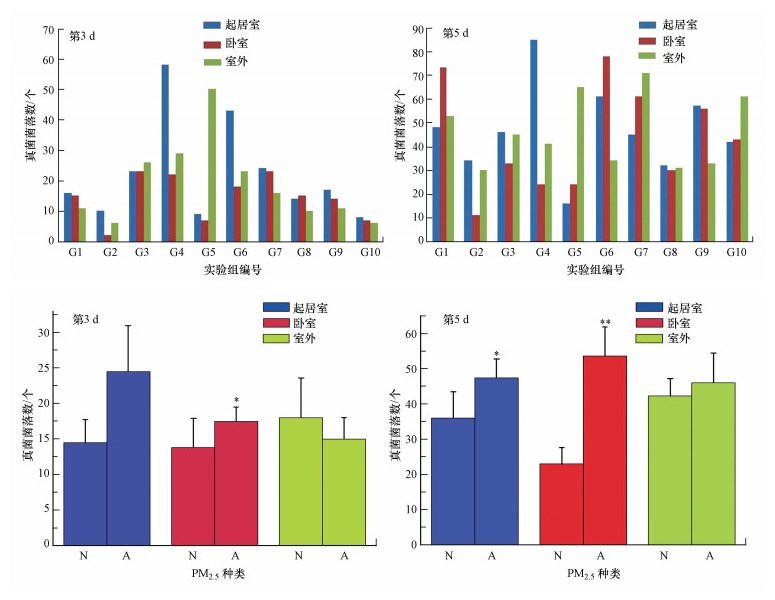 |
| 图 3 室内第3 d和第5 d的真菌菌落数(N:非过敏儿童室内PM2.5;A:过敏儿童室内PM2.5;*p < 0.05, **p < 0.01) Fig. 3 Numbers of fungi colonies of indoor on the 3rd and 5th day |
巨噬细胞与PM2.5共培养24 h后, 通过显微镜观察到巨噬细胞的形态发生了显著变化, 如图 4所示, 空白组的巨噬细胞肥大较圆, 而经PM2.5暴露后的巨噬细胞变为皱缩;且随着PM2.5浓度的增大, 核质固缩也就越明显.与空白组(生理盐水, 图 4a)比较, 暴露组的巨噬细胞似乎皱缩明显(图 4b~e).需要指出的是, 无论来自非过敏儿童的室内, 还是过敏儿童的室内, 巨噬细胞暴露在高浓度(200 μg·mL-1)PM2.5下时明显会发生不同程度的皱缩.然而, 图 4c与4e对比显示, 过敏儿童室内PM2.5对巨噬细胞的影响要比非过敏儿童室内PM2.5更加显著.
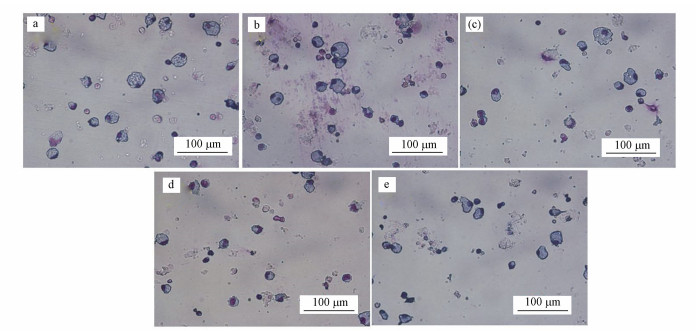 |
| 图 4 巨噬细胞经PM2.5暴露24 h后的形态图(Giemsa染色, ×20)(a.对照组, b.非过敏儿童室内10 μg·mL-1 PM2.5, c.非过敏儿童室内200 μg·mL-1 PM2.5, d.过敏儿童室内10 μg·mL-1 PM2.5, e.过敏儿童室内200 μg·mL-1 PM2.5) Fig. 4 Morphological images of macrophages exposed to PM2.5 after 24 h |
巨噬细胞与PM2.5共培养48 h后, 吞噬鸡红细胞的情况如图 5所示, 高剂量(200 μg·mL-1)PM2.5暴露组中, 巨噬细胞的形态发生变化, 数量相应地减少, 对吞噬鸡红细胞的不利影响越大;而且PM2.5浓度越大, 巨噬细胞的吞噬能力下降越明显.图 5a显示, 巨噬细胞可吞噬大多数鸡红细胞, 但图 5b和5c表明, 仍有部分鸡红细胞尚未被巨噬细胞吞噬.从图 5b和5c对比可以看出, 经非过敏儿童室内PM2.5暴露后的巨噬细胞彼此间交联较为紧密, 可以聚集在鸡红细胞周围;相反, 过敏儿童室内PM2.5暴露后的巨噬细胞彼此间交联不够紧密, 并没有向鸡红细胞周围聚集.巨噬细胞的吞噬能力下降这一结果, 可以通过数据直观地反映.表 2显示的是相应的吞噬率和吞噬指数, 由表可知, 过敏儿童室内PM2.5暴露组巨噬细胞的吞噬能力减弱, 反映吞噬能力的两项关键指标都不及非过敏儿童室内PM2.5暴露组.这也从侧面反映过敏儿童室内PM2.5暴露对吞噬细胞的不利影响要比非过敏儿童室内PM2.5暴露组显著的多.
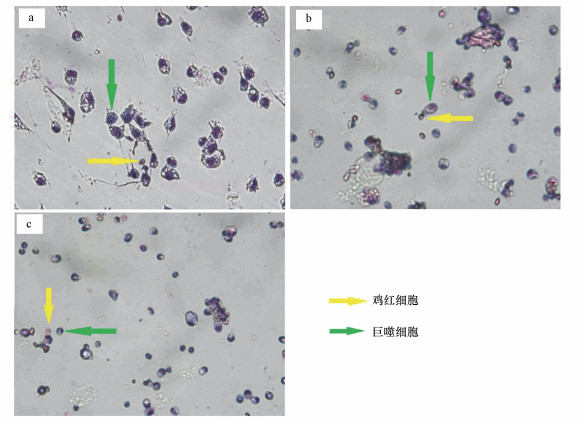 |
| 图 5 巨噬细胞经PM2.5暴露48 h后吞噬鸡红细胞(CRBC)的观察图(Giemsa染色)(a.对照组, ×40倍;b.非过敏儿童室内200 μg·mL-1 PM2.5, ×20倍;c.过敏儿童室内200 μg·mL-1 PM2.5, ×20倍) Fig. 5 Effect on phagocytic response of peritoneal macrophages exposed to PM2.5 after 48 h to chicken red blood cells |
| 表 2 不同PM2.5暴露组的巨噬细胞吞噬能力比较 Table 2 Comparison of phagocytic function in different PM2.5 groups |
PM2.5诱导巨噬细胞的毒性可通过MTT比色法测定的细胞活力反映.巨噬细胞经PM2.5分别暴露24、48 h后细胞活力的变化如图 6所示.图 6a表明, 与空白组相比, 过敏儿童室内PM2.5暴露组与非过敏儿童室内PM2.5暴露组有显著差异(p < 0.05);图 6b表明, 随着PM2.5暴露时间增加至48 h, 巨噬细胞的细胞活力极显著降低(p < 0.01).此外, 巨噬细胞经PM2.5暴露后, 其中, 死细胞或受损的细胞会在培养液中释放出LDH, 通过对LDH的检测可以作为反映PM2.5对细胞通透性的指示.图 7显示的是巨噬细胞经PM2.5分别暴露24、48 h后LDH的活性.实验结果表明, 巨噬细胞经PM2.5暴露48 h后释放LDH的量明显较暴露24 h更高, 且呈时间-浓度效应关系, 即随着PM2.5暴露时间、浓度的增加, 检测出的LDH活性越高, 反映PM2.5对巨噬细胞的细胞膜损伤程度有加深趋势.
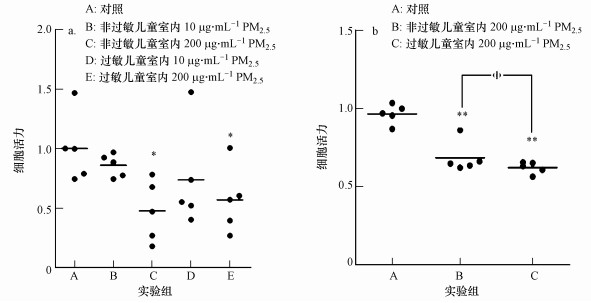 |
| 图 6 PM2.5对巨噬细胞的细胞活力的影响(n=5, *p < 0.05, **p < 0.01, Φ表示p < 0.05)(a.暴露24 h, b.暴露48 h) Fig. 6 Effect of PM2.5 on cell viability of macrophages |
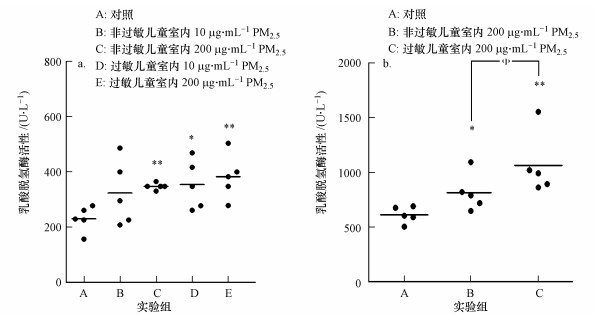 |
| 图 7 PM2.5对巨噬细胞的乳酸脱氢酶活性的影响(n = 5, *p < 0.05, **p < 0.01, Φ表示p < 0.05) (a.暴露24 h, b.暴露48 h) Fig. 7 LDH activity of PM2.5 on macrophages |
大量研究表明, PM2.5主要通过呼吸道进入体内, 危害人体健康, 甚至易诱发多种不良疾病(朱建超, 2012), 大量的研究有助于扩大对PM2.5的关注与再认识.一些研究指出, PM2.5产生的不利影响与其复杂的组成成分有着密切的关系(Schins et al., 2004).已有研究表明, 含碳组分作为PM2.5中主要的化学成分, PM2.5中有机碳和元素碳含量的增加会导致哮喘儿童的发病率增加(McConnell et al., 2003).本实验中, 虽然收集的PM2.5样品都来自同一地区, 但过敏儿童室内PM2.5的有机碳和元素碳含量明显与非过敏儿童室内PM2.5不同且较高, 而有机碳和元素碳是反映PM2.5中含碳组分的重要指标, 这表明过敏儿童室内PM2.5可能还有其他碳来源.根据本研究的调查统计, 在过敏儿童中, 室内墙的喷漆材料与木质地板占了相当比重, 这些材料会释放出苯及其他挥发性有机物, 容易形成二次粒子, 而且易于附着其他污染物, 包括微生物、过敏原.这也从另一个方面反映室内PM2.5的微观环境不同, 其碳来源不同, 这种成分的差异也就使得PM2.5的暴露对人体健康产生不同程度的危害.
PM2.5复杂的化学成分是造成不良健康效应的关键因素, 其携带的微生物、过敏原、甚至有毒重金属可直接进入人体.有研究指出, PM2.5上的微生物虽未得到全面评价, 但已知微生物的存在会增加PM2.5暴露致过敏性疾病的风险(Degobbi et al., 2011).因此, 除了分析PM2.5化学成分外, 附着于PM2.5上的真菌种类及其数量也是需要考虑的.本研究初步统计了过敏与非过敏儿童室内PM2.5的真菌数量, 结果表明, 过敏儿童室内PM2.5携带的真菌数量要多于非过敏儿童室内PM2.5.PM2.5的组成成分(如有机碳、元素碳等)、附着物(如真菌等)可以影响并介导PM2.5的毒性.儿童长期暴露在这样的环境下, 自然就增加了过敏性疾病发病的机率.流行病学研究强有力地显示, 城市环境中高浓度的PM2.5与儿童哮喘之间有关联(Mar et al., 2005; Nikasinovic et al., 2006);近几年国外权威的研究也证实, 儿童过敏性症状与PM2.5暴露有关(Lee et al., 2014).
巨噬细胞是免疫系统中重要的一类细胞, 其形态及功能的异常与过敏性疾病密切相关.Meng等(2007)的研究表明, PM2.5暴露会使肺泡巨噬细胞和大鼠肺细胞出现DNA损伤;Hiraiwa等(2013)的研究也指出, PM2.5诱导肺巨噬细胞发生炎症反应.本研究就巨噬细胞与PM2.5共培养24 h后的观察结果来看, 随着PM2.5暴露浓度增大, 巨噬细胞的数量有一定程度的下降, 巨噬细胞的形态也发生了显著皱缩, 当PM2.5暴露浓度增加到200 μg·mL-1时, 形态异常的巨噬细胞增多, 且部分严重的巨噬细胞会出现核固缩的现象, 这一趋势也与PM2.5暴露时间的延长结果相一致.另外, 从巨噬细胞的吞噬功能来看, 经PM2.5暴露48 h后的巨噬细胞吞噬鸡红细胞的能力明显减弱.在本实验中, 与空白组相比, 过敏儿童室内PM2.5暴露组与非过敏儿童室内PM2.5暴露组, 二者吞噬率和吞噬指数都呈明显下降趋势.然而, 过敏儿童室内PM2.5暴露组对巨噬细胞吞噬能力的不利影响更加显著.造成这些结果的原因很大程度上源于PM2.5暴露可诱导细胞产生毒性.
本研究中, 随着PM2.5暴露浓度、时间的增加, 巨噬细胞的细胞活力会降低;而乳酸脱氢酶泄露率越高, 则说明巨噬细胞受到细胞膜损伤的程度也越大.两项数据一致的反映出PM2.5对巨噬细胞有毒性作用.多项研究也证实, PM2.5暴露能使巨噬细胞功能失调, 并最终诱发哮喘或其他过敏性疾病(Kulkarni et al., 2006).通过对过敏儿童室内PM2.5与非过敏儿童室内PM2.5的比较分析, 结果表明, 同一浓度下, 前者比后者诱导巨噬细胞产生的毒性风险可能更大, 这也间接反映PM2.5暴露与儿童的过敏症有潜在关联.
5 结论(Conclusions)1) 高剂量(200 μg·mL-1)PM2.5暴露后的巨噬细胞, 其形态和吞噬功能会受到不同程度的影响.
2) 基于PM2.5暴露对巨噬细胞的细胞毒性检测比较发现, 与非过敏儿童室内PM2.5暴露组相比, 过敏儿童室内PM2.5暴露组诱导巨噬细胞产生的毒性作用更明显, 提示儿童的过敏症与室内PM2.5的组分及含量有潜在关联.
Bagchi D, Bagchi M, Hassoun E A, et al. 1995. In vitro and in vivo generation of reactive oxygen species, DNA damage and lactate dehydrogenase leakage by selected pesticides[J]. Toxicology, 104(1): 129–140.
|
Bai Z, Wang Z, Zhu T, et al. 2003. Developing indoor air quality related standards in China[J]. Journal of Asian Architecture & Building Engineering, 2(1): 55–60.
|
蔡翠. 2014. 武汉市城市发展的大气污染问题与治理对策[J]. 今日湖北旬刊, 2014(2): 84–85.
|
Degobbi C, Lopes F D, Carvalho-Oliveira R, et al. 2011. Correlation of fungi and endotoxin with PM2.5 and meteorological parameters in atmosphere of Sao Paulo, Brazil[J]. Atmospheric Environment, 45(13): 2277–2283.
DOI:10.1016/j.atmosenv.2010.12.005
|
Gao B, Guo H, Wang X M, et al. 2012. Polycyclic aromatic hydrocarbons in PM2.5 in Guangzhou, southern China:Spatiotemporal patterns and emission sources[J]. Journal of Hazardous Materials, 239: 78–87.
|
Geller M D, Chang M C, Sioutas C, et al. 2002. Indoor/outdoor relationship and chemical composition of fine and coarse particles in the southern California deserts[J]. Atmospheric Environment, 36: 1099–1110.
DOI:10.1016/S1352-2310(01)00340-5
|
郭翔, 闫庆倩, 赵学彬, 等. 2012. 不同地区大气PM2.5对大鼠肺泡巨噬细胞毒性作用的实验研究[J]. 环境与健康杂志, 2012, 29(1): 12–16.
|
Hiraiwa K, van Eeden S F. 2013. Contribution of lung macrophages to the inflammatory responses induced by exposure to air pollutants[J]. Mediators of Inflammation, 2013: 619523–619533.
|
贾玉巧, 赵晓红, 郭新彪. 2011. 大气颗粒物PM10和PM2.5对人肺成纤维细胞及其炎性因子分泌的影响[J]. 环境与健康杂志, 2011, 28(3): 206–208.
|
阚海东. 2012. 《环境空气质量标准》(GB3095-2012)细颗粒物(PM2.5)标准值解读[J]. 中华预防医学杂志, 2012, 46(5): 396–398.
|
Klepeis N E, Nelson W C, Ott W R, et al. 2001. The National Human Activity Pattern Survey (NHAPS):a resource for assessing exposure to environmental pollutants[J]. Journal of Exposure Analysis and Environmental Epidemiology, 11(3): 231–252.
DOI:10.1038/sj.jea.7500165
|
Kulkarni N, Pierse N, Rushton L, et al. 2006. Carbon in airway macrophages and lung function in children[J]. New England Journal of Medicine, 355(1): 21–30.
|
Lee J Y, Lee S, Bae G. 2014. A review of the association between air pollutant exposure and allergic diseases in children[J]. Atmospheric Pollution Research, 5(4): 616–629.
DOI:10.5094/APR.2014.071
|
Liu Q. 2012. Impact of fine particulate matter(PM2.5) on asthma among children:a review of recent studies[J]. Journal of Environment & Health, 29(7): 665–668.
|
Liu Y, Chen R, Shen X, et al. 2004. Wintertime indoor air levels of PM10, PM2.5 and PM1 at public places and their contributions to TSP[J]. Environment International, 30(2): 189–197.
|
Li Y, Liu D, Ai H, et al. 2010. Biological evaluation of layered double hydroxides as efficient drug vehicles[J]. Nanotechnology, 21(10): 105–117.
|
Mar T F, Jansen K, Shepherd K, et al. 2005. Exhaled nitric oxide in children with asthma and short-term PM2.5 exposure in Seattle[J]. Environmental Health Perspectives, 113(12): 1791–1794.
DOI:10.1289/ehp.7883
|
McConnell R, Berhane K, Gilliland F, et al. 2003. Prospective study of air pollution and bronchitic symptoms in children with asthma[J]. American Journal of Respiratory and Critical Care Medicine, 168(7): 790–797.
DOI:10.1164/rccm.200304-466OC
|
Meng Z, Zhang Q. 2007. Damage effects of dust storm PM2.5 on DNA in alveolar macrophages and lung cells of rats[J]. Food and Chemical Toxicology, 45(8): 1368–1374.
DOI:10.1016/j.fct.2007.01.014
|
Nikasinovic L, Just J, Sahraoui F, et al. 2006. Nasal inflammation and personal exposure to fine particles PM2.5 in asthmatic children[J]. Journal of Allergy and Clinical Immunology, 117(6): 1382–1388.
DOI:10.1016/j.jaci.2006.03.023
|
Schins R P F, Lightbody J H, Borm P J A, et al. 2004. Inflammatory effects of coarse and fine particulate matter in relation to chemical and biological constituents[J]. Toxicology and Applied Pharmacology, 195(1): 1–11.
|
Seinfeld J H, Pandis S N, Seinfeld J H, et al. 1998. Atmospheric chemistry and physics:from air pollution to climate change[J]. Environment:Science and Policy for Sustainable Development, 51(7): 88–90.
|
Trasande L, Thurston G D. 2005. The role of air pollution in asthma and other pediatric morbidities[J]. Journal of Allergy and Clinical Immunology, 115(4): 689–699.
DOI:10.1016/j.jaci.2005.01.056
|
朱建超. 2012. PM2.5的综述与思考[J]. 中国卫生检验杂志, 2012, 22(10): 2526–2528.
|
 2018, Vol. 38
2018, Vol. 38


