草甘膦(PMG)是一种在全球范围内使用最广泛的有机磷除草剂,具有广谱、高效、无毒等优点,在农业、林业及城市环境中均有应用(Wiliiams et al., 2000; Aparicio et al., 2013).据报道,全球每年草甘膦的使用量高达65万t,在美国自然水体中可检测到的最大含量为0.476 mg·L-1(Battaglin et al., 2014),巴西部分自然水体中其含量高达1.48 mg·L-1(Tzaskos et al., 2012).长期以来,草甘膦被认为对水生环境及人类安全无害,然而,最新研究表明草甘膦对两栖动物和水生无脊椎动物存在显著的毒害作用,世界卫生组织也将草甘膦列为潜在的人类致癌物质(Guytona et al., 2015).草甘膦残留所导致的环境污染问题已引起人们的广泛关注.
草甘膦是一种具有3个极性官能团(羧基、氨基和磷酸基团)的小分子有机物,易与土壤矿物中的金属离子形成表面络合物而从水体中去除(Barja et al., 2005).铝、铁氧化物是土壤中吸附草甘膦的主要物质(Gerritse et al., 1996;Gimsing et al., 2007;Borggaard et al., 2008).Sheals等(2002)通过傅里叶红外光谱和X射线光电子能谱等研究了草甘膦在针铁矿表面的吸附机理,发现草甘膦主要通过磷酸基团与针铁矿表面形成单齿单核的内层络合物,而羧基处于一个相对自由的状态,可以与其他重金属进行络合反应.草甘膦与矿物表面的络合反应是影响其吸附去除及迁移转化的关键因素(Borggaard et al., 2008).
现有的草甘膦去除方法主要有吸附法、离子交换法、膜分离法和沉淀法等.与其他方法相比,吸附法因具有处理量大、简单易行、经济适用等优点而被广泛应用(Ghaedi et al., 2014).二氧化钛作为一种高效的吸附材料,具有较高的化学稳定性,被广泛应用于环境污染物的吸附去除中(Luo et al., 2010).近期研究表明,除比表面积外,二氧化钛的表面能亦是影响其吸附性能的主要因素之一.高指晶面二氧化钛表面具有高密度的原子台阶和悬空键,不饱和的Ti原子较多,其表面能较大,潜在的吸附活性较高(Song et al., 2017).然而,草甘膦在高指二氧化钛上的吸附研究较少,而二者间微观界面的机理研究对进一步认识有机污染物的吸附去除具有重要意义.
本文采用实验室自制高指{201}TiO2为吸附剂,以草甘膦为目标污染物,研究草甘膦在高指{201}TiO2表面的吸附行为.通过水化学吸附实验考察草甘膦在二氧化钛表面的吸附行为,并结合CD-MUSIC模型研究草甘膦的表面络合结构,为二氧化钛吸附去除有机污染物提供理论依据.
2 材料与方法(Materials and methods) 2.1 实验材料草甘膦(C3H8NO5P,标准品,纯度99.6%)、N, N-二甲基甲酰胺(DMF)、钛酸四丁脂(TBOT)均购自美国Sigma-Aldrich公司;实验所用氢氧化钠、盐酸、氯化钠、冰醋酸均为分析纯,购自国药集团化学试剂有限公司;乙腈、甲酸为色谱纯,购自赛默飞世尔科技有限公司.
2.2 实验方法高指晶面{201}TiO2制备方法:将冰醋酸与N, N-二甲基甲酰胺以1: 1物质的量的比混合至总体积20 mL,混合均匀后逐滴加入0.5 mL钛酸四丁酯,充分反应后,倒入100 mL聚四氟乙烯内衬的不锈钢反应釜中在200 ℃下反应11 h.反应结束后,将产物离心分离,用无水乙醇反复洗涤后,置于60 ℃烘箱烘干,得到高指晶面{201}TiO2(Wu et al., 2011).通过场发射扫描电镜(FE-SEM, SU-8000, Hitachi),高分辨透射电镜(HR-TEM,JEM-2100F),X射线衍射(XRD,BRUKER,D8)对其形貌和晶体结构进行表征,结果表明制备的二氧化钛材料具有高指数{201}晶面,形貌为自组装的类似蒲公英的层级结构,比表面积为22.7 m2·g-1 (Song et al., 2017).
吸附等温线实验:吸附实验采用0.04 mol·L-1 NaCl作为背景电解质溶液.将标准草甘膦试剂配制成不同浓度梯度的草甘膦(0.1~10 mg·L-1)溶液.称取40 mg TiO2置于50 mL聚丙烯离心管中,加入40 mL含有不同浓度的草甘膦溶液,用HCl和NaOH调节溶液pH值至7.0,用铝箔纸包好遮光,置于旋转培养仪上室温反应24 h.反应结束后,用0.45 μm水系滤膜进行固液分离,测定滤液中草甘膦的平衡浓度.根据初始溶液与吸附后草甘膦浓度的变化来计算TiO2对草甘膦的吸附量.按式(1)计算平衡吸附量qe(mg·g-1).
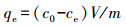
|
(1) |
式中,c0为草甘膦的初始浓度(mg·L-1);ce为吸附后的平衡浓度(mg·L-1);V为溶液的体积(L);m为TiO2的质量(g).
吸附动力学实验:称取100 mg TiO2置于铝箔遮光处理的烧杯内,加入100 mL 10 mg·L-1的草甘膦溶液,混合后用NaOH和HCl调节pH值至7.0,以0.04 mol·L-1 NaCl作为背景电解质溶液.室温条件下,放置于磁力搅拌器上匀速搅拌,分别在0、5、10、20、30、60、90、120、180、240、300、420 min用注射器从烧杯中取出0.5 mL溶液,过0.45 μm水系滤膜后,用高效液相-质谱(HPLC-MS/MS)测定滤液中草甘膦浓度.
pH对草甘膦吸附的影响:称取40 mg TiO2置于50 mL聚丙烯离心管中,加入40 mL浓度为10 mg·L-1的草甘膦溶液,背景电解质溶液为0.04 mol·L-1 NaCl,用铝箔纸包好遮光,置于旋转培养仪上室温反应24 h.反应过程中用HCl和NaOH调节溶液pH值范围为3~10.反应结束后,用0.45 μm水系滤膜进行固液分离,用高效液相质谱(HPLC-MS/MS)测定滤液中草甘膦浓度.
Zeta电位的表征:Zeta电位实验采用0.04 mol·L-1 NaCl作为背景溶液.将含有0.1 g·L-1的TiO2和10 mg·L-1的草甘膦混合溶液用HCl和NaOH调节pH至设定值.用铝箔纸包裹避光,置于旋转培养仪上室温反应24 h,反应结束后,记录最终pH并测定样品中TiO2的Zeta电位.每个样品重复测试3次取平均值.Zeta电位测量使用马尔文激光粒度仪(Zetasizer Nano ZS, Malvern Instrument公司,英国).
红外光谱分析:本实验采用傅里叶变换红外光谱仪(Nicolet 6700)进行红外光谱分析.将TiO2过400目筛后,配制3.5 g·L-1 TiO2溶液,摇匀并超声20 min后,取0.3 mL溶液滴加到ZnSe晶体上,待其自然晾干后,用去离子水清洗2~3次,晾干备用(Ronson et al., 2002).实验采用流动槽智能多次衰减全反射附件(ATR-FTIR)进行光谱采集,分辨率取4 cm-1,扫描次数为512次.
电荷分布多位点络合(CD-MUSIC)模型:本研究使用1-pK TPM的CD-MUSIC模型来模拟草甘膦在TiO2表面的吸附行为,所用软件是Visual MINTEQ3.0.1-pK TPM模型中,TiO2表面的电性只需一步质子化和一个pK值即可以描述,即1-pK模型.TiO2表面氧称为0层;吸附质中心原子靠近液相部分配体,位于假定的静电面(Stern层)范围内,称为1层;吸附质中心原子的电荷按照电荷分布原则将自身电荷分配给0层和1层,双电层中的电解质离子称为2层,此即3层模型(three-plane model, TPM).CD-MUSIC模型综合考虑了固体表面的空间电荷分布及吸附质中心原子(如磷)对不同电位层的电荷贡献,能够通过对宏观吸附数据的模拟得到配合物的微观结构.若中心P原子对0层氧原子的电荷中和贡献分数为f,对于1层原子电荷中和贡献分数为1-f,可根据公式(2)和(3)计算络合物0层和1层的电荷(Hiemstra et al., 1996; Tadanier et al., 2002),该电荷值用于CD-MUSIC模拟的输入.
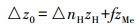
|
(2) |
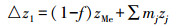
|
(3) |
式中,z0为0层的电荷变化,nH为0层表面反应的质子数目,zH为质子的电荷(+1),f为电荷分布系数,即中心P原子对0层的电荷贡献分数.zMe为吸附络合物中心原子的电荷.mj为位于1层的配体数目,zj为位于1层的配体所带的电荷.
2.3 实验仪器与方法草甘膦浓度使用高效液相质谱(HPLC-MS/MS)测定,色谱条件:Sielc Obelisc N (5 μm, 2.1 mm × 100 mm, SIELC Technologies)色谱柱;流动相A为含0.1%甲酸的乙腈,B为含0.1%甲酸的水,等度洗脱,水/乙腈(80/20), 流速0.4 mL·min-1;进样量50 μL;柱温40 ℃.质谱条件为电喷雾离子源(ESI);扫描方式为多反应监测(MRM);Negative模式,离子喷雾电压-4500 V,离子源温度600 ℃,气帘气30 psi.
3 结果与讨论(Results and discussion) 3.1 草甘膦在TiO2表面的吸附动力学在pH=7条件下,TiO2对草甘膦的吸附动力学曲线及相关拟合曲线如图 1所示.在吸附开始阶段,TiO2对草甘膦的吸附速率较快,在30 min时其吸附量已经达到了平衡吸附量的80%,在40 min内达到吸附平衡,吸附量约为7 mg·g-1.为了进一步了解TiO2对草甘膦的吸附动力学特征,分别采用拟一级和拟二级动力学方程对实验数据进行拟合:
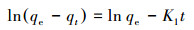
|
(4) |

|
(5) |
 |
| 图 1 TiO2对草甘膦吸附过程的拟一级动力学(a)和拟二级动力学(b)拟合 Fig. 1 The pseudo-first order (a) and the pseudo-second-order (b) kinetics plots for PMG adsorption on TiO2 |
式中,K1和K2分别为拟一级动力学方程和拟二级动力学方程的速率常数,qt和qe分别为t时刻和吸附平衡时草甘膦的吸附量(mg·g-1),t为吸附时间(min).拟合结果见表 1.由图 1和表 1可知,本研究中TiO2对草甘膦的吸附动力学使用拟二级动力学模型拟合结果更好,其拟合所得的可决系数R2高达0.999,说明控制该吸附速率的过程是化学吸附(Mayakaduwa et al., 2016).
| 表 1 TiO2吸附草甘膦的吸附动力学拟合参数 Table 1 Adsorption kinetics model parameters for PMG adsorption on TiO2 |
TiO2对草甘膦的吸附等温线见图 2.结果表明,随着初始浓度的增大,草甘膦在TiO2上的吸附量逐渐增大,最终趋于吸附平衡.分别采用Langumir和Freundlich方程对吸附等温线进行拟合:
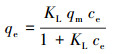
|
(6) |

|
(7) |
 |
| 图 2 TiO2对草甘膦的吸附等温线(a. Langmuir和Freundlich模型; b.CD-MUSIC模型) Fig. 2 Adsorption isotherm of PMG on TiO2 with Langmuir and Freundlich model(a) and CD-MUSIC model(b) |
式中,qe是单位质量吸附剂上面吸附物质的总量(mg·g-1), qm是最大吸附量(mg·g-1);KL是Langmuir方程常数(L·mg-1),表示吸附质与吸附剂表面的亲和力,KL值越大,吸附亲和力越强;ce是溶液中吸附质的平衡浓度(mg·L-1);KF和n为Freundlich方程常数,分别代表了吸附容量和吸附非线性程度.
Langmuir和Freundlich方程拟合的吸附等温线见图 2a,拟合参数见表 2.结果表明,Langmuir和Freundlich方程均可以描述草甘膦的吸附过程,Freundlich吸附模型拟合结果R2为0.969, 小于Langmuir吸附模型拟合结果(R2=0.989),表明Langmuir吸附模型更适合描述草甘膦在TiO2上的吸附行为,表明草甘膦的吸附过程主要是近似单分子层的化学吸附(Nourouzi et al., 2010).CD-MUSIC模型拟合的草甘膦在TiO2上的吸附等温线如图 2b所示,拟合参数见表 3.结果表明,草甘膦在TiO2表面可能形成单齿或双齿络合结构,其中双齿络合结构的络合反应稳定常数logK=23,单齿络合结构的logK=16,表明双齿吸附构型更为有利.
| 表 2 TiO2吸附草甘膦的吸附等温线拟合参数 Table 2 Adsorption isotherm model parameters for PMG adsorption on TiO2 |
大量研究表明,溶液pH对草甘膦的吸附过程有重要影响(Mcconnell et al., 1985).草甘膦在TiO2上的pH吸附实验如图 3所示.结果表明,草甘膦在TiO2上的吸附量随着pH的升高明显降低.当溶液pH=3时,草甘膦的吸附率高达92%;当溶液pH=7时, 草甘膦的吸附率为79%;当溶液pH=10时,草甘膦的吸附率降至25%.这是因为不同的pH条件下草甘膦和TiO2所带电荷不同导致的.
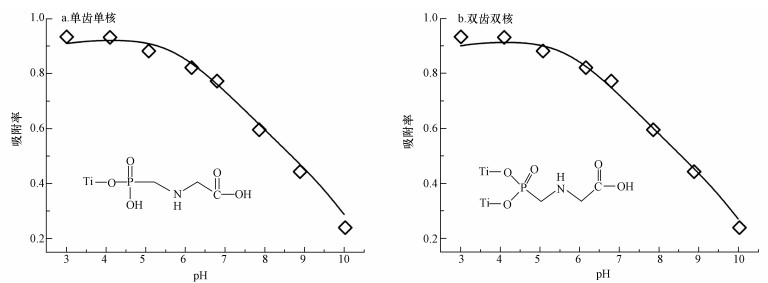 |
| 图 3 溶液pH对TiO2吸附草甘膦的影响 Fig. 3 Effect of solution pH on PMG adsorption on TiO2 |
草甘膦分子中包含有羧基、氨基和磷酸基团,各级电离常数分别为pKa1=2.22,pKa2=5.44,pKa3=10.13(Sheals et al., 2002).在不同pH条件下,草甘膦在水溶液中会存在不同的离子状态.采用Visual MINTEQ软件分析草甘膦在水溶液中的形态分布,结果如图 4所示.当pH < 2.22时,草甘膦多以电中性的H3PMG形式存在;在pH=2.22附近,H3PMG形态的草甘膦会脱掉羧酸基团(—COOH)上的氢,形成带一个负电荷的H2PMG-1,随着pH增大,H3PMG含量减少,H2PMG-1含量增多.当pH为2.22~5.44时,H2PMG-1形态占主导地位;在pH=5.44附近,H2PMG-1形态的草甘膦会继续脱掉磷酸基团(P—O—H)处的氢,形成带两个负电荷的HPMG-2,当pH为5.44~10.13时,HPMG-2占主导地位;当pH值大于10.13时,HPMG-2草甘膦会脱掉氨基上的氢,以PMG-3形式存在(Li et al., 2013;Tomaas et al., 2002; 兰华春等,2013).根据实验选取的pH范围,在pH值为3时,草甘膦多以H2PMG-1形式存在,而二氧化钛的等电点pzc=5.6,此时二氧化钛表面带正电荷,根据静电作用,草甘膦易吸附在TiO2表面;随着pH增大,TiO2表面电负性逐渐增强,此时溶液中草甘膦多以带2个和3个负电荷的HPMG-2,PMG-3形态存在,由于静电力的排斥作用,TiO2对HPMG-2和PMG-3形态的草甘膦吸附能力逐渐降低.因此,pH会显著影响草甘膦在TiO2表面的吸附,酸性条件下,TiO2对草甘膦的吸附能力更强.
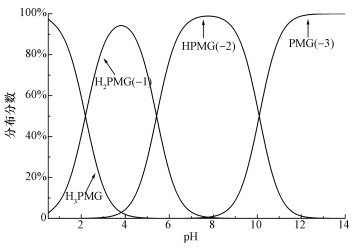 |
| 图 4 草甘膦在不同pH下的形态分布 Fig. 4 Species distribution of PMG at different pH |
二氧化钛吸附草甘膦后Zeta电位变化曲线如图 5所示.结果表明,实验所用二氧化钛的等电点pzc为5.6,草甘膦吸附后TiO2的pzc左移至4.2.金属氧化物的pzc是由其表面羟基的去质子化和质子化作用决定的.若被吸附物质为外层吸附,由于被吸附物质与金属氧化物表面未成键,金属氧化物的pzc不会发生变化.若被吸附物质为内层吸附,由于被吸附物质与金属氧化物表面羟基发生反应,使金属氧化物表面带电情况发生改变,导致其pzc发生变化.吸附草甘膦后二氧化钛pzc左移说明草甘膦与TiO2表面形成带负电的内层配合物(胡珊等,2011).
 |
| 图 5 不同pH条件下TiO2和草甘膦吸附后TiO2的Zata电位及CD-MUSIC模拟结果 Fig. 5 Zeta potential of TiO2 as blank, PMG adsorption samples as a function of pH (symbols) and CD-MUSIC models (line). Error bars represent the standard deviation (n=3) |
草甘膦溶液和吸附态草甘膦的FTIR红外谱如图 6所示.结果表明,溶解态草甘膦位于1608、1402 cm-1处的特征峰分别由羧基中—CO2的非对称和对称伸缩振动引起(υasCOO和υsCOO),位于1325 cm-1处特征峰由氨基及相连碳链的复合振动产生,位于1093 cm-1处峰由P—O的非对称性伸缩振动引起,位于979 cm-1处峰由P—O对称伸缩振动引起(Sheals et al., 2001)(图 6a).当草甘膦吸附在二氧化钛上时,羧基伸缩振动产生的特征峰没有发生明显变化,说明羧基几乎不与二氧化钛发生反应.位于1093和979 cm-1处磷酸基团的伸缩振动峰分别偏移至1121和1006 cm-1,说明草甘膦主要通过磷酸基团与二氧化钛表面结合,形成含P—O—Ti键的内层络合物(图 6b).
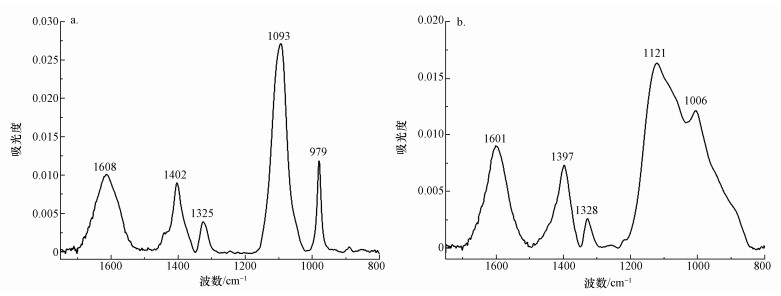 |
| 图 6 pH=7条件下溶解态草甘膦(a)及草甘膦吸附在TiO2上(b)的红外谱图 Fig. 6 ATR-FTIR spectra of PMG in aqueous solution and PMG adsorption on TiO2 at pH 7 |
拟一级和拟二级吸附动力学模型及Langmuir和Freundlich吸附等温式是描述吸附现象和评价吸附剂性能的重要工具.但这些经验吸附模型将吸附过程划分为单层吸附和多层吸附等几种简单类型,只考虑了化学自由能,对吸附位点做了平均化的描述(Hiemstra et al., 2006).吸附剂表面的性质及其吸附的微界面吸附构型不能得到很好的体现,因此这些经验模型无法揭示固液界面的内在吸附反应机理.电荷分布多位点络合模型(CD-MUSIC)考虑了固体表面电荷的空间分布及吸附中心原子对相邻电层氧原子的电荷中和贡献f,能够通过拟合宏观吸附数据获得配合物的微观结构.
本研究分别以单齿单核及双齿双核的吸附配合物模拟了草甘膦在二氧化钛上的吸附行为.参考Zeta电位表征的带负电内层配合结构,在吸附产物中分别加入[TiPMG-7/3]和[Ti2PMG-5/3],其模拟反应稳定常数logK分别为16和23,f值为0.3和0.7.草甘膦在二氧化钛上的吸附反应方程式见式(8)和(9),模拟所用的参数及具体种类见表 3.

|
(8) |
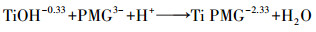
|
(9) |
| 表 3 CD-MUSIC模型中所用的反应种类及参数 Table 3 Surface parameters and species used in the CD-MUSIC modeling |
CD-MUSIC模型对不同pH值下TiO2对草甘膦吸附的拟合结果如图 3所示,对TiO2表面Zeta电位的拟合结果如图 5所示,结果表明所选用的吸附方程和拟合参数能较好地拟合实验结果.本研究使用滑动层(1层)和扩散层(2层)之间的经验距离来模拟TiO2吸附草甘膦后表面Zeta电位的变化趋势.将0、1、2层的描述用到此处Zeta电位的计算公式如式(6)所示,式中,κ为德拜-赫克参数,ψd为扩散层(2层)电势,d为滑移层到扩散层距离,T、R及F分别为绝对温度、阿伏伽德罗常数和法拉第常数.参数计算公式为:
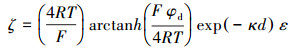
|
(10) |
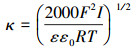
|
(11) |
式中,ε为介质的相对介电常数,ε0为真空介电常数,I为背景离子强度.式(10)中唯一未知量为滑移层厚度d.通过拟合草甘膦吸附前后TiO2表面的Zeta电位,即可得到滑动层厚度的变化,吸附前TiO2表面的滑移层d值为1.1,吸附草甘膦后变为1.0,说明草甘膦的吸附压缩双电层,草甘膦表面官能团与TiO2表面成键,草甘膦中心原子向吸附层贡献电荷(Jing et al., 2005).
通过拟合结果可知,CD-MUSIC模型可以将微观吸附态结构体现在模型的化学方程式中,准确解释和预测草甘膦在不同pH时的宏观吸附行为和TiO2表面Zeta电位的变化,从而深入理解TiO2对草甘膦的吸附机理.
4 结论(Conclusions)1) TiO2对草甘膦的吸附符合拟二级动力学方程和Langmuir吸附等温线模型,反应可在40 min内达到平衡;通过Langmuir吸附等温线模型可知草甘膦在TiO2上的最大吸附量为7.89 mg·g-1.
2) 草甘膦在不同pH条件下具有不同的解离形态,pH对TiO2吸附草甘膦影响较大,草甘膦吸附量随着pH升高明显降低,在低pH条件下,TiO2对草甘膦具有较好的去除效果.
3) 通过Zeta电位和红外光谱的表征可知,草甘膦以内层络合形式吸附在TiO2上;CD-MUSIC模型能够准确地模拟草甘膦在TiO2表面上的吸附行为.
Aparicioa V C, Marino D, De G E. 2013. Environmental fate of glyphosate and aminomethylphosphonic acid in surface waters and soil of agricultural basins[J]. Chemosphere, 93(9): 1866–1873.
DOI:10.1016/j.chemosphere.2013.06.041
|
Battaglin W, Meyer M, Kuivila K, et al. 2014. Glyphosate and its degradation product AMPA occur frequently and widely in US soils, surface water, groundwater, and precipitation[J]. JAWRA Journal of the American Water Resources Association, 50(50): 275–290.
|
Barja B C, Afonso M D. 2005. Aminomethylphosphonic acid and glyphosate adsorption onto goethite:A comparative study[J]. Environmental Science & Technology, 39(2): 585–592.
|
Borggaard O K, Gimsing A L. 2008. Fate of glyphosate in soil and the possibility of leaching to ground and surface waters:a review[J]. Pest Management Science, 64(4): 441–456.
DOI:10.1002/(ISSN)1526-4998
|
Guytona K Z, Loomis D, Grosse Y, et al. 2015. Carcinogenicity of tetrachlorvinphos, parathion, malathion, diazinon, and glyphosate[J]. Lancet Oncology, 16(5): 490–491.
DOI:10.1016/S1470-2045(15)70134-8
|
Ghaedi M, Ansari A, Habibi M H, et al. 2014. Removal of malachite green from aqueous solution by zinc oxide nanoparticle loaded on activated carbon:kinetics and isotherm study[J]. Journal of Industrial and Engineering Chemistry, 20(20): 17–28.
|
Gimsing A L, Szilas C, Borggaard O K. 2007. Sorption of glyphosate and phosphate by variable-charge tropical soils from Tanzania[J]. Geoderma, 138(1): 127–132.
|
Gerritse R G, Beltran J, Hernandez F. 1996. Adsorption of atrazine, simazine, and glyphosate in soils of the Gnangara Mound, Western Australia[J]. Australian Journal of Soil Research, 34(4): 599–607.
DOI:10.1071/SR9960599
|
Hiemstra T, Riemsdijk W H V. 1996. A surface structural app roach to ion adsorption:the charge distribution (CD) model[J]. Journal of Colloid and Interface Science, 179(2): 488–508.
DOI:10.1006/jcis.1996.0242
|
胡珊, 聂麦茜, 卢金锁, 等. 2011. 镉对砷在二氧化钛上吸附性能的影响[J]. 环境化学, 2011, 30(4): 739–746.
|
Hiemstra T, Riemsdijk W H V. 2006. On the relationship between charge distribution, surface hydration, and the structure of the interface of metal hydroxides[J]. Journal of Colloid and Interface Science, 301(1): 1–18.
DOI:10.1016/j.jcis.2006.05.008
|
Jing C Y, Meng X G, Liu S Q, et al. 2005. Surface complexation of organic arsenic on nanocrystalline titanium oxide[J]. Journal of Colloid and Interface Science, 290(1): 14–21.
DOI:10.1016/j.jcis.2005.04.019
|
Luo T, Cui J L, Hu S, et al. 2010. Arsenic removal and recovery from copper smelting wastewater using TiO2[J]. Environmental Science & Technology, 44(23): 9094–9098.
|
Li W, Wang Y J, Zhu M, et al. 2013. Inhibition mechanisms of Zn precipitation on aluminum oxide by glyphosate:A 31P NMR and Zn EXAFS study[J]. Environmental Science & Technology, 47(9): 4211–4219.
|
兰华春, 焦兆飞, 赵旭, 等. 2013. MnO2吸附-氧化去除草甘膦的研究[J]. 环境科学学报, 2013, 33(8): 2181–2186.
|
Mayakaduwa S S, Kumarathilaka P, Herath I, et al. 2016. Equilibrium and kinetic mechanisms of woody biochar on aqueous glyphosate removal[J]. Chemosphere, 144: 2516–2521.
DOI:10.1016/j.chemosphere.2015.07.080
|
Mcconnell J S, Hossner L R. 1985. pH-Dependent adsorption isotherms of glyphosate[J]. Journal of Agricultural and Food Chemistry, 33(6): 1075–1078.
DOI:10.1021/jf00066a014
|
Nourouzi M M, Chuah T G, Choong T S Y. 2010. Adsorption of glyphosate onto activated carbon derived from waste newspaper[J]. Desalination and Water Treatment, 24: 321–326.
DOI:10.5004/dwt.2010.1461
|
Ronson T K, McQuillan A J. 2002. Infrared spectroscopic study of calcium and phosphate ion coadsorption and of brushite crystallization on TiO2[J]. Langmuir, 18(12): 5019–5022.
DOI:10.1021/la011676q
|
Sheals J, Sjoberg S, Persson P. 2002. Adsorption of glyphosate on goethite:Molecular characterization of surface complexes[J]. Environmental Science & Technology, 36(14): 3090–3095.
|
Sheals J, Persson P, Hedman B. 2001. IR and EXAFS spectroscopic studies of glyphosate protonation and copper(Ⅱ) complexes of glyphosate in aqueous solution[J]. Inorganic Chemistry, 40(17): 4302–4309.
DOI:10.1021/ic000849g
|
Song J Y, Yan L, Duan J M, et al. 2017. TiO2 crystal facet-dependent antimony adsorption and photocatalytic Oxidation[J]. Journal of Colloid and Interface Science, 496: 522–530.
DOI:10.1016/j.jcis.2017.02.054
|
Tzaskos D F, Marcovicz C, Dias N M P, et al. 2012. Development of sampling for quantification of glyphosate in natural waters[J]. Ciência E Agrotecnologia, 36(4): 399–405.
DOI:10.1590/S1413-70542012000400003
|
Tomaas U, Esmeralda M, Celia Q. 2002. Study of glyphosate-coppercomplexes[J]. Journal of Agricultural and Food Chemistry, 50: 1918–1921.
DOI:10.1021/jf010988w
|
Tadanier C J, Eick M J. 2002. Formulating the charge-distribution multisite surface comp lexation model using F ITEQL[J]. Soil Science Society of America Journal, 66(5): 1505–1517.
DOI:10.2136/sssaj2002.1505
|
Williams G M, Kroes R, Munro I C, et al. 2000. Safety evaluation and risk assessment of theherbicide Roundup and its active ingredient, glyphosate, for humans[J]. RegulatoryToxicology and Pharmacology, 31(2): 117–165.
|
Wu H B, Chen J S, Lou X W, et al. 2011. Asymmetric anatase TiO2 nanocrystals with exposed high-index facets and their excellent lithium storage properties[J]. Nanoscale, 3(10): 4082–4084.
DOI:10.1039/c1nr10854a
|
 2018, Vol. 38
2018, Vol. 38


