乳化油是由大豆油、食品级乳化剂和去离子水混合形成的稳定乳浊液, 粒径多为微米级, 也称微米乳化油(赵阅坤等, 2016;生贺等, 2015), 具有廉价、高能、无毒、缓释和长效等特性(Zawtocki, 2005).与葡萄糖、醋酸盐、乙醇等相比, 能够有效弥补小分子碳源易被微生物利用、消耗快、需要频繁补充的缺陷.基于该优势, 乳化油被广泛用于原位修复硝酸盐(Hunter, 2001), 铝、锰、铜及六价铬等重金属(Lindow et al., 2005; 生贺等, 2015)、氯代溶剂(Borden, 2007; Newman et al., 2006; Harkness et al., 2013)、高氯酸盐(Borden, 2007)、放射性元素铀(Tang et al., 2013; Watson et al., 2013; Deng et al., 2016)污染地下水等领域, 且取得了良好的效果.但在实际应用中也出现了一些失败的案例, 其中最主要的原因之一即为:乳化油注入含水层进行修复时, 往往导致含水层介质渗透性在一定程度上有所损失, 严重时甚至会引起堵塞.这种情况一旦发生, 受污染的地下水流经反应带时难免会产生绕流现象, 从而导致修复效率降低或者丧失.
Hunter(2001)通过沙箱实验模拟乳化油反应带去除地下水中的硝酸盐污染时发现, 受微生物繁殖及N2、CO2生成的影响, 多孔介质渗透性损失为27%.Borden(2007)的研究显示, 在场地修复四氯乙烯及氯化溶剂污染地下水实验中, 乳化油注入激活了含水层中微生物的活性, 微生物的过度繁殖导致含水层渗透性损失高达39%~91%.温春宇等(2013)利用柱实验模拟乳化油降解硝基苯时发现,乳化油注入后实验柱渗透性下降约31.5%~72.0%, 分析认为微生物繁殖累积和乳化油截留可能是引起渗透性损失的原因.Coulibaly等(2004)在开展乳化油注入对含水层介质渗透性的影响研究中指出, 在没有微生物的前提条件下, 单纯乳化油迁移造成多孔介质渗透性损失可达40%.目前, 关于生物量的累积和气体的生成对多孔介质渗透性损失的影响已得到了广泛的关注(杨靖等, 2011).然而, 对于乳化油粒径、介质颗粒大小、介质形状、表面粗糙程度及孔隙尺寸等引起的渗透性变化却依然关注较少.
Newman等(2006)指出, 乳化油在多孔介质中的吸附残留及乳化油粒径大于含水层介质孔径产生的物理截留也可能是引起渗透性损失的重要原因之一.为此, 本文尝试从降低乳化油粒径的角度出发, 采用升温相转变技术手段, 制备出纳米乳化油, 并采用柱实验模拟对比的方式, 探索纳米乳化油注入后多孔介质渗透性损失降低的可能性及程度、纳米乳化油的迁移特性, 揭示乳化油在地下水原位修复过程中造成含水层透性损失及堵塞的原因, 以期为解决该类问题提供理论依据.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 实验试剂及介质纳米乳化油配制用试剂包括金龙鱼大豆油、吐温80、斯盘80;柱实验用试剂及介质包括EDTA、去离子水、中颗粒(0.25~0.50 mm)及细颗粒(0.10~0.25 mm)石英砂.石英砂基本理化性质见表 1.
| 表 1 石英砂基本理化性质 Table 1 The basic physical and chemical properties of silica sand |
主要包括电动增力搅拌器(JJ-1, 常州市环宇科技仪器厂)、超声仪(DFD-700, 高电电子仪器厂)、恒温水浴箱(HH-M6, 上海赫田科学仪器有限公司)、高压锅(XFS-280MB, 上海上天精密仪器有效公司)、动态光散射粒度分析仪(LB-550, 日本HARIBA仪器公司).
2.1.3 纳米乳化油的制备纳米乳化油制备采用升温相转变的方法(Pan et al., 2014).将食品级乳化剂吐温80、斯盘80与大豆油、去离子水按照一定比例混合, 在电动增力搅拌器下, 以1500 r·min-1的速率搅拌10 min, 超声仪超声处理20 min.超声处理结束后, 利用恒温水浴箱加热至相转变温度, 得到稳定的纳米乳化油, 静置48 h无破乳分层现象.利用动态光散射粒度分析仪对纳米乳化油粒径进行表征, 得到的纳米乳化油粒径分布如图 1所示, 平均粒径255.1 nm.
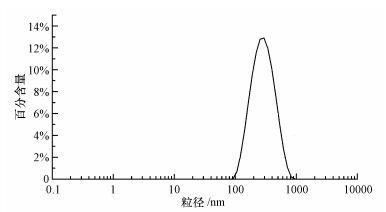 |
| 图 1 纳米乳化油粒径分布 Fig. 1 The particle size distribution of nano emulsified oil |
实验柱设计及装填:实验采用有机玻璃柱, 规格(内径×长度)为5 cm×65 cm, 实验装置见图 2.实验柱水平放置, 采用定水头方式供水, 进出水口两端为U形管构造, 达到连通饱水的目的.实验柱两端各填充2.5 cm厚、粒径为1 mm左右的粗颗粒石英砂, 用于缓冲进水.柱体分别采用中砂和细砂装填, 总填充长度65 cm.距离进水口17.5 cm处设置乳化油注入口, 内插内径0.5 cm、四周有孔且充满玻璃棉的花管, 用于注入和分散乳化油.距离乳化油注入口左7.5 cm、右37.5 cm处设置两测压管, 用来观察测压水位, 以反映乳化油注入前后实验柱渗透系数的变化.
 |
| 图 2 实验装置示意图 Fig. 2 Schematic diagram of experimental set-up |
实验柱预处理:实验柱装填完毕后, 先进行多孔介质孔径的测定.待孔径测定结束, 将实验柱垂直放置, 从底部向砂柱内缓慢通水, 用来驱除砂柱内的气泡.待完全饱水后停止供水, 让实验柱在自然状态下进行重力释水, 获取有效孔隙体积等相关参数.参数获取完毕后, 将实验柱水平放置, 继续供水, 以形成稳定的饱和流场.与此同时, 校正测压管水位, 检验杂质离子, 并使用锡箔纸包裹实验柱, 以达到模拟含水层的目的.
实验柱运行及取样:共设置3根实验柱, 填充介质和乳化油类型见表 2.其中, 所用微米乳化油由本课题组赵阅坤等(2016)配制而成, 平均粒径为59.7 μm.在乳化油注入之前, 向实验柱内通入0.01 mol·L-1的氯化钠溶液进行氯离子示踪实验, 水流速度为0.1 m·d-1, 判定实验柱是否存在优先流;同时, 拟合获取实验柱弥散系数(李宵等, 2012).实验过程中氯离子的测定采用硝酸银滴定法(国家环保总局《水和废水监测分析方法》编辑委员会, 2012).氯离子穿透后, 冲洗实验柱, 至实验柱中无氯离子检出为止.冲洗完毕后, 迅速关闭进水口, 向3根实验柱一次性注入各类型乳化油15 mL, 乳化油注入量约占实验柱孔隙体积的2.4%~2.5%, 考察各类型乳化油注入对多孔介质渗透性的影响.乳化油注入后, 每3 h采集一次出水样品进行化学需氧量(COD)的测试, 样品量为5 mL, 测试方法为重铬酸钾法(文福姬等, 2010).
| 表 2 模拟柱实验条件 Table 2 The experiment conditions of simulated column |
利用滴管向实验柱中滴入2 mL环氧树脂AB胶来固结已完成装填的石英砂介质, 其中, A胶与B胶的混合体积比为3:1.常温下, 固化时间在40 min左右.石英砂固结后, 对其进行电镜扫描, 在北达燕园微构分析测试中心完成.根据电镜扫描结果, 采用Nano Measure 1.2图像处理软件在电镜扫描图中随机获取150个孔径样本, 统计样本孔径大小及分布区间, 绘制孔径分布直方图, 即可得到多孔介质平均孔径的大小(Li et al., 2013).
2.2.3 渗透系数计算方法使用固定于测压管上的菲林软尺(精确度0.01 mm)读取各测压管水位, 计算测压管之间的压差, 并利用达西定律计算渗透系数(王大纯等, 1995):

|
(1) |
式中, K为渗透系数(m·d-1);V为出水体积(m3);L为两测压孔之间的距离(m);△H为水头损失, 即两测压管之间的压差(m);A为实验柱的横截面积(m2);t为出水时间(d).
2.2.4 乳化油在多孔介质中的理论释放及迁移模型乳化油注入实验柱后, 在实验柱中的释放等价于等速流场中瞬时注入溶质的一维对流弥散问题, 用溶质运移模型表示.乳化油在多孔介质中的截留情况可根据乳化油理论释放结果与柱实验实际测试结果反演得出.在不考虑吸附、截留与衰变等作用下, 乳化油理论释放模型如下:
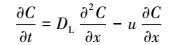
|
(2) |
半无限介质初始及边界条件如下式所示:
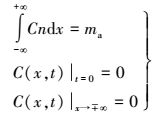
|
(3) |
根据溶质运移数学模型, 结合初始及边界条件, 得到该问题的解析解(Bear, 1972):
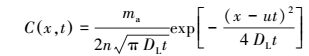
|
(4) |
式中, ma为单位过水断面注入溶质的质量(g);n为多孔介质有效孔隙度;DL为弥散系数(cm2·d-1);u为水流速度(m·s-1);x为溶质在水平向的迁移距离(m);t为溶质迁移的时间(h);C(x, t)为相应距离、时间上溶质的浓度(mg·L-1).
经典深层滤床模型主要由颗粒数量平衡方程和颗粒沉积动力方程组成, 是当前用于模拟颗粒迁移最为广泛的一种理论(Sole et al., 2006; 2010).基于深层滤床模型, 一维稳定流条件下, 乳化油在饱和多孔介质中迁移性的对流弥散方程如下:

|
(5) |

|
(6) |
式中, C为乳化油的渗流浓度(mg·L-1);θ为多孔介质孔隙度;DL为弥散系数(m2·d-1);t为时间(d);u为孔隙水流速(m·d-1);ρ为介质干密度(g·cm-3);x为乳化油迁移距离(m);σ为沉积在多孔介质表面的颗粒体积占多孔介质固体的比例;Ks为乳化油颗粒沉积系数, 与单个收集体效率有关:
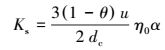
|
(7) |
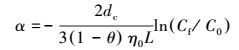
|
(8) |
式中, η0为单个收集效率参数, α为附着效率参数, dc为介质的平均粒径(m), L为实验柱有效长度(m), Cf/C0为实验柱进出水乳化油相对浓度.
在层流状态下, 地下水流速较慢, 一般忽略水动力弥散作用的影响, 且假设颗粒沉积系数在时间和空间上恒定, 即Ks为定值.在x=0处注入恒定浓度C0的乳化油, 时间为t0, 初始时刻多孔介质洁净, 不含乳化油, 得到解析解如下:
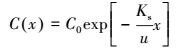
|
(9) |
纳米颗粒在多孔介质中的最大迁移距离被定义为:当99%的颗粒被截留在多孔介质中时颗粒迁移过的距离或Cf/C0为0.01时的迁移距离(Elimelech et al., 1995).由式(7)、(8)、(9)联立得出乳化油在多孔介质中迁移最大距离(Lmax)为:
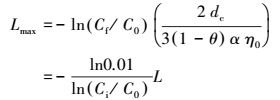
|
(10) |
式中, L为有效实验柱长度, 本实验中有效实验柱长度为47.5 cm;Ci/C0为纳米颗粒稳定出流的相对浓度, 也表示多孔介质中纳米颗粒出流百分比.
3 结果与讨论(Results and discussion) 3.1 实验柱基本参数及孔径分析氯离子示踪及拟合结果如图 3所示.Koestel等(2013)统计研究了65组穿透曲线的数据库发现, 当弥散性λ大于19.28 cm时, 通常出现优先流.经验证, 本实验所有λ均小于0.5 cm, 故认为各实验柱均不存在优先流.采用对流弥散均衡模型(CDE)对氯离子示踪结果进行拟合(CXTFIT 2.1), 结果显示, 可决系数均大于0.98, 拟合效果较好, 表明将氯离子的弥散系数应用于乳化油理论释放模型中是切实可行的.同时, 根据拟合结果获取各实验柱弥散系数.实验柱基本参数包括孔隙体积、有效孔隙度和弥散系数等, 各参数结果见表 3.
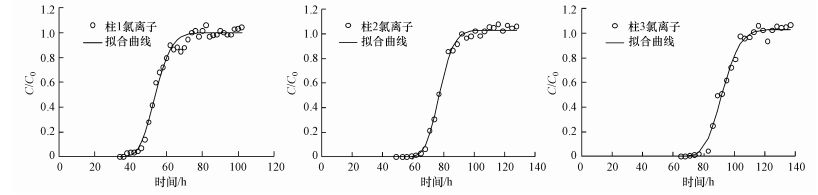 |
| 图 3 氯离子示踪及拟合结果 Fig. 3 The chloride ion tracer and the fitting results |
| 表 3 实验柱基本参数 Table 3 The basic parameters of experiment column |
实验柱中填充的中、细砂介质扫描电镜如图 4所示, 经Nano Measure处理得到填充介质的孔径分布直方图见图 5.结果显示, 70%的中砂(柱1、柱2)孔径范围主要集中在22.6~47.5 μm, 最大与最小孔径分别为88.37 μm和6.38 μm, 平均孔径为38.27 μm.80%的细砂(柱3)孔径范围主要集中在4.8~26.0 μm, 最大孔径为47.42 μm, 最小孔径为4.00 μm, 平均孔径为18.24 μm.乳化油粒径与多孔介质孔径对比显示, 大于中、细砂介质孔径的各粒径纳米乳化油百分含量为零, 而各粒径的微米乳化油百分含量为96.3%.
 |
| 图 4 中颗粒(a)、细颗粒(b)石英砂介质电镜扫描图 Fig. 4 The electron microscope scanning figure of medium (a) and fine (b) sand |
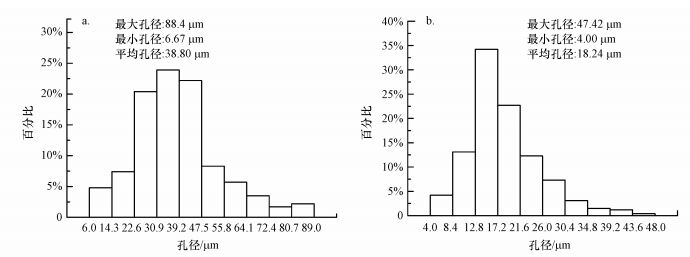 |
| 图 5 中颗粒(a)、细颗粒(b)石英砂介质孔径分布直方图 Fig. 5 The pore size distribution histogram of medium (a) and fine (b) sand |
实验柱渗透性损失通过乳化油注入前后多孔介质渗透系数比值(K/K0)的变化来体现.乳化油注入前, 实验柱1、2、3所对应渗透系数分别为13.01、12.90和8.35 m·d-1.乳化油注入后, 实验柱渗透性变化如图 6所示, 乳化油注入造成3根实验柱渗透性迅速降低,其中, 柱2渗透性降低程度最大, 柱3次之, 柱1最小.渗透性降低至一定程度后, 随着出水体积的增加逐渐恢复, 但均小于初始的渗透性水平.最终, 各实验柱渗透性均维持在一定范围内稳定波动.纳米乳化油注入致使柱1中砂介质渗透性损失可达32.1%, 随着出水体积的增加, 渗透性有所恢复, 最终渗透性损失约为3.20%.微米乳化油注入柱2中砂介质后, 造成永久性的渗透性损失为20.40%.纳米乳化油注入后, 柱3细砂介质渗透性损失可达30.1%, 随后逐渐恢复并稳定至7.46 m·d-1, 导致最终渗透性损失10.70%.
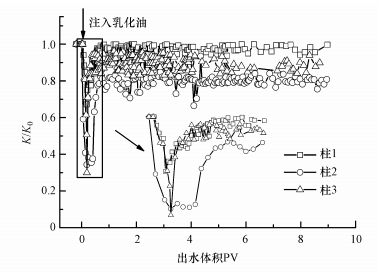 |
| 图 6 乳化油注入对多孔介质渗透性的影响 Fig. 6 Impact of emulsified oil injection on the permeability of porous media |
柱1与柱2对比显示, 在中砂介质中, 纳米乳化油注入造成的渗透性损失远小于微米乳化油.柱1与柱3对比显示, 纳米乳化油在中砂介质中的渗透性损失小于细砂介质.根据多孔介质渗透性损失结果, 结合乳化油粒径及多孔介质孔径大小, 分析认为乳化油在多孔介质中的截留可能是影响渗透性损失的重要因素.乳化油粒径越小, 介质孔径越大, 则越不易发生截留, 相应渗透性损失越小;反之渗透性损失越大.乳化油粒径及多孔介质孔径分析结果显示, 纳米乳化油粒径远小于中、细砂介质孔径, 不易被截留.因此, 无论是中砂还是细砂, 纳米乳化油注入后造成的渗透性损失均小于微米乳化油, 表明纳米乳化油原位修复时, 确实可以有效降低多孔介质渗透性损失.与此同时, 纳米乳化油还可被用于介质颗粒更小、渗透性更低的含水层介质中, 一定程度上扩大了其在含水层中的应用范围.与微米乳化油注入造成中砂的渗透性损失相比, 纳米乳化油有效减少中、细砂介质渗透性损失分别为84.3%和47.5%.然而, 无论中砂还是细砂, 渗透性降低至一定程度后, 随着出水体积的增加均有所恢复, 分析认为乳化油在水中的溶解作用是影响渗透性恢复的主要因素, 在水流冲刷下, 部分截留的乳化油逐渐溶解于水中, 堵塞程度得到逐步缓解, 多孔介质渗透性损失逐渐恢复, 乳化油在水中溶解达到最大时, 渗透性损失恢复程度也达到最大.
3.3 纳米乳化油在多孔介质中的截留为进一步明确乳化油截留与多孔介质渗透性损失的关系, 根据乳化油一维对流弥散释放理论和实际的COD释放情况来探究其在多孔介质中的截留, 其中, 理论值由式(4)计算得到.各实验柱COD释放的理论与实际值如图 7所示, 起始阶段, 在3根实验柱中, 乳化油COD释放的理论值均高于实际值, 表明乳化油在多孔介质中迁移时确实产生截留, 受截留作用的影响, 乳化油未能完全释放, 导致实际COD释放量小于理论值.该阶段过后, 乳化油在多孔介质中的实际COD释放量高于理论值, 表明乳化油截留量已经达到极限状态, 将不再被多孔介质截留, 且随出水体积的增加, 之前截留的那部分乳化油也开始缓慢释放COD, 致使乳化油实际的COD释放值高于理论值.
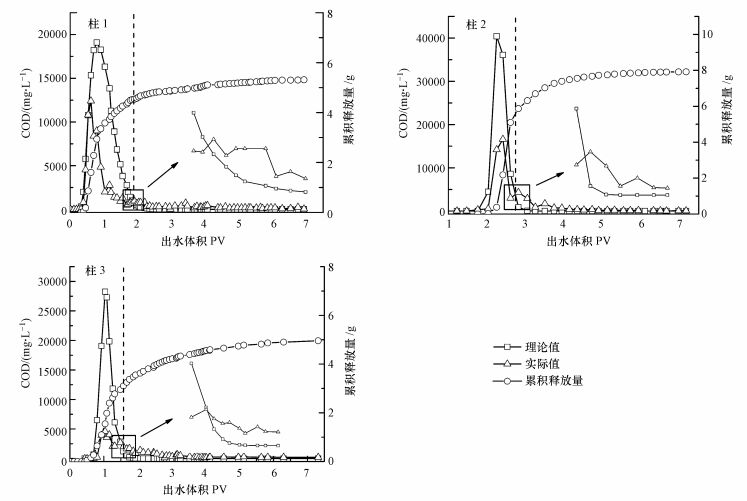 |
| 图 7 乳化油在多孔介质中COD释放理论值与实际值 Fig. 7 The theoretical and practical COD value of emulsified oil releasing in porous media |
根据质量守恒定律, 结合多孔介质中乳化油释放COD的理论值、实际值及出水体积, 计算得到乳化油在实验柱1、2和3中的截留比率分别为20.15%、28.51%和25.71%.对应乳化油截留量表现为:柱2>柱3>柱1.在中砂介质中, 微米乳化油截留量大于纳米乳化油;介质类型对纳米乳化油截留表现为:细砂介质截留量大于中砂介质.
图 8显示, 乳化油在多孔介质中的截留比率与多孔介质渗透性损失呈明显的正向变化关系.截留比率越高, 渗透性损失越大;截留比率越小, 渗透性损失越小.表明乳化油在多孔介质中的截留确实对多孔介质渗透性损失有重要影响.
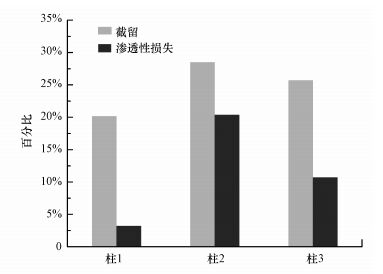 |
| 图 8 乳化油截留比率与多孔介质渗透性损失关系 Fig. 8 The relationship between emulsified oil entrapment ratio and porous media permeability |
迁移距离的变化是截留及渗透性损失对乳化油在多孔介质中迁移特性影响的直接体现.Borden(2007)采用深层滤床理论描述乳化油在多孔介质中的迁移特性.参照该理论, 根据乳化油注入及累积释放情况, 结合出水体积, 预测得出乳化油在多孔介质中的最大迁移距离(式(10)), 结果见表 4.
| 表 4 乳化油在多孔介质中最大迁移距离 Table 4 The biggest distance of emulsified oil migration in porous media |
由表 4可知, 乳化油在实验柱1、2、3中的迁移距离表现为:柱1>柱3>柱2.介质类型相同时, 纳米乳化油迁移距离大于微米乳化油, 这是由于纳米乳化油能够有效降低其在中砂介质中的截留比率和渗透性损失, 在一定程度上, 更利于自身迁移.中、细砂介质对纳米乳化油迁移特性影响表现为:纳米乳化油在中砂介质中的迁移距离大于细砂, 迁移能力更强.细砂介质较大的截留比率及渗透性损失是限制纳米乳化油迁移的主要因素.尽管介质类型对纳米乳化油迁移距离有一定影响, 但总体而言, 纳米乳化油迁移效果均优于微米乳化油, 说明通过缩小乳化油粒径来降低截留量及渗透性损失在一定程度上能够促进乳化油在多孔介质中的迁移.
4 结论(Conclusions)1) 在中砂介质中, 纳米和微米乳化油所导致的渗透性损失分别为3.20%和20.40%, 对应截留比率分别为20.15%和28.51%.相比之下, 纳米乳化油在细砂介质中渗透性损失为10.70%, 截留比率为25.71%.乳化油截留是多孔介质渗透性损失的重要原因, 减小乳化油粒径得到的纳米乳化油可有效缓解多孔介质渗透性损失.其中, 纳米乳化油减少中、细砂介质渗透性损失分别为84.3%和47.5%.
2) 乳化油截留对多孔介质渗透性损失的影响在一定程度上也影响到其在多孔介质中的迁移距离, 微米和纳米乳化油在中砂介质中迁移距离分别为6.53 m和8.19 m, 纳米乳化油在细砂介质中的迁移距离为7.36 m.纳米乳化油在中、细砂介质中的迁移效果均更佳, 说明纳米乳化油可适用的介质范围更广.
Bear J. 1972. Dynamics of Fluids in Porous Media[M].New York:Elsevier
|
Borden R C. 2007. Concurrent bioremediation of perchlorate and 1, 1, 1-trichloroethane in an emulsified oil barrier[J]. Journal of Contaminant Hydrology, 94: 13–33.
DOI:10.1016/j.jconhyd.2007.06.002
|
Coulibaly K M, Borden R C. 2004. Impact of edible oil injection on the permeability of aquifer sands[J]. Journal of Contaminant Hydrology, 71: 219–237.
DOI:10.1016/j.jconhyd.2003.10.002
|
Deng Y, Zhang P, Qin Y, et al. 2016. Network succession reveals the importance of competition in response to emulsified vegetable oil amendment for uranium bioremediation[J]. Environmental Microbiology, 18(1): 205–218.
DOI:10.1111/emi.2016.18.issue-1
|
Elimelech M, Gregory J, Jia X, et al. 1995. Particle Deposition & Aggregation, Measurement, Modelling and Simulation[M]. Woburn, MA:Butter-worth-Heinemann
|
国家环保总局《水和废水监测分析方法》编辑委员会. 2012. 水和废水监测分析方法(第四版)[M]. 北京: 中国环境科学出版社.
|
Harkness M, Fisher A. 2013. Use of emulsified vegetable oil to support bioremediation of tcednapl in soil columns[J]. Journal of Contaminant Hydrology, 151: 16–33.
DOI:10.1016/j.jconhyd.2013.04.002
|
Hunter W J. 2001. Use of vegetable oil in a pilot-scale denitrifying barrier[J]. Journal of Contaminant Hydrology, 53: 119–131.
DOI:10.1016/S0169-7722(01)00137-1
|
Koestel J K, Norgaard T, Luong N M, et al. 2013. Links between soil properties and steady-state solute transport through cultivated topsoil at the field scale[J]. Water Resources Research, 49(2): 790–807.
DOI:10.1002/wrcr.20079
|
Li M D, Hu M, Liu Q L, et al. 2013. Microstructure characterization and NO2 sensing properties of porous silico with intermediate pore size[J]. Applied Surface Science, 268: 188–194.
DOI:10.1016/j.apsusc.2012.12.057
|
Lindow N L, Borden R C. 2005. Anaerobic bioremediation of acid mine drainage using emulsified soybean oil[J]. Mine Water and the Environment, 24: 199–208.
DOI:10.1007/s10230-005-0096-9
|
李宵, 都基众, 崔健, 等. 2012. 应用土柱实验求解地下含水介质弥散系数[J]. 地下水, 2012, 34(4): 20–22.
|
Newman W A, Pelle R C. 2006. Enhanced anaerobic bioremediation of chlorinated solvents utilizing vegetable oil emulsions[J]. Remediation Journal, 16: 109–22.
|
Pan H, Yu L J, Xu J, et al. 2014. Preparation of highly stable concentrated W/O nanoemulsions by PIC method at elevated temperature[J]. Colloids and Surfaces A-physicochemical and Engineering Aspects, 447: 97–102.
|
生贺, 于锦秋, 刘登峰, 等. 2015. 乳化植物油强化地下水中Cr(Ⅵ)的生物地球化学还原研究[J]. 中国环境科学, 2015, 35(6): 1693–1699.
|
Sole I, Maestro A, Pey C M, et al. 2006. Nano-emulsions preparation by low energy methods in an ionic surfactant system[J]. Colloids and Surfaces A-Physicochemical and Engineering Aspects, 288: 138–144.
|
Sole I, Pey C M, Maestro A, et al. 2010. Nano-emulsions prepared by the phase inversion composition method:Preparation variables and scale up[J]. Journal of Colloid and Interface Science, 344: 417–423.
DOI:10.1016/j.jcis.2009.11.046
|
Tang G P, Watson D B, Wu W M. 2013. U(VI) Bioreductionwith emulsified vegetable oil as the electron donor-model application to a field test[J]. Environmental Science & Technology, 47: 3218–3225.
|
Watson D B, Wu W M, Mehlhorn T, et al. 2013. In situ bioremediation of uranium with emulsified vegetable oil as the electron donor[J]. Environmental Science & Technology, 47: 6440–6448.
|
王大纯, 张人权, 史毅虹, 等. 1995. 水文地质学基础[M]. 北京: 地质出版社.
|
温春宇, 王敏, 董军, 等. 2013. 植物油改性纳米铁修复硝基苯污染地下水的研究[J]. 生态环境学报, 2013, 22(6): 1048–1052.
|
文福姬, 李建秀, 左玉香, 等. 2010. 印染废水CODcr值的快速测定法[J]. 印染, 2010(20): 41–43.
|
杨靖, 叶淑君, 吴吉春. 2011. 生物膜对饱和多孔介质渗透性影响的实验和模型研究[J]. 环境科学, 2011, 32(5): 1364–1371.
|
Zawtocki C. 2005. Naturally cleaner groundwater-soybean based emulsion is proving to decontaminate groundwater more quickly than traditional remediation methods[J]. Military Engineer, 97(637): 55–56.
|
赵阅坤, 何江涛, 王磊, 等. 2016. 乳化油碳源原位治理地下水中Cr(Ⅵ)静态批试验研究[J]. 环境工程, 2016(S1): 220–225;420.
|
 2018, Vol. 38
2018, Vol. 38


