2. 东华大学分析测试中心, 上海 201620
2. Research Center of Analysis & Measurement, Donghua University, Shanghai 201620
银是一种重要的贵金属, 广泛应用于工艺品、电子电器、摄影、医疗、成像等行业.大量的含银废水也由此产生:电镀厂含银废水、废照像定影液、半导体生产管芯的处理废液、实验室CODCr分析废液等均含有大量的银离子, 而且大部分的含银废水并不单单只含有银离子, 还含有其他金属离子, 如Cr6+、Cu2+、Ni2+、Zn2+、Fe2+等.如不妥当处理, 会对环境及人体健康造成极大的危害(尚会来等, 2012).当前常用的提取方法有沉淀法、电解法、离子交换法、置换法、吸附法等.但都有一定的局限性, 沉淀法对pH要求高, 需使用过量阴离子溶液, 易造成二次污染;电解法对浓度要求高, 通常与其他方法连用;离子交换法所用离子交换剂易受污染或氧化失效、费用高, 对解吸要求也高;置换法需以其他金属为代价;吸附法虽能够弥补其他方法能耗大、有二次污染、对痕量银作用不大等缺点, 但是不同吸附剂之间差异较大, 且绝大多数的吸附剂不具有选择性吸附的功能, 这对于从复杂环境中提取银离子是不利的(黄美荣等, 2015).制备一种具有选择性吸附Ag(I)的材料既有重大的经济效益, 也有良好的环境效益, 具有研究的价值与意义.
氧化石墨烯是一种准二维层状结构化合物, 拥有巨大的表面积及羧基、羟基、羰基、环氧基等含氧官能团, 具有良好的亲水性、相容性, 能够很好的分散在溶剂中(Hirata et al., 2005).氧化石墨烯极大的比表面积, 可以使其作为很多纳米材料的载体.而这些含氧官能团不仅自身能够与金属离子发生配位络合作用, 还可以通过功能化改性生成具有实用价值的功能性纳米材料.近年来研究结果表明, 氧化石墨烯及其复合材料对重金属离子与染料均有很好的吸附效果(Wang et al., 2013;吴艳等, 2013;Lakshmi et al., 2015;刘伟等, 2015;李成杨等, 2015;Ravishankar et al., 2016;Zare Dorabei et al., 2016;Zhao et al., 2016).
壳聚糖是甲壳素脱乙酰化而得到的一种天然生物高分子, 具有自然界含量丰富, 良好的生物相容性、无毒无害、易于降解等优点, 在去除重金属离子和染料上有广泛的应用(Crini et al., 2008;Ngah et al., 2011;张聪璐等, 2013;张慧敏等, 2015;Xiao et al., 2016;Wang et al., 2016;Habiba et al., 2017).壳聚糖分子链上含有大量的氨基和羟基, 游离的氨基和羟基通过氢键或盐键的作用与金属离子形成不同的配位, 生成稳定的螯合物(郭振楚等, 2001).
关于氧化石墨烯/壳聚糖复合材料吸附重金属的文章多有报道.例如, Zhang等用EDTA-2Na改性氧化石墨烯/壳聚糖复合材料用于Cr(Ⅵ)吸附.在pH=2时, 吸附量达到最大为86.17 mg·g-1.吸附过程是自发的、吸热的而且符合准二级动力学模型, 其吸附等温线符合Freundlich吸附模型, 为多层吸附(Zhang et al., 2016).Wang将一种磁性壳聚糖涂于氧化石墨烯表面制备Pb(Ⅱ)印迹材料用于Pb(Ⅱ)吸附.吸附剂最大吸附量为79 mg·g-1, 而且回用性好, 回用5次后的吸附容量为初始饱和吸附量的90%(Wang et al., 2016).武文琴将质量分数为10%的氧化石墨烯与交联的壳聚糖进行复合以提高对Cu(Ⅱ)吸附性能.结果表明, 与交联壳聚糖相比, Cu(Ⅱ)吸附量提高近一倍(武文琴, 2013).
近些年来, 新型吸附材料多以去除对环境或人体有害的重金属为主, 而对其他金属如银离子之类的贵金属研究甚少.本文研究巯基-氧化石墨烯-壳聚糖复合材料对Ag(I)的选择性吸附性能.在此实验前, 就本实验的前置材料氧化石墨烯及壳聚糖-氧化石墨烯复合材料的Ag(I)吸附性能进行了研究, 结果表明氧化石墨烯对Ag(I)最大吸附量为2.97 mg·g-1, 而壳聚糖-氧化石墨烯复合材料对Ag(I)吸附量为4.58 mg·g-1.根据文献报道巯基对Ag(I)有良好的吸附能力, 因此, 为增加材料对Ag(I)吸附性能, 选用巯基作为接枝基团(黄海兰等, 2004).选用3-巯基丙基三甲氧基硅烷(MPTMS)作为改性剂, 硅烷偶联剂上的硅氧键易发生水解生成硅烷醇, 壳聚糖-氧化石墨烯表面的氨基、羟基通过戊二醛交联作用与硅烷醇上的羟基结合, 从而把巯基接枝到壳聚糖-氧化石墨烯上(肖玲玲等, 2013).通过条件实验, 探究吸附剂投加量、温度、时间、初始浓度对吸附过程的影响, 并初步探究其吸附机理.因pH的变化会导致实验选用的混合标液的成分不稳定, 故本文中未考虑pH的影响.
2 材料与方法(Materials and methods) 2.1 实验试剂与设备主要试剂:天然鳞片石墨(99.99%, 上海一帆石墨有限公司)、硝酸钠(NaNO3)、浓硫酸(H2SO4,98%)、高锰酸钾(KMnO4)、双氧水(H2O2, 30%)、盐酸(HCl, 37.5%)、氯化钡(BaCl2)、壳聚糖((C6H11NO4)n)、戊二醛(C5H8O2, 25%)、冰乙酸(CH3COOH, 99.5%)、氢氧化钠(NaOH)均为分析纯(AR), 且均购于国药集团化学试剂有限公司.3-巯基丙基三甲氧基硅烷(MPTMS, C6H16O3SSi, 95%)为试剂级(RG)且购于阿达玛斯试剂.多离子混合标准溶液(包含Ag、Al、B、Ba、Bi、Ca、Cd、Co、Cr、Cu、Fe、Ga、In、K、Li、Mg、Mn、Na、Ni、Pb、Sr、Tl、Zn, 1000 mg·L-1)购于德国默克公司.
仪器:85-2型恒温磁力搅拌器(上海梅颖浦仪器仪表制造有限公司);超声波清洗器(SK3300LHC, 53 KHz, 180W, 上海科导超声仪器有限公司);恒温水浴振荡器(SHA-BA, 金坛市友联仪器研究所);高速台式(冷冻)离心机(SL 16R, 赛默飞世尔科技);冷冻干燥机(FD-1A-50, 上海豫明仪器有限公司).
2.2 实验方法 2.2.1 材料的制备氧化石墨烯(GO)的制备:将115 mL浓硫酸和2.5 g硝酸钠置于烧杯中, 搅拌, 冰浴冷却至5 ℃, 加入5 g天然鳞片石墨.混合均匀后缓慢加入15 g高锰酸钾, 控制反应液温度不超过20 ℃.完全溶解后, 35 ℃恒温水浴加热, 持续搅拌2 h.加入230 mL去离子水, 控制反应液温度在98 ℃左右, 继续搅拌15 min.加入700 mL去离子水终止反应.同时加入12.5 mL双氧水中和多余高锰酸钾, 混合液的颜色从棕黑色变为亮黄色, 光照下可以看到鳞片状微粒.用体积比为1:10的体积为1 L的稀盐酸和去离子水离心洗涤直至滤液近似中性.真空冷冻干燥, 备用.
壳聚糖-氧化石墨烯复合材料(CTS-GO)的制备:取0.0500 g氧化石墨于20 mL 2%乙酸溶液中, 超声分散均匀, 随后加入0.4500 g壳聚糖, 搅拌使其混合均匀.逐滴加入2 mol·L-1氢氧化钠溶液和3 mL 2.5%戊二醛溶液, 大力搅拌4 h, 随后放置在4 ℃冰箱中24 h, 用去离子水洗至成中性, 真空冷冻干燥, 备用.
巯基改性壳聚糖-氧化石墨复合材料(SFCG)的制备:取0.5000 g壳聚糖-氧化石墨烯复合材料于20 mL 2%乙酸溶液中, 超声分散均匀, 随后加入0.5 mL 3-巯基丙基三甲氧基硅烷, 充分搅拌使其混合均匀.逐滴加入2 mol·L-1氢氧化钠溶液和3 mL 2.5%戊二醛溶液, 大力搅拌4 h, 随后放置在4 ℃冰箱中24 h, 用去离子水洗至成中性, 真空冷冻干燥, 备用.
2.2.2 材料的表征材料的形貌及吸附前后的变化采用扫描电子显微镜(SEM)(JMS-5600LV, 日本JEOL)进行观察.官能团的变化采用傅里叶变换红外光谱仪(FTIR)(Nicolet 6700, 美国Thermo Fisher)在波长400~4000 cm-1范围内进行测定.元素分析采用元素分析仪(EA)(Vario EL Ⅲ, 德国Elementar)来确定.
2.2.3 吸附实验在室温下, 取一定量的SFCG加入到20 mL浓度为100 mg·L-1的混合标液中, 通过改变一系列单因素来研究材料的吸附性能.各单因素的变化范围为:吸附剂用量为0.001~0.025 g, 初始浓度为100~250 mg·L-1, 时间为0~120 min, 温度为25~55 ℃.吸附后用滤纸过滤取样液, 用电感耦合等离子体发射光谱仪(ICP)(Prodigy, 美国Leeman)测定其中各离子含量.
3 结果与讨论(Results and discussion) 3.1 材料表征红外光谱图见图 1.从图 1中可以看出, GO在3415 cm-1(O—H伸缩振动峰)、1723 cm-1(C═O伸缩振动峰)、1627 cm-1(C═C伸缩振动峰)、1400 cm-1(C—OH伸缩振动峰)、1070 cm-1(C—O伸缩振动峰)处出现吸收峰, 说明GO表面含有羟基, 羧基, 环氧基等含氧基团(Tadjarodi et al., 2016).与GO相比, CTS在1078和3422 cm-1同样出现了吸收峰.而3422 cm-1处吸收峰应该为由O—H和N—H伸缩振动重叠而成的多重吸收峰.在2921 cm-1(C—H伸缩振动峰)、1584 cm-1(N—H伸缩振动峰)、1383 cm-1(C—N伸缩振动峰)、898 cm-1(N—H弯曲振动峰)分别出现了新的吸收峰, 说明CTS表面官能团与GO不同, 表面含有氨基而没有羧基(Zhang et al., 2016).CTS-GO的吸收峰与CTS类似, 1651 cm-1为C═O伸缩振动吸收峰, 发生了偏移.因为CTS分子中引入不同取代基后, 分子间的氢键作用减弱, C═O会向低波数方向移动(徐恒志等, 2011).由此可以说明CTS和GO成功交联在一起.SFCG在2930 cm-1吸收峰变得尖锐是由于硅烷偶联剂上的CH2—CH2和C—H重叠而成多重吸收峰, 在1255和691 cm-1出现Si—CH2振动峰, 说明材料已经成功接枝上巯基.其他峰与CTS—GO类似, —SH的峰在2500~2600 cm-1之间, 因比较微弱而未显示出来(罗赞等, 2016).SFCG-Ag在2431和2383 cm-1出现两个新的吸收峰, 在—SH峰附近, 可能是由于—SH与Ag(I)发生反应形成新的S—Ag化学键, 从而产生峰值.
 |
| 图 1 FTIR图 Fig. 1 FTIR of materials in different stage |
SEM图见图 2.由图 2a和2b可以看出壳聚糖表面相对平滑, 结构紧密无孔.而氧化石墨烯呈现薄片状结构.由图 2c可知, 与之前相比, 结构发生明显变化, 壳聚糖与氧化石墨烯结合后, 材料出现层状结构, 片层相对较厚, 可能是壳聚糖包裹在氧化石墨烯表面, 形成复合夹层结构.GO的引入在一定程度上增加CTS的表面积, 提高其吸附能力.这样, 两种纳米结构的有效结合不仅可以有效地利用各自的优势, 而且可以弥补各自的不足.由图 2d可以看出, 材料接枝上—SH后层变得更薄, 表面有明显褶皱, 表面积进一步提高.图 2e所示, 吸附后材料积聚在一起, 表面凹凸不平, 应该是由于SFCG吸附了Ag(I)形成SFCG-Ag复合物, 从而造成了这种结构.
 |
| 图 2 SEM图(a.CTS, b.GO, c.CTS-GO, d.SFCG, e.SFCG-Ag) Fig. 2 SEM of materials in different stage (a.CTS, b.GO, c.CTS-GO, d.SFCG, e.SFCG-Ag) |
C、H、N元素含量见表 1.其中可以看出, CTS-GO与CTS相比, 除N元素外其他元素含量均有升高, 因为GO中基本不含有N元素, N元素含量降低说明CTS成功与GO结合.SFCG的含碳量明显下降, 因为MPTMS上的硅氧基易于与羟基发生水解反应, 生成C—Si—O键, 从而将—SH接枝到材料表面, 同时生成CH3OH留在溶液中.因吸附后引入Ag元素的缘故, SFCG-Ag各元素含量进一步下降.
| 表 1 C、H、N元素含量 Table 1 Elemental analysis of GO, CTS, CTS-GO, SFCG and SFCG-Ag |
室温下, 取20 mL浓度为100 mg·L-1的混合标液, 分别加入0.001、0.003、0.005、0.010、0.015、0.020、0.025 g SFCG, 结果如图 3a所示(仅列出部分离子, 下同).从图 3a可以看出, Ag(I)的吸附率随投加量的增加而增加, 最终达到平衡, 吸附率能够达到99%以上.随着投加量的增加, 有效吸附位点增多, 能够吸引更多的离子, 从而吸附率上升.当吸附剂的量达到一定程度时, 虽然有效位点在增加, 但溶液中已无更多的Ag(I)与其结合, 从而吸附率趋于平衡.而Ag(I)吸附量随投加量的增加而降低, 因为在一定浓度下, 随投加量的增加, 单位质量吸附剂所吸附的Ag(I)减少, 从而吸附量降低.同时可以看出, 除Ag(I)外的其他离子的吸附率基本在基线0处波动且不受投加量的影响.说明即使吸附剂有空余的吸附位点也不会吸附除Ag(I)外的其他离子.从而在一定程度上能够证明此吸附剂具有选择吸附性能.
 |
| 图 3 各因素对吸附效果的影响 Fig. 3 Effect of different factors on adsorption |
室温下, 取20 mL浓度为100 mg·L-1的混合标液, 加入0.005 g SFCG, 测定不同时间下Ag(I)的吸附率, 结果如图 3b所示.从图 3b中可以看出, 在一段时间内, Ag(I)吸附率和吸附量随时间的增加而增加.SFCG对Ag(I)的吸附速率很快, 5 min内即可达到90%以上, 30 min即趋于平衡.吸附率短时间内达到平衡, 主要归功于SFCG表面的功能性基团, 如巯基.同样可以看出, 其他离子的吸附率均处于很低的水平, 说明吸附剂SFCG具有选择性且与吸附时间无关.在120 min, SFGO对Ag(I)吸附率为99.13%, 吸附量为396.51 mg·g-1.
3.2.3 初始浓度室温下, 取0.005 g SFCG加入到20 mL一定浓度的混合标液中, 混合标液的浓度分别为100、150、200、250 mg·L-1.如图 3c所示, Ag(I)吸附率随浓度的增加而降低, 从99.12%下降到57.84%, 而吸附量随浓度的增加而增大, 从396.51 mg·g-1升高至578.41 mg·g-1.出现这种现象的原因可能是由于在吸附剂一定量的情况下, 吸附剂上的有效位点数一定.随浓度的增加, 吸附位点逐渐被填满, 因此吸附量增加.同样随浓度的增加, 虽然有部分Ag(I)被吸附, 但溶液中游离的Ag(I)增多, 吸附率下降.其他离子的吸附情况与之前类似.
3.2.4 温度取0.005 g SFCG加入到20 mL浓度为100 mg·L-1混合标液中分别置于298.15、308.15、318.15、328.15 K下, 1 h和平衡时的吸附情况如图 3d和图 3e.从图 3d中可以看出, Ag(I)吸附率一直处于较高水平, 接近100%, 而图 3e显示平衡时Ag(I)吸附率在55 ℃时降低到50%以下, 为47.43%.其他温度下Ag(I)吸附率也均在99%左右.造成这种现象的原因可能是长时间处于高温下, 壳聚糖不稳定发生分解, 从而改变了SFCG的特性, 使其表面不稳定, 从而导致Ag(I)解吸.另外, SFCG表面基团与Ag(I)的结合的化学键变得不稳定, 发生断裂, 造成Ag(I)解吸, 吸附率下降.其他离子的吸附情况与之前类似.
3.3 吸附等温线用Langmuir和Freundlich吸附等温模型来拟合SFCG对Ag(I)的吸附过程.根据所得数据拟合吸附等温线, 结果见图 4.两种吸附等温线相关参数见表 2.由表 2可以看出Langumir吸附等温线可决系数R2值(R2=0.9835) 远大于Freundlich吸附等温线可决系数R2值(R2=0.7588), 且由Langmuir等温线模型计算得到的SFCG对Ag(I)吸附量的拟合值(584.795 mg·g-1)与实验数据(578.406 mg·g-1)相契合, 说明Langmuir等温吸附模型可有效地描述其吸附过程, SFCG对Ag(I)的吸附为单层吸附.另外, Freundlich吸附等温线参数n=10.4450 >10, 说明Freundlich吸附等温模型不能够用来描述此吸附过程.
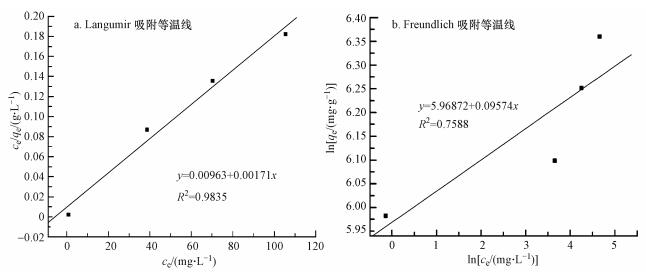 |
| 图 4 吸附等温线 Fig. 4 Adsorption isotherms |
| 表 2 吸附等温方程拟合参数 Table 2 Parameters of the adsorption isotherms |
吸附动力学主要是研究吸附剂对吸附质的吸附速率受何种因素制约, 从而探讨其吸附机理.分别采用准一级动力学方程、准二级动力学方程和粒子内扩散方程对吸附实验数据进行拟合, 拟合结果见图 5.计算得动力学参数见表 3.准一级动力学模型描述以物理扩散为主的初始阶段, 该阶段受吸附界面两侧离子浓度差的影响.准二级动力学模型描述的是吸附的整个过程, 包括外膜扩散、表面吸附和颗粒内扩散等.颗粒内扩散模型主要描述的是吸附质在吸附剂内部扩散的过程.从图 5和表 3中可知, 在不同浓度下, 准二级动力学方程参数R2值均达到0.9990以上, 高于其他两种方程参数的R2值.同时通过准二级动力学方程计算得到的qe值与实验中得到的吸附平衡时的吸附容量很接近, 说明准二级动力学模型能够描述SFCG对Ag(I)的吸附过程, 且以化学吸附为主.另外, 粒子内扩散的拟合系数, 说明吸附初期, 发生了颗粒内吸附, 粒子内扩散是吸附过程速控步骤之一.综合考虑, SFCG对Ag(I)的吸附过程受吸附剂表面的活性位点和内扩散的共同作用.
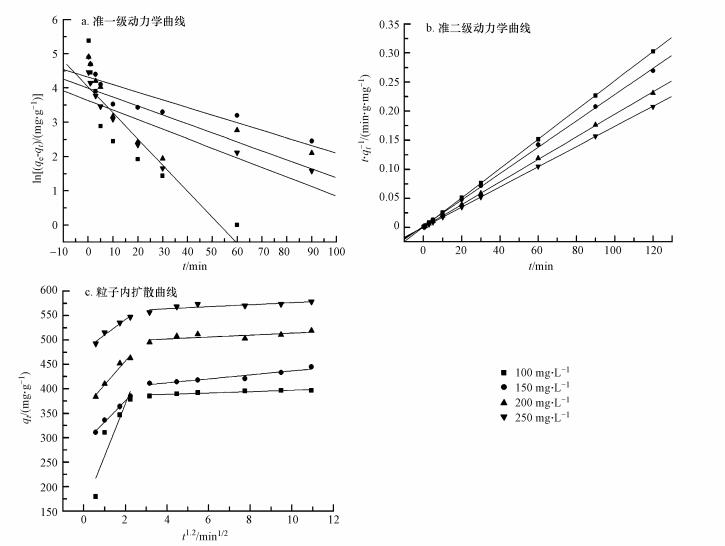 |
| 图 5 吸附动力学方程拟合曲线 Fig. 5 Adsorption kinetic equation fitting curves |
| 表 3 不同浓度下吸附动力学拟合参数 Table 3 Parameters of the adsorption kinetics at different initial concentration |
吸附热力学用来研究吸附过程的自发性及判定吸附过程是放热的还是吸热的, 研究吸附热力学可以了解吸附过程的趋势、程度和驱动力.以lnK对1 /T作图, 结果如图 6所示.通过lnK/T-1直线的斜率和截距求出焓变ΔH和熵变ΔS, 从而求出ΔG, 具体数值见表 4.从表 4中可知, 吉布斯自由能ΔG为负值, 说明SFCG对Ag(I)的吸附过程是自发, 且随温度的升高, ΔG绝对值降低, 说明随着温度的升高, 吸附过程自发趋势降低, 升温不利于吸附的进行;焓变ΔH为负值, 说明该吸附过程为放热反应;熵变ΔS为负值, 说明SFCG对Ag(I)的吸附使得吸附质分子的自由度减少, 吸附过程熵减少.
 |
| 图 6 吸附热力学方程拟合曲线 Fig. 6 Thermodynamic equation fitting curves |
| 表 4 不同温度下吸附热力学拟合参数 Table 4 Parameters of thermodynamic equation at different temperature |
巯基中的大量S配位原子能与银离子形成稳定配合物, 对银离子具有选择性吸附作用.同时, 氧化石墨烯具有独特的稳定片层结构, 氧化石墨烯上的大量羧基可与壳聚糖结构中的氨基发生酰胺化反应形成—NHCO—键, 再通过交联剂与巯基进行交联, 制备出巯基改性壳聚糖-氧化石墨烯复合材料, 这样的结构使得巯基在片层结构上能够有序地排列, 不易形成胶团, 并且—NHCO—合适的键长既能保持相对稳定不易被断开, 同时也能降低相邻银离子之间的排斥力, 正是通过巯基与壳聚糖-氧化石墨烯的这种协同作用, 从而增加了银离子吸附量.
4 结论(Conclusions)1) 通过对各个阶段材料进行表征发现, GO与CTS结合能够在一定程度上增加CTS的表面积, 提高其吸附能力.同时—SH的引入在对Ag(I)选择吸附上起到至关重要的作用.
2) 通过单因素实验发现, SFCG对Ag(I)具有优异的选择性吸附性能.一定浓度下, 10 min内即可达到最佳的吸附效果, Ag(I)吸附量随浓度的增加而增加, 但长时间处在高温下, 会造成材料的变性, 吸附率降低.在室温、初始浓度为250 mg·L-1, 吸附剂用量为0.005 g的条件下, Ag(I)吸附量达到最大为578.41 mg·g-1.
3) SFCG对Ag(I)吸附过程复合Langmuir吸附等温线和伪二级动力学方程, 说明SFCG对Ag(I)吸附为单层吸附, 化学吸附.由热力学方程可知, 吸附过程是自发的, 放热的.
4) SFCG有望成为一种能够从复杂体系中高效提取银的材料.
Crini G, Badot P M. 2008. Application of chitosan, a natural aminopolysaccharide, for dye removal from aqueous solutions by adsorption processes using batch studies:A review of recent literature[J]. Progress in Polymer Science, 33(4): 399–447.
DOI:10.1016/j.progpolymsci.2007.11.001
|
郭振楚, 韩亮, 谭凤姣, 等. 2001. 壳聚糖及其衍生物与金属配位的研究进展[J]. 化学研究与应用, 2001, 13(1): 21–26.
|
Habiba U, Afifi A M, Salleh A, et al. 2017. Chitosan/(polyvinyl alcohol)/zeolite electrospun composite nanofibrous membrane for adsorption of Cr6+, Fe3+, and Ni2+[J]. Journal of Hazardous Materials, 322: 182–194.
DOI:10.1016/j.jhazmat.2016.06.028
|
Hirata M, Gotou T, Ohba M. 2005. Thin-film particles of graphite oxide:Preliminary studies for internal miero fabrication of single particle and carbonaceous electronic circuits[J]. Carbon, 43: 503–510.
DOI:10.1016/j.carbon.2004.10.009
|
黄海兰, 徐波, 曲荣君. 2004. 巯基树脂对Ag+、Hg2+、Cr3+的吸附性能的研究[J]. 应用科技, 2004, 31(12): 61–62.
DOI:10.3969/j.issn.1009-671X.2004.12.022 |
黄美荣, 李振宇, 李新贵. 2005. 含银废液来源及其回收方法[J]. 工业用水与废水, 2005, 36(1): 9–12.
|
Lakshmi P, Lingamdinne J R, Koduru H, et al. 2015. Adsorption removal of Co(Ⅱ) from waste-water using graphene oxide[J]. Hydrometallurgy, 165: 90–96.
|
李成杨, 庄泽超, 金晓英, 等. 2015. 氧化石墨烯对亚甲基蓝和铜离子的共吸附行为研究[J]. 环境科学学报, 2015, 35(10): 3163–3169.
|
刘伟, 杨琦, 李博, 等. 2015. 磁性石墨烯吸附水中Cr(Ⅵ)研究[J]. 环境科学, 2015, 36(2): 537–544.
|
罗赞, 胡鑫, 欧阳瑜婷, 等. 2016. 巯丙基三甲氧基硅烷对黄铁矿包膜条件的优化[J]. 环境化学, 2016, 35(6): 1287–1295.
DOI:10.7524/j.issn.0254-6108.2016.06.2015112006 |
Ngah W S W, Teong L C, Hanafiah M A K M. 2011. Adsorption of dyes and heavy metal ions by chitosan composites:A review[J]. Carbohydrate Polymers, 83(4): 1446–1456.
DOI:10.1016/j.carbpol.2010.11.004
|
Ravishankar H, Wang J, Shu L, et al. 2016. Removal of Pb (Ⅱ) ions using polymer based graphene oxide magnetic nano-sorbent[J]. Process Safety & Environmental Protection, 104: 472–480.
|
尚会来, 张雷, 张静蓉. 2012. 电镀废水处理技术展望[J]. 给水排水, 2012, 38(1): 260–263.
|
Tadjarodi A, Moazen F S, Zare Dorabei R, et al. 2016. Highly efficient ultrasonic-assisted removal of Hg(Ⅱ) ions on graphene oxide modified with 2-pyridinecarboxaldehyde thiosemicarbazone:Adsorption isotherms and kinetics studies[J]. Ultrasonics Sonochemistry, 33: 118–128.
DOI:10.1016/j.ultsonch.2016.04.030
|
Wang H, Yuan X, Wu Y, et al. 2013. Adsorption characteristics and behaviors of graphene oxide for Zn(Ⅱ) removal from aqueous solution[J]. Applied Surface Science, 279(8): 432–440.
|
Wang N, Xu X, Li H, et al. 2016. Enhanced selective adsorption of Pb(Ⅱ) from aqueous solutions by one-pot synthesis of xanthate-modified chitosan sponge:Behaviors and mechanisms[J]. Industrial & Engineering Chemistry Reasearch, 55(47): 12222–12231.
|
Wang Y, Li L, Luo C, et al. 2016. Removal of Pb2+ from water environment using a novel magnetic chitosan/graphene oxide imprinted Pb(2.)[J]. International Journal of Biological Macromolecules, 86: 505–511.
DOI:10.1016/j.ijbiomac.2016.01.035
|
武文琴. 2013. 氧化石墨烯及其复合材料对重金属铜的吸附性能研究[D]. 长沙: 湖南大学
http://cdmd.cnki.com.cn/Article/CDMD-10532-1014119984.htm |
吴艳, 罗汉金, 王侯, 等. 2013. 改性石墨烯对水中亚甲基蓝的吸附性能研究[J]. 环境科学, 2013, 34(11): 4333–4340.
|
Xiao C, Liu X, Mao S, et al. 2016. Sub-micron-sized polyethylenimine-modified polystyrene/Fe3O4/chitosan magnetic composites for the efficient and recyclable adsorption of Cu(Ⅱ) ions[J]. Applied Surface Science, 394: 378–385.
|
肖玲玲, 王娜, 那平. 2013. 巯基功能化活性炭对汞离子的吸附性能研究及机理初探[J]. 现代化工, 2013, 33(10): 70–75.
|
徐恒志, 王焕, 鲍俊杰, 等. 2011. 水性聚氨酯硬段含量对其氢键相互作用及性能的影响[J]. 应用化学, 2011, 28(7): 770–776.
|
Zare Dorabei R, Ferdowsi S M, Barzin A, et al. 2016. Highly efficient simultaneous ultrasonic-assisted adsorption of Pb(Ⅱ), Cd(Ⅱ), Ni(Ⅱ) and Cu (Ⅱ) ions from aqueous solutions by graphene oxide modified with 2, 2'-dipyridylamine:Central composite design optimization[J]. Ultrasonics Sonochemistry, 32: 265–276.
DOI:10.1016/j.ultsonch.2016.03.020
|
张聪璐, 胡筱敏, 英诗颖, 等. 2013. 壳聚糖季铵盐磁性颗粒的制备及其对甲基橙的吸附效果[J]. 环境科学, 2013, 34(5): 1815–1821.
|
张慧敏, 阮弦, 胡勇有, 等. 2015. 静电纺壳聚糖/聚乙烯醇纳米纤维膜对Cu2+、Ni2+及Cd2+的吸附特性[J]. 环境科学学报, 2015, 35(1): 184–193.
|
Zhang L, Luo H J, Liu P P, et al. 2016. A novel modified graphene oxide/chitosan composite used as an adsorbent for Cr(Ⅵ) in aqueous solutions[J]. International Journal of Biological Macromolecules, 87: 586–596.
DOI:10.1016/j.ijbiomac.2016.03.027
|
Zhang L, Zhu T, Liu X, et al. 2016. Simultaneous oxidation and adsorption of As(Ⅲ) from water by cerium modified chitosan ultrafine nanobiosorbent[J]. Journal of Hazardous Materials, 308: 1–10.
DOI:10.1016/j.jhazmat.2016.01.015
|
Zhao D, Gao X, Wu C, et al. 2016. Facile preparation of amino functionalized graphene oxide decorated with Fe3O4 nanoparticles for the adsorption of Cr(Ⅵ)[J]. Applied Surface Science, 384: 1–9.
DOI:10.1016/j.apsusc.2016.05.022
|
 2017, Vol. 37
2017, Vol. 37


