2. 广东省大气环境与污染控制重点实验室, 广州 510006;
3. 华南理工大学工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006
2. Guangdong Provincial Key Laboratory of Atmospheric Environment and Pollution Control, South China University of Technology, Guangzhou Higher Education Mega Centre, Guangzhou 510006;
3. The Key Lab of the Ministry of Education for Pollution Control and Ecosystem Restoration in Industry Clusters, South China University of Technology, Guangzhou 510006
氮氧化物(NOx)是常见的大气污染物之一, 会引发光化学烟雾、酸雨及臭氧层空洞等一系列重大环境问题, 对生态环境和人体健康产生极大危害(杨颖欣等, 2016;Busca et al., 2005).目前, 以NH3为还原剂的氨选择性催化还原(NH3-SCR)技术是最成熟、应用最广泛的治理固定源NOx的方法之一(Skalska et al., 2010).其中, 商业用于固定源脱硝的SCR催化剂主要为钒钨钛基催化剂(V2O5-WO3(MoO3)/TiO2).但该催化剂存在一系列的问题, 如催化剂体系中的金属钒具有生物毒性, 会产生二次污染(孙梦婷等, 2016).另一方面, 该催化剂体系的最佳活性温度较高(300~400 ℃)(Gao et al., 2013), 为避免烟气再加热, SCR装置常置于脱硫与除尘装置之前, 而此时的高浓度SO2和高烟尘反应气氛加速了催化剂的失活(Duan et al., 2012), 降低了催化剂的使用寿命.若将SCR装置安装于除尘以及脱硫之后, 则烟气温度过低(低于250 ℃), 而传统的V-W-Ti催化剂在低温时不具备良好的催化活性.因此, 研究和开发出环境友好、低温和高效的NH3-SCR催化剂(100~250 ℃)具有极其重要的意义.
目前, 对低温NH3-SCR催化剂活性组分的研究主要集中在过渡金属氧化物上, 包括Fe、Mn、Ni、Cu和Co等.由于铁基催化剂在NH3-SCR反应中具有环境友好、高活性、高N2选择性和较好的抗硫抗水性等特点, 近年来受到了科研人员的格外关注.尽管目前有关铁基催化剂的文献报道较多, 但这些铁基催化剂的操作温度主要集中在中温或高温段(200~500 ℃)(Liu et al., 2008), Mou等(2012)采用沉淀法制备的Fe2O3纳米棒在200~400 ℃内仅表现出80%的NO转化率, 低温SCR活性的不足大大限制了铁基催化剂的实际应用(Liu et al., 2010;Liu et al., 2013).因此, 如何提高铁基催化剂的低温SCR活性是一个亟需解决的问题.研究者尝试采用不同载体负载铁氧化物以提高催化剂低温SCR活性, 如Fe/ZSM-5(Du et al., 2015)、Fe/BEA(Nedyalkova et al., 2013)、Fe/CNTs(Qu et al., 2015;Han et al., 2015)和Fe2O3/TiO2(Liu et al., 2016), 但仍未能使铁基催化剂达到较佳的低温SCR活性.SAPO-34分子筛是磷酸硅铝(SAPO)系列分子筛中的一种, 具有菱沸石型(CHA)拓扑结构, 平均孔径为0.38 nm, 属于小孔分子筛(Corma, 1997;Borade et al., 1994).近年来, 由于SAPO-34分子筛具有较大的比表面积和适宜的表面酸性, 作为载体时能够使活性组分较分散地负载在其表面, 因而在催化领域得到了广泛应用(Álvaro Muñoz et al., 2012).本课题组(Yu et al., 2016;Yu et al., 2016;杨颖欣等, 2016)前期以SAPO-34分子筛为载体制备了高分散MnOx/SAPO-34的低温NH3-SCR催化剂, 且该催化剂表现出了较高的低温SCR活性和较宽的反应温度窗口.然而, 目前针对SAPO-34分子筛负载Fe2O3催化剂的低温NH3-SCR性能研究却鲜有报道.
本文采用尿素沉淀法在不同焙烧温度下制备了一系列的Fe2O3/SAPO-34催化剂, 考察催化剂的焙烧温度对低温NH3-SCR性能的影响, 并通过N2吸附-脱附、XRD、AAS、FE-SEM、XPS、NH3-TPD、H2-TPR等多种表征手段分析不同焙烧温度的催化剂的表面结构、氧化还原性能及表面酸性的差异, 深入地探讨焙烧温度对催化剂的低温NH3-SCR性能的影响.
2 实验部分(Experiment part) 2.1 催化剂的制备SAPO-34分子筛购买于南开大学催化剂厂, 其余所有化学试剂均购买于阿拉丁试剂有限公司.按Fe与SAPO-34质量比为20%制备Fe2O3/SAPO-34, 先将4.33 g硝酸铁(分析纯)和9.64 g尿素(分析纯)(n[Fe(NO3)3·9H2O]:n[CO(NH2)2]=1:10) 溶于200 mL乙二醇(分析纯)溶液中, 再加入3 g SAPO-34粉末, 在室温下搅拌30 min后超声分散1 h, 于80 ℃水浴中磁力搅拌12 h.待反应完毕后, 用真空泵进行抽滤, 使用去离子水和无水乙醇(分析纯)洗涤至中性, 将得到的滤饼置于120 ℃鼓风干燥箱中干燥12 h.最后, 将干燥得到的粉末置于马弗炉中焙烧, 以2 ℃·min-1速率升温至所需温度后保持3 h, 焙烧后所得粉末即为Fe2O3/SAPO-34催化剂.所得催化剂样品记作Fe2O3/SAPO-34(x), 其中, x表示焙烧温度(℃).作为对照样品, 纯Fe2O3和纯SAPO-34分子筛通过直接焙烧得到.
2.2 催化剂的SCR活性测试催化剂活性测试在内径为12 mm的石英反应管中进行, 经研磨、过筛(40~60目)后的催化剂用量为500 mg, 填充高度为6 mm.活性测试中所采用的烟道模拟反应气体组成(体积分数)为:NH3 0.06%, NO 0.06%, O2 5%, H2O 10%, 0.01% SO2, Ar作为平衡气, 反应空速(GHSV)为45000 h-1.使用42i-HL型化学发光NO-NO2-NOx分析仪(美国Thermo公司)对反应前后气体组成中NO、NO2进行在线分析, 使用气相色谱仪(5A分子筛填充柱, GC9560, 上海华爱色谱)对反应产物N2进行检测.活性测试的温度范围为80~240 ℃.NO转化率(η)及N2选择性(S)分别按公式(1) 和(2) 计算.

|
(1) |

|
(2) |
式中, CNOin为反应器进口NO的浓度(10-6), CNOout和CN2out是反应器出口NO和N2的浓度(10-6).
2.3 催化剂的表征N2吸附-脱附测试采用ASAP 2020M物理吸附分析仪(美国Micromeritics公司), 测定催化剂的孔结构参数和比表面积.测定时, 取100 mg样品在真空条件下于100 ℃脱气1 h, 再于350 ℃下脱气3 h以上.脱气完毕后, 以N2为饱和压力测定气体吸附质和分析气体, 在-196 ℃下进行测定.然后, 采用t-Plot方法计算孔径和孔容, BET曲线线性积分方法计算比表面积.
X射线衍射(XRD)分析在D8 Advance型号X射线衍射仪(德国Bruker公司)上进行, 以Cu Ka射线为入射源(λ=1.5406 nm), 采用40 kV的操作电压和40 mA的操作电流, 扫描范围2θ=20°~80°.
元素分析(AAS)在PinAAcle 900T型原子吸收光谱仪(美国PerkinElmer公司)上进行, 对Fe元素含量进行测定.
场发射扫描电镜(FE-SEM)分析在德国ZEISS Merlin上进行, 观察催化剂表面的微观形貌及结构.主要操作参数:分辨率为0.6 nm, 放大倍率为12×~2000000×, 加速电压为0.05~30 kV.
X射线光电子能谱(XPS)测试在Escalab250Xi型X射线光电子能谱仪(美国Thermofisher Scientific公司)上进行, 主要操作参数:Al Ka射线(h=1253.6 eV), 真空度3.33×10-6 Pa, C 1s校准结合能为284.8 eV.采用XPS PEAKER 4.1软件对所有测试结果进行分析.
氢气程序升温还原(H2-TPR)测试在AutoChem Ⅱ 2920全自动化学吸附仪(美国Micromeritics公司)上进行, 称取50 mg样品, 在400 ℃下通入Ar气吹扫120 min, 冷却至室温.随后通入30 mL·min-1的10% H2/Ar, 按10 ℃·min-1的速率程序升温还原至800 ℃.
NH3程序升温脱附(NH3-TPD)测试在TL5090多用吸附仪(天津先权)上进行, 称取50 mg样品, 以He为载气, 流量为50 mL·min-1, 在400 ℃下吹扫120 min, 以脱除表面杂质, 冷却至室温.随后通入5% NH3/He混合气体吸附60 min, 再用载气吹扫60 min以去除表面物理吸附的NH3.最后按10 ℃·min-1的速率程序升温脱附至700 ℃.
3 结果与讨论(Results and discussion) 3.1 催化剂的SCR活性测试结果图 1为不同反应温度下Fe2O3/SAPO-34(x)催化剂的SCR活性测试结果.由图可知, 催化剂的SCR活性随着温度的升高总体呈上升趋势, 但不同焙烧温度的催化剂的低温SCR活性存在明显差异.对比各催化剂在80~240 ℃时的催化活性, 发现:随着焙烧温度的提高, 催化剂的低温SCR活性先增加后降低, N2选择性则略有下降;300 ℃焙烧的催化剂具有最优的低温SCR性能, 在190~240 ℃时保持90%以上的NO转化率和接近100%的N2选择性.由以上结果可以推测:当焙烧温度过低, 催化剂的前驱体β-FeOOH尚未完全分解而导致反应活性位点不足(Musić et al., 2004), 催化剂催化活性不高;当焙烧温度过高, 催化剂表面则会出现活性组分Fe2O3晶粒长大、聚集现象而不利于反应物在活性位点上的吸附和活化, 降低了催化剂的催化活性.
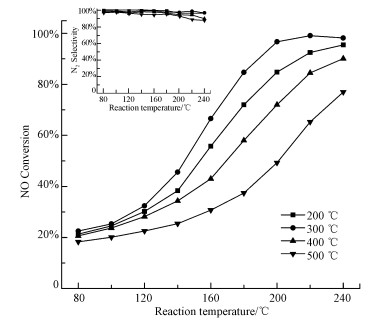 |
| 图 1 Fe2O3/SAPO-34催化剂在不同焙烧温度下的NO转化率 Fig. 1 NO conversion vs. Calcination temperature over the Fe2O3/SAPO-34(x)catalysts |
表 1所示为纯SAPO-34(300)、纯Fe2O3(300) 和Fe2O3/SAPO-34(x)催化剂的BET比表面积(SBET)、总孔容(VTota)和平均孔径.从表中可见, 作为载体的纯SAPO-34提供了较大的比表面积(541.2 m2·g-1), 有利于活性组分的均匀负载.SAPO-34在负载了Fe2O3后, 其比表面积有所下降, 而总孔容和平均孔径则变化不大, 表明负载的Fe2O3主要分散于载体材料外表面上, 极少进入孔道内.此外, 随着焙烧温度的升高, Fe2O3/SAPO-34(x)的比表面积从403.7 m2·g-1下降至287.3 m2·g-1, 总孔容从0.27 cm3·g-1下降至0.22 cm3·g-1, 而平均孔径则从2.09 nm增大至2.87 nm.由此可推测较高焙烧温度使催化剂表面发生烧结、Fe2O3晶粒长大以及载体局部骨架结构发生坍塌, 从而导致比表面积和总孔容降低, 平均孔径增大.根据文献报道(管斌, 2012), 催化剂的比表面积越大, 则活性组分分散度越高, 所暴露出的活性位点也越多, 越有利于催化剂活性的提高.比表面积略小的Fe2O3/SAPO-34(300) 表现出了最佳的低温SCR活性, 表明比表面积不是催化剂催化活性的唯一决定性因素, 催化剂催化活性还与催化剂的晶相结构、元素化学状态等因素相关(Zhang et al., 2004).
| 表 1 纯SAPO-34(300) 和Fe2O3/SAPO-34(x)催化剂的物理性质 Table 1 Physical properties of pure SAPO-34(300) and Fe2O3/SAPO-34(x)catalysts |
图 2是纯SAPO-34(300)、纯Fe2O3(300) 和Fe2O3/SAPO-34(x)催化剂的XRD谱图结果.从图中可见, 负载Fe2O3前后, SAPO-34分子筛的基本结构无明显变化.但负载Fe2O3后, SAPO-34分子筛的XRD衍射峰强度有所减弱, 由此推测Fe2O3与SAPO-34之间存在一定的相互作用.显然地, 在较低焙烧温度的Fe2O3/SAPO-34(c, d)上并未检测出明显的Fe2O3衍射峰, 说明铁物种在SAPO-34上高度分散或以无定型存在;而在较高焙烧温度的Fe2O3/SAPO-34(e, f)上检测出明显的Fe2O3衍射峰, 且峰强度随着焙烧温度的继续升高而增强, 说明Fe2O3在催化剂表面逐渐形成较大晶粒且结晶逐渐趋于完好, 这和BET分析结果一致.
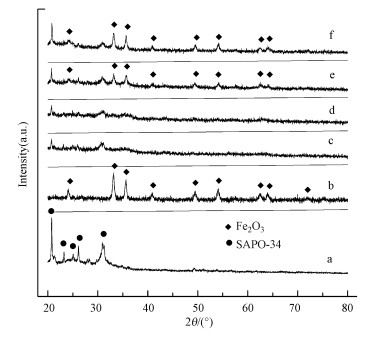 |
| 图 2 Fe2O3/SAPO-34(x)催化剂的XRD图谱(a. pure SAPO-34(300);b. Fe2O3(300);c. Fe2O3/SAPO-34(200); d. Fe2O3/SAPO-34(300); e. Fe2O3/SAPO-34(400); f. Fe2O3/SAPO-34(500)) Fig. 2 X-ray diffraction patterns of Fe2O3/SAPO-34(x)catalysts |
然而, 当活性组分的微粒以非晶态存在或者结晶度非常弱, 即在XRD图谱中检测不到明显的衍射特征峰时, 就难以分析催化剂表面的化学组成.因此, 本文采用AAS测试分析催化剂体相中实际元素含量, 结果如表 1所示.从表中可见, 不同焙烧温度的催化剂的活性组分均为铁物种, 且实际Fe质量分数均在14%左右.
3.4 FE-SEM分析纯SAPO-34(300) 和Fe2O3/SAPO-34(300, 500) 催化剂的FE-SEM图如图 3所示.从图中可见, 纯SAPO-34分子筛(a1, a2)为六面立方体, 该分子筛表面干净光滑, 无杂质, 尺寸为500 nm~3 μm.由Fe2O3/SAPO-34(300) 的扫描电镜图(b1, b2)和元素扫描图(b3)可观察到, Fe2O3颗粒以10~25 nm的粒径在SAPO-34分子筛表面上均匀分散, 且EDS结果(d)中的催化剂表面Fe实际负载量与AAS分析中的催化剂实际Fe含量基本一致, 表明较低焙烧温度有利于Fe2O3以极小的粒径高度分散在载体表面.相反, Fe2O3/SAPO-34催化剂(500) 的扫描电镜图(c1, c2)和元素扫描图(c3)显示Fe2O3在SAPO-34表面上分布不均且颗粒大小极不均匀(50~200 nm), 表明较高焙烧温度易于导致载体表面的Fe2O3粒径增大且出现团聚现象, 这与BET和XRD分析结果一致.一般认为, 催化剂的活性与催化剂载体上的金属氧化物分散程度密切相关, 结合活性测试结果, 可以说明高分散状态的Fe2O3使催化剂具有更大的比表面积, 能够暴露出更多的活性位, 更加有利于NH3-SCR反应的进行.
 |
| 图 3 纯SAPO-34(300) 和Fe2O3/SAPO-34(300, 500) 催化剂的FE-SEM图 Fig. 3 FE-SEM images of pure SAPO-34(300) and Fe2O3/SAPO-34(300, 500) catalysts |
图 4a和4b分别为Fe2O3/SAPO-34(x)催化剂Fe 2p和O 1s轨道的XPS谱图.从图 4a可见, Fe 2p谱图中725.0~725.4 eV、710.1~710.4 eV的峰分别归属于Fe 2P1/2和Fe 2p3/2.这两个2p峰之间的距离是13.9 eV, 且它们之间存在一个低强度的振动卫星峰(718.0~718.5 eV), 说明催化剂表面的主要活性物种为Fe2O3(Gao et al., 2013;Han et al., 2015;Yang et al., 2013).从表 2可见, 随着焙烧温度的升高, Fe元素含量呈现逐渐下降趋势, 且在焙烧温度达400 ℃之后下降幅度增大.结合XRD和FE-SEM的结果, 说明Fe元素含量的下降是由于较高焙烧温度增大了Fe2O3的结晶程度和晶粒大小, 降低了Fe2O3在载体表面的分散度, 即降低了Fe物种的暴露程度.
 |
| 图 4 Fe2O3/SAPO-34(x)催化剂的Fe 2p(A)和O 1s(B)的XPS图谱(a. Fe2O3/SAPO-34(200); b. Fe2O3/SAPO-34(300);c. Fe2O3/SAPO-34(400);d. Fe2O3/SAPO-34(500)) Fig. 4 Fe 2p(A) spectra and O 1s(B) spectra of Fe2O3/SAPO-34(x)catalysts |
| 表 2 Fe2O3/SAPO-34(x)催化剂表面Fe和O元素含量 Table 2 Surface element content and binding energy of Fe and O determined from XPS |
由图 4b可知, O 1s图谱中531.5~531.9 eV、529.5~529.8 eV的峰分别归属于化学吸附氧Oα(包括O2、O-和O22-)和表面晶格氧Oβ(O2-)(Han et al., 2015).化学吸附氧Oα相对于晶格氧Oβ具有更高的氧化性和移动性, 其浓度的提高有利于NO氧化为NO2及NH3的吸附和活化, 从而促进催化剂的低温NH3-SCR反应(Fang et al., 2013).从表 2可见, 较低焙烧温度的催化剂中化学吸附氧Oα比例较高且基本维持不变.随着焙烧温度的提高, 催化剂化学吸附氧的比例由88.54%下降至69.65%, 同时表面晶格氧比例由11.46%上升至30.35%, 变化趋势明显, 该结果也与XRD中得到的随着焙烧温度的升高, Fe2O3结晶程度增加的结果一致.化学吸附氧比例的下降趋势与催化剂的SCR活性顺序相匹配, 说明化学吸附氧Oα为Fe2O3/SAPO-34(x)的主要活性氧物种, 是影响催化剂低温活性的关键因素.另一方面, 较低焙烧温度有助于化学吸附氧Oα的产生及Fe元素质量分数的提升, 这也是化学吸附氧Oα比例和Fe元素质量分数较高的Fe2O3/SAPO-34(300) 表现出最佳低温SCR活性的原因之一.
3.6 H2-TPR分析催化剂需要参与SCR反应中的氧化还原循环, 因此其氧化还原能力极其重要.图 5为Fe2O3/SAPO-34(x)催化剂的H2-TPR图谱, 活性位点氧化还原性能可由还原峰的位置表征, 而该活性位点的数量可由还原峰的面积(耗氢量)表征.还原峰对应的温度越低, 峰面积越大, 则催化剂的氧化还原性能越好.
 |
| 图 5 Fe2O3/SAPO-34(x)催化剂的H2-TPR图(a. Fe2O3/SAPO-34(200); b. Fe2O3/SAPO-34(300); c. Fe2O3/SAPO-34(400); d. Fe2O3/SAPO-34(500)) Fig. 5 H2-TPR profiles of Fe2O3/SAPO-34(x)catalysts |
从图中可见, 催化剂的H2-TPR曲线均出现了3个明显的还原峰, 270~370 ℃内的低温还原峰可归属于Fe2O3向Fe3O4的还原, 500~550 ℃内的中温还原峰可归属于Fe3O4向FeO的还原, 以及620~650 ℃内的高温还原峰可归属于FeO向Fe的还原(Neri et al., 1999).其中, 不同焙烧温度的催化剂的还原峰位置及面积有所不同, 结合表 3可知, 4种催化剂还原峰温度高低顺序为:Fe2O3/SAPO-34(500)(368 ℃)>Fe2O3/SAPO-34(400)(340 ℃)>Fe2O3/SAPO-34(200)(306 ℃)>Fe2O3/SAPO-34(300)(277 ℃), 而还原峰的耗氢量顺序则相反, 即为:Fe2O3/SAPO-34(300)(5.03 mmol·g-1)>Fe2O3/SAPO-34(200)(4.66 mmol·g-1)>Fe2O3/SAPO-34(400)(4.02 mmol·g-1)>Fe2O3/SAPO-34(500)(3.89 mmol·g-1).这一结果表明, 与其它3种催化剂相比较, Fe2O3/SAPO-34(300) 的低温还原性能更好.另一方面, 较高焙烧温度使催化剂的还原峰明显向高温方向偏移(温度升高了91 ℃)且峰面积显著减少(耗氢量减少了1.14 mmol·g-1), 即催化剂的氧化还原能力大幅下降.结合前面FE-SEM和XPS分析结果可知, 300 ℃焙烧的Fe2O3/SAPO-34表面上存在着更多的高分散状态的活性物种, 这些暴露的活性位点增强了催化剂的氧化还原能力, 且能够将NO在低温下氧化成中间产物NO2, 促进快速SCR反应的进行(Zhang et al., 2013), 从而提高催化剂的低温SCR活性.
| 表 3 Fe2O3/SAPO-34(x)催化剂的NH3脱附量 Table 3 NH3 temperature-programmed desorption amount of Fe2O3/SAPO-34(x)catalysts |
NH3吸附在催化剂表面的Lewis酸位和Bronsted酸位上分别形成吸附态的NH3和NH4+(Ettireddy et al., 2007), 吸附态NH3脱氢形成的—NH2可与气相NO或表面吸附NOx物种形成活性中间体, 遵循Eley-Rideal(E-R)机理或Langmuir-Hinshelwood(L-H)机理;而NH4+可与NOx吸附物形成活性中间体, 然后分解成N2和H2O, 遵循L-H机理(Wang et al., 2012).一般而言, E-R机理和L-H机理同时存在于SCR反应过程中, 即吸附态NH3和NH4+均能参与SCR反应.研究者认为SCR反应的第一步是NH3在催化剂表面的吸附, 因此, 提高催化剂表面酸性以促进NH3的吸附有利于提高催化剂的SCR活性.
图 6为Fe2O3/SAPO-34(x)催化剂的NH3-TPD表征结果.可见看到, 负载Fe2O3前后, 纯SAPO-34(300) 和催化剂的NH3-TPD曲线在Ⅰ(140~200 ℃)和Ⅱ(420~450 ℃)两个位置均出现一个明显的NH3脱附峰, 分别记为Ⅰ峰和Ⅱ峰, 说明催化剂上存在两种不同强度的酸位, 同时可将Ⅰ峰和Ⅱ峰分别归属于弱酸位点和强酸位点的NH3脱附峰(Gao et al., 2016).结合图 6分析表 3中催化剂各峰位的NH3脱附量可知, 各催化剂在峰位置上变化不大, 但峰面积(即NH3脱附量)却变化明显.其中, 与纯SAPO-34(300) 相比, 各催化剂的Ⅰ峰NH3脱附量均大幅增加, 增加率为88.6%~151.4%, 而Ⅱ峰NH3脱附量则变化不大, 表明Fe的负载可增加催化剂弱酸性位点数量, 但不影响强酸性位点的形成.此外, 催化剂的总NH3脱附量大小顺序为:Fe2O3/SAPO-34(300)(1.41 mmol·g-1)>Fe2O3/SAPO-34(200)(1.30 mmol·g-1)>Fe2O3/SAPO-34(400)(1.20 mmol·g-1)>Fe2O3/SAPO-34(500)(1.01 mmol·g-1), 与催化剂的SCR活性高低规律一致, 说明催化剂的酸性是影响SCR反应的一个重要因素.当催化剂的焙烧温度为300 ℃时, 催化剂的NH3总脱附量比其他催化剂的大, 尤其是Ⅱ峰NH3脱附量大幅增加, 此时催化剂具有较高的SCR活性, 说明高度分散的Fe2O3使催化剂暴露出较多强酸位点, 且强酸位点在反应中起关键作用.随着焙烧温度的继续升高, 催化剂的Ⅰ、Ⅱ峰的NH3脱附量总体呈减少趋势, 说明较高焙烧温度会减少催化剂中的酸性位点数量, 从而降低SCR活性.
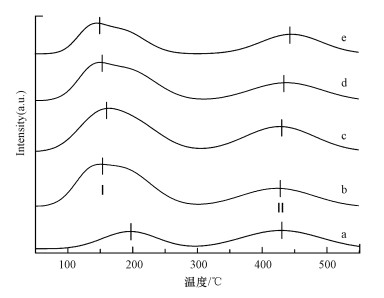 |
| 图 6 Fe2O3/SAPO-34(x)催化剂的NH3-TPD图(a. pure SAPO-34(300); b. Fe2O3/SAPO-34(200); c. Fe2O3/SAPO-34(300); d. Fe2O3/SAPO-34(400); e. Fe2O3/SAPO-34(500)) Fig. 6 NH3-TPD profiles of Fe2O3/SAPO-34(x)catalysts |
在实际的脱硝工业应用中, 烟气即使经过除尘和脱硫装置, 仍然存在一定量的SO2和H2O.H2O可能会与气态NH3分子结合, 影响NH3的吸附, 也可能与NH3竞争吸附催化剂表面活性位点, 从而抑制NH3的吸附和活化, 甚至可能改变金属活性组分的价态(Zhang et al., 2002;Zhang et al., 2003).而SO2会与NH3及H2O反应生成硫酸铵盐, 还可能与金属活性组分生成硫酸盐和亚硫酸盐, 且在低温下不易分解, 从而导致催化剂中毒失活(Gong et al., 2003;Jiang et al., 2010).SO2和H2O对催化剂的SCR脱硝活性有着极其重要的影响.因此, 本文将催化剂的抗硫抗水性能作为一项重要的考察指标.
图 7显示了SO2和H2O对Fe2O3/SAPO-34(300) 催化剂的SCR反应活性的影响.从图中可见, 当单独通入H2O时, 催化剂活性略微降低, 最终维持在90%以上并且不变;当停止通入H2O后, 催化剂活性能迅速恢复.可以推断, H2O对Fe2O3/SAPO-34(300) 催化剂活性具有一定的抑制作用, 且该抑制作用是可逆的.当单独通入SO2时, 催化剂活性迅速下降并稳定在86%左右;当停止通入SO2后催化剂的活性有所回升, 但不能恢复回初始活性.可以推断, 催化剂表面可能生成了少量的硫酸盐物种而覆盖了活性位.
 |
| 图 7 H2O和SO2对Fe2O3/SAPO-34(300) 催化剂的SCR活性的影响 Fig. 7 Effect of H2O and SO2 on SCR activity of Fe2O3/SAPO-34(300) catalyst |
相对地, SO2和H2O同时存在对催化剂活性的影响较大, 且毒害作用为不可逆, 但催化剂活性最终仍能够维持在80%以上.综合以上结果可知, 该Fe2O3/SAPO-34(300) 催化剂具有较强的抗硫抗水性能.
4 结论(Conclusions)1) 300 ℃焙烧的催化剂具有最佳的低温NH3-SCR性能和较强的抗硫抗水性能, 在190~240 ℃时, NO转化率达90%以上且N2选择性接近100%.
2) 在较低的焙烧温度下, 催化剂具有较大的比表面积, Fe2O3以高分散状态存在于载体上, 这使催化剂能够暴露出更多的活性位点和酸性位点, 尤其是对SCR反应起关键作用的强酸位点, 同时具有更高的化学吸附氧比例, 并由此促进低温SCR反应中的氧化还原循环以及NH3和NO的活化过程, 从而提高Fe2O3/SAPO-34催化剂的低温SCR活性.
Álvaro Muñoz T, Márquez Álvarez C, Sastre E. 2012. Use of different templates on SAPO-34 synthesis:Effect on the acidity and catalytic activity in the MTO reaction[J]. Catalysis Today, 179(1): 27–34.
DOI:10.1016/j.cattod.2011.07.038
|
Busca G, Larrubia M A, Arrighi L, et al. 2005. Catalytic abatement of NOx:Chemical and mechanistic aspects[J]. Catalysis Today, 107: 139–148.
|
Borade R B, Clearfield A. 1994. A comparative study of acidic properties of SAPO-5, -11, -34 and-37 molecular sieves[J]. Journal of Molecular Catalysis, 88(2): 249–265.
DOI:10.1016/0304-5102(93)E0262-F
|
Corma A. 1997. From microporous to mesoporous molecular sieve materials and their use in catalysis[J]. Chemical Reviews, 97(6): 2373–2420.
DOI:10.1021/cr960406n
|
Duan J, Shi W, Xia Q, et al. 2012. Characterization and regeneration of deactivated commercial SCR catalyst[J]. Journal of Functional Materials, 43(16): 2191–2195.
|
Du T Y, Qu H G, Liu Q, et al. 2015. Synthesis, activity and hydrophobicity of Fe-ZSM-5@silicalite-1 for NH3-SCR[J]. Chemical Engineering Journal, 262: 1199–1207.
DOI:10.1016/j.cej.2014.09.119
|
Ettireddy P R, Ettireddy N, Mamedov S, et al. 2007. Surface characterization studies of TiO2 supported manganese oxide catalysts for low temperature SCR of NO with NH3[J]. Applied Catalysis B:Environmental, 76(1): 123–134.
|
Fang C, Zhang D S, Shi L Y, et al. 2013. Highly dispersed CeO2 on carbon nanotubes for selective catalytic reduction of NO with NH3[J]. Catalysis Science&Technology, 3(3): 803–811.
|
Gao R, Zhang D S, Liu X G, et al. 2013. Enhanced catalytic performance of V2O5-WO3/Fe2O3/TiO2 microspheres for selective catalytic reduction of NO by NH3[J]. Catalysis Science&Technology, 3(1): 191–199.
|
管斌. 2012低温选择性催化还原氮氧化物的基础研究[D]. 上海: 上海交通大学
http://cdmd.cnki.com.cn/Article/CDMD-10248-1012016742.htm |
Gao F, Zheng Y, Kukkadapu R K, et al. 2016. Iron Loading Effects in Fe/SSZ-13 NH3-SCR Catalysts:Nature of the Fe Ions and Structure-Function Relationships[J]. ACS Catalysis, 6(5): 2939–2954.
DOI:10.1021/acscatal.6b00647
|
Gong S Q, Ralph T Y. 2003. Low-temperature selective catalytic reduction of NO with NH3 over iron and manganese oxides supported on titania[J]. Applied Catalysis B:Environmental, 44(3): 217–225.
DOI:10.1016/S0926-3373(03)00100-0
|
Han J, Zhang D S, Maitarad P, et al. 2015. Fe2O3 nanoparticles anchored in situ on carbon nanotubes via an ethanol-thermal strategy for the selective catalytic reduction of NO with NH3[J]. Catalysis Science&Technology, 5(1): 438–446.
|
Jiang B Q, Wu B Z, Liu Y, et al. 2010. DRIFT study of the SO2 effect on low-temperature SCR reaction over Fe-Mn/TiO2[J]. The Journal of Physical Chemistry C, 114(11): 4961–4965.
DOI:10.1021/jp907783g
|
Liu F D, He H, Zhang C. 2008. Novel iron titanate catalyst for the selective catalytic reduction of NO with NH3 in the medium temperature range[J]. Chemical Communications(17): 2043–2045.
DOI:10.1039/b800143j
|
Liu F D, He H, Lian Z H, et al. 2013. Highly dispersed iron vanadate catalyst supported on TiO2 for the selective catalytic reduction of NOx with NH3[J]. Journal of Catalysis, 307: 340–351.
DOI:10.1016/j.jcat.2013.08.003
|
Liu F D, He H. 2010. Structure-Activity Relationship of Iron Titanate Catalysts in the Selective Catalytic Reduction of NOx with NH3[J]. The Journal of Physical Chemistry C, 114(40): 16929–16936.
DOI:10.1021/jp912163k
|
Liu Z M, Su H, Chen B H, et al. 2016. Activity enhancement of WO3 modified Fe2O3 catalyst for the selective catalytic reduction of NOx by NH3[J]. Chemical Engineering Journal, 299: 255–262.
DOI:10.1016/j.cej.2016.04.100
|
Mou X L, Zhang B S, Li Y, et al. 2012. Rod-Shaped Fe2O3 as an efficient catalyst for the selective reduction of nitrogen oxide by ammonia[J]. Angewandte Chemie International Edition, 51(12): 2989–2993.
DOI:10.1002/anie.201107113
|
Musić S, Krehula S, Popović S. 2004. Thermal decomposition of β-FeOOH[J]. Materials Letters, 58(3): 444–448.
|
Nedyalkova R, Shwan S, Skoglundh M, et al. 2013. Improved low-temperature SCR activity for Fe-BEA catalysts by H2-pretreatment[J]. Applied Catalysis B:Environmental, 138: 373–380.
|
Neri G, Visco A M, Galvagno S, et al. 1999. Au/iron oxide catalysts:temperature programmed reduction and X-ray diffraction characterization[J]. Thermochimica Acta, 329(1): 39–46.
DOI:10.1016/S0040-6031(98)00664-9
|
Qu Z P, Miao L, Wang H, et al. 2015. Highly dispersed Fe2O3 on carbon nanotubes for low-temperature selective catalytic reduction of NO with NH3[J]. Chemical Communications, 51(5): 956–958.
DOI:10.1039/C4CC06941B
|
Skalska K, Miller J S, Ledakowicz S. 2010. Trends in NOx abatement:A review[J]. Science of the Total Environment, 408(19): 3976–3989.
DOI:10.1016/j.scitotenv.2010.06.001
|
孙梦婷, 黄碧纯, 马杰文, 等. 2016. 二氧化锰在低温NH3-SCR催化反应上的形貌效应[J]. 物理化学学报, 2016, 32(6): 1501–1510.
DOI:10.3866/PKU.WHXB201603171 |
Wang L S, Huang B C, Su Y X, et al. 2012. Manganese oxides supported on multi-walled carbon nanotubes for selective catalytic reduction of NO with NH3:Catalytic activity and characterization[J]. Chemical Engineering Journal, 192: 232–241.
DOI:10.1016/j.cej.2012.04.012
|
杨颖欣, 马杰文, 喻成龙, 等. 2016. 不同SAPO分子筛负载MnOx催化剂的低温NH3-SCR性能研究[J]. 环境科学学报, 2016, 36(9): 3400–3408.
|
Yu C L, Huang B C, Dong L F, et al. 2016a. In situ FT-IR study of highly dispersed MnOx/SAPO-34 catalyst for low-temperature selective catalytic reduction of NOx by NH3[J]. Catalysis Today, 281(3): 610–620.
|
Yu C L, Dong L F, Chen F, et al. 2016b. Low-temperature SCR of NOx by NH3 over MnOx/SAPO-34 prepared by two different methods:a comparative study[J]. Environmental Technology, 0: 1–13.
|
Yang S J, Wang C Z, Ma L, et al. 2013. Substitution of WO3 in V2O5/WO3-TiO2 by Fe2O3 for selective catalytic reduction of NO with NH[J]. Catalysis Science&Technology, 3(1): 161–168.
|
Zhang P, Li D Y. 2014. Selective Catalytic reduction of NO with NH3 over iron-vanadium mixed oxide catalyst[J]. Catalysis Letters, 144(5): 959–963.
DOI:10.1007/s10562-014-1203-y
|
Zhang D S, Zhang L, Shi L Y, et al. 2013. In situ supported MnOx-CeOx on carbon nanotubes for the low-temperature selective catalytic reduction of NO with NH3[J]. Nanoscale, 5(3): 1127–1136.
DOI:10.1039/c2nr33006g
|
Zhang G H, Zhen P Z, Zhen Y L, et al. 2003. Formation and reaction of ammonium sulfate salts on V2O5/AC catalyst during selective catalytic reduction of nitric oxide by ammonia at low temperatures[J]. Journal of Catalysis, 214(2): 213–219.
DOI:10.1016/S0021-9517(02)00157-4
|
Zhang G H, Zhen P Z, Zhen Y L. 2002. Combined effect of H2O and SO2 on V2O5/AC catalysts for NO reduction with ammonia at lower temperatures[J]. Applied Catalysis B:Environmental, 39(4): 361–368.
DOI:10.1016/S0926-3373(02)00122-4
|
 2017, Vol. 37
2017, Vol. 37


