2. 澳大利亚纽卡斯尔大学环境修复中心, 卡拉汉 澳大利亚 NSW 2308
2. Global Centre for Environmental Remediation, University of Newcastle, Callaghan, NSW 2308
微生物燃料电池(Microbial fuel cell, MFC)是以微生物为反应主体, 利用微生物将生物质转化为电能的装置, 是一种在处理污水的同时又能产生电能的新技术(Logan et al., 2012; 涂丽杏等, 2013; Liu et al., 2008), 在能源紧缺的今天具有巨大的发展前景.然而, 输出功率低成为了微生物燃料电池在实际中无法应用的主要限制因素.电极的相对表面积、导电性能及电子在生物体与电极表面的传递效率会在极大程度上影响微生物燃料电池产电效率, 因此, 开发高性能的新型阳极材料, 对提高微生物燃料电池的产电能力有至关重要的作用(Wei et al., 2011).
近年来, 随着人们对氧化石墨烯(GO)各种优异性能的研究, 越来越多的研究者将其应用于MFC的阳极改性中, 但随着研究的不断深入, 人们逐渐发现用化学方法合成的GO能够与细胞直接作用, 引发细胞膜损伤, 导致细胞死亡, 或者通过细胞的氧化应激反应诱导细胞凋亡甚至坏死, 因而具有一定的生物毒性(Liu et al., 2011); 且GO还存在导电性较差、易发生团聚、分散性较差等缺点(黄毅等, 2009).因此, 比表面积更大、导电性和生物相容性更为优异的的氧化石墨烯(rGO)(次素琴等, 2012)引起了人们极大的兴趣.目前, 制备石墨烯最常见的方法是传统化学法, 但在其还原过程中所用的强还原剂大多具有毒性和腐蚀性, 可能对人体和环境产生毒害作用.除此之外, 环境友好型的绿色还原法也引起了人们的关注, 如Wang等(2011)用绿茶将GO还原为rGO, 发现其导电性能得到显著改进.
本文采用改良的Hummer法制备出GO, 通过层层组装技术将带正电荷的聚乙烯亚胺与带负电荷的GO依次交替吸附至碳刷表面, 制备出均匀且形态和厚度可控的均一薄膜; 然后利用更为普遍和廉价的桉树叶提取液还原碳刷表面的GO, 成功制备出G-rGO电极作为MFC阳极; 最后采用红外光谱(FTIR)、X射线衍射(XRD)、扫描电镜(SEM)对所制备的电极进行表征, 并测试电极的电化学性能, 以期为绿色合成石墨烯修饰阳极提高MFC的产电效率提供理论依据.
2 材料与方法(Materials and methods) 2.1 微生物燃料电池的构型实验采用的碳纤维刷购自荆州浩特新材料有限公司, 其表面尺寸为3 cm×3 cm×5 cm.微生物燃料电池采用亚克力材料构建的双室型池, 每侧的可用容积为28 mL, 阴极与阳极之间使用质子交换膜相隔, 外加电阻阻值为1000 Ω, 在温度为(30±3) ℃的恒温箱中间歇厌氧运行.微生物燃料电池阳极室接种物为取自福州祥板污水厂的厌氧污泥.
阳极培养基(g·L-1):NaAc 1.44, NaHCO3 0.488, NH4Cl 0.03, NaH2PO4·2H2O 0.92, CaCl2·2H2O 0.0056, MgSO4·7H2O 0.035, KCl 0.0052, NaNO3 0.044, 微量元素为0.1 mL·L-1 (Puig et al., 2011).
阴极铁氰化钾缓冲液(g·L-1):K3 [Fe(CN)6]32.929, Na2HPO4·12H2O 23.084, NaH2PO4·2H2O 5.5422.
2.2 阳极电极改性碳刷在使用前, 先用1 mol·L-1的HCl和NaOH溶液浸泡24 h, 再用食人鱼洗液(Piranha洗液)(Gupta et al., 2016)小心清洗, 洗净吹干, 备用, 此时得到未经改性的碳刷.
使用层层组装技术(Guo et al., 2014; Bucur et al., 2016; Gupta et al., 2016), 将带正电荷的聚乙烯亚酰胺(PEI)溶液(Ma et al., 2016)和带负电荷的GO溶液(Dikin et al., 2007)交替吸附至碳刷表面, 循环10次(PEI/GO), 然后放入桉树叶提取液(Wang et al., 2014)中浸泡12 h, 洗涤后吹干, 备用(G-rGO).将上述PEI/GO碳刷放入MFC中, 一段时间后在微生物的作用下被还原为rGO(B-rGO).
2.3 分析测试方法 2.3.1 材料的表征对于改性后的阳极电极PEI/GO和G-rGO, 采用X射线衍射(X-ray diffraction, XRD)分析表面元素成分, 用红外光谱(Infrared Spectroscopy, IR)对它们存在的官能团进行分析, 用扫描电子显微镜(Scanning Electron Microscope, SEM)对G-rGO和B-rGO阳极表面形貌进行观察.
2.3.2 电池性能分析方法微生物燃料电池的外电压由数据采集卡(众泰ZTIC USB-7660) 进行监测, 每隔20 min记录一次数据.利用CHI660D电化学工作站(上海辰华仪器有限公司)对微生物燃料电池进行循环伏安法(CV)和交流阻抗法(EIS)测试, 采用变阻器对其极化曲线和功率密度曲线进行测定. CV测试的电势范围为-0.8~0.8 V, 扫描速度为1 mV·s-1.进行EIS分析时, 以电池的开路电压为起始电压, 扫描的频率变化范围为0.01~100000 Hz.在MFC稳定运行后, 对其进行稳态放电测试, 外电阻的阻值变化范围为10000~10 Ω, 每20 min调整一次外电阻.电极上生物可溶性蛋白的测定参照Bradford G-250法(郭燊等, 2015), 将相同质量的碳刷加蒸馏水离心后滤去上清液, 加入蒸馏水、Tris-HCl缓冲液和NaOH进行反应, 100 ℃水浴30 min, 取出摇匀并冷却, 取1 mL上清液, 用考马斯亮蓝显色10 min, 于595 nm下测定吸光值, 根据标准曲线得出可溶性蛋白含量.化学需氧量(COD)的测定采用国际方法.库伦效率(CE)的计算参照公式(1)(Kim et al., 2005).
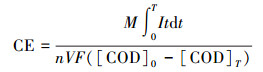
|
(1) |
式中, M为氧分子质量(32 g·L-1), n为氧分子转移电荷量, 无量纲, 取值为4, T为周期时间(s), t为时间(s), I为时刻电流(A), F为常数(取值为96485 C·mol-1), V为MFC阳极室容积(本文取值为28 mL), [COD]0-[COD]T则表示一个周期前后COD的变化值(mg·L-1).
3 结果与分析(Results and Discussion) 3.1 X射线衍射能谱用X射线衍射能谱(XRD)对石墨、GO和G-rGO进行表征, 结果见图 1.可以观察到在用Hummer法合成GO(Hummers et al., 1958)的过程中, 2θ=26.09°处很强很尖的石墨(002) 面衍射峰完全消失, 在2θ=9.15°左右出现了很强的GO(001) 面衍射峰, 表明经过氧化反应, 具有非常规整的片层空间排列的石墨微晶结构被破坏, 生成了新的晶体结构.在用桉树叶提取液绿色还原氧化石墨烯的过程中GO的衍射峰消失, 而在2θ=22.98°处出现了较宽但强度较小的衍射峰, 这说明GO在绿色还原后, 层间距有所减小, 新的晶体结构生成(闻雷等, 2014).
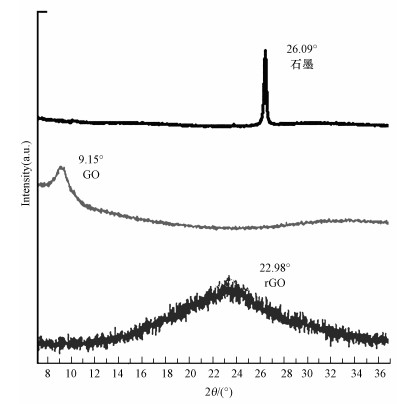 |
| 图 1 石墨、GO和rGO的XRD图谱 Fig. 1 XRD spectra of graphite, graphite oxide and graphene |
从GO、rGO、PEI、PEI/GO和G-rGO阳极的红外光谱(FTIR)图可以看出(图 2), 在3441 cm-1处均有羟基的伸缩振动峰, GO在绿色还原的过程中, 1051、1234、1399和1628 cm-1处的吸收峰的强度均减弱, 表明部分C—O—C、—OH和C=O基团已被去除(Guo et al., 2009), 并在1572 cm-1附近出现了C=C氧化还原峰, 说明GO在绿色还原的过程中, 含氧官能团被还原, 生成了rGO(Singhal et al., 2011).此外, PEI在1583和1470 cm-1处有—NH和—CH2的特征吸收峰(Cao et al., 2015), PEI/GO的吸收峰曲线与GO和PEI的吸收曲线峰型非常相似, 说明B-rGO在放入MFC被微生物还原为rGO之前仅含有GO和PEI, 而G-rGO的吸收峰曲线与rGO和PEI的吸收峰曲线峰型非常相似, 说明GO已经被绿色还原为rGO并与PEI一同修饰到碳刷的表面上.
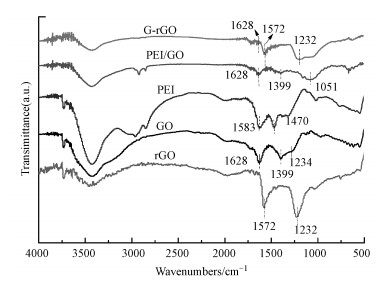 |
| 图 2 rGO、GO、PEI、PEI/GO和G-rGO的红外光谱图 Fig. 2 FTIR spectrum of rGO, GO, PEI, PEI/GO and G-rGO powders |
采用扫描电子显微镜(SEM)对不同电极进行形貌表征.由图 3a、3b、3c可见, 碳刷表面比较光滑, 经过修饰后电极的碳纤维上不同程度地覆盖着修饰物, G-rGO电极比PEI/GO电极表面更粗糙.这是因为GO在发生还原反应生成rGO时, 各类含氧官能团将在生成C=C键的过程中形成褶皱以降低表面能, 使其稳定存在(Gnana et al., 2014).
 |
| 图 3 不同电极产电前后的SEM图(a.碳刷电极, b.PEI/GO电极, c.G-rGO电极, d.产电后碳刷电极, e.产电后B-rGO电极, f.产电后G-rGO电极) Fig. 3 SEM images of unmodified anode(a), PEI/GO anode(b), G-rGO anode(c), unmodified anode with electricigens(d), B-rGO anode with electricigens(e) and G-rGO anode with electricigens(f) |
为验证电极在经修饰后其表面微生物附着性能确有改善, 在MFC运行一周期后(图 4产电图中箭头处为取样点)用SEM对MFC阳极表面形貌进行观察.从图 3d、3e、3f可以看出, 由于碳刷电极表面比较光滑, 微生物难以在其表面大量附着, 因此, 其表面的细菌量最少.而G-rGO和B-rGO电极由于修饰后电极表面的粗糙度和比表面积增大, 表面附着的细菌量明显多于碳刷电极.为了进一步比较电极表面附着的微生物量, 将3种电极用Bradford G-250法进行定量分析, 其中, G-rGO的可溶性蛋白含量为173.6 mg·g-1, 比富集菌降解有机废水的双室MFC的可溶性蛋白含量(130 mg·g-1)稍多(Kim et al., 2004), B-rGO的可溶性蛋白含量与Kim等(2004)的研究结果相似, 达到128.8 mg·g-1, 而碳刷的可溶性蛋白含量较少, 仅为84.0 mg·g-1, 这与SEM图中观察到的G-rGO电极表面细菌量比B-rGO多的结果基本一致.这可能是由于G-rGO利用桉树叶提取液将GO还原为rGO的效率大于B-rGO, 使得G-rGO电极表面形成的褶皱更多, 有更多有利于细菌附着和生长的活性位点.
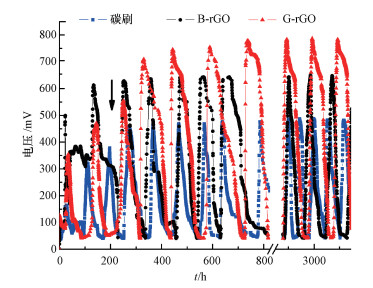 |
| 图 4 不同电极的电压-时间曲线 Fig. 4 Star-up voltage of different electrodes |
以G-rGO、B-rGO和碳刷为阳极的3个MFC装置的启动及产电性能如图 4所示.从图 4可以看出, 3个反应器在接种后的几个周期中电压均稳步上升并趋于稳定, 以碳刷为阳极的MFC反应器在100 h后电压开始明显的稳步上升并在280 h后趋于稳定, 其最高输出电压在480 mV左右; 以G-rGO为阳极的MFC反应器, 电极表面粗糙程度大, 物质比较稳定, 因此, 在接种后输出电压一直稳步上升, 在接种后320 h时, 达到的稳定平台电压为760 mV左右; 而以B-rGO为阳极的MFC在开始的启动过程中产电极不稳定, 这可能是因为一开始电极表面含有大量GO, 产电菌附着后可消耗底物产生的电子, 电子经阳极传递使GO逐渐被微生物还原为rGO(Yuan et al., 2012).待还原反应达到饱和后, 产电逐渐上升并趋于稳定, 在220 h左右达到稳定平台电压635 mV.由此可见, G-rGO电极比B-rGO电极的电子传递效率更快, 启动时间更短, 产电性能更高.由此推测, B-rGO电极利用微生物将其表面GO还原为rGO的效率并没有用桉树叶提取液进行绿色还原的G-rGO电极好.
3.5 电化学测试 3.5.1 循环伏安测试对上述3种电极进行循环伏安测试, 结果如图 5所示.在CV曲线中, 闭合曲线的面积大小一方面与材料的电容相关, 若材料的电容越大, 则曲线的闭合面积越大; 另一方面, 与电极在氧化还原过程中的电荷转移量有关, 若电极传递电荷的能力越强, 导电性能越好, 则闭合面积越大(刘兴倩等, 2013).B-rGO和G-rGO电极的闭合曲线面积相对碳刷电极有显著的提高.其中, G-rGO电极的闭合曲线面积最大, B-rGO电极次之, 碳刷电极最小.除此之外, 碳刷电极只出现微弱的氧化峰和还原峰, 而G-rGO和B-rGO电极出现了比较明显的氧化还原峰, 并且G-rGO电极的峰型更为显著.一方面, PEI聚合物修饰电极可在很大程度上增强电极的导电性能; 另一方面, B-rGO电极表面导电性差的GO被微生物还原为导电性好的rGO, 增加了其电子传递效率和阳极材料的电容.而G-rGO电极的导电能力比B-rGO电极更好, 可能是由于桉树叶提取液绿色还原去除GO表面含氧官能团的效率比微生物还原更高, 因此, G-rGO电极表面rGO含量更多, 电极的导电效率越高, 更有利于电子的传递.
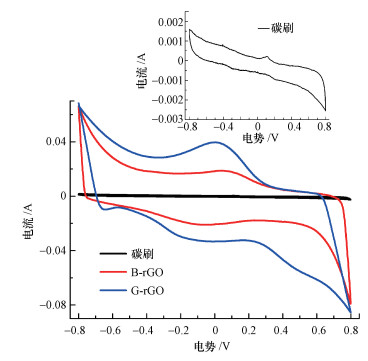 |
| 图 5 不同电极在磷酸盐缓冲液中扫描的循环伏安曲线 Fig. 5 Cyclic voltammogram of different electrodes in phosphate buffer solution |
采用交流阻抗法对G-rGO、B-rGO和碳刷电极材料的电化学性能进行进一步的表征, 交流阻抗图的横坐标为实部阻抗(Z′), 纵坐标为虚部阻抗(-Z″).从图中圆弧的直径能够直观地看出电极的活化阻抗的大小, 圆弧的直径越短说明阻抗越小, 电极表面发生氧化还原反应的速率越快.由图 6的交流阻抗曲线可知, 碳刷的阻值远大于G-rGO和B-rGO电极, 通过电化学软件拟合得出, G-rGO、B-rGO和碳刷电极的活化阻抗分别为91、107和179 Ω.负载后电极材料阻抗减小, 可能是因为通过层层自组装法将具有高导电率的PEI和高比表面、良好生物相容性、导电性能优越的rGO进行负载后, 使电极具有更优良的导电性能和更高的电化学活性.
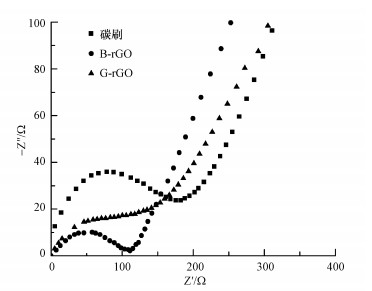 |
| 图 6 不同电极的电化学交流阻抗曲线 Fig. 6 Electrochemical impedance spectroscopy of different electrodes |
从图 7可以看出, G-rGO的性能远比B-rGO和碳刷优越.其中, 碳刷电极在运行过程中的最大功率密度为8.97 W·m-3, 此时对应的电流密度和表观内阻分别为29.22 A·m-3和375.21 Ω, B-rGO电极的最大功率密度提高至13.16 W·m-3, 电流密度提高至39.64 A·m-3, 对应的表观内阻降低至299.11 Ω.这是由于在阳极上修饰的GO被微生物还原为rGO(张凯等, 2014), 促进了产电, 降低了电池内阻, 提高了产电效率.而经过PEI和绿色还原rGO修饰后的G-rGO电极, 比表面积大大增加, 改善了电极的电子传递效率, 使得G-rGO电极最大功率密度达到18.77 W·m-3, 电流密度提高至52.43 A·m-3, 对应的表观内阻降低至243.87 Ω.相关报道中, 使用聚醚醚酮作为质子交换膜的单室MFC(Ayyaru et al., 2011)和以亚硝酸盐为阴极电子受体的MFC装置(Li et al., 2014)的最大功率密度分别可达到5.7和8.3 W·m-3.本实验中G-rGO的性能优于相关报道, 这可能是由于将绿色还原rGO和PEI负载至电极上, 降低了体系的内阻, 提高了MFC的功率密度和电流密度, 使得G-rGO电极的产电性能更为优越(涂丽杏等, 2013).
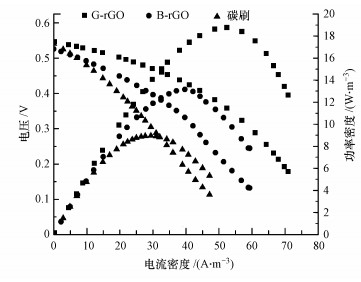 |
| 图 7 不同电极的极化曲线和功率密度曲线 Fig. 7 Polarization and power density curves of different electrodes |
库伦效率(CE)是指MFC在利用废水中的有机物产电的过程中, 实际产生的电量与消耗底物中有机物应该产生的理论电量的比值, 是衡量MFC将化学能转化为电能能力的重要参数.从图 8中可以看出, 碳刷电极的库伦效率和COD去除率最低, 分别为26.2%和75.1%, 而B-rGO的库伦效率和COD去除率分别达到36.6%和81.9%, G-rGO的库伦效率和COD去除率最优, 分别高达62.3%和86.5%.根据相关文献报道, 3.2 g·L-1浓度的纯甘油发电的双室MFC装置(Tremouli et al., 2016)和铜酞菁/C作为阴极催化剂的双室MFC装置(Ghasemi et al., 2013)的库伦效率分别达到34.1%和29.3%, 相较于这2种装置, 本文中G-rGO的库伦效率更高.从本文的实验结果可以看出, 3个装置的COD去除率相差不大, 但库伦效率差值较大, 可能是因为它们的电流密度和内阻相差较大, 所以将化学能转化为电能的能力相差较大.其中, G-rGO电极由于导电能力最好, 电流密度最高, 内阻最低, 因而库伦效率最高.
 |
| 图 8 不同电极的COD去除率和库伦效率 Fig. 8 Chemical oxygen demand removal efficiency and culombic efficiency of different electrodes |
修饰后的G-rGO和B-rGO电极具有更好的生物相容性, 更多的生物活性位点, 可明显降低电极的内阻, 提高电荷转移量, 增强电极的导电能力.但由于G-rGO较之B-rGO有更好的还原效率, 故G-rGO电极的生物相容性更好, 电化学性能和产电性能更优.综上所述, G-rGO电极使得MFC内阻减小, 产电效率提高, 是一种高效、绿色的MFC阳极.
Ayyaru S, Dharmalingam S. 2011. Development of MFC using sulphonated polyether ether ketone (SPEEK) membrane for electricity generation from waste water[J]. Bioresource technology, 102(24): 11167–11171.
DOI:10.1016/j.biortech.2011.09.021
|
Bucur C B, Muldoon J, Lita A. 2016. A layer-by-layer supramolecular structure for a sulfur cathode[J]. Energy & Environmental Science, 9(3): 992–998.
|
Cao L, Sun Q, Gao Y, et al. 2015. Novel acid-base hybrid membrane based on amine-functionalized reduced graphene oxide and sulfonated polyimide for vanadium redox flow battery[J]. Electrochimica Acta, 158: 24–34.
DOI:10.1016/j.electacta.2015.01.159
|
次素琴, 吴娜, 温珍海, 等. 2012. 微生物燃料电池电极材料研究进展[J]. 电化学, 2012, 18(3): 243–251.
|
Dikin D A, Stankovich S, Zimney E J, et al. 2007. Preparation and characterization of graphene oxide paper[J]. Nature, 448(7152): 457–460.
DOI:10.1038/nature06016
|
Ghasemi M, Daud W R W, Rahimnejad M, et al. 2013. Copper-phthalocyanine and nickel nanoparticles as novel cathode catalysts in microbial fuel cells[J]. International Journal of Hydrogen Energy, 38(22): 9533–9540.
DOI:10.1016/j.ijhydene.2013.01.177
|
Gnana Kumar G, Kirubaharan C J, Udhayakumar S, et al. 2014. Synthesis, structural, and morphological microbial fuel cell performances[J]. ACS Sustainable Chemistry & Engineering, 2(10): 2283–2290.
|
Guo H L, Wang X F, Qian Q Y, et al. 2009. A green approach to the synthesis of graphene nanosheets[J]. ACS Nano, 3(9): 2653–2659.
DOI:10.1021/nn900227d
|
Guo W, Cui Y, Song H, et al. 2014. Layer-by-layer construction of graphene-based microbial fuel cell for improved power generation and methyl orange removal[J]. Bioprocess and Biosystems Engineering, 37: 1749–1758.
DOI:10.1007/s00449-014-1148-y
|
郭燊, 林加奖, 陈智超, 等. 2015. 石墨烯是促进还是抑制嗜酸性氧化亚铁硫杆菌生长?[J]. 环境科学学报, 2015, 35(8): 2613–2619.
|
Gupta S, Heintzman E, Price C. 2016. Electrostatic layer-by-layer self-assembled graphene/multi-walled carbon nanotubes hybrid multilayers as efficient 'all carbon'supercapacitors[J]. Journal of Nanoscience and Nanotechnology, 16(5): 4771–4782.
DOI:10.1166/jnn.2016.12413
|
黄毅, 陈永胜. 2009. 石墨烯的功能化及其相关应用[J]. 中国科学B辑化学, 2009, 39(9): 887–896.
|
Hummers Jr W S, Offeman R E. 1958. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 80(6): 1339–1339.
DOI:10.1021/ja01539a017
|
Kim B H, Park H S, Kim H J, et al. 2004. Enrichment of microbial community generating electricity using a fuel-cell-type electrochemical cell[J]. Applied Microbiology and Biotechnology, 63(6): 672–681.
DOI:10.1007/s00253-003-1412-6
|
Kim J R, Min B, Logan B E. 2005. Evaluation of procedures to acclimate a microbial fuel cell for electricity production[J]. Applied Microbiology and Biotechnology, 68(1): 23–30.
DOI:10.1007/s00253-004-1845-6
|
Liu H, Cheng S, Huang L, et al. 2008. Scale-up of membrane-free single-chamber microbial fuel cells[J]. Journal of Power Sources, 179(1): 274–279.
DOI:10.1016/j.jpowsour.2007.12.120
|
Liu S, Zeng T H, Hofmann M, et al. 2011. Antibacterial activity of graphite, graphite oxide, graphene oxide, and reduced graphene oxide:membrane and oxidative stress[J]. Acs Nano, 5(9): 6971–6980.
DOI:10.1021/nn202451x
|
Li W, Zhang S, Chen G, et al. 2014. Simultaneous electricity generation and pollutant removal in microbial fuel cell with denitrifying biocathode over nitrite[J]. Applied Energy, 126: 136–141.
DOI:10.1016/j.apenergy.2014.04.015
|
刘兴倩, 王许云, 郭庆杰. 2013. Pedot/Mwcnts复合阳极的制备及在MFC中的应用[J]. 化工学报, 2013(5): 1773–1779.
|
Logan B E, Rabaey K. 2012. Conversion of wastes into bioelectricity and chemicals by using microbial electrochemical technologies[J]. Science, 337(6095): 686–690.
DOI:10.1126/science.1217412
|
Ma Y, Zhang B, Ma H, et al. 2016. Polyethylenimine nanofibrous adsorbent for highly effective removal of anionic dyes from aqueous solution[J]. Science China Materials, 59(1): 38–50.
DOI:10.1007/s40843-016-0117-y
|
Puig S, Serra M, Vilar-Sanz A, et al. 2011. Autotrophic nitrite removal in the cathode of microbial fuel cells[J]. Bioresource Technology, 102(6): 4462–4467.
DOI:10.1016/j.biortech.2010.12.100
|
Singhal G, Bhavesh R, Kasariya K, et al. 2011. Biosynthesis of silver nanoparticles using Ocimum sanctum (Tulsi) leaf extract and screening its antimicrobial activity[J]. Journal of Nanoparticle Research, 13(7): 2981–2988.
DOI:10.1007/s11051-010-0193-y
|
Tremouli A, Vlassis T, Antonopoulou G, et al. 2016. Anaerobic degradation of pure glycerol for electricity generation using a MFC:the effect of substrate concentration[J]. Waste and Biomass Valorization, 7(6): 1339–1347.
DOI:10.1007/s12649-016-9498-0
|
涂丽杏, 朱能武, 吴平霄, 等. 2013. 羧基化碳纳米管载铂催化剂对微生物燃料电池阴极氧还原性能的影响[J]. 环境科学, 2013, 34(4): 1617–1622.
|
Wang T, Jin X, Chen Z, et al. 2014. Green synthesis of Fe nanoparticles using eucalyptus leaf extracts for treatment of eutrophic wastewater[J]. Science of the Total Environment, 466: 210–213.
|
Wang Y, Shi Z X, Yin J. 2011. Facile synthesis of soluble graphene via a green reduction of graphene oxide in tea solution and its biocomposites[J]. ACS Applied Materials & Interfaces, 3(4): 1127–1133.
|
Wei J, Liang P, Huang X. 2011. Recent progress in electrodes for microbial fuel cells[J]. Bioresource Technology, 102(20): 9335–9344.
DOI:10.1016/j.biortech.2011.07.019
|
闻雷, 刘成名, 宋仁升, 等. 2014. 石墨烯材料的储锂行为及其潜在应用[J]. 化学学报, 2014, 72(3): 333–344.
|
Yuan Y, Zhou S, Zhao B, et al. 2012. Microbially-reduced graphene scaffolds to facilitate extracellular electron transfer in microbial fuel cells[J]. Bioresource Technology, 116(4): 453–458.
|
张凯, 丁春梅, 刘欢, 等. 2014. 希瓦氏菌介导制还原氧化石墨烯薄膜及其增强的胞外电子传递[J]. 高等学校化学学报, 2014, 35(10): 2201–2206.
DOI:10.7503/cjcu20140303 |
 2017, Vol. 37
2017, Vol. 37


