2. 广东省大气环境与污染控制重点实验室, 广州 510006;
3. 大气污染控制广东高校工程技术研究中心, 广州 510006
2. Guangdong Provincial Key Laboratory of Atmospheric Environment and Pollution Control, Guangzhou 510006;
3. Guangdong High Education Engineering Technology Research Center for Air Pollution Control, Guangzhou 510006
柴油发动机以其良好的动力与经济性得到广泛应用,而其尾气中以碳烟(soot)为主的污染物却对大气环境和人体健康造成严重危害(Bueno López,2014;Pahalagedara et al., 2012).颗粒物过滤器(DPF)作为去除发动机尾气中碳烟的有效装置,其核心在于高活性的催化剂(Kumar et al., 2012;Russo et al., 2008),MnOx-CeO2复合氧化物催化剂因其优异的低温活性得到广泛的研究(Wu et al., 2012;Shan et al., 2010).CeO2具备优异的储氧性能、负载金属高分散度及存在强酸和强碱中心(Fu et al., 2014;Piumetti et al., 2016).MnOx存在多种价态具有优异的氧化还原特性,而在MnOx-CeO2中,Mn进入CeO2的晶格形成Mn-Ce-O固溶体,使其具备更大的比表面积、更多的表面氧空位和更强的表面活性氧迁移转化能力,这些也是MnOx-CeO2催化氧化碳烟的关键因素.
研究表明,介质阻挡放电(pulse dielectric barrier discharge,PDBD)对碳烟催化氧化具有一定的强化作用(Sekine et al., 2013;Chae et al., 2003;Ye et al., 2005),其原因主要包括两个方面,①在放电过程中催化剂表面活性物种的生成、迁移和转化会得到加强,其表面氧化还原性质得到调节(Chae et al., 2003;Ouyang et al., 2013);②放电会在气氛中产生O3、OH和O自由基等强氧化性活性物种(Yao et al., 2004;Fushimi et al., 2008;Tang et al., 2013),这一现象在脉冲放电中更为明显(Yao et al., 2004;Fushimi et al., 2008).但OH和O等自由基寿命很短,且在传输过程中不断消耗,而O3也不稳定,200 ℃以上时很容易分解,同时作为多相催化反应,碳烟氧化在无催化剂体系中,PDBD对反应的强化作用并不明显(Yao et al., 2004;Ding et al., 2006).一般认为PDBD的强化效应与MnOx-CeO2的关键表面活性物种如活性氧(Sekine et al., 2013)和Mn物种(Tikhomirov et al., 2006)的量及其变化关系密切.
如前所述,PDBD从改变气氛和催化剂表面性质两方面强化碳烟的催化氧化,且一定条件下发生的等离子体对催化剂性能改变的具体原因仍需进一步探讨.然而,PDBD对MnOx-CeO2催化氧化碳烟中催化剂表面结构与性质的改变作为重要因素,其引发的强化作用重复性如何,尤其这一催化剂表面结构与性质的改变是否可逆值得探讨.
因此,本文使用前期研究中优选的柠檬酸络合法制备的Mn/(Mn+Ce)原子比为0.4的MnOx-CeO2催化剂(Zhang et al., 2011).将新鲜催化剂分别在引入PDBD(简称放电)和未引入(简称无放电)这两种条件下,各重复3次进行活性评价,对比活性高低及各次反应后活性的变化,并利用各种表征手段分析催化剂结构性质及表面活性物种的变化,研究PDBD对MnOx-CeO2催化氧化碳烟强化作用的重复性及其对催化剂表面结构与性质的改变,并在此基础上对PDBD强化MnOx-CeO2催化氧化碳烟的本质原因进行探讨.
2 实验部分 (Experiments) 2.1 催化剂制备MnOx-CeO2的制备方法采用柠檬酸络合法,选用的前体物为Ce(CH3COO)3·5H2O(AR,阿拉丁试剂厂)和Mn(CH3COO)2·4H2O(AR,阿拉丁试剂厂).首先,配置离子溶液,分别配置一定浓度的Ce(CH3COO)3·5H2O和Mn(CH3COO)2·4H2O溶液,并按照Mn/(Mn + Ce) 的原子比为0.4进行混合,调节温度为70 ℃,加入柠檬酸(AR,国药集团化学试剂有限公司)进行络合,使用柠檬酸控制pH为1.5.然后,将混合溶液在95 ℃下进行蒸发,直至产生胶状粘稠物,此时迅速转移至油浴锅,温度为150 ℃,待沉淀物结为砖块,取出研磨并干燥除去水分.最后,于马弗炉进行焙烧,温度为550 ℃,时间5 h.
2.2 表征 2.2.1 XRDXRD测试使用德国Bruker D8 Advance X射线衍射仪,铜靶辐射,入射线λ=0.15418 nm,管流40 mA,管压40 kV,Ni滤波片,步长0.02°,衍射角20°~80°.
2.2.2 BETSSA(specific surface area),BET测定使用美国Micromeritics ASAP 2020N比表面积及微孔孔隙分析仪,样品重量200 mg,N2作吸附质,300 ℃抽真空,预处理4 h,-196 ℃测定.
2.2.3 Raman拉曼光谱仪使用LabRAM HR Evolution,可见光激发波长为532 nm,功率为5 mW,扫描范围300~800 cm-1,紫外光激发波长为325 nm,扫描范围300~1350 cm-1,CCD检测拉曼信号.
2.2.4 XPSXPS测定使用的美国Thermo-VG Scientific ESCALAB 250光电子能谱仪,Mg Ka射线(hv=1253.6 eV)测定,C1s校准结合能284.6 eV,使用XPS peak分峰软件对数据进行分峰.
2.3 活性评价为检验催化剂重复反应的性能,将新鲜制备未反应过的催化剂(标记为fresh)分别在没有引入脉冲放电等离子体(简称无放电)条件下进行1次(标记为TPO-1st)、2次(标记为TPO-2nd)和3次(标记为TPO-3rd)活性评价,同时也在引入PDBD(简称放电)条件下进行1次(标记为D-TPO-1st)、2次(标记为D-TPO-2nd)和3次(标记为D-TPO-3rd)活性评价.最后,对未反应过的催化剂和两种条件下各次反应后的催化剂进行表征.
使用TPO(temperature programmed oxidation)对催化剂催化氧化碳烟的活性进行评(Ouyang et al., 2013),反应物为模拟碳烟(德国,Printex-U),反应气氛为10%O2/Ar混合气,流量100 mL·min-1,反应过程温度由30 ℃升至700 ℃,升温速率为3 ℃·min-1.首先,混合270 mg催化剂与30 mg碳烟并研磨2 min,碳烟与催化剂为松散接触,再加入900 mg的石英砂,以防止反应时温度失控.然后,将混合物放入石英玻璃反应管(I.D.=12 mm, O.D.=16 mm),用石英棉进行固定,反应前混合物先在300 ℃的Ar气氛下进行预处理.尾气使用气相色谱检测,活性评价过程中,未检测到CO,因此, 使用CO2作为催化剂氧化碳烟的活性评价数据.Ti为起燃温度,是尾气中CO2浓度为5000×10-6(Liang et al., 2008;Wu et al., 2010)时的温度;Tm为最大燃烧速率温度,是尾气中CO2浓度达到最高时的温度;Tc为燃尽温度,尾气中CO2浓度从最大值降回至1000×10-6时的温度;△T为燃烧区间,△T = Tc -Ti.
放电是使用脉冲介质阻挡放电装置,放电反应装置结构如图 1所示,在石英玻璃管(I.D.=12 mm, O.D.=16 mm)中心放置一根不锈钢直管作为放电反应的正极,外壁则缠绕一段电线并接地,用做放电过程的负极,催化剂与碳烟所构成的反应区的长度约为1.5 cm,其完全处于放电区域内,组成一个线-筒式的介质阻挡沿面放器.放电反应装置:大连泰思曼科技有限公司生产,频率和脉宽可调的TP3025高压脉冲电源.实验条件:50 Hz频率和11 kV电压.
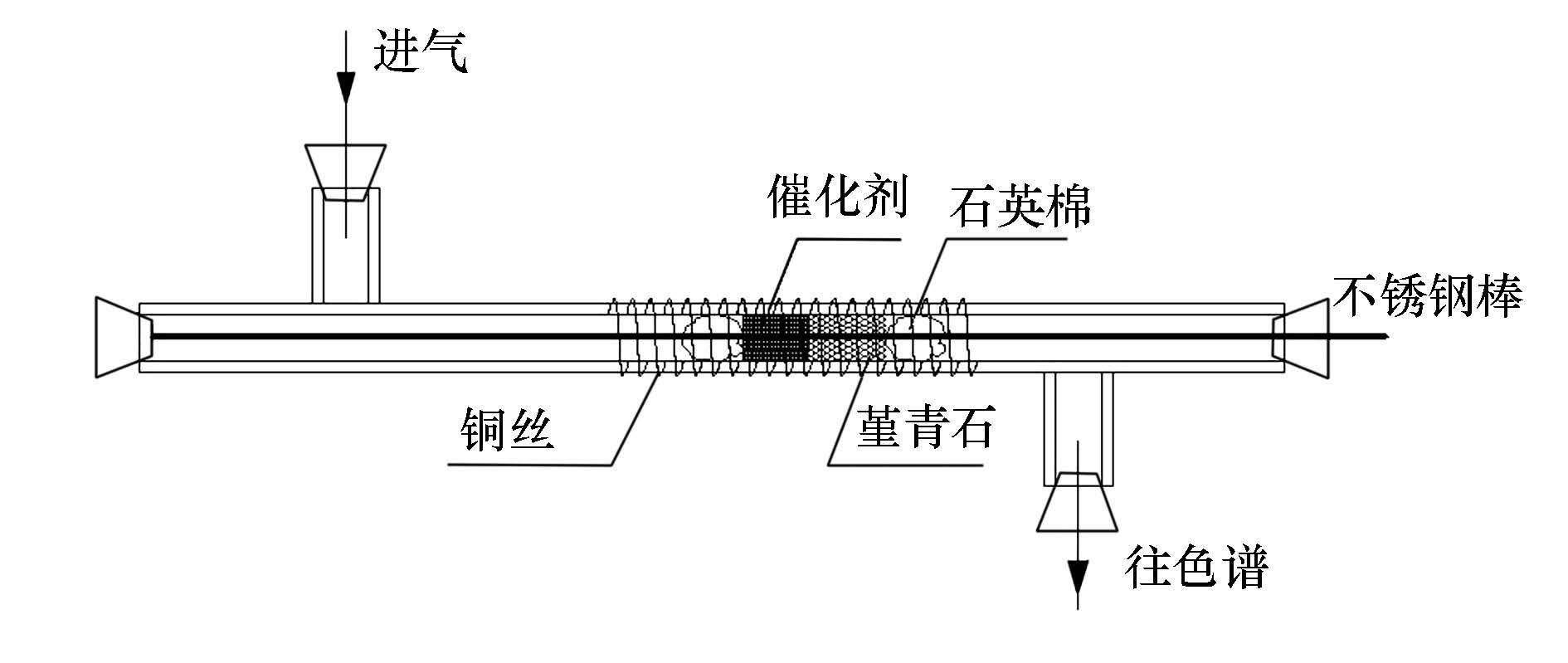 |
| 图 1 脉冲介质阻挡放电反应装置示意图 Fig. 1 Reactor of pulse dielectric barrier discharge |
2种条件下各次反应的Ti、Tm和△T值见表 1,由此可知,在首次反应中,在放电条件下,MnOx-CeO2的起燃温度为252 ℃低于无放电条件下的260 ℃,放电对碳烟的催化氧化起了强化作用.而无论是放电与否,MnOx-CeO2在第二次反应时的Ti值和Tm值均有所升高,而在第3次反应时则不再增高,在首次反应后MnOx-CeO2的结构与性质可能发生了一些不可逆的转变,致使其活性下降,而在这之后的反应中则保持了相对稳定,即反应活性未发生明显变化.
| 表 1 MnOx-CeO2催化氧化碳烟的Ti、Tm和△T Table 1 Ti, Tmand △T for soot oxidation on MnOx-CeO2 |
在无放电条件下,MnOx-CeO2的起燃温度从第一次到第二次增加了12 ℃,而在放电条件下从第一次到第二次则增加了26 ℃.也就是说,放电条件下MnOx-CeO2首次反应后活性降低程度更大.推测相对于没有放电的情况,脉冲介质阻挡放电使MnOx-CeO2在其首次反应中发生了一些更大程度的结构与性质的不可逆转变.对比两种条件,催化剂各次反应的Tm值均很接近,说明脉冲介质阻挡放电对催化剂结构与性质的改变,主要影响的是催化剂对碳烟的起燃温度,而不是最大燃烧速率.
3.2 XRD和BET对新鲜MnOx-CeO2催化剂,以及其分别在有无放电两种条件下重复反应的样品进行XRD测试,结果见图 2.从图中可以看出,未反应过的MnOx-CeO2表现出良好的立方萤石结构(Bueno López,2014;Shan et al., 2010;Tikhomirov et al., 2006),且只观测到CeO2的立方萤石相的衍射峰,未发现任何MnOx相的衍射峰,表明MnOx-CeO2中的Mn进入到CeO2的萤石结构中,形成了Mn-Ce-O的固溶体(Venkataswamy et al., 2015;Xing et al., 2015).而无论在放电还是没有放电的条件下,第一次反应后,MnOx-CeO2的CeO2立方萤石相的衍射峰,与未反应过的MnOx-CeO2的相比,其峰强均增加并发生了锐化,推测于550 ℃焙烧的催化剂,在700 ℃的高温反应后发生了一定程度的烧结(Wu et al., 2011).
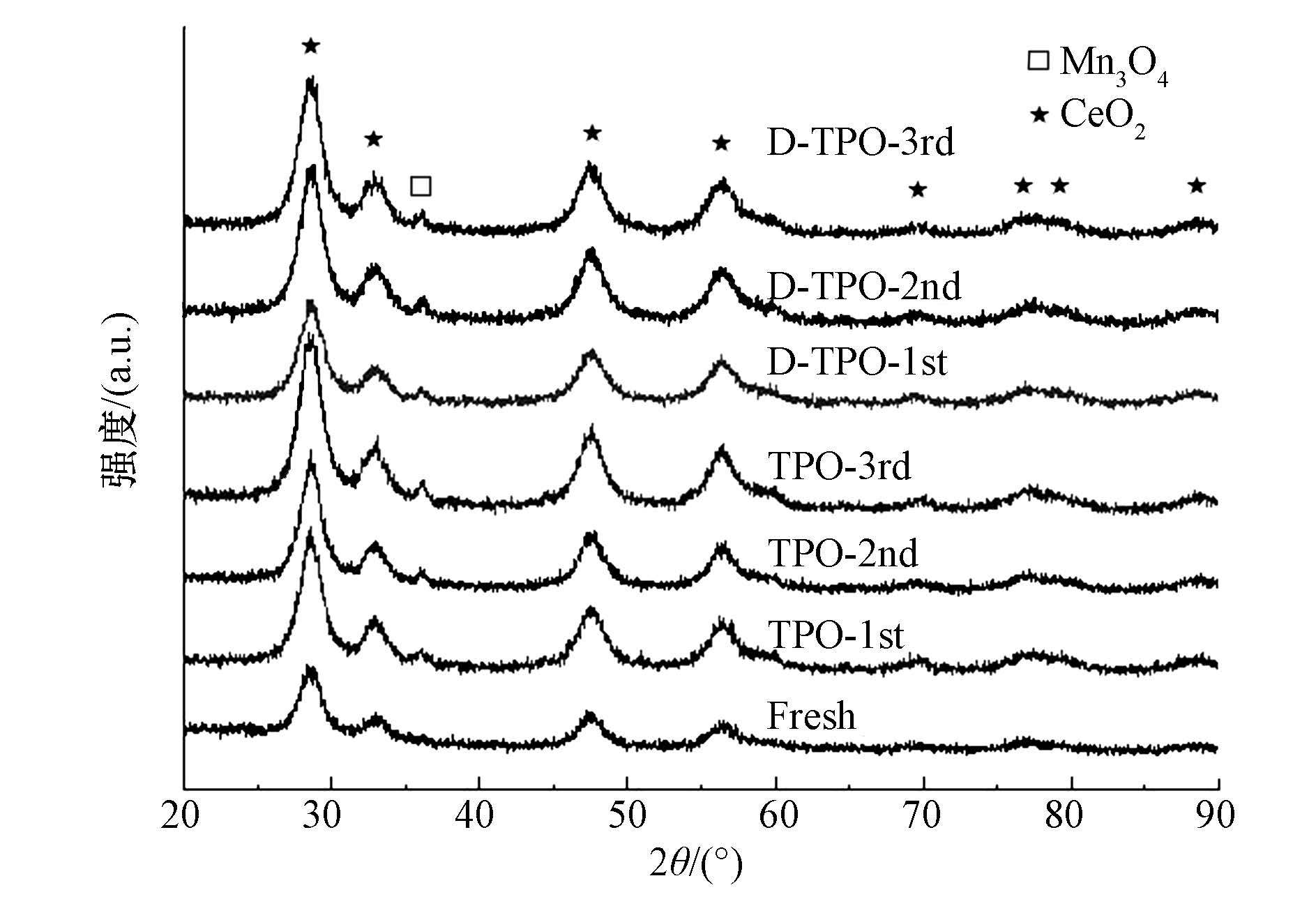 |
| 图 2 MnOx-CeO2未反应时及其各次反应后的XRD谱图 Fig. 2 XRD patterns of fresh and reacted MnOx-CeO2 catalysts |
同时,2种条件下,MnOx-CeO2在首次反应后均出现了Mn3O4的衍射峰,说明MnOx-CeO2在首次反应的过程中,发生了不可逆的相分离,Mn从其与CeO2形成的萤石结构固溶体中析出,生成了Mn3O4(Wu et al., 2011).而以上现象在第2和第3次反应后并没有进一步扩大,说明第1次反应后催化剂结构趋于稳定,这也解释了MnOx-CeO2在首次反应后活性降低但随后保持了稳定的现象.
对新鲜的及其各次反应后的MnOx-CeO2进行了BET测试,所得比表面积结果见表 2.可知在两种条件下,MnOx-CeO2在首次反应后比表面积均有降低,推测是因为MnOx-CeO2首次反应后发生了烧结(Wu et al., 2011),同时在随后的反应中比表面积基本不再降低,与XRD测试结果一致.
| 表 2 MnOx-CeO2未反应时及其各次反应后的比表面积 Table 2 Specific surface area (SSA) of fresh and reacted MnOx-CeO2 catalysts |
图 3是MnOx-CeO2未反应时及其各次反应后,在可见光和紫外光激发下的Raman谱图.在图 3a中,可以明显观察到,无论放电与否,MnOx-CeO2首次反应后在650 cm-1左右位置均出现一个特征峰,并在随后保持稳定,归属于Mn3O4(Han et al., 2007).这进一步说明MnOx-CeO2首次反应后发生了不可逆的相分离,Mn从Mn-Ce-O的萤石结构固溶体中析出,生成了独立的Mn3O4晶相,这与XRD的结果一致.同时在图 3a中,位于465 cm-1的特征峰为CeO2的立方萤石结构F2g的特征振动(何丽芳等2013) ,在放电和无放电两种条件下,MnOx-CeO2的F2g特征峰在反应后均出现一定了程度的锐化,表明了MnOx-CeO2在反应后其CeO2的立方萤石结构结晶程度得到了提高,归因于初次反应后催化剂发生了一定程度的烧结,这与SSA结果一致.值得注意的是,相比于放电条件,MnOx-CeO2未放电直接反应后的F2g特征峰发生了一定程度的红移,因F2g特征峰的红移程度与氧化铈表面本征氧空位浓度正相关(Lee et al., 2011),由此可知其表面生成了更多的本征氧空位.本征氧空位可吸附活化气相中的氧分子,是反应的活性位点,其快速生成与转化的能力是氧化铈拥有高储氧能力的本质原因(Campbell et al., 2005),而紫外拉曼光谱对氧空位的表征更为灵敏(Taniguchi et al., 2009).
 |
| 图 3 MnOx-CeO2未反应时及其各次反应后的可见光(a)和紫外光(b)激发Raman谱图 Fig. 3 Visible (a) and UV (b) raman spectrum of fresh and reacted MnOx-CeO2 catalysts |
在图 3b中,位于465 cm-1的特征峰为CeO2的立方萤石结构F2g的特征振动,600 cm-1归属于CeO2的填隙式氧空位(Wu et al., 2010).值得注意的是,在无放电条件下,MnOx-CeO2在首次反应后于575 cm-1处出现了一个肩峰,其归属于本征氧空位(Agarwal et al., 2014),但在放电条件下,这一变化并不明显,推测PDBD不利于本征氧空位的出现,这与可见光激发下的拉曼谱图观测的结果一致.
氧化铈基固溶体中氧空位的浓度观察值可由氧空位特征峰与F2g振动特征峰的峰面积之比(AOV/AF2g)表示(Taniguchi et al., 2009),图 4为 MnOx-CeO2未反应时及其各次反应后填隙式氧空位峰面积与CeO2的立方萤石结构F2g特征峰的峰面积比值(A600/A465)的变化情况,由图可知,MnOx-CeO2表面填隙式氧空位浓度在有无放电两种条件下于首次反应后均出现下降,推测该氧空位浓度在首次反应下降对催化剂活性的产生了一定影响.同时,在无放电条件下填隙式氧空位浓度下降更为明显,说明有更多的氧离子填隙子脱除,考虑到无放电条件下本征氧空位的出现,推测减少的填隙式氧空位可能部分转化为了本征氧空位.
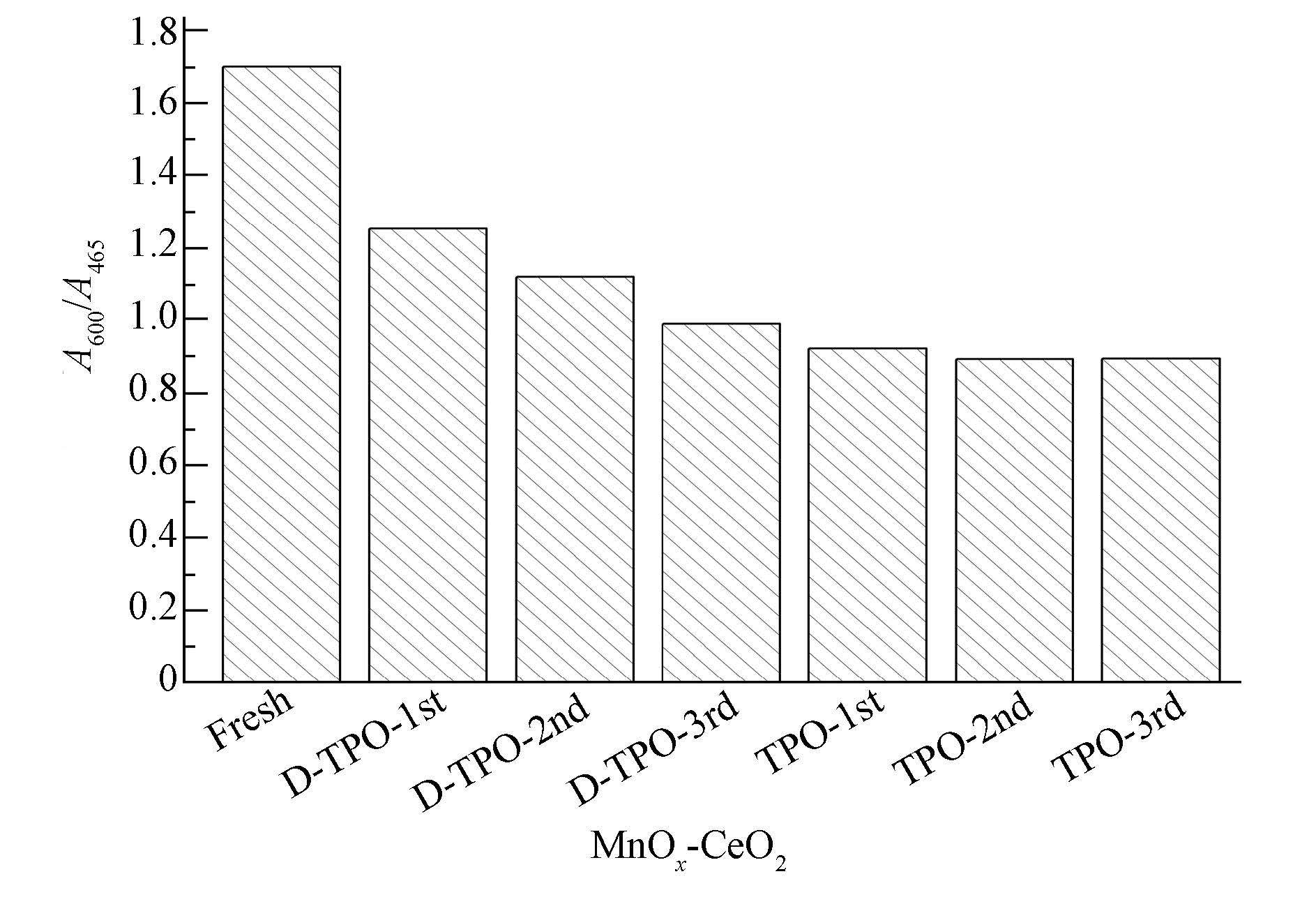 |
| 图 4 MnOx-CeO2未反应时及其各次反应后的A600/A465值变化情况 Fig. 4 Ratio of A600/A465 between fresh and reacted MnOx-CeO2 catalysts |
对放电和无放电两种条件下各次反应前后MnOx-CeO2进行了XPS测试,结果见表 3.在O1s 谱图中结合能在533~534 eV 间的特征峰归属为吸附氧(Oads),在530~532 eV间为表面氧(Osur),在529~530 eV间是晶格氧(Olatt)(Wang et al., 2009;Li et al., 2011).
| 表 3 无放电和放电条件下MnOx-CeO2各次反应前后的XPS表面元素分析结果 Table 3 Atomic ratios by XPS surface compositional analysis of fresh and reacted MnOx-CeO2 catalysts |
由表 3可知,无论放电与否,Mn4+/(Mn2++Mn3+)比值在MnOx-CeO2首次反应后均降低,且在放电条件下降低程度更为明显,但在随后的反应中保持了相对稳定.也就是说在两种反应条件下,MnOx-CeO2首次反应后部分Mn4+均不可逆地转变成了Mn2+和Mn3+,此后则保持了稳定.结合XRD和Raman中观测到的MnOx-CeO2首次反应后发生相分离生成Mn3O4的现象,可以认为MnOx-CeO2首次反应后其Mn-Ce-O固溶体中的Mn4+析出并生成Mn3O4,即Mn4+还原为Mn2+和Mn3+生成Mn3O4,且这一过程并不可逆.
放电条件下有更多的Mn4+不可逆地转变为了Mn2+和Mn3+,而Ce4+/Ce3+的值在MnOx-CeO2首次反应后,于无放电条件下降低而在放电条件下整体升高.Ce3+的存在会在催化剂表面产生本征氧空位,而更多Ce3+的存在将使本征氧空位的浓度增大更易观测,因而在Raman测试中,无放电条件下反应后的MnOx-CeO2存在更容易观测到的本征氧空位.同时,无放电条件下,MnOx-CeO2首次反应后产生了更多的表面氧而晶格氧的比例减少,而在放电条件下,MnOx-CeO2首次反应后晶格氧的比例增加而表面氧的比例减少.鉴于更多的本征氧空位会产生更多的表面活性氧,这说明相较于放电条件,在无放电条件下MnOx-CeO2首次反应后更少的Mn4+不可逆地转化为低价态,而Ce3+的比例更高,有更多的本征氧空位及表面氧.
综上所述,一方面在放电和无放电两种条件下,新鲜MnOx-CeO2在首次氧化碳烟反应后,再反应时活性均有所降低,这归因于MnOx-CeO2在首次反应后比表面积下降,并出现了不可逆的相分离,部分Mn从其与CeO2形成的萤石结构固溶体中析出成为了Mn3O4,部分Mn4+不可逆地转成Mn2+和Mn3+,同时表面填隙式氧空位浓度减少.考虑到CeO2中Mn4+的掺杂会提高表面填隙式氧空位的浓度,可以推测,于550 ℃焙烧制备而成的催化剂,在700 ℃的高温反应后发生了一定程度的烧结以及相分离,部分Mn4+从其与CeO2成的萤石结构固溶体中析出,同时表面填隙式氧空位减少,CeO2发生一定程度的烧结,而Mn4+不可逆地转成Mn2+和Mn3+.这表明Mn-Ce-O固溶体的生成不仅宏观上会使MnOx-CeO2拥有更大的比表面积利于碳烟的催化氧化,而且在微观上会使MnOx-CeO2产生更多的填隙式氧空位,而催化剂表面该氧空位的富集程度与其碳烟氧化活性又呈现出一定的相关性,可以认为其为MnOx-CeO2催化碳烟的关键因素.虽然两种条件下,柠檬酸络合法制备的MnOx-CeO2在首次氧化碳烟反应后结构与性质发生了一定程度的不可逆转变,并伴随一定程度的活性降低,当在随后的反应中,不管是催化剂的结构和性质,还是其反应活性均保持了稳定,说明柠檬酸络合法制备的MnOx-CeO2拥有较好的稳定性.
另一方面,虽然新鲜MnOx-CeO2催化剂在介质阻挡放电条件下初次反应时具备更高的活性,但其在重复反应时起燃温度却升得更高,首次反应后活性降低程度更大,说明在本研究条件下的脉冲介质阻挡放电产生的强化作用不具备良好的重复性.这归因于在本研究的放电条件下,更多的Mn4+不可逆地转成Mn2+和Mn3+,而无放电条件下则较少,并且拥有更多的本征氧空位及表面氧.由此可见脉冲介质阻挡放电在首次反应过程中对Mn4+的还原有一定程度地促进作用,释放出更多的氧物种(Xu et al., 2010),因而产生更高的反应活性,然而对于Mn4+的恢复则没有促进作用,致使首次反应后Mn4+减少,以至于在随后的反应过程中放电条件下活性降低更为明显.与此同时,在无放电条件下,MnOx-CeO2首次反应后,拥有相对更多的Mn4+,而Ce4+却更少,推测Mn4+在反应过程中脱氧消耗后,CeO2的晶格氧对其进行了补充(Zhang et al., 2010),更多Ce4+转化为Ce3+,同时产生了本征氧空位,其可促使晶格氧和气相氧转化为表面氧,并作为活性位点利于表面活性物种的生成、迁移和转化(Esch et al., 2005),这一系列作用都有利于碳烟的催化氧化,而可以推测脉冲介质阻挡放电可能对这种作用具有一定的抑制效应.另外值得注意的是,虽然没有放电时催化剂表面发生不可逆还原的Mn4+量更少,且产生了本征氧空位及更多的表面氧,但结合起燃温度和最大燃烧温度来看,催化剂在初次反应后,再进行反应时的活性与放电条件下却较为相当.这暗示即使本研究中脉冲介质阻挡放电对催化剂表面结构与性质的不可逆改变对活性产生了不利影响,但其在反应气氛中产生的活性自由基对反应仍具有促进作用.由此可知,以上因素会对MnOx-CeO2催化氧化碳烟反应产生关键影响.
图 5为新鲜MnOx-CeO2在有无引入PDBD条件下,初次反应时的表面物种变化示意图.没有放电时,高反应温度会使催化剂发生相分离,部分Mn4+脱除并还原为Mn2+和Mn3+,生成Mn3O4,填隙式氧空位(Frenkel-type oxygen vacancy,简写为FOV)减少,而CeO2具备供氧能力,恢复了部分Mn4+,同时Ce4+转化为Ce3+,生成本征氧空位(Intrinsic oxygen vacancy,简写为IOV)并产生表面氧.PDBD会加剧Mn4+向Mn2+和Mn3+的转化,提供更高的反应活性,却抑制了Mn4+的恢复.无论是否引入PDBD,MnOx-CeO2在初次反应发生一定程度的结构与性质的不可逆转变后,随后均保持了稳定.
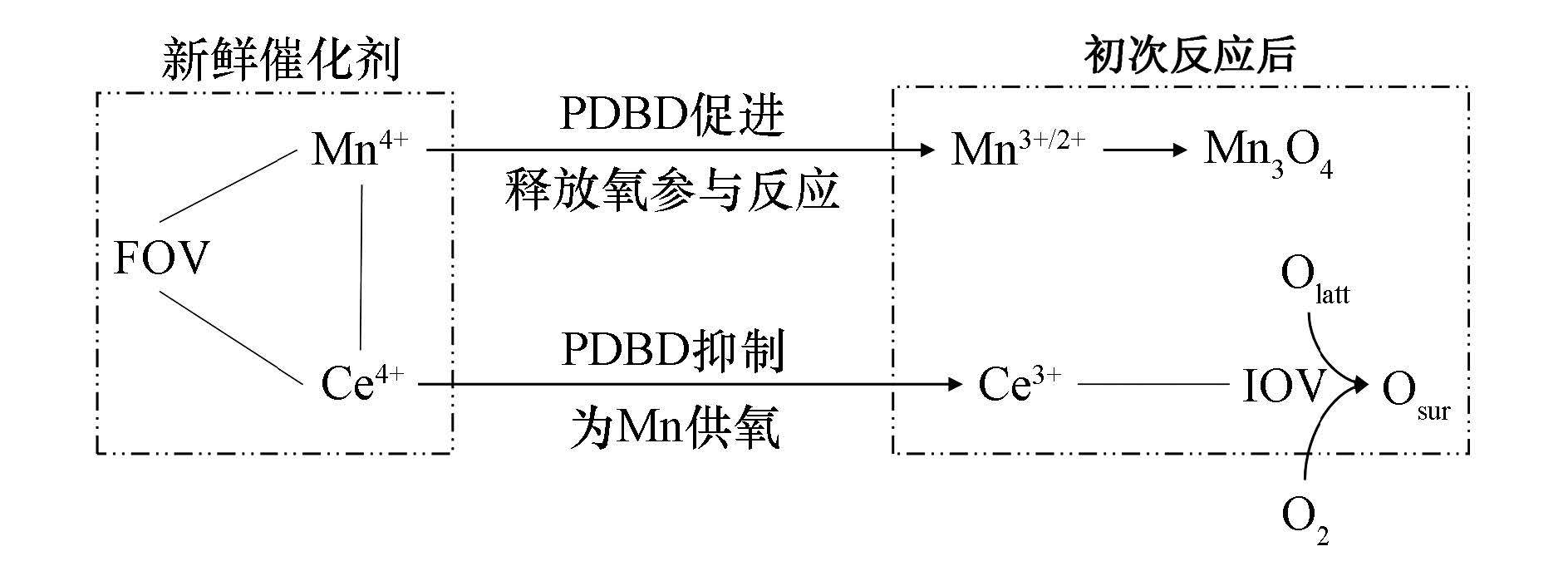 |
| 图 5 MnOx-CeO2初次反应表面物种变化示意图 Fig. 5 Diagram of first catalysis of soot oxidation by MnOx-CeO2 |
1) 柠檬酸络合法制备的MnOx-CeO2在有无放电两种条件下氧化碳烟的初次反应中,均发生了一定程度的相分离,部分Mn从其与CeO2形成的萤石结构固溶体中析出生成Mn3O4,表面填隙式氧空位浓度减少,再次反应时活性有所下降,但在随后的反应中催化剂的活性和表面物种保持了稳定.
2) 在50 Hz及11 kV条件下引发的PDBD,在MnOx-CeO2初次催化氧化碳烟时起了强化作用,但也加剧了反应关键因素的不可逆转变,影响了强化作用的重复性.初次反应后,放电使MnOx-CeO2中更多的Mn4+不可逆地转变为Mn2+和Mn3+,表面本征氧空位浓度更低,表面氧更少.虽然催化剂在随后的反应中保持了稳定,但PDBD对MnOx-CeO2催化氧化碳烟反应关键因素的不可逆影响值得关注及深入探讨.
| [${referVo.labelOrder}] | Agarwal S, Zhu X, Hensen E J M, et al. 2014. Defect chemistry of ceria nanorods[J]. Journal of Physical Chemistry C, 118(8) : 4131–4142. DOI:10.1021/jp409989y |
| [${referVo.labelOrder}] | Bueno López A. 2014. Diesel soot combustion ceria catalysts[J]. Applied Catalysis B:Environmental, 146 : 1–11. DOI:10.1016/j.apcatb.2013.02.033 |
| [${referVo.labelOrder}] | Chae J O. 2003. Non-thermal plasma for diesel exhaust treatment[J]. Journal of Electrostatics, 57(3/4) : 251–262. |
| [${referVo.labelOrder}] | Campbell C T, Peden C H F. 2005. Oxygen vacancies and catalysis on ceria surfaces[J]. Science, 309(5735) : 713–714. DOI:10.1126/science.1113955 |
| [${referVo.labelOrder}] | Ding H X, Zhu A M, Lu F G, et al. 2006. Low-temperature plasma-catalytic oxidation of formaldehyde in atmospheric pressure gas streams[J]. Journal of Physics D:Applied Physics, 39(16) : 3603–3608. DOI:10.1088/0022-3727/39/16/012 |
| [${referVo.labelOrder}] | Esch F, Fabris S, Zhou L, et al. 2005. Electron localization determines defect formation on ceria substrates[J]. Science, 309(5735) : 752–755. DOI:10.1126/science.1111568 |
| [${referVo.labelOrder}] | Fu M L, Lin J M, Zhu W B, et al. 2014. Surface reactive species on MnOx(0.4)-CeO2 catalysts towards soot oxidation assisted with pulse dielectric barrier discharge[J]. Journal of Rare Earths, 32(2) : 153–158. DOI:10.1016/S1002-0721(14)60045-4 |
| [${referVo.labelOrder}] | Fushimi C, Madokoro K, Yao S, et al. 2008. Influence of polarity and rise time of pulse voltage waveforms on diesel particulate matter removal using an uneven dielectric barrier discharge reactor[J]. Plasma Chemistry and Plasma Processing, 28(4) : 511–522. DOI:10.1007/s11090-008-9134-2 |
| [${referVo.labelOrder}] | Han Y F, Ramesh K, Chen L W, et al. 2007. Observation of the reversible phase-transformation of r-Mn2O3 nanocrystals during the catalytic combustion of methane by in Situ Raman Spectroscopy[J]. Journal of Physical Chemistry C, 111(7) : 2830–2833. DOI:10.1021/jp0686691 |
| [${referVo.labelOrder}] | 何丽芳, 廖银念, 陈礼敏, 等. 2013. 纳米CeO2催化氧化甲苯的形貌效应研究[J]. 环境科学学报, 2013, 33(9) : 2412–2421. |
| [${referVo.labelOrder}] | Kumar P A, Tanwar M D, Bensaid S, et al. 2012. Soot combustion improvement in diesel particulate filters catalyzed with ceria nanofibers[J]. Chemical Engineering Journal, 207-208 : 258–266. DOI:10.1016/j.cej.2012.06.096 |
| [${referVo.labelOrder}] | Li H, Lu G, Dai Q, et al. 2011. Efficient low-temperature catalytic combustion of trichloroethylene over flower-like mesoporous Mn-doped CeO2 microspheres[J]. Applied Catalysis B:Environmental, 102(3/4) : 475–483. |
| [${referVo.labelOrder}] | Liang Q, Wu X, Weng D, et al. 2008. Oxygen activation on Cu/Mn-Ce mixed oxides and the role in diesel soot oxidation[J]. Catalysis Today, 139(1/2) : 113–118. |
| [${referVo.labelOrder}] | Lee Y J, He G H, Akey A J, et al. 2011. Raman analysis of mode softening in nanoparticle CeO2-δ and Au-CeO2-δ during CO oxidation[J]. Journal of the American Chemical Society, 133(33) : 12952–12955. DOI:10.1021/ja204479j |
| [${referVo.labelOrder}] | Ouyang J H, Lin J M, Liu Y F, et al. 2013. Studies on the active oxygen species of Cu0.95O catalyst for soot combustion-promoting effect of plasma[J]. China Environmental Science, 33 : 243–250. |
| [${referVo.labelOrder}] | Piumetti M, Bensaid S, Russo N, et al. 2016. Investigations into nanostructured ceria-zirconia catalysts for soot combustion[J]. Applied Catalysis B:Environmental, January, 180 : 271–282. DOI:10.1016/j.apcatb.2015.06.018 |
| [${referVo.labelOrder}] | Pahalagedara L, Sharma H, Kuo C H, et al. 2008. Structure and oxidation activity correlations for carbon blacks and diesel soot[J]. Energy Fuel, 26(11) : 6757–6764. |
| [${referVo.labelOrder}] | Russo N, Fino D, Saracco G, et al. 2008. Promotion effect of Au on perovskite catalysts for the regeneration of diesel particulate filters[J]. Catalysis Today, 137(2) : 306–311. |
| [${referVo.labelOrder}] | Sekine Y, Koyama H, Matsukata M, et al. 2013. Plasma-assisted oxidation of carbon particle by lattice oxygen on/in oxide catalyst[J]. Fuel, 103 : 2–6. DOI:10.1016/j.fuel.2011.03.046 |
| [${referVo.labelOrder}] | Shan W J, Ma N, Yang J L, et al. 2010. Catalytic oxidation of soot particulates over MnOx-CeO2 oxides prepared by complexation-combustion method[J]. Journal of Natural Gas Chemistry, 19 : 86–90. DOI:10.1016/S1003-9953(09)60033-5 |
| [${referVo.labelOrder}] | Taniguchi T, Watanabe T, Sugiyama N, et al. 2009. Identifying defects in ceria-based nanocrystals by UV resonance raman spectroscopy[J]. Journal of Physical Chemistry C, 113(46) : 19789–19793. DOI:10.1021/jp9049457 |
| [${referVo.labelOrder}] | Tang X, Lu H, Lin L, et al. 2013. Experimental Investigation of plasma oxidization of diesel particulate matter[J]. Plasma Chemistry and Plasma Processing, 33(1) : 281–292. DOI:10.1007/s11090-012-9430-8 |
| [${referVo.labelOrder}] | Tikhomirov K, Kröcher O, Elsener M, et al. 2006. MnOx-CeO2 mixed oxides for the low-temperature oxidation of diesel soot[J]. Applied Catalysis B:Environmental, 64(1/2) : 72–78. |
| [${referVo.labelOrder}] | Venkataswamy P, Deshetti P, Lin F, et al. 2015. Structural properties of alumina supported Ce-Mn solid solutions andtheir markedly enhanced catalytic activity for CO oxidation[J]. Applied Surface Science, 349 : 299–309. DOI:10.1016/j.apsusc.2015.04.220 |
| [${referVo.labelOrder}] | Wu X D, Lee H R, Liu S, et al. 2012. Sulfur poisoning and regeneration of MnOx-CeO2-Al2O3 catalyst for soot oxidation[J]. Journal of Rare Earths, 30(7) : 659–664. DOI:10.1016/S1002-0721(12)60108-2 |
| [${referVo.labelOrder}] | Wu X, Lin F, Xu H, et al. 2010. Effects of adsorbed and gaseous NOx species on catalytic oxidation of diesel soot with MnOx-CeO2 mixed oxides[J]. Applied Catalysis B:Environmental, 96(1/2) : 101–109. |
| [${referVo.labelOrder}] | Wu X, Liu S, Weng D, et al. 2011. MnOx-CeO2-Al2O3 mixed oxides for soot oxidation:Activity and thermal stability[J]. Journal of Hazardous Materials, 187(1/3) : 283–290. |
| [${referVo.labelOrder}] | Wang X Y, Qian K, Dao L. 2009. Catalytic combustion of chlorobenzene over MnOx-CeO2 mixed oxide catalysts[J]. Applied Catalysis B:Environmental, 86(3/4) : 166–175. |
| [${referVo.labelOrder}] | Wu Z L, Li M J, Howe J, et al. 2010. Probing defect sites on CeO2 nanocrystals with well-defined surface planes by Raman spectroscopy and O2 adsorption[J]. Langmuir, 26(21) : 16595–16606. DOI:10.1021/la101723w |
| [${referVo.labelOrder}] | Xing X X, Cai Y, Chen N, et al. 2015. Synthesis of mixed Mn-Ce-Ox one dimensional nanostructures and their catalytic activity for CO oxidation[J]. Ceramics International, 41(3) : 4675–4682. DOI:10.1016/j.ceramint.2014.12.014 |
| [${referVo.labelOrder}] | Xu J, Li P, Song X F, et al. 2010. Operando raman spectroscopy for determining the active phase in one-dimensional Mn1-xCexO2±y nanorod catalysts during methane combustion[J]. Journal of Physical Chemistry Letters, 1(10) : 1648–1654. DOI:10.1021/jz1004522 |
| [${referVo.labelOrder}] | Yao S, Okumoto M, Yashima T, et al. 2004. Diesel particulate matter and NOx removals using a pulsed corona surface discharge[J]. AIChE Journal, 50(3) : 715–721. DOI:10.1002/(ISSN)1547-5905 |
| [${referVo.labelOrder}] | Ye D, Gao D, Yu G, et al. 2005. An investigation of the treatment of particulate matter from gasoline engine exhaust using non-thermal plasma[J]. Journal of Hazardous Materials, 127(1/3) : 149–155. |
| [${referVo.labelOrder}] | Zhang M, Fu ML, Wu J L, et al. 2011. Characteristic of surface oxygen species and catalytic property on MnOx-CeO2 for soot combustion[J]. Journal of the Chinese Rare Earth Society, 29(3) : 303–309. |
| [${referVo.labelOrder}] | Zhang Z, Han D, Wei S, et al. 2010. Determination of active site densities and mechanisms for soot combustion with O2 on Fe-doped CeO2 mixed oxides[J]. Journal of Catalysis, 276(1) : 16–23. DOI:10.1016/j.jcat.2010.08.017 |
 2017, Vol. 37
2017, Vol. 37


