2. 华南理工大学环境与能源学院, 广州 510006;
3. 华南理工大学亚热带建筑科学国家重点实验室, 广州 510640
2. School of Environment and Energy, South China University of Technology, Guangzhou 510006;
3. State Key Laboratory of Subtropical Building Science, South China University of Technology, Guangzhou 510640
Fe3O4作为一种尖晶石铁氧体,具有良好的磁性和生物相容性,被认为是理想的生物应用材料,亦被应用于给水污水处理领域(Deng et al., 2005).目前Fe3O4磁性纳米颗粒的合成方法有很多,其中比较常见的有化学共沉淀法、微乳液合成法(Jian et al., 2011)、水热合成法(Deng et al., 2005;Liu et al., 2009)和热分解法(Jana et al., 2004).近年来有关Fe3O4功能化改性的研究工作中,较多采用原位化学共沉淀法对Fe3O4进行同步制备及改性,但因调控因素多且较繁琐,往往得到的Fe3O4纳米颗粒不符合功能化的应用要求.而由水热法先制得Fe3O4后加以改性的相对较少,此方法调控因素少,得到的磁性纳米颗粒具有粒径小、尺寸均一、晶体结构完整、饱和磁化强度高等特点(褚四敏,2014),所以本研究采用非原位共沉法制备Fe3O4并进行改性.
磁性纳米颗粒作为一种吸附剂,虽然可利用外界磁场迅速分离,但吸附性能较差.为弥补这一缺陷,通常采用表面活性剂或高分子聚合物对其进行表面改性,增加其功能性基团,从而增强磁性纳米颗粒的吸附能力(Mahmoodi, 2015).多糖类物质具有价廉易得,生物相容性好,易于降解等特点,并且因含有多种功能性基团(如羟基、氨基、羧基等),使其容易被修饰,其中,β-环糊精(β-cyclodextrin /β-CD)因其分子内包含丰富的伯、仲羟基,可和具有双官能团或多官能团的化合物发生聚合反应,其内疏水、环外亲水的桶状结构,能与多种客体化合物形成超分子包合物(Zhang et al., 2014;周志武,2012;Huang et al., 2013).壳聚糖是甲壳素的部分脱乙酰基化产物,是自然界存在的唯一带阳离子的多糖,属氨基多糖天然高分子聚合物,具复杂的双螺旋结构,链上包含有许多羟基、氨基,N-乙酰基等官能基团(Reddy et al., 2013;范露露,2013;肖玲等,2012),因此选择这两种多糖类物质对Fe3O4纳米材料进行改性.
腐殖质是一种呈棕黑色或棕褐色、无定形、酸性、亲水、多分散的天然高分子有机质(NOM)(郑可等,2012),根据溶解性可分为腐殖酸(HA,只溶于碱不溶于酸)、富里酸(FA,既溶于酸又溶于碱)和胡敏素(酸碱都不溶)(李会杰,2012),其中FA含量超过70%,且不可生物降解.FA的主要官能团有羧基(-COOH)、酚羟基(C6H6O-)、羰基及醌类物质等(Oriekhova et al., 2016;Yang et al., 2016).富里酸普遍存在水体中,且在垃圾渗滤液中含量极高.富里酸难生化降解且危害较大:能够在消毒过程中和含氯消毒剂反应生成消毒副产物DPBS和三卤甲烷类致癌物质THMS;并且还能与重金属离子络合,增强其生物毒性;此外,富里酸还是引起水体色度的重要物质(Makunina et al., 2015;Yan et al., 2016).因此,寻找一种有效去除水体中溶解性富里酸的技术显得极其重要.
β-CD交联壳聚糖磁性纳米粒子一般通过羧甲基、丁二酰基或顺丁烯二酰基以共价键结合的方式制备CS-β-CD(Binello et al., 2004),再通过原位共沉合成CS-β-CD MNPs,虽有较好处理效果,但制备过程繁琐,周期较长,且一般用于药物输送(Ding et al., 2015)、吸附重金属离子(Badruddoza et al., 2013)及染料(Fan et al., 2012),很少有用于处理富里酸的报道,所以本研究采用简易方法以非共价键结合的方式制备β-CD@CS MNPs,并用于富里酸的去除,经β-CD和壳聚糖改性的磁性纳米颗粒β-CD@CS MNPs,既具有良好的吸附作用,在外界磁场作用下,也能快速富集分离,达到对富里酸的有效去除.本文主要研究了β-CD@CS MNPs对富里酸的吸附特性,探究pH、温度、初始浓度、反应时间对吸附性能的影响,分析吸附机理,为其在实际水体中去除富里酸的应用提供理论基础.
2 材料与方法(Materials and methods) 2.1 材料与仪器材料:β-CD,相对分子质量1134.98,纯度99%;壳聚糖,高粘度(>400 mPa.s),FeSO4,Na2S2O3·5H2O,NaOH,28%浓氨水,环氧氯丙烷,均采自阿拉丁.
仪器:紫外分光光度计,UV-2800A,上海Unico;Merlin扫描电镜,德国蔡司公司;CCR-1傅里叶红外光谱,美国尼高力公司;Empyrean锐影X射线衍射仪,荷兰帕纳科公司;pH计,pHS-25C,上海精科.
2.2 合成方法 2.2.1 Fe3O4纳米颗粒(MNPs)的合成Fe3O4纳米颗粒的合成采用水热法,使1.39 g(0.005 mol)FeSO4和1.24 g(0.005 mol)Na2S2O3·5H2O溶于14 mL蒸馏水,将所得混合液置于50 mL反应釜内,用滴定管滴加10 mL(1.0 mol·L-1)NaOH于釜内,同时不断搅拌以形成黑色胶状介质,随后将反应釜置于140 ℃保持12 h,再取出冷却至室温,所得灰黑色沉淀过滤收集,并用温蒸馏水和无水乙醇洗涤数次,再置于70 ℃真空干燥4 h(Fan et al., 2001).
2.2.2 β-CD@CS MNPs的合成0.15 g壳聚糖溶于100 mL 0.5%(V/V)醋酸溶液,使0.1 g Fe3O4和1.1 g β-CD溶于60 mL蒸馏水,所得混合液超声2 h后置于三角烧瓶中1000 r·min-1 45 ℃搅拌12 h,随后,将乙醇/壳聚糖溶液(1/1,V/V,40 mL)逐滴加入Fe3O4/β-CD溶液,所得混合液45 ℃持续搅拌1 h,以提供足够的时间和合适的条件供β-CD和壳聚糖水解鳌合铁,覆盖于Fe3O4纳米颗粒表面,之后,将5 mL 28%的浓氨水逐滴加入反应体系,30 min后,加入6 mL环氧氯丙烷,所得混合液800 r·min-1 70 ℃搅拌3 h,最终产物由永磁铁分离收集,并用去离子水和无水乙醇洗涤数次,50 ℃真空干燥12 h.
2.3 富里酸(FA)来源及贮备液的配制本实验采用的富里酸(Fulvic acid, FA)采自阿拉丁,含量≥90%,在较大的pH范围内可溶( Oriekhova O, 2016).称取800 mg的富里酸固体粉末溶于中性的去离子水中,将所得溶液稀释至1000 mL制得800 mg·L-1的富里酸储备液,再用锡箔纸将容量瓶包紧并置于冰箱中冷藏保存.实验过程中所用的富里酸溶液首先用蒸馏水稀释到所需浓度,再用0.45 μm微孔滤膜过滤.
2.4 吸附试验取100 mL已知浓度的富里酸溶液于250 mL三角瓶中,加入50 mg β-CD@CS MNPs吸附剂后置于200 r·min-1、(25±0.2) ℃条件下的恒温气浴摇床中振荡,按预定的时间取样,磁场分离,取上层清夜,本试验采用UV254表征富里酸的相对含量(Wang et al., 2008;张月等,2015;Wang et al., 2006),UV254采用紫外可见分光光度计测定,采用1 mol·L-1 盐酸、1 mol·L-1 NaOH溶液调节pH,同时以0.01 mol·L-1盐酸和0.01 mol·L-1 NaOH溶液辅助调节,pH采用酸碱度计测定.计算吸附量Qe(mg·g-1)和去除率E公式如下:

|
(1) |

|
(2) |
式中:C0和Ce分别为吸附前和吸附达到平衡后上清液中富里酸的质量浓度(mg·L-1);V为吸附溶液的体积(L);M为吸附剂的质量(g)(张莉祥等,2015).
2.5 脱附再生试验为探究β-CD@CS MNPs的再生和可重用性,取200 mL 100 mg·L-1的富里酸溶液于250 mL三角瓶中,加入100 mg β-CD@CS MNPs吸附剂后置于200 r·min-1、(25±0.2) ℃条件下的恒温气浴摇床中振荡,达到吸附平衡后,在外加磁性导向下进行分离,收集吸附饱和的β-CD@CS MNPs吸附剂.向收集的吸附饱和的β-CD@CS MNPs吸附剂中加入100 mL 0.01 mol·L-1 NaOH溶液,再置于(25±0.2) ℃、200 r·min-1条件下的恒温气浴摇床中振荡12 h,在外加磁性导向下进行分离,使用0.45 μm醋酸纤维滤膜取上清液,测FA吸光度.再用蒸馏水对吸附剂进行洗涤,直至洗涤所得上清液中FA相对含量为零后停止洗涤,在吸附剂中重新加入200 mL 100 mg·L-1 FA溶液,吸附后再进行脱附.
3 结果与讨论(Results and discussion) 3.1 吸附剂的表征 3.1.1 FTIR表征MNPs、β-CD MNPs和β-CD@CS MNPs的FTIR分析如图 1所示.由图可知,在565 cm-1处,由于磁性Fe-O键的作用,这3种材料都具有明显的特征吸收峰,说明磁性纳米颗粒Fe3O4已成功嵌入所制备的改性磁性吸附剂中.对于MNPs的红外谱图,在3431 cm-1处出现特征峰是由于Fe3O4表面以氢键结合的-OH的伸缩振动,在1628 cm-1左右出现特征峰可能的原因是MNPs存在水分子的弯曲振动(Yao et al., 2014).对于β-CD MNPs的红外谱图,与MNPs相比,明显差异为在1024 cm-1及1148 cm-1处出现明显吸收峰,对应于C-O-C非对称糖苷键振动吸收峰以及C-C/C-O耦合伸缩振动吸收峰,另外,在1025~1148 cm-1内出现伯仲羟基伸缩振动峰,而MNPs表面的-OH的伸缩振动在β-CD MNPs红外图谱中有了细微的变化,由3431 cm-1移向3425 cm-1,可能是由于β-CD的-OH及自身形成氢键,根据上述可得到β-CD已成功覆于Fe3O4颗粒表面.对于β-CD@CS MNPs的红外谱图,β-CD MNPs的所有特征吸收峰均可见,除此以外,最大区别则是1628 cm-1处特征峰强度明显增大,这是由于壳聚糖游离氨基的N-H伸缩振动叠加水分子的弯曲振动(Badruddoza et al., 2013),同时3433 cm-1处特征峰也明显变强变宽,这是形成氢键缔合的-OH伸缩振动吸收峰与-NH的伸缩振动吸收峰重叠而增宽的重叠吸收峰,以上说明β-CD@CS MNPs成功合成(Reddy et al., 2013).
 |
| 图 1 MNPs(a)、β-CD MNPs(b)、β-CD@CS MNPs(c)的红外光谱图 Fig. 1 FTIR spectra of MNPs(a)、β-CD MNPs(b)、β-CD@CS MNPs(c) |
图 2为MNPs和吸附前后β-CD@CS MNPs的XRD图,在2θ=30.1°、35.5°、43.3°、53.4°、57.2°和62.5°处,Fe3O4纳米粒子具有明显的特征峰,分别对应反尖晶石型面心立方相(220) 、(331) 、(400) 、(422) 、(511) 和(440) 晶面位置,与Fe3O4晶体的标准XRD数据吻合,说明制备的磁性纳米粒子为立方尖晶石结构.由吸附前β-CD@CS MNPs XRD图可知,壳聚糖和β-CD对磁性纳米粒子进行表面包裹,没有明显改变其晶型结构.而吸附前β-CD@CS MNPs与Fe3O4极度相似的XRD图可初步确定磁性Fe3O4纳米颗粒已成功嵌入所制备的改性磁性吸附剂中.另外,由吸附后β-CD@CS MNPs XRD图可知,β-CD@CS MNPs对FA的吸附,也没有明显的改变其晶型结构.
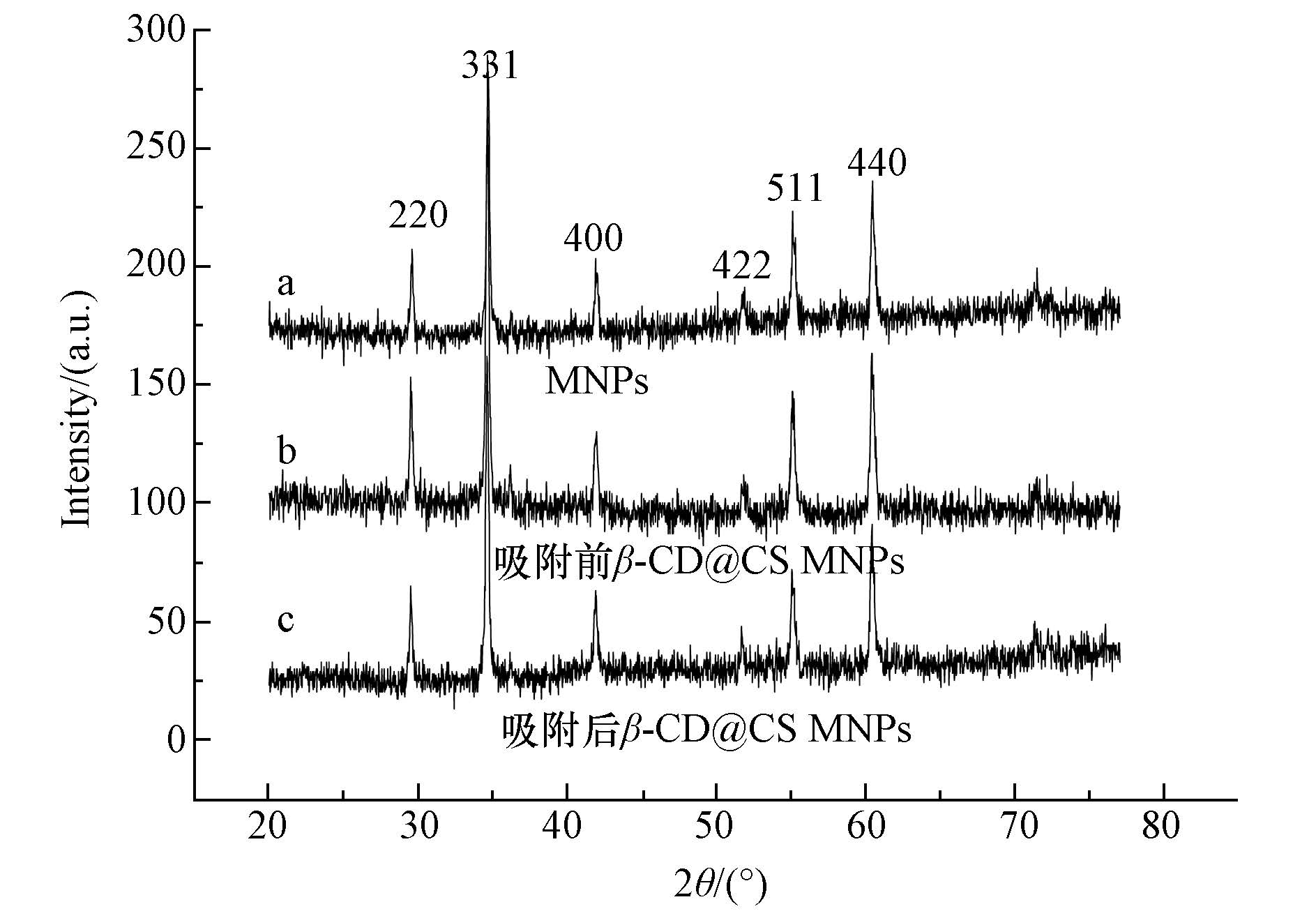 |
| 图 2 MNPs(a)、吸附前β-CD@CS MNPs(b)、吸附后β-CD@CS MNPs(c)的 XRD谱图 Fig. 2 XRD patterns of MNPs (a) β-CD@CS MNPs before adsorption(b) and β-CD@CS MNPs after adsorption(c) |
MNPs及β-CD@CS MNPs的扫描电镜(SEM)和β-CD@CS MNPs的透射电镜(TEM)分析如图 3所示.由图 3a可知,从整体上看,颗粒形状为类球形,粒径分布较窄.有文献提及,球形分子聚合物具有大的表面积,这表明在水溶液中β-CD@CS MNPs表面可能具有较多的有效位点,用于与FA结合(Fan et al., 2012).由图 3b可看到,β-CD@CS MNPs大致为核-壳结构,深色Fe3O4外表面被一层浅色的物质包裹,由图 3c可看到,β-CD@CS MNPs平均粒径约为(52±3) nm,直径略微大于MNPs,这是由于壳聚糖及β-CD聚合物包覆于Fe3O4颗粒表面.MNPs及β-CD@CS MNPs的SEM图像可说明壳核结构β-CD@CS功能化磁性纳米粒子制备成功.同时,制备颗粒显示出一定的团聚,这可能是由于其粒径小以及表面能和表面活性较高,复合纳米粒子很容易相互吸引,以形成一个稳定状态(Ding et al., 2015).
 |
| 图 3 MNPs的SEM(a),β-CD@CS MNPs的SEM(b)和β-CD@CS MNPs的TEM(c) Fig. 3 The SEM micrographs of MNPs (a) and β-CD@CS MNPs(b) and the TEM micrographs of β-CD@CS MNPs(c) |
吸附剂磁性的强弱是决定其磁性分离效果好坏的重要指标.图 4为β-CD@CS MNPs在室温条件下的磁滞曲线.由包覆前后两种纳米材料的磁滞曲线可以看出,MNPs和β-CD@CS MNPs的矫顽力和剩余磁化强度都接近于零,无磁滞现象,这表明两种磁性纳米材料具有超顺磁性,且Fe3O4和β-CD@CS MNPs的饱和磁化强度分别为72、62 emu·g-1.在β-CD和壳聚糖包覆于Fe3O4后,纳米粒子的饱和磁性强度值有一定的减少,这可能是壳聚糖及β-CD聚合物均匀覆盖于磁性纳米粒子表面,降低了表面淬火,从而减小了颗粒的磁矩.任何晶体,由于表面原子显著增加而表面层紊乱,会引起饱和磁化强度的降低(Ding et al., 2015).处于均匀分散溶液中的β-CD@CS MNPs纳米粒子在外加磁场作用下1.5 min后能完全分离开,当外加磁场撤除后,β-CD@CS MNPs经过轻微振动又会再次迅速分散开,这充分保证了吸附剂的净化和分离功能.图 5为β-CD@CS MNPs吸附FA前后磁分离3 min的磁分离效果图.图 5a是未加入β-CD@CS MNPs的FA溶液,图 5b是加入β-CD@CS MNPs后的FA溶液,图 5c是经过外加磁场分离后的FA溶液,由图 5可以看出,β-CD@CS MNPs吸附剂对FA具有良好的吸附效果和磁分离特性.
 |
| 图 4 MNPs(a)、β-CD@CS MNPs(b)的磁滞回线 Fig. 4 Magnetic hysteresis loops of MNPs(a) and β-CD@CS MNPs(b) |
 |
| 图 5 β-CD@CS MNPs的磁性分离效果图 Fig. 5 Vision of β-CD@CS MNPs on magnetic separation |
Zeta电位是衡量粒子间排斥力或吸引力的重要指标,图 6为吸附FA前后β-CD@CS MNPs的Zeta电位与pH的关系图.由图 6可以看出,在吸附FA前,pH在3~6的范围内,β-CD@CS MNPs的Zeta电位均为正值,这是壳聚糖上的氨基基团嫁接到Fe3O4上,氨基质子化的缘故.随着pH的增加,β-CD@CS MNPs的Zeta电位不断降低,由31.5 mV变化至-35.47 mV,这是由于在碱性条件下,当pH很高时,β-CD@CS MNPs吸附剂表面的功能性基团可能会接触到溶液中的OH-离子,导致吸附剂表面的聚合物呈负电(Yao et al., 2014),因此在pH为7~11的范围内,β-CD@CS MNPs的Zeta
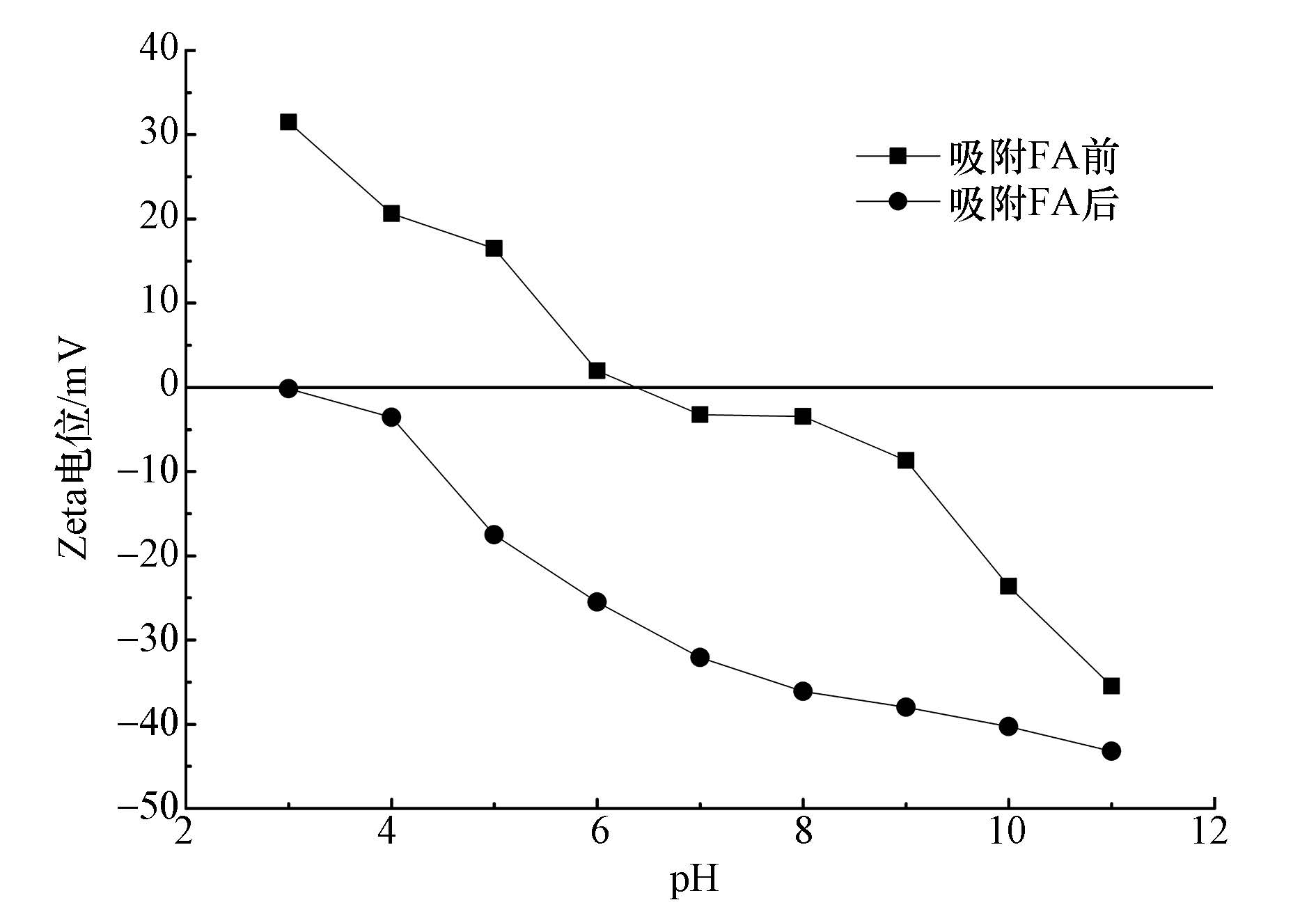 |
| 图 6 pH对β-CD@CS MNPs Zeta电位的影响 Fig. 6 Effect of pH on Zeta potential of β-CD@CS MNPs |
电位均为负值,由图中可以看出,β-CD@CS MNPs的Zeta电位随pH值变化明显,而在吸附FA后,pH在3~11的范围内均为负值,其变化范围由-0.16 mV至-43.2 mV,这主要是由于FA含酸性官能团较多,在溶液中去质子化后呈负电,当β-CD@CS MNPs对FA的吸附达到饱和后,β-CD@CS MNPs的Zeta电位明显降低(Ding et al., 2015),这表明β-CD@CS MNPs对FA的吸附可能受静电吸附机制影响较大.
3.2 pH对吸附性能的影响pH是水溶液中决定β-CD@CS MNPs对FA吸附量的重要参数,在25 ℃,初始浓度为50 mg·L-1时,pH在4~10的范围内对β-CD@CS MNPs吸附FA的影响如图 7所示.从图中可以看出,溶液pH的变化对吸附过程产生了较大影响,并且pH在 4~6内,β-CD@CS MNPs对FA的吸附量较高,这是由于溶液中存在较多的质子促进β-CD@CS MNPs吸附剂表面壳聚糖的氨基质子化,壳聚糖的pKa为6.0~7.0,使得吸附剂带正电(Zhu et al., 2010),而FA在酸性条件下,部分或完全未解离,呈电中性,在碱性条件下,由于羧基和酚羟基的去质子化作用,使得溶液中的FA分子呈负电性,因此增强了β-CD@CS MNPs与FA间的静电作用(Wang et al., 2008).当pH不断增大时,过多的OH-离子可能会与带负电的FA竞争,从而导致β-CD@CS MNPs对FA的吸附量明显降低.
与此同时,在pH较低时,FA大分子呈部分或完全的未解离形式,FA结构变得更为疏水(Zhang et al., 2016),因此更容易吸附于β-CD@CS MNPs表面.在pH较高时,FA呈部分或完全解离形式,分子间与分子内的静电排斥凸显,FA结构疏水性减
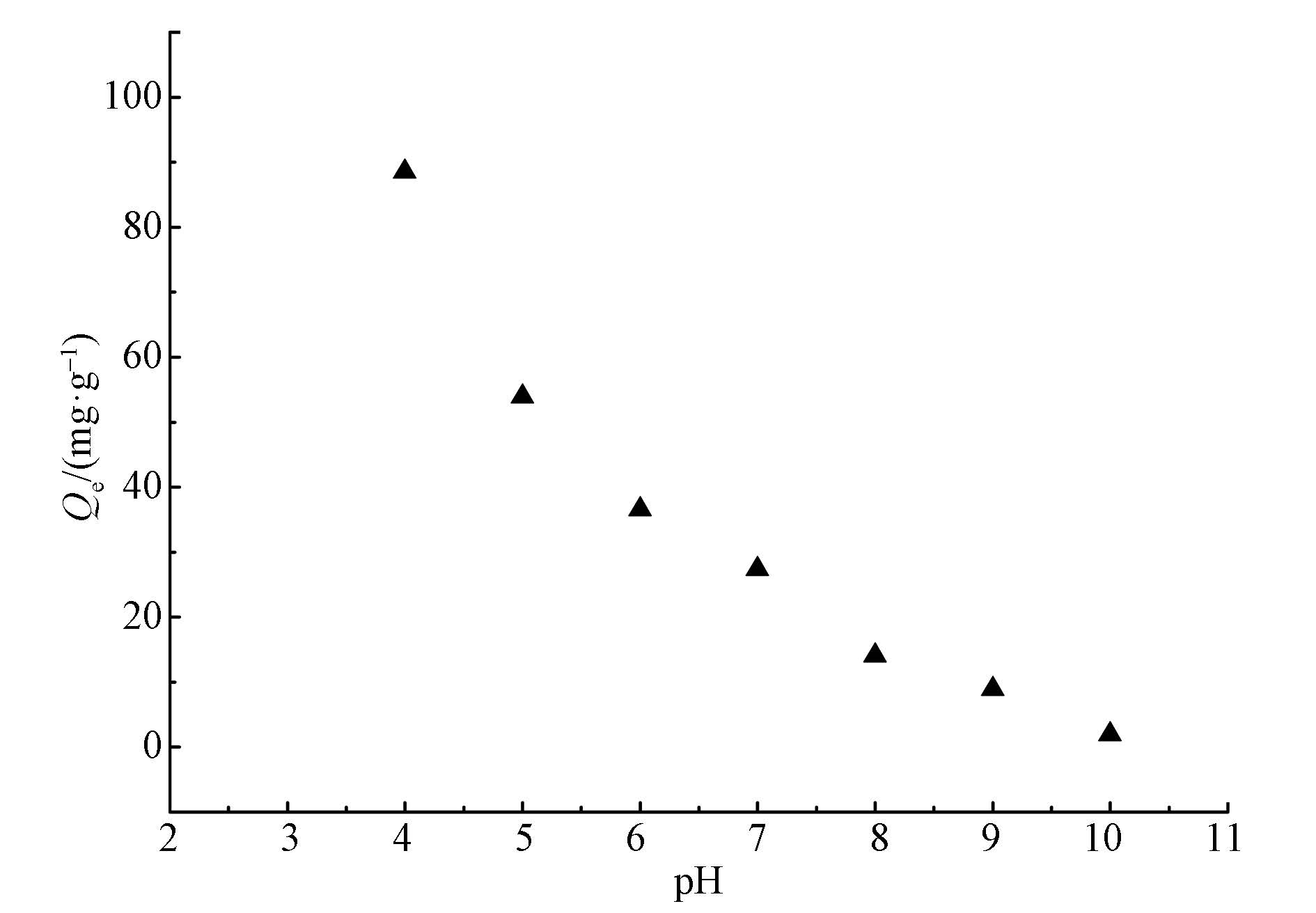 |
| 图 7 溶液pH值对β-CD@CS MNPs去除FA的影响 Fig. 7 Effect of solution pH on β-CD@CS MNPs remove FA |
弱,解离的FA大分子呈环面或环状结构,这也导致了β-CD@CS MNPs对FA吸附量的减少.通过测得吸附前后初始pH与最终pH发现,当初始pH为3.18时,最终pH为7.12,当初始pH为9.05时,最终pH为7.25,表明吸附后溶液pH在酸性条件下增大,在碱性条件下减小,这可能是由于氨基在酸性和碱性条件下不断质子化和去质子化过程所导致的(Wang et al., 2006).
3.3 吸附剂含量对吸附性能的影响在25 ℃、pH=7,初始浓度为100 mg·L-1时,不同吸附剂含量(10、20、30、40、50、60、80 mg)对β-CD@CS MNPs吸附FA的影响如图 8所示.随着吸附剂含量的增多,β-CD@CS MNPs对FA的去除率均逐渐增大,主要是因为吸附剂吸附面的增多,提供了更多可利用的吸附位点与FA结合,但吸附剂对FA的吸附量逐渐减小,这可能是因为吸附位点的重合或团聚,造成可吸附FA的总表面积减少以及扩散路径长度的增加,阻碍了FA分子到达β-CD@CS MNPs表面的有效吸附位点.
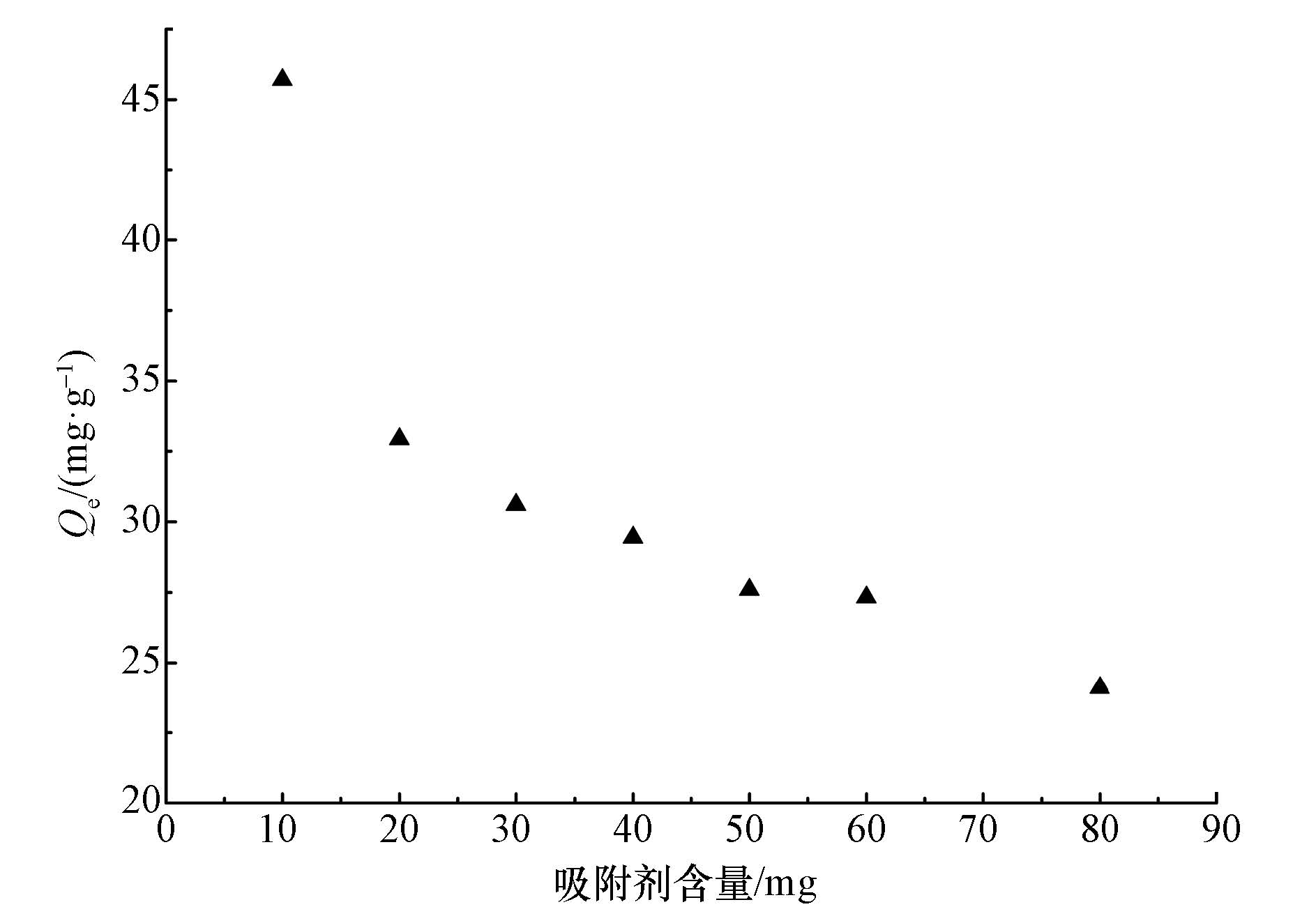 |
| 图 8 吸附剂含量对β-CD@CS MNPs去除FA的影响 Fig. 8 Effect of absorbent content on β-CD@CS MNPs remove FA |
吸附等温线通常用来确定在恒定温度下吸附质浓度和积累到吸附剂表面的具体关系,对优化吸附剂的使用具有重要作用(Huang et al., 2013).图 9显示了在初始pH为7.0左右时,不同温度(15、25和35 ℃)下β-CD@CS MNPs对FA的吸附等温线.由图可知,随着温度的升高,β-CD@CS MNPs对FA的吸附量逐渐增大,并逐渐达到饱和.β-CD@CS MNPs对FA的最大吸附量分别为40.06、51.35、66.01 mg·g-1.由此可知,β-CD@CS MNPs对FA的吸附为吸热反应.吸附通常可被看做物质在两相界面的积累,在吸附剂含量保持一定的基础上,吸附剂对FA的吸附量逐渐增大,这主要是由于随着初始浓度的增大,浓度梯度所带来的驱动力更强,FA分子可更快到达吸附剂表面(Yao et al., 2014).
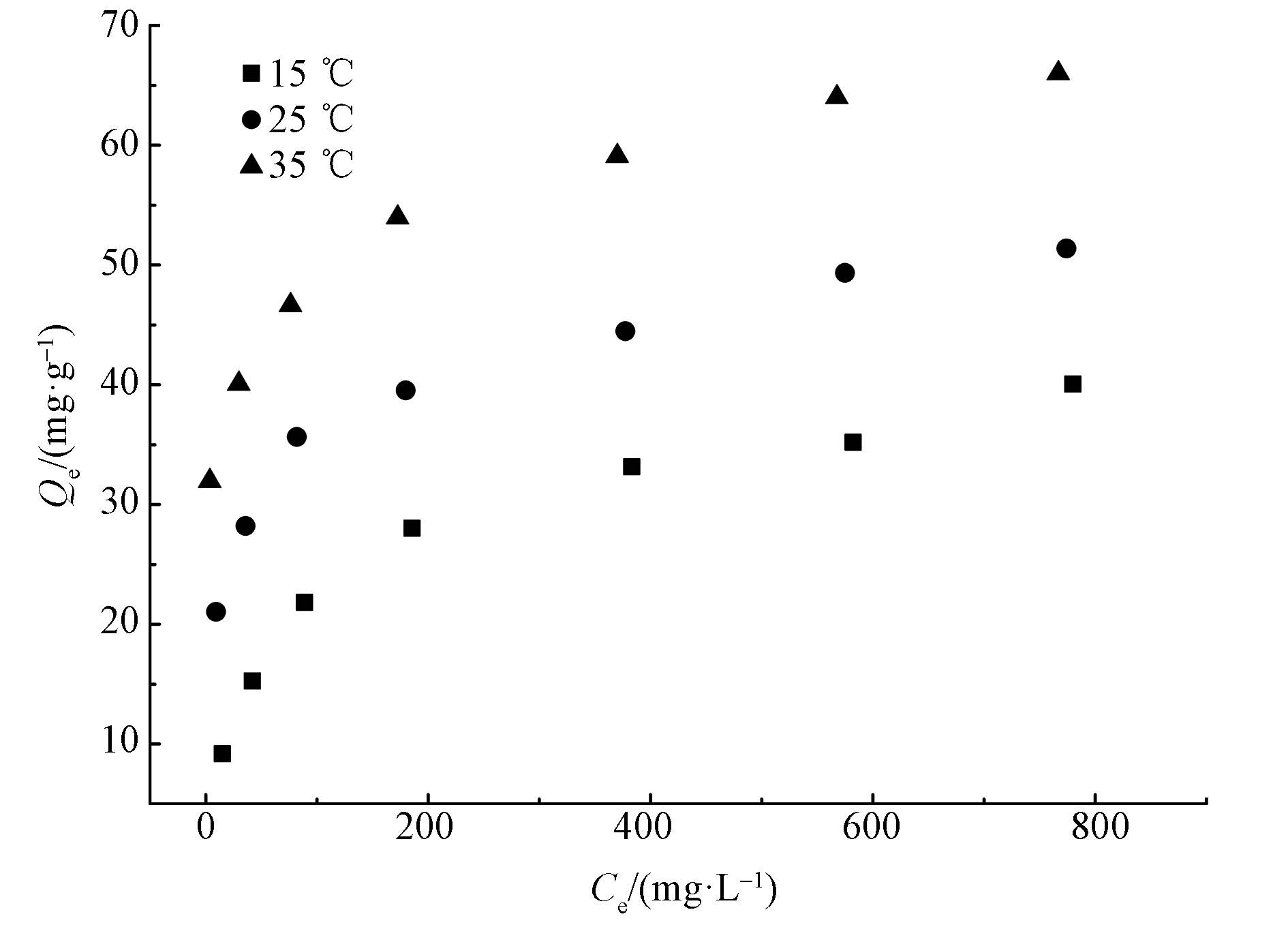 |
| 图 9 不同温度下β-CD@CS MNPs对FA的吸附等温线 Fig. 9 Adsorption isotherm of FA on β-CD@CS MNPs at 15, 25 and 35℃ |
本文通过等温线模型来探究β-CD@CS MNPs对FA的吸附机制,选择2种主要的等温线模型,即Langmuir模型和Freundlich模型进行模拟,并且以拟合直线的线性相关系数R2作为拟合程度是否理想的依据(柳欢欢等,2009).
Langmuir模型为广泛应用的吸附等温线模型,该模型假定每个分子的吸附能是相同的,吸附发生在吸附位点有限的均质表面,吸附层为单层,一旦有分子占据一个位点,就不能再进行吸附,可用如下公式表示:
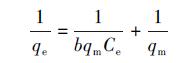
|
(3) |
式中:qe为平衡吸附量(mg·g-1);Ce为平衡浓度(mg·L-1);qm为理论最大吸附量(mg·g-1);b为吸附平衡常数(1·mg-1),与结合位点的亲和力有关.以Ce为x轴,Ce/qe为y轴得到一条直线,斜率代表 1/qm,截距代表 1/bqm,如图 10a所示.
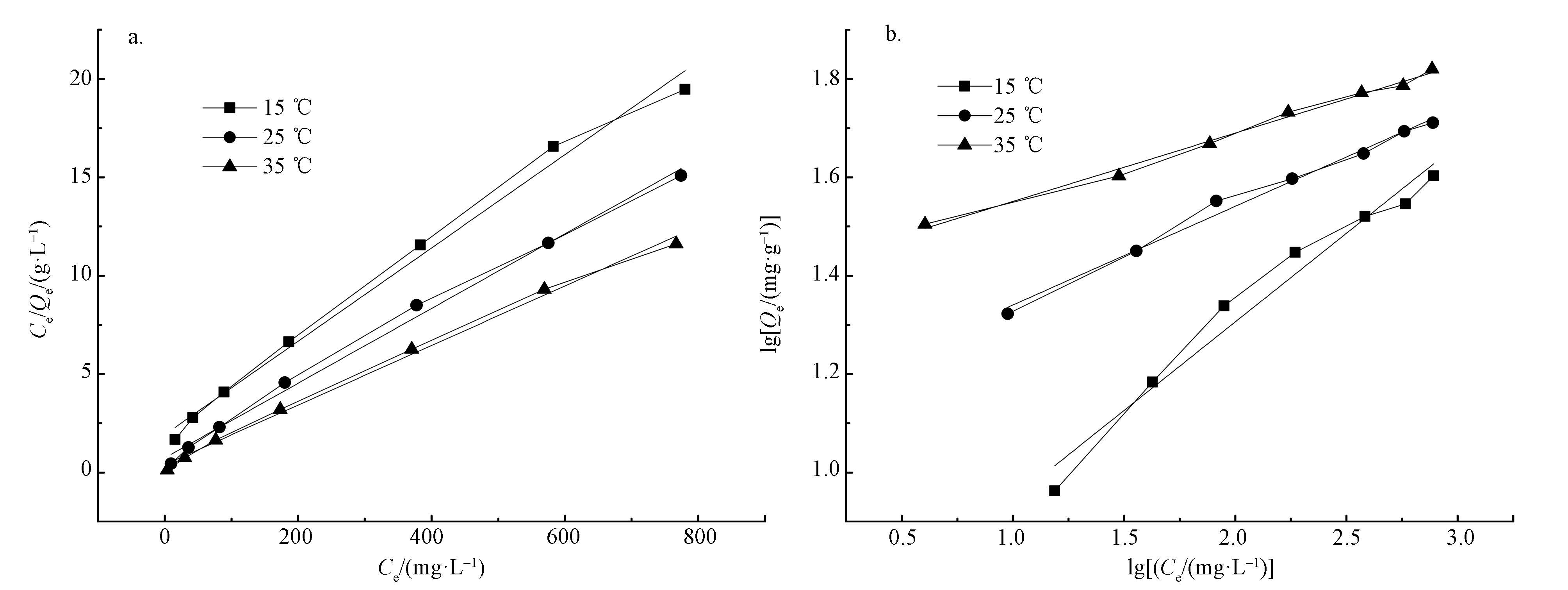 |
| 图 10 不同温度下富里酸的Langmuir(a)和Freundlich(b)线性拟合曲线 Fig. 10 The Langmuir(a) and Freundlich(b) linear fitting curve of FA at different temperatures |
| 表 1 不同温度下β-CD@CS MNPs去除FA的吸附等温线拟合参数 Table 1 Langmuir and Freundlich model parameters for β-CD@CS MNPs remove FA at 15, 25 and 35 ℃ |
Freundlich模型被广泛应用于描述非均质表面的吸附可逆性,以及多层吸附,该模型假定吸附量是所有吸附位点吸附的总和,强的结合位点首先被占据,吸附过程完成后,吸附能迅速降低.可用如下公式表示:
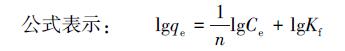
|
(4) |
式中:qe为平衡吸附量(mg·g-1);Ce为平衡浓度(mg·L-1);Kf为特征常数;n为经验常数.以lgCe为x轴,lgqe为y轴得到一条直线,斜率代表 1/n,截距代表lgKf,如图 10 b所示.
在15、25、35 ℃条件下,pH为7.0左右,实验测定了β-CD@CS MNPs对不同初始浓度FA溶液的吸附量,并分别用Langmuir和Freundlich等温线方程对数据进行拟合,吸附等温线拟合参数见表 1.
由表 1可以看出Langmuir方程拟合可决系数R2均高于Freundlich方程拟合可决系数,并且Langmuir方程的理论最大平衡吸附量更接近于实验结果,这说明在整个浓度范围内,β-CD@CS MNPs对FA的吸附行为符合Langmuir等温吸附模型.由常数b和n变化可知,β-CD@CS MNPs对FA的吸附为单层吸附,且吸附过程发生在均质表面的具体吸附位点(Mahmoodi et al., 2015),这可能是因为FA结构比较复杂.
3.5 吸附动力学动力学模型是探究吸附机理的重要方法,在25 ℃,pH=7.0±0.1,不同初始浓度(10、20和50 mg·L-1)条件下,β-CD@CS MNPs去除FA的吸附动力学曲线如图 11所示,β-CD@CS MNPs对FA的吸附量随着FA初始浓度的增加而增大,在吸附的前80 min,曲线呈单调趋势,陡峭上升,而后趋于平缓,在600 min基本达到平衡,吸附剂达到最大吸附量,达到吸附平衡时,pH并无明显变化(pH分别为7.12、7.25、7.33) .在初始阶段,吸附剂表面是相对自由的,传质阻力小,FA浓度高,而吸附动力学则可看成FA分子从溶液到吸附剂表面的传质工具,当FA分子到达吸附剂表面时,可立即与表面质子化的氨基结合,大量空置的表面吸附位点被FA分子占据(Wang et al., 2008).当超过初始阶段,吸附量的增加变得缓慢,吸附剂表面吸附一定量FA分子后,后续到达的FA分子需先经过分子内扩散才可与吸附剂表面质子化的氨基-NH+3结合,同时,传入的FA分子与吸附的FA分子也因同带负电而产生静电排斥作用(Wan et al., 2015),从而进一步减缓吸附速率.
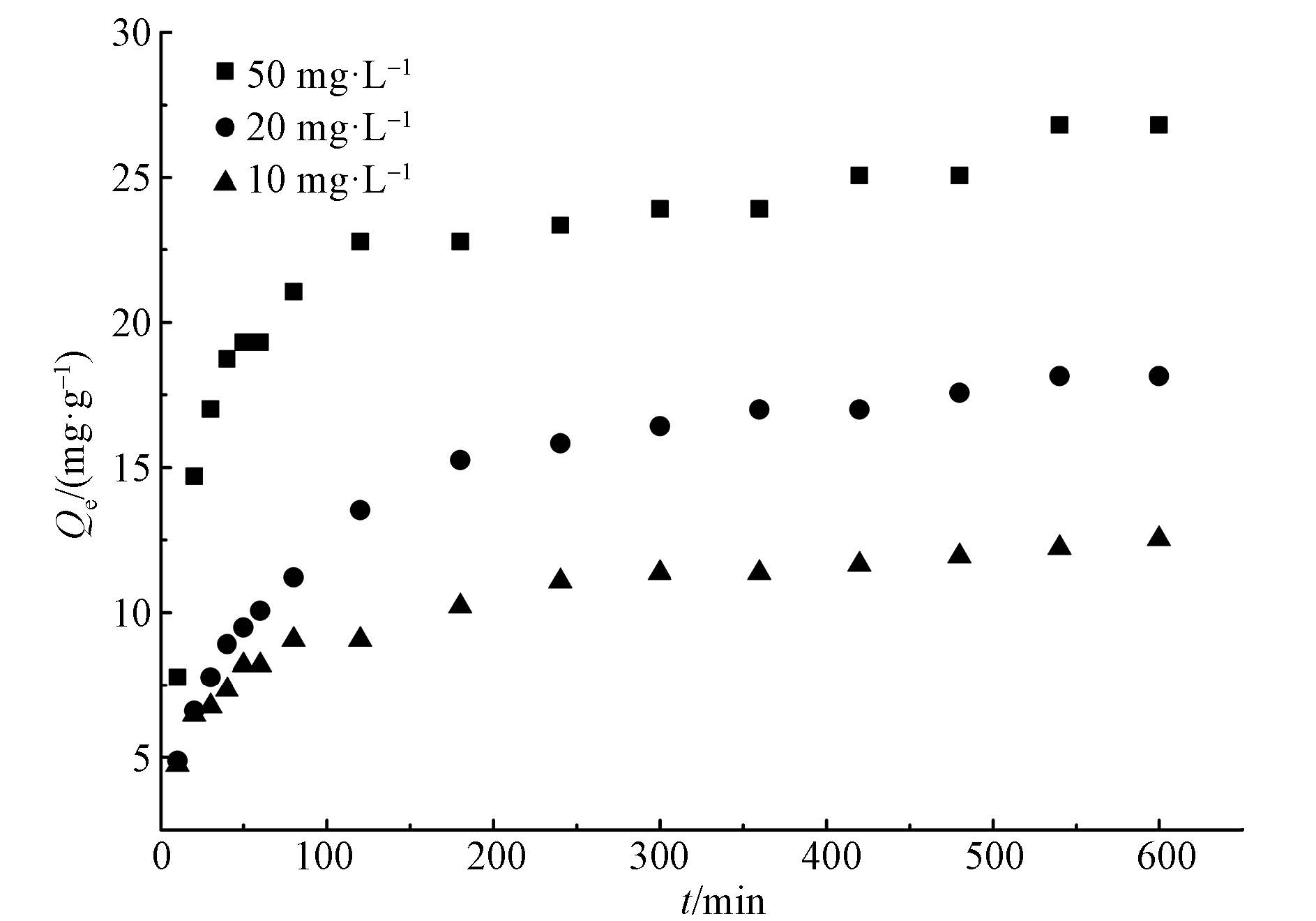 |
| 图 11 不同FA初始浓度下β-CD@CS MNPs去除FA的吸附动力学 Fig. 11 Adsorption kinetics of β-CD@CS MNPs remove FA at initial concentration of 10, 20 and 50 mg·L-1 |
为进一步说明β-CD@CS MNPs对FA的吸附动力学过程,对吸附动力学方程实验数据分别进行了拟一级动力学方程和拟二级动力学方程的拟合.
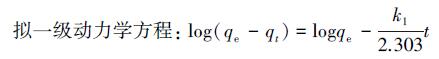
|
(5) |
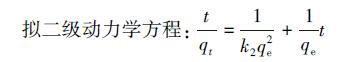
|
(6) |
式中:t为吸附时间(min);qe为平衡吸附量(mg·g-1);qt为t时刻的吸附量(mg·g-1);k1为拟一级动力学方程常数(g·mg·min-1);k2为拟二级动力学方程常数(g·mg-1·min-1).以t为x轴,log(qe-qt)为y轴得到一条直线,斜率为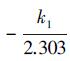
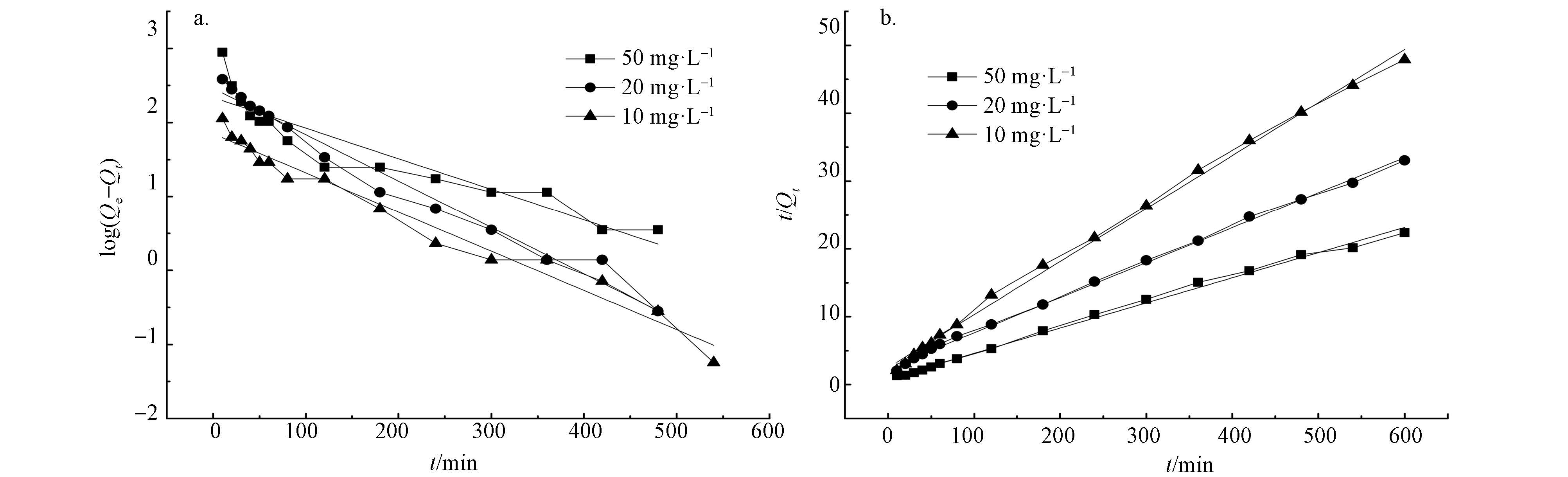 |
| 图 12 不同浓度下富里酸的一级(a)和二级(b)动力学线性拟合曲线 Fig. 12 The pseudo-first-order (a) and pseudo-second-order(b) fitting curve of FA at 10, 20 and 50 mg·L-1 |
利用拟一级动力学方程和拟二级动力学方程对β-CD@CS MNPs吸附FA进行拟合,拟合参数见表 2.
由表 2可以看出,拟二级动力学相关系数R2均高于拟一级动力学相关系数,而且拟二级动力学方程计算的最大理论吸附量比拟一级动力学方程的更接近实验实测值,因此可以说明拟二级动力学方程能更好的模拟β-CD@CS MNPs吸附FA的实验动力学.
| 表 2 不同浓度下β-CD@CS MNPs去除FA的拟一级、拟二级动力学参数 Table 2 The fitting parameters of β-CD@CS MNPs remove FA based on The pseudo-first-order and pseudo-second-order kinetics models at 10, 20 and 50 mg·L-1 |
为探究β-CD@CS MNPs的再生和可重用性,采用0.01 mol·L-1 NaOH溶液对吸附饱和的β-CD@CS MNPs进行了5次吸附和脱附再生实验.再生吸附中,吸附剂对FA的吸附量如图 13所示,可以看到,吸附剂对FA的吸附量为26.5~31.3 mg·g-1,且基本保持稳定.这说明再生的β-CD@CS MNPs吸附剂仍具有较好的吸附特性,材料具有良好的循环再生性.而在碱性条件下脱附的机理可能是吸附剂表面的-NH+3去质子化后形成-NH2,与带负电的FA间的静电作用减弱.同时-NH2形成氢键的趋势较小,使得氢键键能减弱(Yao et al., 2014),这有助于β-CD@CS MNPs的脱附再生.
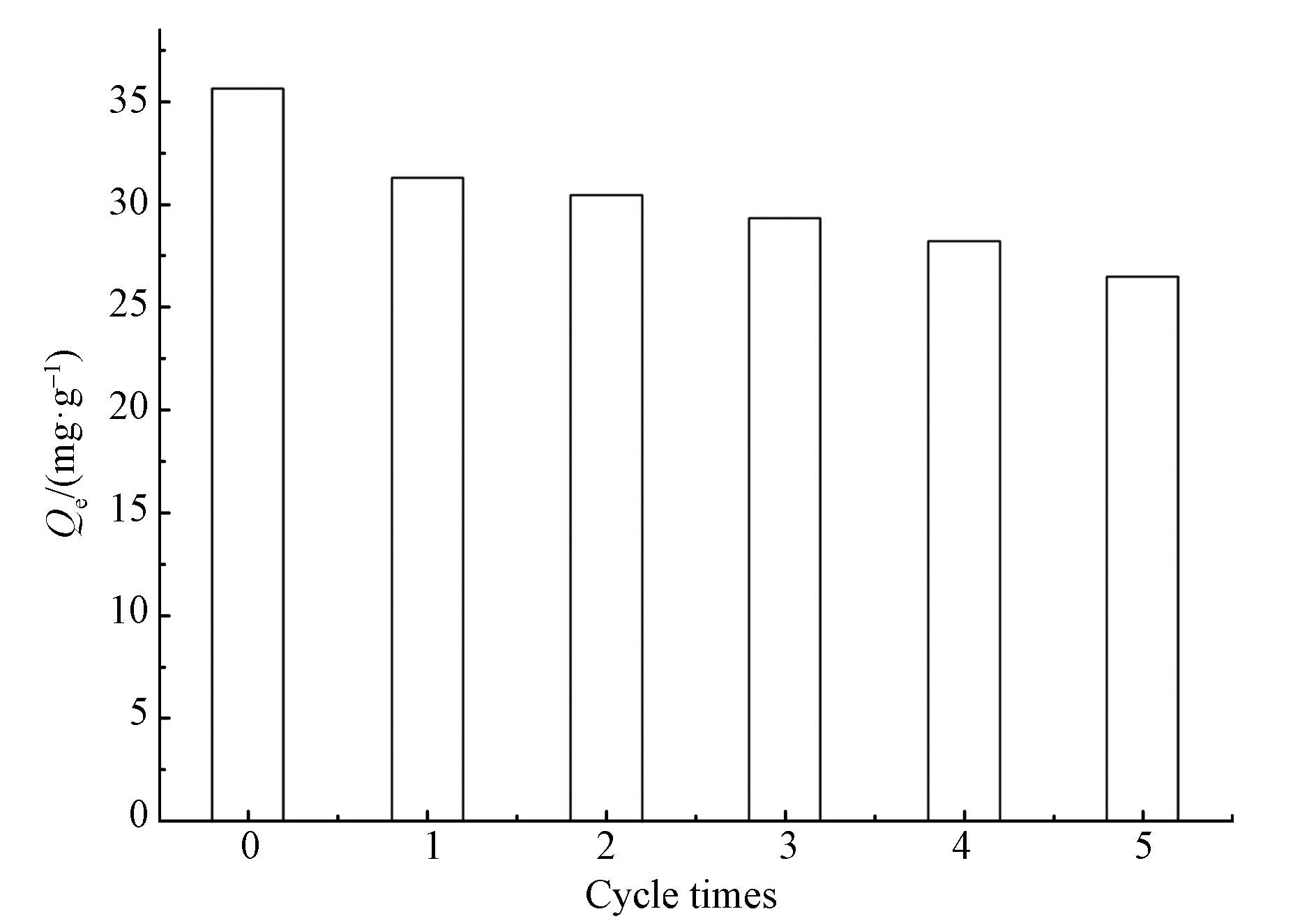 |
| 图 13 β-CD@CS MNPs和再生吸附剂对FA的吸附 Fig. 13 Adsorption amount of FA on absorbed and regenerated β-CD@CS MNPs |
另外,β-CD@CS MNPs在25 ℃对富里酸的实际吸附量为51.35 mg·g-1,商用活性炭在25 ℃对腐殖质的吸附量是6.9 mg·g-1(Ferro-Garcia et al., 1998),碳纳米管在25 ℃对FA的吸附量约为21.5 mg·g-1(Wang et al., 2007),天然沸石对腐殖质的吸附量是8.5 mg·g-1(Capasso et al., 2005),经十六烷基三甲基溴化铵改性沸石对FA的吸附量为25 mg·g-1(Wang et al., 2006),经十六烷基三甲胺改性的黏土矿物(蛭石)25 ℃对FA的吸附量为18.6 mg·g-1(Abate et al., 2006),Fe3O4@SiO2-PANI在25 ℃对腐殖质的吸附量是36.5 mg·g-1(毕丽娟,2014),Fe@Fe2O3壳核纳米线在室温下对腐殖质的吸附量是65.1 mg·g-1(Hao et al, .2014) .其中,活性炭因分离再生性较差,很少直接用于腐殖质的去除,多与其他技术联用如高级氧化(Ferro-Garcia et al., 1998;Abouleish et al., 2015),Fe@Fe2O3壳核纳米线因零价铁不稳定,再生性较差,经十六烷基三甲基溴化铵改性沸石由30%(V/V)乙醇溶液洗脱再生1次后吸附量即下降10%,碳纳米管及胺基化磁性吸附剂Fe3O4@SiO2-PANI在5次再生试验中吸附量基本保持稳定,具有较好的再生性(Wang et al., 2007;Wang et al., 2006;毕丽娟,2014),故从吸附性能和再生性角度看,相比其他用于去除FA的常见吸附剂,本文制备材料β-CD@CS MNPs具有较明显优势.而由传统方法制备的β环糊精交联壳聚糖磁性纳米颗粒,因很少直接用于FA的去除,无法从吸附性能和再生性再进行对比,但同为磁性材料,β-CD@CS MNPs具有更高的饱和磁化强度,更易于吸附剂的快速分离(Ding et al., 2015).
4 结论(Conclusions)1) 采用非原位共沉法简易合成β-CD@CS MNPs吸附剂,通过FTIR、XRD、SEM、TEM、VSM、Zeta电位表征手段,得到β-CD@CS MNPs的纳米尺寸为(52±3) nm、且比较均一,晶体结构完整,饱和磁化强度为62 emu·g-1,具有超顺磁性,能在短时间内达到较好的分离效果.
2) 探究了pH、初始浓度和吸附时间对吸附性能的影响,发现β-CD@CS MNPs在酸性条件下对富里酸有更好的去除,吸附实验结果表明β-CD@CS MNPs对富里酸的实际吸附量为51.35 mg·g-1(pH=7.0±0.1,25 ℃),吸附过程在600 min内达到吸附平衡.
3) 由等温线模型拟合结果可知,该吸附剂对富里酸的吸附符合Langmuir等温线模型,是均质表面的单层吸附,且吸附过程是自发的、吸热的.吸附机理涉及静电作用、氢键结合、疏水作用以及因β-CD的疏水空腔与有机污染物的主客体作用而具有的包合作用,实验吸附数据符合拟二级动力学方程.
4) 基于其有效的吸附过程和快速的分离特性,以及良好的循环再生性,该吸附剂是潜在的可用于富里酸去除的环境友好型吸附剂,可用于富里酸含量较低的天然水体,也可试用于富里酸含量较高的垃圾渗滤液生化出水.
| [${referVo.labelOrder}] | Abate G, Santos L B O D, Colombo S M, et al. 2006. Removal of fulvic acid from aqueous media by adsorption onto modified vermiculite[J]. Applied Clay Science, 32(3/4) : 261–270. |
| [${referVo.labelOrder}] | Abouleish M Y Z, Wells M J M. 2015. Trihalomethane formation potential of aquatic and terrestrial fulvic and humic acids:Sorption on activated carbon[J]. Science of the Total Environment, 521 . |
| [${referVo.labelOrder}] | 毕丽娟. 2014. 胺基化磁性纳米吸附剂去除水体中腐殖酸的机理研究[D].西安:陕西科技大学 http://d.wanfangdata.com.cn/Thesis/Y2554545 |
| [${referVo.labelOrder}] | Binello A, Cravotto G, Nano G M, et al. 2004. Synthesis of chitosan-cyclodextrin adducts and evaluation of their bitter-masking properties[J]. Flavour & Fragrance Journal, 19(5) : 394–400. |
| [${referVo.labelOrder}] | Badruddoza A Z M, Shawon Z B Z, Wei J D T, et al. 2013. Fe3O4/cyclodextrin polymer nanocomposites for selective heavy metals removal from industrial wastewater[J]. Carbohydrate Polymers, 91(1) : 322–332. DOI:10.1016/j.carbpol.2012.08.030 |
| [${referVo.labelOrder}] | 褚四敏. 2014.基于环糊精修饰的磁性纳米吸附剂的制备及其应用研究[D]. 大连:大连理工大学 http://cdmd.cnki.com.cn/Article/CDMD-10141-1015569185.htm |
| [${referVo.labelOrder}] | Capasso S, Salvestrini S, Coppola E, et al. 2005. Sorption of humic acid on zeolitic tuff:a preliminary investigation[J]. Applied Clay Science, 28(1) : 159–165. |
| [${referVo.labelOrder}] | Deng H, Li X, Peng Q, et al. 2005. Monodisperse magnetic single-crystal ferrite microspheres[J]. Angewandte Chemie, 117(18) : 2842–2845. DOI:10.1002/(ISSN)1521-3757 |
| [${referVo.labelOrder}] | Ding Y, Shen S Z, Sun H, et al. 2015. Design and construction of polymerized-chitosan coated Fe3O4, magnetic nanoparticles and its application for hydrophobic drug delivery[J]. Materials Science & Engineering C Materials for Biological Applications, 48 : 487–498. |
| [${referVo.labelOrder}] | 范露露.2013. 基于壳聚糖的磁性吸附剂的制备及在水处理中的应用[D]. 保存地:济南大学 http://d.wanfangdata.com.cn/Thesis/Y2364621 |
| [${referVo.labelOrder}] | Fan R, Chen X H, Gui Z, et al. 2001. A new simple hydrothermal preparation of nanocrystalline magnetite Fe3O4[J]. Materials Research Bulletin, 36(3) : 497–502. |
| [${referVo.labelOrder}] | Fan L, Zhang Y, Luo C, et al. 2012. Synthesis and characterization of magnetic β-cyclodextrin-chitosan nanoparticles as nano-adsorbents for removal of methyl blue[J]. International Journal of Biological Macromolecules, 50(2) : 444–450. DOI:10.1016/j.ijbiomac.2011.12.016 |
| [${referVo.labelOrder}] | Ferro-Garcia M A, Rivera-Utrilla J, Bautista-Toledo I, et al. 1998. Adsorption of humic substances on activated carbon from aqueous solutions and their effect on the removal of Cr(III) Ions[J]. Langmuir, 14(7) : 1880–1886. DOI:10.1021/la970565h |
| [${referVo.labelOrder}] | Huang Z, Wu Q, Liu S, et al. 2013. A novel biodegradable β-cyclodextrin-based hydrogel for the removal of heavy metal ions[J]. Carbohydrate Polymers, 97(2) : 496–501. DOI:10.1016/j.carbpol.2013.04.047 |
| [${referVo.labelOrder}] | Hao W, Ai Z, Zhang L. 2014. Anoxic and oxic removal of humic acids with Fe@Fe2O3 core-shell nanowires:a comparative study[J]. Water Research, 52 . |
| [${referVo.labelOrder}] | Jian L, Shi Z Q, Qiu H H, et al. 2011. Magnetic Nanocomposites:Magnetic Nanocomposites with Mesoporous Structures:Synthesis and Applications (Small 4/2011)[J]. Small, 7(7) : 425–443. |
| [${referVo.labelOrder}] | Jana N R, Chen Y F, Peng X G. 2004. Size-and Shape-Controlled Magnetic (Cr, Mn, Fe, Co, Ni) Oxide Nanocrystals via a Simple and General Approach[J]. Chemistry of Materials, 16(20) : 11–22. |
| [${referVo.labelOrder}] | Liu J, Sun Z, Deng Y, et al. 2009. Highly Water-Dispersible Biocompatible Magnetite Particles with Low Cytotoxicity Stabilized by Citrate Groups[J]. Angewandte Chemie International Edition, 48(32) : 5875–5879. DOI:10.1002/anie.v48:32 |
| [${referVo.labelOrder}] | 李会杰. 2012.腐殖酸和富里酸的提取与表征研究[D]. 武汉:华中科技大学 http://d.wanfangdata.com.cn/Thesis/D232342 |
| [${referVo.labelOrder}] | 柳欢欢, 柯玉娟, 陈泉源, 等. 2009. 活性炭负载纳米TiO对腐殖酸光催化降解动力学[J]. 环境科学学报, 2009, 29(9) : 1923–1931. |
| [${referVo.labelOrder}] | Mahmoodi N M. 2015. Surface modification of magnetic nanoparticle and dye removal from ternary systems[J]. Journal of Industrial and Engineering Chemistry, 27 : 251–259. DOI:10.1016/j.jiec.2014.12.042 |
| [${referVo.labelOrder}] | Makunina M P, Pozdnyakov I P, Yong C, et al. 2015. Mechanistic study of fulvic acid assisted propranolol photodegradation in aqueous solution[J]. Chemosphere, 119 : 1406–1410. DOI:10.1016/j.chemosphere.2014.10.008 |
| [${referVo.labelOrder}] | Oriekhova O, Stoll S. 2016. Stability of uncoated and fulvic acids coated manufactured CeO2 nanoparticles in various conditions:From ultrapure to natural Lake Geneva waters[J]. The Science of the Total Environment, 562 : 327–334. DOI:10.1016/j.scitotenv.2016.03.184 |
| [${referVo.labelOrder}] | Reddy D H K, Lee S M. 2013. Application of magnetic chitosan composites for the removal of toxic metal and dyes from aqueous solutions[J]. Cambridge Quarterly of Healthcare Ethics Cq the International Journal of Healthcare Ethics Committees, 202(4) : 68–93. |
| [${referVo.labelOrder}] | Wang S, Gong W, Liu X, et al. 2006. Removal of fulvic acids using the surfactant modified zeolite in a fixed-bed reactor[J]. Separation & Purification Technology, 51(3) : 367–373. |
| [${referVo.labelOrder}] | Wang S G, Sun X F, Liu X W, et al. 2008. Chitosan hydrogel beads for fulvic acid adsorption:Behaviors and mechanisms[J]. Chemical Engineering Journal, 142(3) : 239–247. DOI:10.1016/j.cej.2007.11.025 |
| [${referVo.labelOrder}] | Wan Z, Chen W, Liu C, et al. 2015. Preparation and characterization of gamma-AlOOH@CS magnetic nanoparticle as a novel adsorbent for removing fluoride from drinking water[J]. Journal of Colloid and Interface Science, 443 : 115–124. DOI:10.1016/j.jcis.2014.12.012 |
| [${referVo.labelOrder}] | Wang S G, Liu X W, Gong W X, et al. 2007. Adsorption of fulvic acids from aqueous solutions by carbon nanotubes[J]. Journal of Chemical Technology & Biotechnology, 82(8) : 698–704. |
| [${referVo.labelOrder}] | Wang J, Bi L, Ji Y, et al. 2014. Removal of humic acid from aqueous solution by magnetically separable polyaniline:Adsorption behavior and mechanism[J]. Journal of Colloid & Interface Science, 430(430) : 140–146. |
| [${referVo.labelOrder}] | Wang C L, Huang L Z, Song S M, et al. 2015. Targeted delivery and pH-responsive release of stereoisomeric anti-cancer drugs using β-cyclodextrin assemblied Fe3O4 nanoparticles[J]. Applied Surface Science, 357 : 2077–2086. DOI:10.1016/j.apsusc.2015.09.189 |
| [${referVo.labelOrder}] | 肖玲, 马珊. 2012. 纳米磁性壳聚糖对腐殖酸和重金属离子混合吸附研究[J]. 武汉大学学报:工学版, 2012, 45(6) : 855–859. |
| [${referVo.labelOrder}] | Yang Y, Shu L, Wang X, et al. 2011. Impact of de-ashing fulvic acid and humin on organic matter structural properties and sorption mechanisms of phenanthrene[J]. Environmental Science & Technology, 45(9) : 3996–4002. |
| [${referVo.labelOrder}] | Yan W Y, Zhou Q, Chen X, et al. 2016. Size-Controlled TiO2 nanocrystals with exposed {001 and {101 facets strongly linking to graphene oxide via p-Phenylenediamine for efficient photocatalytic degradation of fulvic acids[J]. Journal of Hazardous Materials, 314 : 41–50. DOI:10.1016/j.jhazmat.2016.04.026 |
| [${referVo.labelOrder}] | Yao W, Rao P, Lo I M C, et al. 2014. Preparation of cross-linked magnetic chitosan with quaternary ammonium and its application for Cr(Ⅵ) and P(Ⅴ) removal[J]. Journal of Environmental Sciences, 26(12) : 2379–2386. DOI:10.1016/j.jes.2014.03.005 |
| [${referVo.labelOrder}] | 张莉祥, 杨志泉, 李婷, 等. 2015. 改性橘子皮对水中高氯酸盐及共存阴离子的竞争吸附研究[J]. 环境科学学报, 2015, 35(10) : 3137–3143. |
| [${referVo.labelOrder}] | Zhu H Y, Jiang R, Xiao L, et al. 2010. Preparation, characterization, adsorption kinetics and thermodynamics of novel magneticchitosan enwrapping nanosized γ-Fe2O3, and multi-walled carbon nanotubes with enhanced adsorption properties for methyl orange[J]. Bioresource Technology, 101(14) : 5063–5069. DOI:10.1016/j.biortech.2010.01.107 |
| [${referVo.labelOrder}] | Zhang X, Wang Y, Yang S. 2014. Simultaneous removal of Co(II) and 1-naphthol by core-shell structured Fe3O4@cyclodextrin magnetic nanoparticles[J]. Carbohydrate Polymers, 114 . |
| [${referVo.labelOrder}] | 周志武. 2012.乙二胺和β-环糊精改性壳聚糖微球的制备及其吸附T1(Ⅲ)的试验研究[D].衡阳:南华大学 http://cdmd.cnki.com.cn/Article/CDMD-10555-1012458740.htm |
| [${referVo.labelOrder}] | Zhang J, Gong J L, Zenga G M, et al. 2016. Simultaneous removal of humic acid/fulvic acid and lead from landfill leachate using magnetic graphene oxide[J]. Applied Surface Science, 370 : 335–350. DOI:10.1016/j.apsusc.2016.02.181 |
| [${referVo.labelOrder}] | 郑可, 周少奇, 杨梅梅. 2012. 臭氧降解高浓度富里酸动力学[J]. 环境科学, 2012, 33(3) : 879–884. |
 2017, Vol. 37
2017, Vol. 37


