水土环境中的铜污染不仅影响植物、动物及微生物的生命活动,也会对人体健康产生不利影响(陈贵英等,2011).传统治理铜污染的方法包括化学沉淀法、离子交换法、吸附法、反渗透法等(樊文井等,2014),但这些方法普遍存在效率不高、操作条件苛刻、费用高昂等不足.
纳米零价铁(nZⅥ)具有高的比表面积和反应活性,在环境修复中应用广泛(Zhang,2003).然而,暴露的nZⅥ颗粒易氧化甚至自燃,在水中易团聚,使其分散性和稳定性较差(Liu et al., 2010),实际应用效果不佳.目前,常用的固定nZⅥ的载体可分为无机(活性炭、蒙脱石等)和有机(壳聚糖、海藻酸钠)材料.其中,无机材料自身所具有的空隙结构,可有效克服nZⅥ单独使用时的缺点,提高对污染物的去除能力(杨麒等,2013;刘凯等,2011;Bhowmick et al., 2014),但存在难以从水中分离,且材料的重复利用率低的问题.有机材料在形成凝胶时可将nZⅥ包埋在内部结构中(金晓英等,2013;Bezbaruah et al., 2009;Kim et al., 2010),但包埋小球孔径及机械强度有待提高.目前,将无机和有机材料混合制备复合载体来固定nZⅥ的研究鲜有报.
因此,本文将吸附力强的蒙脱石(Mt)和可生物降解的海藻酸钠(SA)混合使用来固定nZⅥ,以发挥无机和有机负载材料各自的优点,在有效提高nZⅥ处理效率的同时降低其分离操作难度,提高出水水质和重复利用率.
2 材料与方法(Materials and methods) 2.1 试剂与仪器试剂:铜标准溶液、硫酸亚铁、硼氢化钠、海藻酸钠、氯化钙、硫酸铜、硝酸、盐酸、氢氧化钠、无水乙醇均为AR级别,以上药品都购自上海国药;蒙脱石(钠基蒙脱石).
仪器:pH计、JJ-1精密增力电动搅拌器、LGJ-10C冷冻干燥机、电子天平,RH-Q恒温振荡器、TAS-986原子吸收分光光度计、扫描电子显微镜(JSM-5600LV,JEOL)、X射线衍射(日本Rigaku,D/Max-2550 PC)、X射线光电子能谱仪,比表面积和孔径分析仪.
2.2 材料的制备 2.2.1 Mt-nZⅥ颗粒的制备采用液相还原法(Huang et al., 2014;Pang et al., 2014)制备Mt-nZⅥ,具体操作为:取24.88 g FeSO4·7H2O溶解于200 mL体积比为4∶1的乙醇-水溶液中,然后加入到500 mL三口烧瓶中;再将20 g Mt(Mt与Fe2+的质量比为4∶1)加入上述FeSO4溶液中,搅拌30 min,使其充分混匀;将50 mL NaBH4溶液置于恒压漏斗中,其中,BH4-/Fe2+为3∶1(物质的量比),逐滴加入FeSO4-Mt混合液中,滴速为每秒2滴;待NaBH4溶液滴加完毕后,继续搅拌30 min,整个反应过程持续通入N2;反应结束后,用无水乙醇洗涤3次,再用无氧去离子水冲洗数次,抽滤,置于真空冷冻干燥箱中干燥24 h,取出备用.
2.2.2 SA/ Mt-nZⅥ小球的制备取一定量的SA于50 mL无氧去离子水中,置于55 ℃下加热溶解,然后静置60 min排出溶胶中的气泡;称取一定量的Mt-nZⅥ加入到一定浓度的SA中,搅拌均匀,然后用注射器将上述混合溶液滴入4%的脱氧CaCl2中,交联60 min,用去离子水清洗3遍.再将SA/Mt-nZⅥ小球投入到0.05 mol·L-1的NaBH4中振荡进行还原处理,然后取出,用无水乙醇洗涤3次,再用去离子水冲洗数次,抽滤,置于真空冷冻干燥箱中干燥24 h,取出备用.
2.3 实验方法取100 mL一定浓度的Cu(Ⅱ)溶液于250 mL锥形瓶中,用3 mol·L-1的HCl和1 mol·L-1的NaOH调节pH后,加入一定量的Mt-nZⅥ和SA/Mt-nZⅥ小球.在转速为120 r·min-1、温度为25 ℃的恒温振荡器上进行反应,每隔一定时间取样,经0.45 μm滤膜进行过滤后,用原子吸收法测定Cu(Ⅱ)的浓度.
3 结果与讨论(Results and discussion) 3.1 材料表征 3.1.1 扫描电镜分析(SEM)和比表面积(BET)图 1为SA小球和SA/Mt-nZⅥ小球的扫描电镜(SEM)图及SA/Mt-nZⅥ小球的直观图.由直观图可见,包埋Mt-nZⅥ颗粒后小球呈黑色,且SA/Mt-nZⅥ小球大小均一,粒径大约为3~4 mm,整体颜色也较均匀,表明Mt-nZⅥ在SA包埋材料内分散良好.从高、低倍镜下SA小球和SA/Mt-nZⅥ小球的形貌(图 1a~d)可以看出,包埋Mt-nZⅥ前小球表面褶皱均匀规整,而包埋之后可以清晰地看到小球表面凹凸不平(王清萍等,2014).同时,对SA/Mt-nZⅥ小球进行比表面积测定分析(表 1)可知,SA包埋Mt-nZⅥ后其比表面积略微减小,但孔容和孔径都有所增大,这表明Mt-nZⅥ颗粒的加入增大了SA小球的孔径,从而减小了传质阻力,有利于Cu(Ⅱ)进入小球内部与Fe0进行反应.
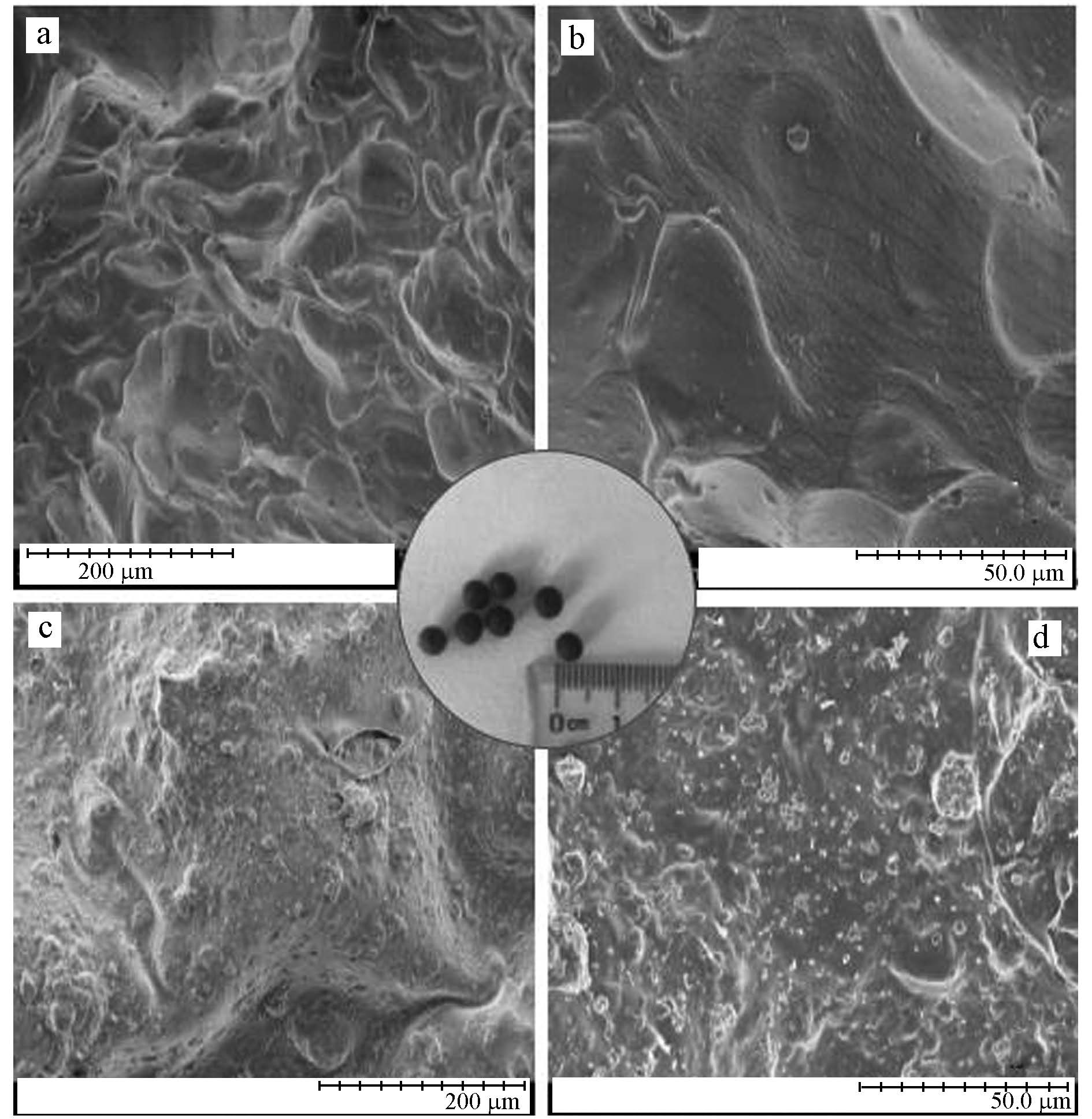 |
| 图 1 Mt-nZⅥ包埋前后SA小球(a.包埋前,b.包埋后)和SA/Mt-nZⅥ小球(c.包埋前,d.包埋后)形貌对比图(中间为直观照片,其余为SEM图) Fig. 1 The SEM images for SA beads(a,b)and SA/Mt-nZⅥ beads(c,d)before/after immobilization process(macroscopic photos for immobilized beads at middle) |
| 表 1 Mt-nZⅥ包埋前后小球的比表面积 Table 1 The Surface area of beads before/after immobilization process |
由于SEM只能分析材料外貌,无法直接得到SA/Mt-nZⅥ小球内部nZⅥ颗粒存在的信息,使用X射线光电子能谱对SA/Mt-nZⅥ小球内部Fe0进行分析.从图 2b中Fe 2p能谱图可知,在706.7、711.8和724.8 eV处出现的特征峰分别对应Fe(0)2p3/2、Fe(ⅡI)2p3/2和Fe(ⅡI)2p1/2结合能(Li et al., 2007),结果表明,在SA/Mt-nZⅥ小球内部确实存在Fe0,三价铁氧化物存在可能是因为有部分Mt-nZⅥ颗粒裸露在小球表面而被氧化.图 3为 SA/Mt-nZⅥ小球的XRD谱图.由图可知,SA/Mt-nZⅥ小球在2θ=44.56°处有一衍射峰,与体心立方结构α-Fe(110)的晶面特征峰一致(樊文井等,2014),可见,SA/Mt-nZⅥ小球中有Fe0存在.而在SA/Mt-nZⅥ小球的衍射图谱中未发现铁氧化物的峰,这可能是因为小球表面形成的铁氧化物是无定形的,在XRD谱图中不会形成明显的衍射峰(雷蕾等,2013).
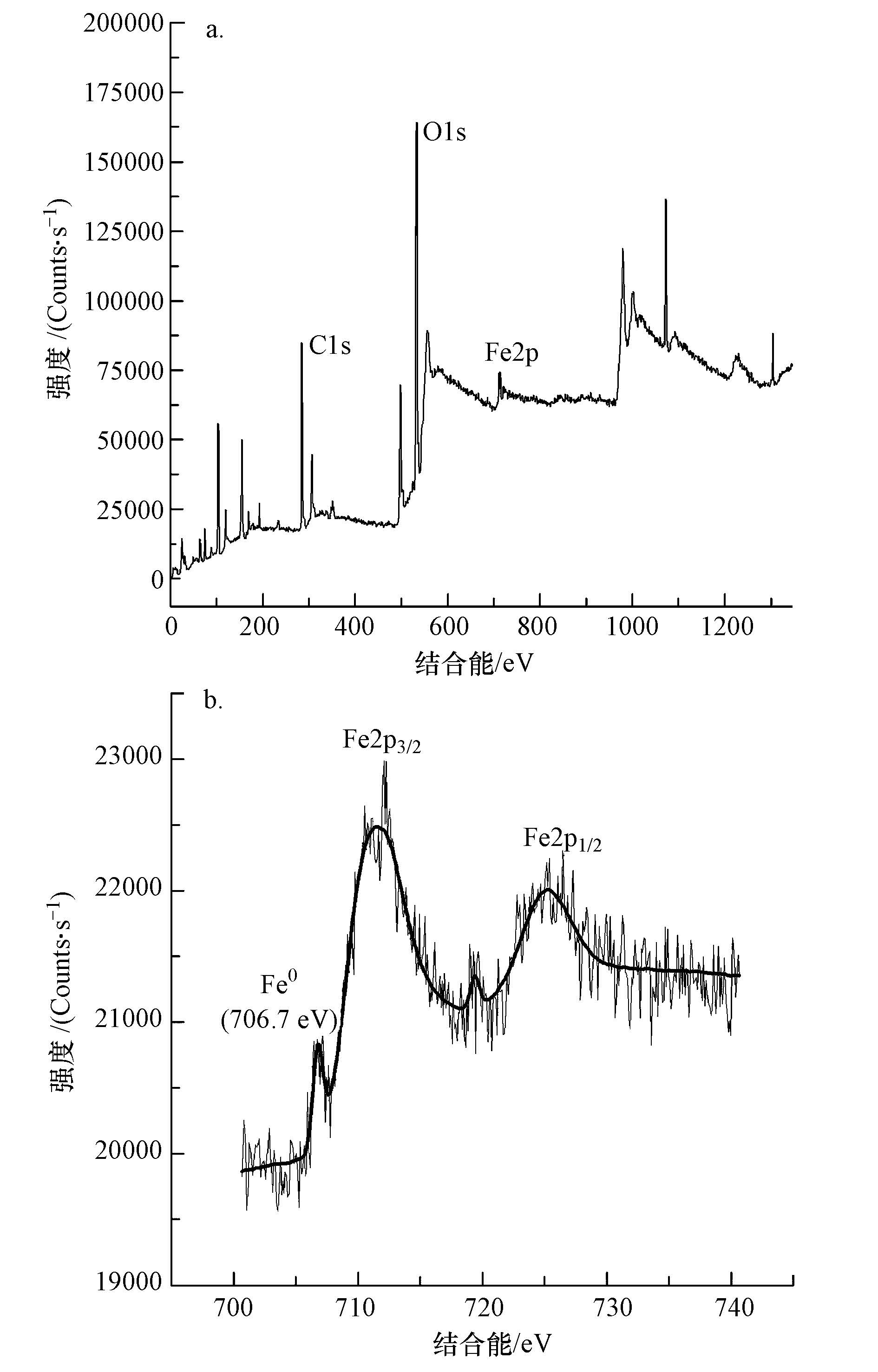 |
| 图 2 SA/Mt-nZⅥ小球的XPS谱图(a.全谱图,b.Fe谱图) Fig. 2 XPS pattern of SA/Mt-nZⅥ beads(a.full scan,b.high resolution scan of Fe) |
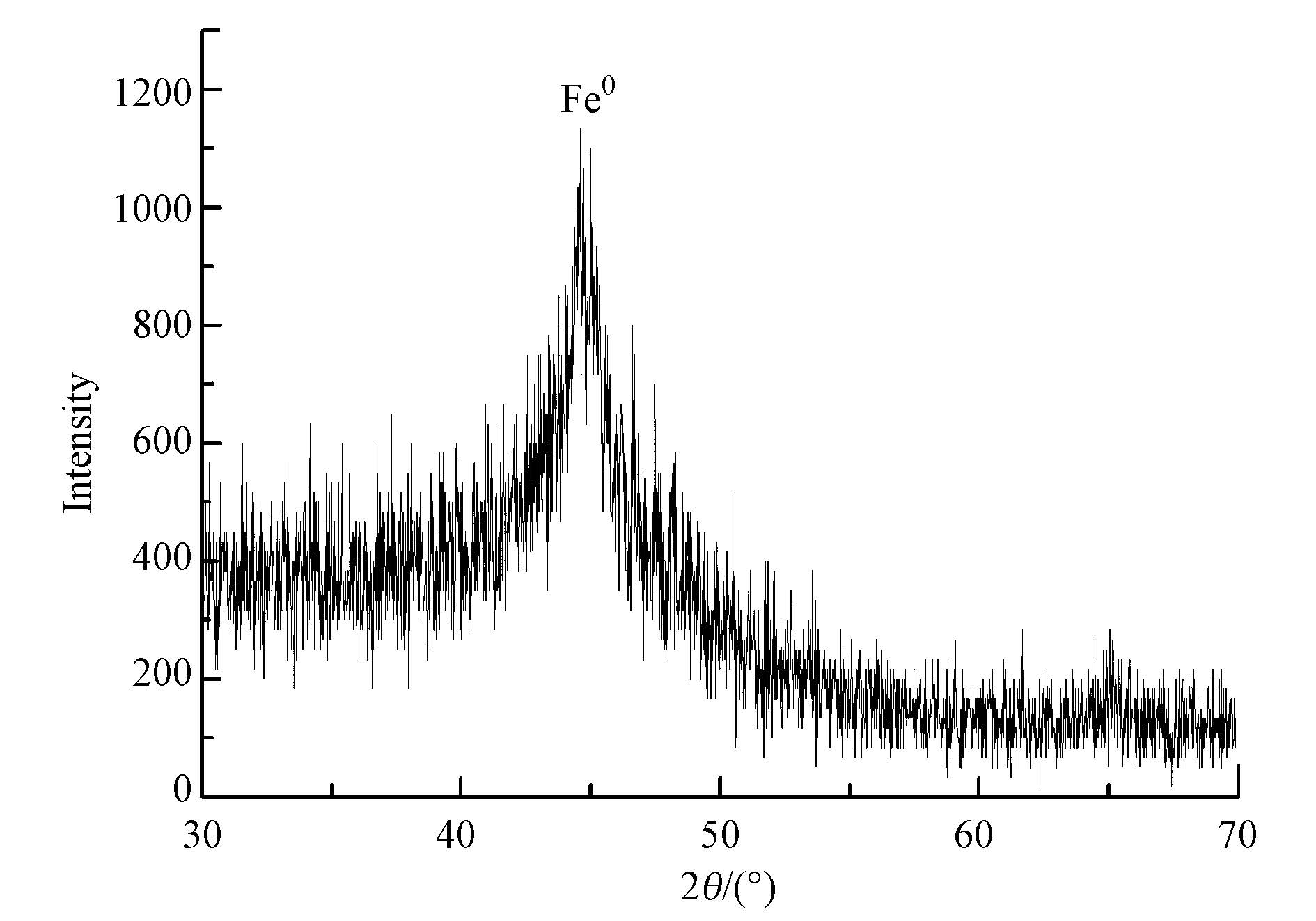 |
| 图 3 SA/Mt-nZⅥ小球的XRD谱图 Fig. 3 XRD pattern of SA/Mt-nZⅥ beads |
图 4为pH=5.11时,12组不同Mt-nZⅥ∶SA比例制备的SA/Mt-nZⅥ小球对浓度为40 mg·L-1 Cu(Ⅱ)24 h后的去除效果.整体上看,随Mt-nZⅥ质量分数增加,Cu(Ⅱ)去除率显著增加(p<0.05).Cu(Ⅱ)去除率随SA质量分数变化因Mt-nZⅥ质量分数不同而异,当Mt-nZⅥ质量分数为2%时,Cu(Ⅱ)去除率随SA质量分数的增加而提高;当Mt-nZⅥ质量分数为4%和6%时,SA质量分数从1%增加到2%,Cu(Ⅱ)去除率随着SA质量分数的增加而提高,但当SA质量分数增加到3%时,其去除率反而下降.这表明Mt-nZⅥ的加入为小球提供了较好的内部孔隙率,有利于Cu(Ⅱ)进入小球内部与Fe0进行反应,提高了Cu(Ⅱ)的去除率.SA质量分数适当提高,有利于提高小球的包覆性能,使Fe0被包覆于SA小球中,不易被氧化.但当SA质量分数过高时,由于颗粒内部过于致密而增加其传质阻力(康海彦,2015),反而影响Fe0还原Cu(Ⅱ)的能力.因此,从提高小球的机械强度和对Cu(Ⅱ)的去除能力角度分析,6%Mt-nZⅥ和2%SA是制备SA/Mt-nZⅥ小球的最佳条件,在后续实验中均采用此比例.
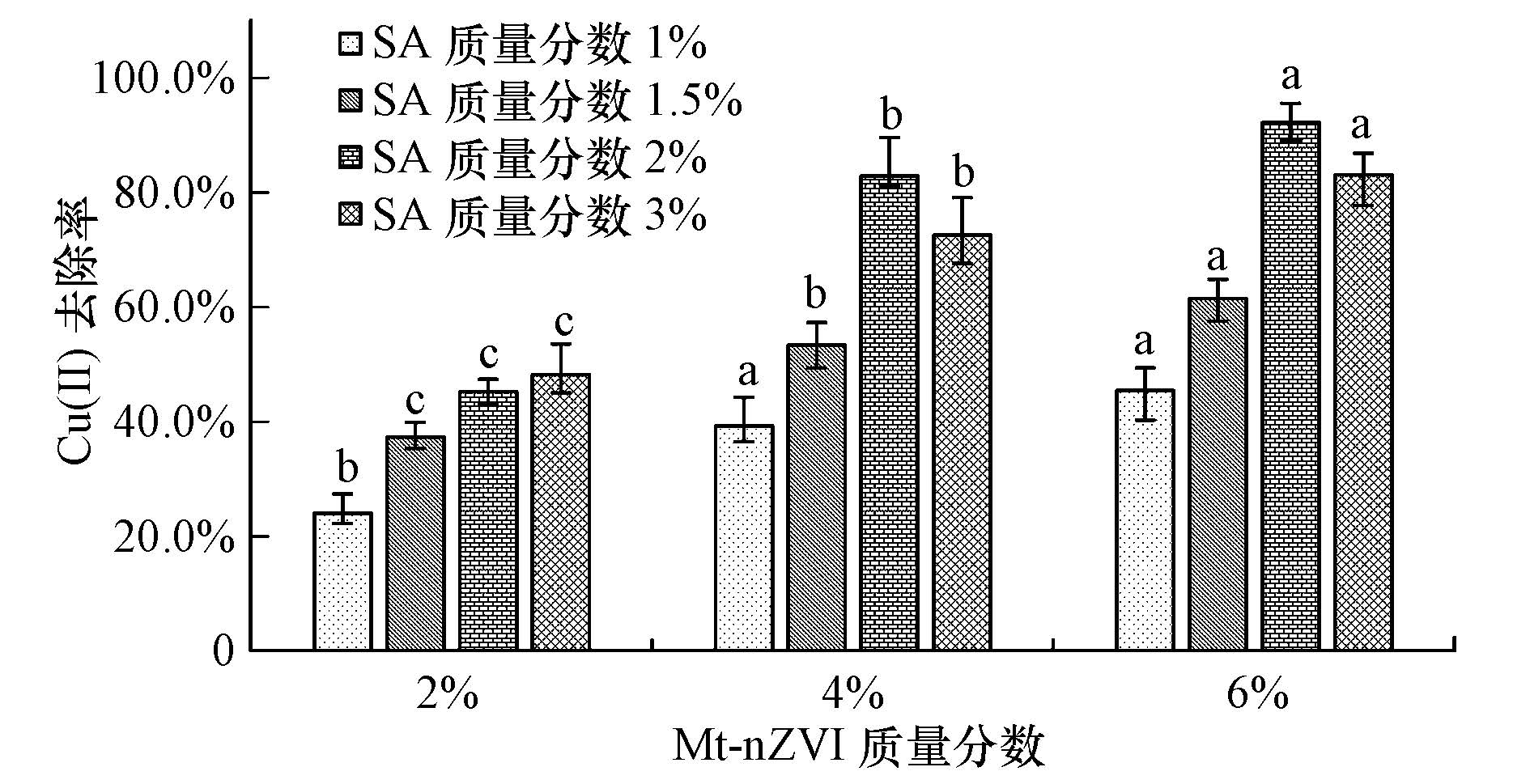 |
| 图 4 不同Mt-nZⅥ∶SA比例制备的SA/Mt-nZⅥ小球对Cu(Ⅱ)去除率的影响(图中表示在相同SA质量分数下,不同Mt-nZⅥ质量分数对Cu(Ⅱ)去除率的显著性比较(n=3),其中,同系列柱形图上具有相同字母的表示差异不显著(p>0.05)) Fig. 4 Cu(Ⅱ) removal efficiency by SA/Mt-nZⅥ beads under different mass proportion of Mt-nZⅥ and SA |
对Mt-nZⅥ质量分数和SA质量分数做两因素分析(表 2)可知,Mt-nZⅥ质量分数和SA质量分数对Cu(Ⅱ)去除率都有显著影响(p<0.05),且两者具有交互作用.三者对Cu(Ⅱ)去除率贡献大小为:Mt-nZⅥ质量分数>SA质量分数> Mt-nZⅥ质量分数×SA质量分数.
| 表 2 Mt-nZⅥ质量分数与SA质量分数的主体间效应的检验 Table 2 The test of main-body effects between Mt-nZⅥ coated and SA concentration |
将Mt-nZⅥ颗粒、SA/Mt-nZⅥ小球和SA小球分别投入40 mg·L-1 Cu(Ⅱ)溶液中进行去除反应,结果如图 5所示.由图 5可见,Mt-nZⅥ表现出快速而强力的去除能力,在反应1 h后对Cu(Ⅱ)的去除率就达到98.26%.相较于游离的Mt-nZⅥ,用海藻酸钠包埋的SA/Mt-nZⅥ小球反应速率明显减慢,1 h后去除率仅为21.37%,原因可能是海藻酸钠包埋会带来一定的传质阻力,从而影响Cu(Ⅱ)和Fe0的接触.但随着时间延长,SA/Mt-nZⅥ小球对Cu(Ⅱ)的去除可持续进行,并在12 h增加到91.32%,在24 h达到92.11%.表明Mt-nZⅥ经SA包覆后活性并没有显著降低,只是延长了反应时间.而SA/Mt-nZⅥ小球对Cu(Ⅱ)的去除率明显高于SA小球,由BET结果可知,这是因为Mt-nZⅥ颗粒的加入增大了小球内部的孔径(柳听义,2011),减小了传质阻力,使Cu(Ⅱ)更易进入小球内部与Fe0发生氧化还原反应,从而提高了Cu(Ⅱ)的去除率.经海藻酸钠包覆后克服了Mt-nZⅥ不易回收,出水水质混浊等缺陷,适用于作为人工湿地的可更换式填料和可渗透格栅技术(PRB)的填充介质.
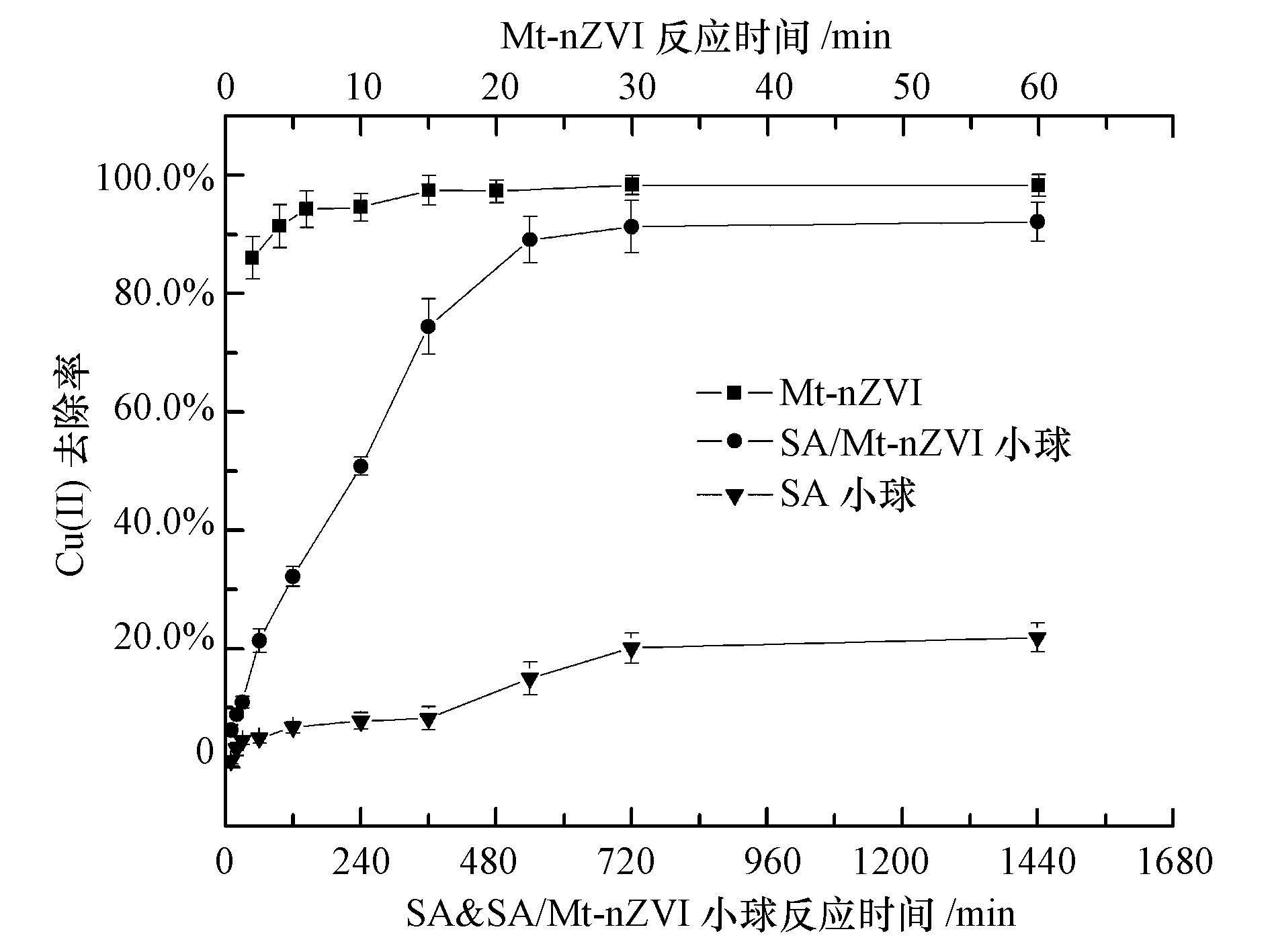 |
| 图 5 Mt-nZⅥ、SA/Mt-nZⅥ小球和SA小球对水中Cu(Ⅱ)的去除效果 Fig. 5 The Cu(Ⅱ)removal efficiencies of Mt-nZⅥ,SA/Mt-nZⅥ and SA beads |
图 6为不同初始pH值对SA/Mt-nZⅥ小球去除Cu(Ⅱ)的影响.可见,总体上Cu(Ⅱ)去除率随着pH的升高而升高.当pH由2.0、3.0、4.0上升到5.0时,反应24 h后去除率从11.35%、38.03%、88.27%增加到92.11%,这表明强酸性条件不利于材料对Cu(Ⅱ)的去除.我们推测一方面是因为溶液中过多的H+会抢占材料的活性位点,从而与Cu(Ⅱ)产生竞争;另一方面可能是因为包埋小球中含有大量的含氧基团,随着pH的升高,—COOH和—OH等将发生电离,从而使得小球表面逐渐带上负电(吕晓书,2015),利于吸附Cu(Ⅱ)进入小球内部与Fe0发生反应.此外,随pH升高,Cu(OH)2沉淀生成.本实验中,初始Cu(Ⅱ)浓度为40 mg·L-1,根据溶度积计算Cu(OH)2沉淀开始形成的pH值为5.77,因此,pH在6时,Cu(Ⅱ)的去除率很高,此时Cu(OH)2沉淀已经开始生成.
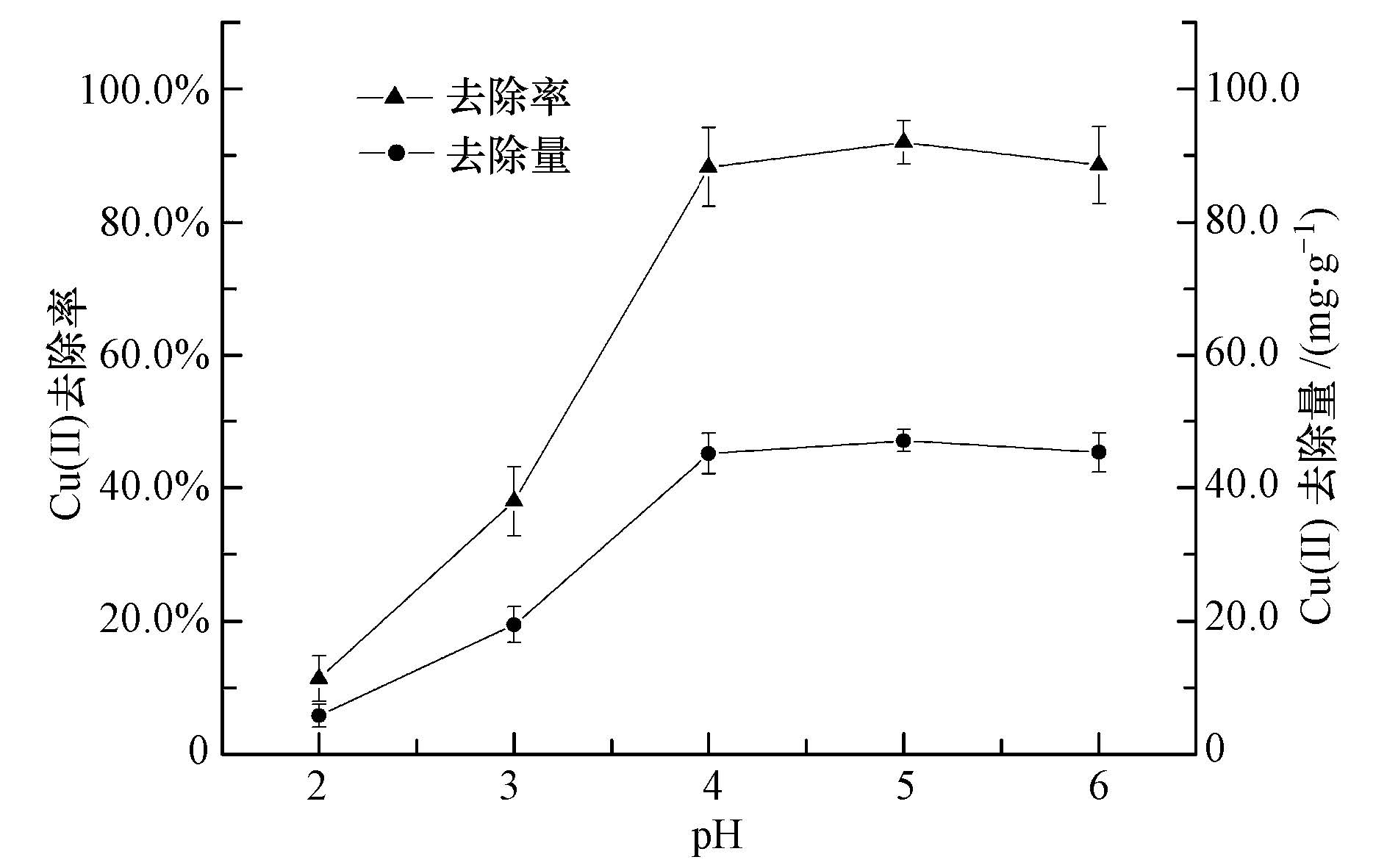 |
| 图 6 不同pH对SA/Mt-nZⅥ小球去除水中Cu(Ⅱ)的影响 Fig. 6 The effect of pH on Cu(Ⅱ)removal by SA/Mt-nZⅥ beads |
图 7为pH=5时,不同初始Cu(Ⅱ)浓度对SA/Mt-nZⅥ小球去除水中Cu(Ⅱ)的影响.可见,随着初始Cu(Ⅱ)浓度的增加,相同时间内的去除率降低,同时,SA/Mt-nZⅥ小球去除Cu(Ⅱ)的平衡时间随之延长.这是由于随着Cu(Ⅱ)初始浓度的增加,小球活性位点逐渐饱和,导致部分Cu(Ⅱ)不能被去除,从而导致去除率降低(曾淦宁等,2015;Bezbaruah et al., 2011).
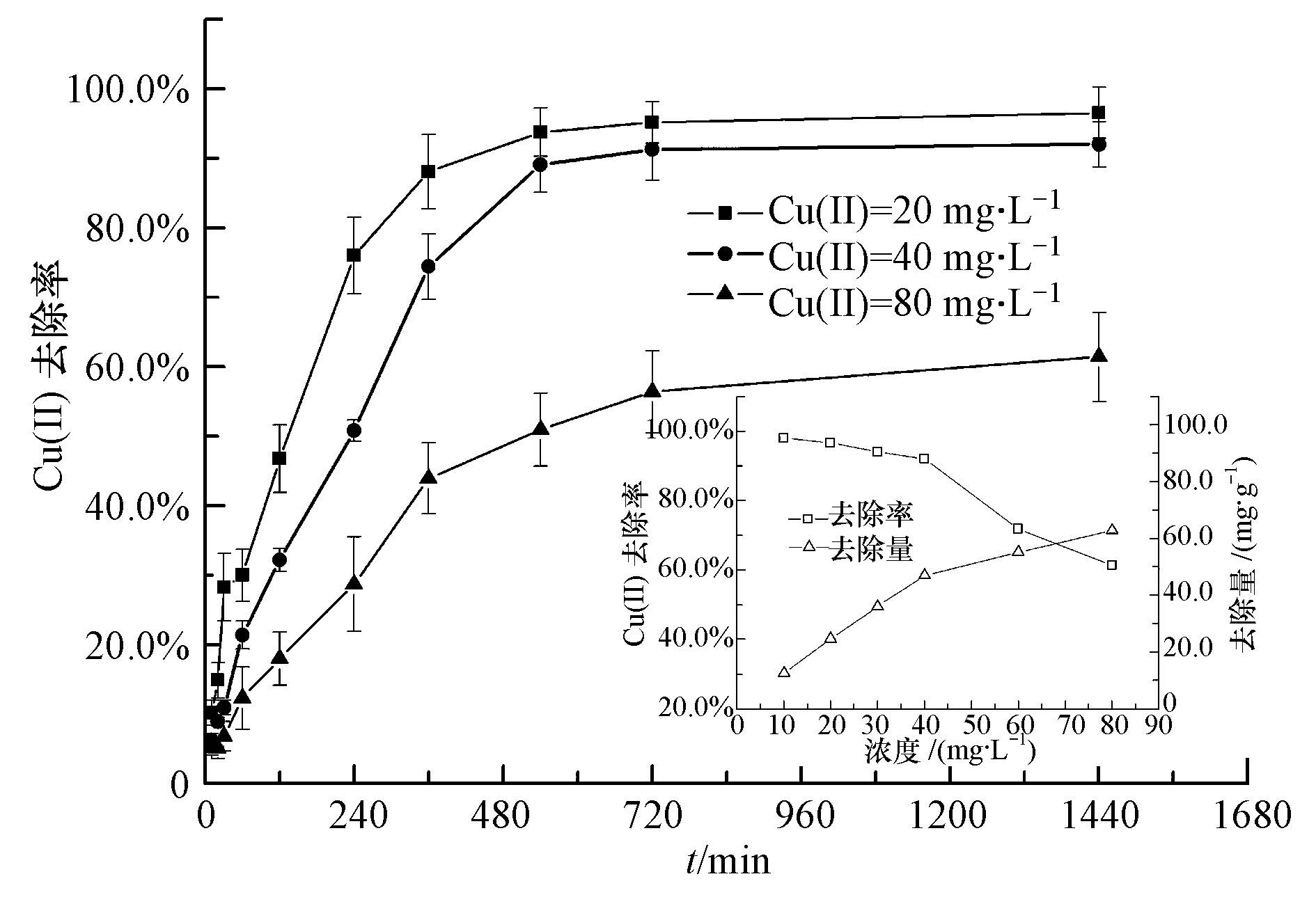 |
| 图 7 不同初始浓度对SA/Mt-nZⅥ小球去除水中Cu(Ⅱ)的影响(内嵌图为不同初始浓度下Cu(Ⅱ)的去除率和去除量) Fig. 7 The effect of initial concentration on Cu(Ⅱ)removal by SA/Mt-nZⅥ beads |
尽管去除率会有所下降,但SA/Mt-nZⅥ小球对Cu(Ⅱ)的去除量随着初始Cu(Ⅱ)浓度的增加而增加.从图 7内嵌图可知,随着Cu(Ⅱ)初始浓度由10、20、30、40、60 mg·L-1提高至80 mg·L-1,小球24 h内对Cu(Ⅱ)的去除量从12.54、24.69、36.09、47.07、55.17 mg·g-1增加到62.84 mg·g-1.原因是对于低浓度的Cu(Ⅱ)溶液,材料活性位点周围浓度低,可提供的活性位点较多,因此,去除率很高,但去除量不大,随着Cu(Ⅱ)初始浓度的增加,在材料活性位点周围聚集较多的Cu(Ⅱ),从而使反应更充分,导致去除量增大(郭晶晶,2014).
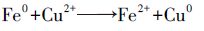
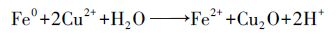
3.3 SA/Mt-nZⅥ小球去除Cu(Ⅱ)的机理分析SA/Mt-nZⅥ小球处理Cu(Ⅱ)溶液后的XPS全谱图如图 8a所示,与反应前(图 2a)对比可知,反应后其表面元素组成增加了Cu,这说明废水中的Cu(Ⅱ)已经从水中分离出来吸附在SA/Mt-nZⅥ小球上.图 8b、8c中给出了SA/Mt-nZⅥ小球处理Cu(Ⅱ)溶液后,Fe2p和Cu2p的XPS图谱.由图 8b可见,对应Fe0(706 eV)附近没有检测到谱峰,而Fe2p3/2和Fe2p1/2的电子结合能谱峰分别出现在711.6 eV和725.8 eV处,这表明反应后材料上主要是Fe(ⅡI),几乎没有Fe0的存在,说明去除过程发生了化学反应,Fe0被氧化为Fe(ⅡI),并被吸附在材料表面.图 8c中932.3 eV和952.8 eV附近出现的峰对应于Cu0的Cu2p3/2和Cu2p1/2谱峰,说明反应后溶液中的Cu(Ⅱ)主要被还原为Cu0,反应过程中Fe0对Cu(Ⅱ)的还原起了主要作用.Cu2O中的Cu1+谱峰在(932.4±0.3)eV处,与Cu0的Cu2p3/2位置非常接近,所以,产物中极有可能存在Cu2O,其反应方程式可能如下(Karabelli et al., 2008):
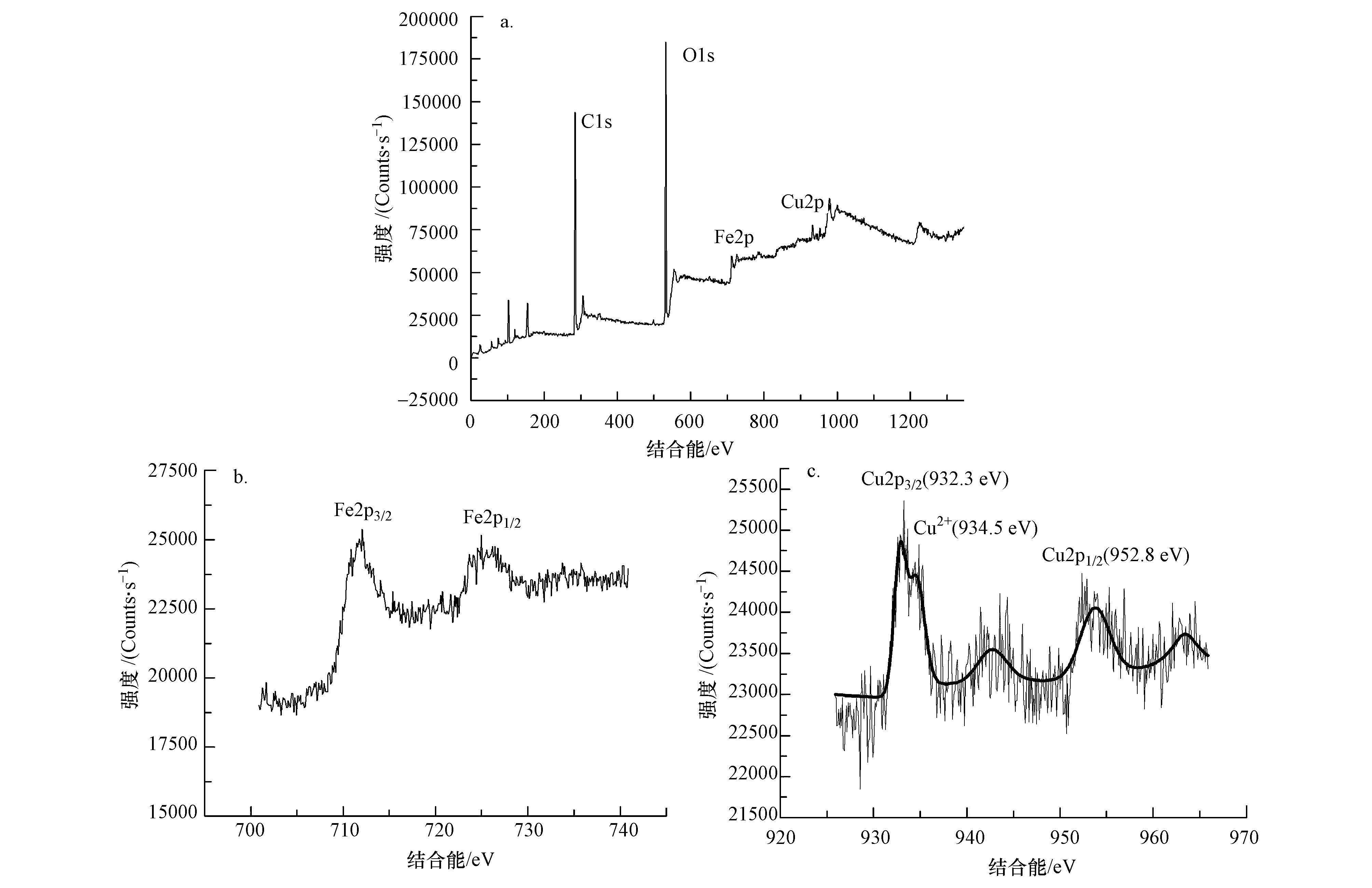 |
| 图 8 反应后SA/Mt-nZⅥ小球的XPS谱图(a.反应后的全谱图,b.反应后的Fe谱图,c.反应后的Cu谱图) Fig. 8 XPS pattern of SA/Mt-nZⅥ beads after reaction with Cu(Ⅱ)solution(a.full scan of the reacted SA/Mt-nZⅥ beads,b.high resolution scan of Fe,c.high resolution scan of Cu) |
|
(1) |
|
(2) |
此外,在934.5 eV处出现Cu(Ⅱ)的谱峰,但与Cu0的特征峰相比,其峰强较小,由此可知,去除过程中SA/Mt-nZⅥ小球除将Cu(Ⅱ)转化为Cu0和Cu2O外,还将少量未被还原的Cu(Ⅱ)以吸附的形式去除.结果表明,SA/Mt-nZⅥ小球在去除Cu(Ⅱ)时,化学还原过程起主要作用.
3.4 SA/Mt-nZⅥ小球的重复利用情况相较于游离的Mt-nZⅥ,用海藻酸钠包埋的SA/Mt-nZⅥ小球的优点在于非常容易分离,且出水水质澄清,不会有纳米颗粒残留,分离后的小球可以用于再生重复循环实验.再生过程为:将反应24 h后的小球分离后用去离子水清洗3次,再用0.1 mol·L-1的稀HCl溶液进行酸处理后,用0.05 mol·L-1的NaBH4进行还原使SA/Mt-nZⅥ小球恢复活性,最后处理完成后用无水乙醇清洗3次,再用去离子水清洗多次待用.图 9为SA/Mt-nZⅥ小球重复利用的情况,可见,SA/Mt-nZⅥ小球反应24 h后的去除率从第1次的92.11%下降到第2次的73.64%、第3次的59.52%.从重复利用实验可以看出,SA/Mt-nZⅥ小球虽然因为传质阻力延长了对Cu(Ⅱ)的去除时间,但其分离回收操作简单,有利于对小球进行重复利用,且包埋后使得小球内部的Fe0与氧气接触缓慢,避免了Fe0的钝化.
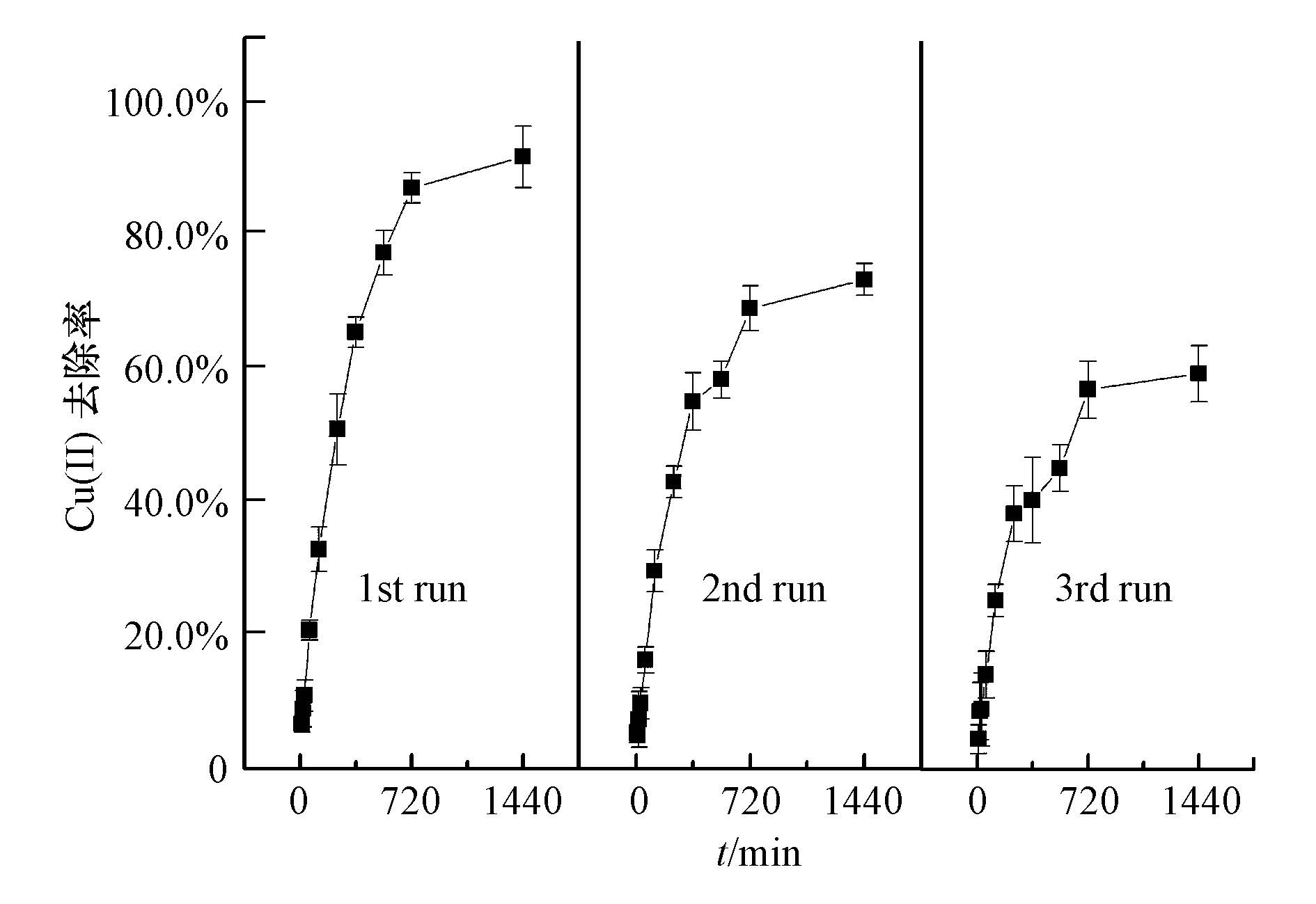 |
| 图 9 SA/Mt-nZⅥ小球重复使用3次后Cu(Ⅱ)去除率的变化 Fig. 9 The variation of Cu(Ⅱ)removal efficiency by SA/Mt-nZⅥ beads after treatment for three times |
1)以2%SA和6%Mt-nZⅥ条件制备的SA/Mt-nZⅥ小球对Cu(Ⅱ)具有较好的处理效果,Mt-nZⅥ颗粒可以被成功地包覆在SA小球中且包覆后的Mt-nZⅥ并没有被氧化.
2 )Mt-nZⅥ被SA包覆后,与游离的Mt-nZⅥ相比,虽然延长了对Cu(Ⅱ)的去除时间,但其活性并未降低,且分离回收操作简单,有利于对小球进行重复利用.
3)SA/Mt-nZⅥ小球对水中Cu(Ⅱ)的去除率随初始浓度的升高而降低,随pH的升高而升高.
4 )重复使用SA/Mt-nZⅥ小球处理含Cu(Ⅱ)废水,结果发现,经过3次使用后对Cu(Ⅱ)的去除率仍维持在59.52%.
| [${referVo.labelOrder}] | Bezbaruah A N, Krajangpan S, Chisholm B J, et al. 2009. Entrapment of iron nanoparticles in calcium alginate beads for groundwater remediation applications[J]. Journal of Hazardous Materials, 166(2/3) : 1339–1343. |
| [${referVo.labelOrder}] | Bezbaruah A N, Shanbhogue S S, Simsek S, et al. 2011. Encapsulation of iron nanoparticles in alginate biopolymer for trichloroethylene remediation[J]. Journal of Nanoparticle Research, 13(12) : 6673–6681. DOI:10.1007/s11051-011-0574-x |
| [${referVo.labelOrder}] | Bhowmick S, Chakraborty S, Mondal P, et al. 2014. Montmorillonite-supported nanoscale zero-valent iron for removal of arsenic from aqueous solution:Kinetics and mechanism[J]. Chemical Engineering Journal, 243 : 14–23. DOI:10.1016/j.cej.2013.12.049 |
| [${referVo.labelOrder}] | 陈贵英, 李维, 陈顺德, 等. 2011. 环境铜污染影响及修复的研究现状综述[J]. 绿色科技, 2011(12) : 125–128. |
| [${referVo.labelOrder}] | 樊文井, 成岳, 余淑贞, 等. 2014. 琼脂包裹纳米零价铁的制备及处理废水中Cu (Ⅱ)试验研究[J]. 陶瓷学报, 2014, 35(6) : 608–612. |
| [${referVo.labelOrder}] | 郭晶晶.2014.蒙脱石/零价铁纳米复合材料修复水体重金属污染效率及机理研究[D].呼和浩特:内蒙古大学 |
| [${referVo.labelOrder}] | Huang L H, Zhou S J, Jin F, et al. 2014. Characterization and mechanism analysis of activated carbon fiber felt-stabilized nanoscale zero-valent iron for the removal of Cr (VI) from aqueous solution[J]. Colloids and Surface A:Physicochemical and Engineering Aspects, 447 : 59–66. |
| [${referVo.labelOrder}] | 金晓英, 陈征贤, 郭飞鹏, 等. 2013. 超声波辅助壳聚糖/零价纳米铁降解酸性品红[J]. 环境科学学报, 2013, 33(4) : 1004–1009. |
| [${referVo.labelOrder}] | Kim H J, Hong H J, Jung J, et al. 2010. Degradation of trichloroethylene (TCE) by nanoscale zero-valent iron (nZVI) immobilized in alginate bead[J]. Journal of Hazardous Materials, 176(1/3) : 1038–1043. |
| [${referVo.labelOrder}] | 康海彦, 杨治广, 黄晓楠. 2015. 海藻酸钠/β-环糊精固定化纳米Fe0去除重金属的性能研究[J]. 环境工程, 2015, 33(6) : 144–147. |
| [${referVo.labelOrder}] | Karabelli D, Üzüm C, Shahwan T, et al. 2008. Batch removal of aqueous Cu2+ ions using nanoparticles of zero-valent iron:A study of the capacity and mechanism of uptake[J]. Industral Engineering Chemistry Research, 47(14) : 4758–4764. DOI:10.1021/ie800081s |
| [${referVo.labelOrder}] | 刘凯, 庞志华, 李小明, 等. 2011. 有机蒙脱石负载纳米铁去除4-氯酚的研究[J]. 环境科学学报, 2011, 31(12) : 2616–2623. |
| [${referVo.labelOrder}] | 雷蕾, 李筱琴, 殷其亮, 等. 2013. 聚苯乙烯磺酸钠对零价纳米铁表面结构和去除水中As (Ⅲ)的影响[J]. 环境科学学报, 2013, 33(2) : 408–414. |
| [${referVo.labelOrder}] | 柳听义.2011.包埋型纳米铁(nZVI)的制备及其去除废水中铬(Cr(VI))的研究[D].天津:天津大学 |
| [${referVo.labelOrder}] | Liu T Y, Zhao L, Sun D S, et al. 2010. Entrapment of nanoscale zero-valent iron in chitosan beads for hexavalent chromium removal from wastewater[J]. Journal of Hazardous Materials, 184(1/3) : 724–730. |
| [${referVo.labelOrder}] | Li X Q, Zhang W X. 2007. Sequestration of a metal cations with zerovalent iron nanoparticles-A study with high resolution X-ray photoelectron spectroscopy (HR-XPS)[J]. Journal Physical Chemistry C, 111(19) : 6939–6946. DOI:10.1021/jp0702189 |
| [${referVo.labelOrder}] | 吕晓书.2015.稳定化纳米级零价铁的制备及对水中Cr(VI)的去除机制研究[D].杭州:浙江大学 |
| [${referVo.labelOrder}] | Pang Z H, Yan M Y, Jia X S, et al. 2014. Debromination of decabromodiphenyl ether by organo-montmorillonite supported nanoscale zero-valent iron:Preparation Characterization and influence factors[J]. Journal of Environmental Sciences, 26(2) : 483–491. DOI:10.1016/S1001-0742(13)60419-2 |
| [${referVo.labelOrder}] | 王清萍, 况烨, 金晓英, 等. 2014. 海藻酸钙包覆纳米Ni/Fe颗粒用于同时去除水中铜离子和氯苯[J]. 环境科学学报, 2014, 34(5) : 1228–1235. |
| [${referVo.labelOrder}] | 杨麒, 伍秀琼, 钟宇, 等. 2013. 活性炭负载纳米零价铁去除溴酸盐的研究[J]. 湖南大学学报(自然科学版), 2013, 40(12) : 97–102. |
| [${referVo.labelOrder}] | 曾淦宁, 武晓, 郑林, 等. 2015. 负载纳米零价铁铜藻基活性炭的制备及其去除水中Cr (Ⅵ)的研究[J]. 环境科学, 2015, 36(2) : 530–536. |
| [${referVo.labelOrder}] | Zhang W X. 2003. Nanoscale iron particles for environmental remediation:An overview[J]. Journal of Nanoparticle Research, 5(3/4) : 323–332. DOI:10.1023/A:1025520116015 |
 2017, Vol. 37
2017, Vol. 37


