近年来,随着我国水源污染日渐严重和饮用水水质标准日益严格,对现行的水处理工艺和技术提出了更为严峻的要求.在我国广东、天津、四川等地区曾发生过较为严重的摇蚊幼虫污染城市净水工艺的事件(周令等,2003).摇蚊幼虫(chironomid larvae)俗称“红虫”,是典型的大型浮游动物中的一种,属双翅目长角亚目昆虫,可作为污染物质急性和慢性毒性测试生物的一种(Crane et al.,2002; Watts et al., 1996;Osano et al., 2002).当天然水体受外界环境影响污染程度加重,水体富营养化剧烈,摇蚊幼虫作为适应该种水体的种群,在水体中占优势地位(熊金林等,2003),大量的摇蚊幼虫代谢产生含有蛋白质、氨基酸及脂肪等消毒副产物的前体物,对消毒副产物的生成有很大的影响.孙兴滨等(2013)试验表明,摇蚊幼虫在氯化消毒过程中会产生三氯甲烷(TCM)、二氯乙腈(DCAN)、1,1-二氯丙酮(1,1-DCP)、1,1,1-三氯丙酮(1,1,1-TCP)、三氯乙腈(TCAN)、二氯乙酸(DCAA)等几种消毒副产物.自1974年Rook等检测出经氯化消毒处理后的水中含有三卤甲烷类物质,并确认其具有致癌性后(Rook,1974),消毒副产物便引起相关学者的重视.
传统氯化消毒副产物对人体健康的危害问题,日益受到社会的广泛关注(Chang et al., 2000;叶少帆等,2010 罗凡等,2010;赵玉丽等,2011).预氧化作为一种有效控制消毒副产物的技术应运而生,而高锰酸盐复合药剂是一种成熟的预氧化技术,其对很多种地表水表现出明显的强化混凝助凝作用(张锦等,2003;陈卫等,2001).高锰酸盐复合药剂(Potassium permanganate composites,PPC)是以高锰酸钾为主剂,高分子活性物质以及一些无机物质为辅剂所组成的一种除污药剂(梁恒等,2004),充分发挥了主剂与辅剂的协同氧化作用,降低氯化消毒副产物的生成,提高出水水质.虽然高锰酸盐复合药剂已在国内外得到了较为广泛的应用,并在除藻方面取得了显著效果,但是关于高锰酸盐复合药剂对摇蚊幼虫生成氯化消毒副产物前体物的控制研究的报道较少,本研究通过高锰酸盐复合药剂预氧化处理模拟含摇蚊幼虫的污染水源水,研究不同pH、预氧化时间、氧化剂浓度及混凝剂浓度条件下,高锰酸盐复合药剂对消毒副产物三卤甲烷(THMs)和卤乙酸(HAAs)的生成影响,为饮用水消毒副产物的有效控制提供理论基础.
2 材料与方法(Materials and methods) 2.1 试验水样试验所用花翅摇蚊幼虫(Chironomus kiiensis)为市场买回在实验室经标准方法繁殖后所得,试验中选择第4龄期的摇蚊幼虫为试验对象(Watts et al., 1996).取180只长势相当的摇蚊幼虫个体,放置于2 L的烧杯内,加入1000 mL去离子水,在温度为(20±2)℃的条件下放置1 d进行培养,并及时替换取出少量已死的摇蚊幼虫后再放置1 d.用多层无菌纱布过滤掉摇蚊幼虫个体,将所得溶液用抽滤装置过滤,使其通过0.45 μm孔径滤膜,取样测定总有机碳(Total Organic Carbon-TOC).根据所测的TOC将水溶液稀释成ρ(TOC)为5 mg·L-1,即为摇蚊幼虫代谢产物的使用液.
2.2 提取消毒副产物前处理方法遵循美国环保局的EPA551.1(Munch et al., 1995)中所述方法进行前处理.
2.3 消毒副产物检测方法样品检测采用美国Agilent公司生产的Agilent GC-7890气相测谱仪,检测条件如下:使用HP-5石英毛细管柱(30 mm×0.25 mm,薄膜的厚度0.25 mm ID);进样口温度为200 ℃;ECD检测温度为290 ℃;进样量为1 mL;采用高纯氮(≥99.999%)作为载气;程序升温控制为起始5 min升至35 ℃,10 ℃·min-1攀升至75 ℃,保持5 min,10 ℃·min-1升至100 ℃并持续2 min.
2.4 试验方法氯化消毒试验在密封的玻璃瓶中进行,反应基本条件为:氯投量为20 mg·L-1,高锰酸盐复合药剂投量为1 mg·L-1,反应pH=7.0,温度控制在(20±2)℃,氯化反应时间为48 h,在此基本条件下,分别改变pH值(5、6、7、8、9),高锰酸盐复合药剂投加量(0.5、1.0、2.0、2.5、3.0 mg·L-1),预氧化时间(15、30、45、60、75 min),混凝剂投加量(10、20、30、40 mg·L-1).每一试验组设置3个平行样,每组均设空白对照.试验所用预氧化药剂为哈尔滨工业大学马军教授专利药品,经购买获得.
3 结果与讨论(Results and discussion) 3.1 pH的影响由图 1可知,随着pH的升高,TCM、TCAN、1,1-DCP、1,1,1-TCP的浓度呈现出先减少后增加的趋势,TCAA与DCAA的浓度呈现出逐渐减少的趋势.当pH由5增加7时,TCM和TCAN的浓度分别由5.13、7.83 μg·L4-1 降低到2.04、4.27 μg·L-1,其去除率高达60.23%、45.47%,有效的减少了消毒副产物的产生;1,1-DCP和1,1,1-TCP则在pH为8时浓度最低;这主要是由预氧化药剂的主要成分高锰酸钾所导致.高锰酸钾在酸性条件下易被还原成Mn2+,在碱性条件下,易被还原成MnO2-,只有在中性条件下,氧化反应产生的新生态水合二氧化锰对消毒副产物前质的产生起到控制作用,其主要机理是新生态水合二氧化锰带有负电,且具有胶体的性质,活性很高,能够吸附水中的金属水解产物、金属离子和有机物等,形成絮体核心,促进胶体的成长(Raveendran et al., 2002),从而降低消毒副产物前质的产生,这也就导致了pH为7时,TCM和TCAN的浓度达到最低值的原因;而1,1-DCP和1,1,1-TCP为不稳定的消毒副产物,其水解速率随着pH的升高而加快(Yang et al., 2007),当pH为8.5时,1,1,1-TCP的水解速率常数为20.90,是pH为7时的5倍,这就导致了1,1,1-TCP的浓度随着pH的增大而增大的原因,且在与高锰酸盐预氧化的共同作用下,1,1,1-TCP和1,1-DCP的浓度在pH为8时,到达最低值.试验发现,高pH对TCAA的生成有明显的控制作用,当pH为9时,效果最佳,去除率可达66.32%;DCAA的浓度则随着pH的升高缓慢减少,主要是由于DCAA是氯化反应的最终产物,由方程反应HOCl+OH-→H2O+ClO-可知,pH的增大导致HOCl量的减小,进而减少DCAA的浓度.因此,在高的pH条件下,后续氯化消毒生成的HAAs得到有效的控制.
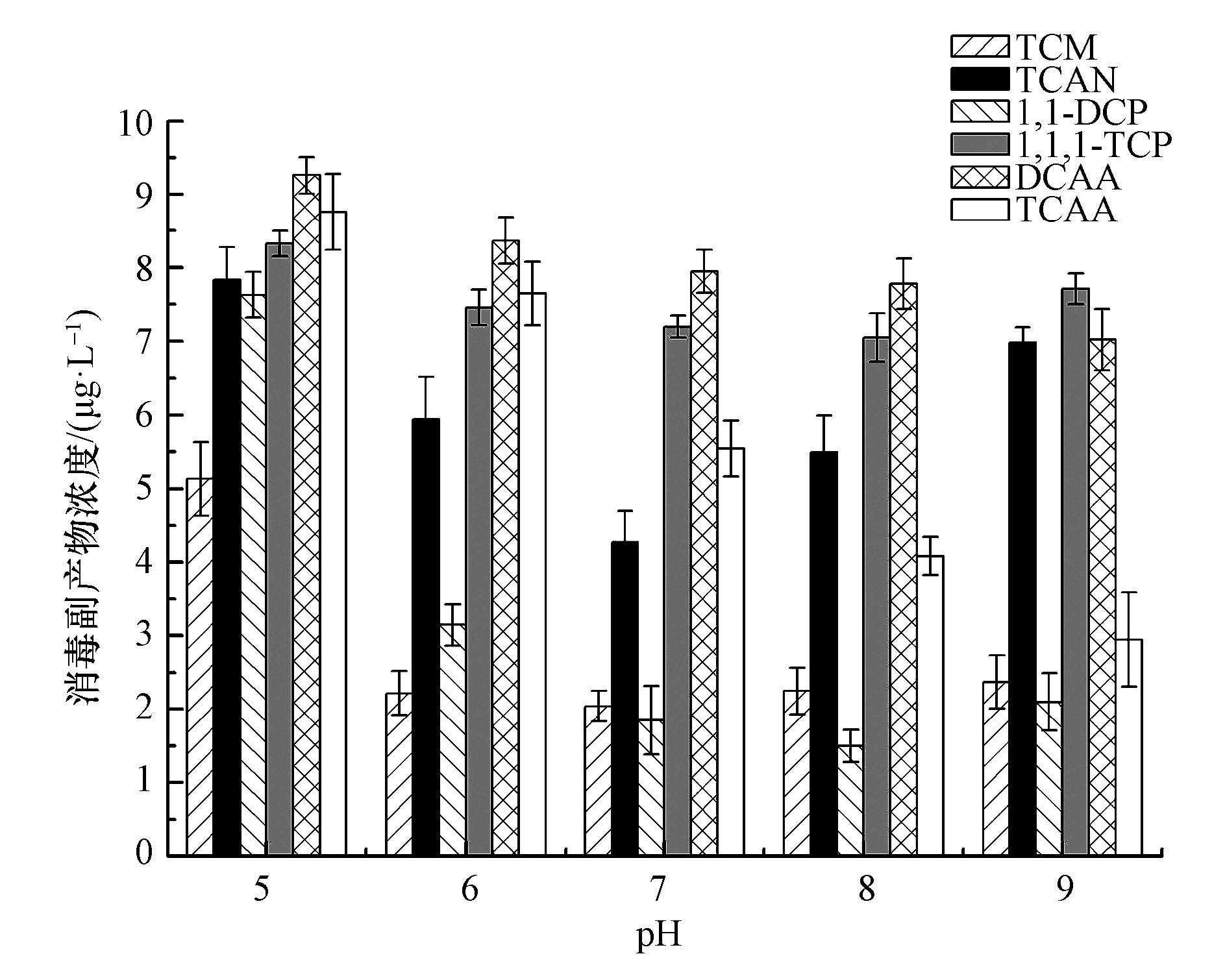 |
| 图 1 不同pH对消毒副产物浓度的影响 Fig. 1 Effect of different pH on DBPs concentration |
由图 2可知,随着高锰酸盐复合药剂浓度的增加,TCM呈现出持续稳定增长的趋势,TCAN、1,1-DCP、1,1,1-TCP和TCAA呈先增加后减少的趋势,DCAA呈现总体减少趋势.其中TCM在3 mg·L-1时达到峰值3.65 μg·L-1,提高了194.35%,主要是由于高锰酸盐复合药剂将一部分大分子有机物氧化分解成肽链等小分子有机物,增加了消毒副产物三氯甲烷的前体物浓度,此外部分1,1-DCP、1,1,1-TCP等不稳定的消毒副产物前质继续水解还会生成TCM的前体物,故TCM浓度稳定增长.当高锰酸盐复合药剂的投加量为0.5 mg·L-1 时,1,1-DCP、1,1,1-TCP浓度达到最大值,分别提高了95.62%、28.49%,随后呈逐渐减少趋势,在投加量为3 mg·L-1时,去除率分别为72.99%、26.60%,去除效果明显.有研究表明,投加低浓度的高锰酸盐氧化有机物生成较多的酮类中间产物,进而生成1,1-DCP、1,1,1-TCP;投加高浓度的高锰酸盐时,生成的酮类物质可以继续氧化生成较多的羧酸类物质(谢鹏超等,2015),从而降低了1,1-DCP、1,1,1-TCP的前体物,故1,1-DCP、1,1,1-TCP的浓度先增加后减少.TCAN为N-DBPs,其主要是由摇蚊幼虫代谢产物中含氮有机物与氯反应产生,由于其前体物存在不稳定性,在高锰酸盐的投加量为2 mg·L-1后,前体物被氧化分解,故出现先增加后减少的趋势.经试验可知,高锰酸盐预氧化有助于减少HAAs前体物,去除率可达30.4%.其中,高锰酸盐的投加对DCAA的生成有显著的控制作用,去除率可达35.81%,由于DCAA前体物不稳定,易被氧化为TCAA前体物,故TCAA呈现出先增加后减少的趋势.
 |
| 图 2 不同浓度预氧化药剂对消毒副产物浓度的影响 Fig. 2 Effect of different concentrations of pre oxidation on DBPs concentration |
由图 3可知,随着预氧化反应时间的延长,TCM呈总体上升趋势,而1,1-DCP、DCAA、TCAA呈下降趋势,TCAN、1,1,1-TCP呈先增加后减少的趋势.TCM浓度由1.68 μg·L-1增长到2.56 μg·L-1,增长了52.38%,这主要是由三氯甲烷本身性质和预氧化药剂共同作用导致.首先TCM为稳定消毒副产物,不易发生水解反应,其次,随着预反应时间的延长,高锰酸盐不断被消耗,氧化性逐渐降低,TCM前质不能有效的去除,故TCM浓度稳定增长.相比较而言,卤乙酸前体物活性高,易被氧化,经高锰酸盐氧化后,DCAA、TCAA浓度分别降低了51.51%、43.41%,使得后续氯化消毒生成的HAAs得到有效控制.TCAN、1,1,1-TCP的浓度分别在预反应45、30 min时,达到最大值,分别为5.49、7.20 μg·L-1,是因为DCAN、1,1-DCP前质物被高锰酸盐氧化为TCAN、1,1,1-TCP前质物,随着预反应时间的延长,TCAN、1,1,1-TCP的水解速率大于生成速率,其含量呈逐渐下降的趋势,在预反应75 min时浓度达到最低值,去除率分别为27.90%、37.02%.
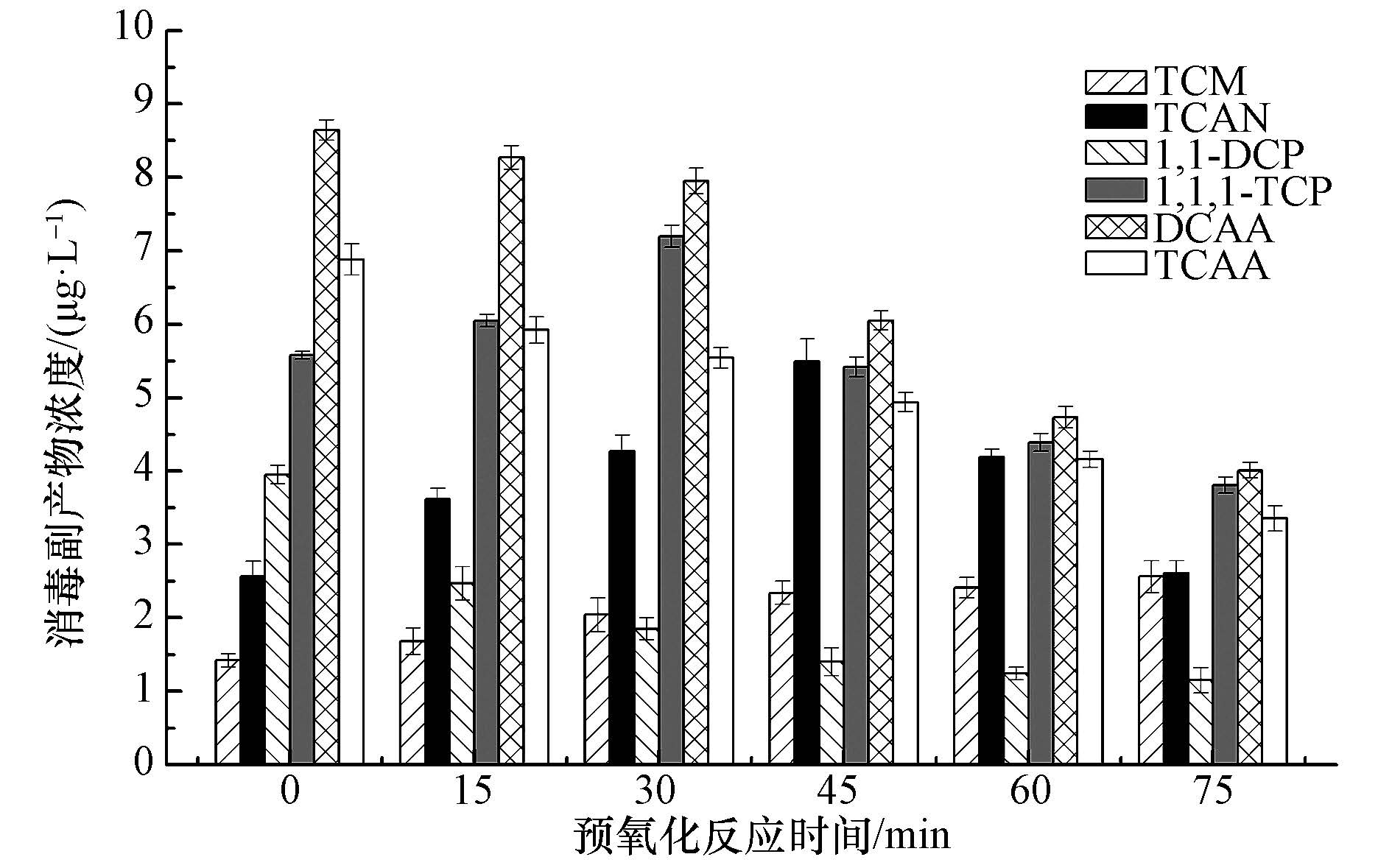 |
| 图 3 不同预氧化反应时间对消毒副产物浓度的影响 Fig. 3 Effect of different pre-oxidation time on DBPs concentration |
 |
| 图 4 不同混凝剂浓度对消毒副产物浓度的影响 Fig. 4 Effect of different coagulant concentrations on DBPs concentration |
试验选用10 g·L-1硫酸铝(Al2O3计)溶液,在500 mL烧杯中进行,将抽滤过的摇蚊幼虫储备溶液倒入烧杯中,投加混凝剂,采用ZR-6型数显式自动控制六联搅拌机,模拟水厂实际情况,依次加入10、20、30、40 mL进行混凝试验,如无特殊说明,搅拌程序如下:快速搅拌300 r·min-1、1 min,中速搅拌150 r·min-1、10 min,慢速搅拌100 r·min-1、10 min,静沉20 min.
由图 4可知,随着混凝剂浓度的增加,消毒副产物TCM、1,1,1-TCP呈先增加后减少的趋势,而TCAN、1,1-DCP、DCAA、TCAA呈总体下降的趋势.在高锰酸盐复合药剂与混凝剂的共同作用下,大分子有机物被氧化分解成小分子有机物,增加了TCM前体物浓度,在混凝剂的投量为30 mg·L-1,达到最大值4.42 μg·L-1,增长了116.67%.1,1,1-TCP在反应初始急剧升高到峰值8.27 μg·L-1,是由1,1-DCP前质物的转换导致,由于1,1,1-TCP的不稳定性,其浓度随着混凝剂浓度的增加而逐渐降低,当混凝剂的投加量为40 mg·L-1时,1,1,1-TCP的去除率达到58.66%.混凝剂的投加使得消毒副产物TCAN、1,1-DCP、DCAA、TCAA前体物的产生得到了有效的控制,从而减少其副产物的生成,其中TCAN、DCAA在硫酸铝的投加量为20 mg·L-1时急剧下降,1,1-DCP、TCAA在硫酸铝投加量为30 mg·L-1时,去除效果明显.张永吉等(2009)研究表明,混凝剂有助于增加水中胶体表面正电荷的数量,而高锰酸盐复合药剂的强氧化性破坏了水中的有机物,使其表面所带的负电性减弱,稳定性降低,从而有利于提高高锰酸盐在混凝剂表面上的吸附凝聚作用,强化了对消毒副产物前质的去除.经试验发现,强化混凝有助于减少THMs与HAAs前体物的生成,去除率可达53.3%、61.1%.
4 结论(Conclusions)1)pH对几种消毒副产物有不同的影响.在pH由5升高到9时,TCAA与DCAA的浓度一直呈现减少的趋势;pH由5升高到7时,TCM和TCAN的浓度减幅最大,去除率分别为60.23%和45.47%;1,1-DCP和1,1,1-TCP则在pH为8时浓度达到最低值.
2 )随着高锰酸盐复合药剂浓度的增加,TCM呈现持续稳定增长趋势,DCAA呈总体下降趋势,而TCAN、1,1-DCP、1,1,1-TCP和TCAA则先增加后减少.1,1-DCP、1,1,1-TCP、TCAA在高锰酸盐复合药剂浓度为0.5 mg·L-1时达到最大值,而TCAN的最大值出现在1 mg·L-1,它们的最小值点出现在3 mg·L-1.
3)随着预氧化反应时间的延长,TCM呈总体上升趋势,而1,1-DCP、DCAA、TCAA呈下降趋势,TCAN、1,1,1-TCP呈先增加后减少的趋势.根据我国饮用水卫生标准,考虑过长的预氧化时间,增加了水处理工艺的经济负担,最佳的预氧化时间宜定为30 min.
4)预氧化强化混凝对消毒副产物前体物的产生具有良好的控制作用.随着混凝剂的不断增加,TCM、1,1,1-TCP呈先增加后减少的趋势,TCAN、1,1-DCP、DCAA、TCAA浓度则不断的降低,在硫酸铝浓度为20~30 mg·L-1时,消毒副产物去除率较高,综合经济因素考虑,混凝剂硫酸铝的最佳浓度为30 mg·L-1.
5)试验研究发现,pH的增加与预氧化时间的延长,均有助于减少HAAs前体物的生成,使得消毒副产物得到有效控制.预氧化强化混凝效果明显优于高锰酸盐单独预氧化,当混凝剂投加量为40 mg·L-1时,THMs、HAAs去除率可达53.3%、61.1%.
| [${referVo.labelOrder}] | Chang C Y, Hsieh Y H, Hsu S S, et al. 2000. The formation of disinfection by-products in water treated with chlorine dioxide[J]. Journal of hazardous materials, 79(1) : 89–102. |
| [${referVo.labelOrder}] | 陈卫, 邹浩春. 2001. 高锰酸钾复合药剂去除太湖水中蓝藻的室内试验研究[J]. 哈尔滨建筑大学学报, 2001, 34(3) : 72–74. |
| [${referVo.labelOrder}] | Crane M, Sildanchandra W, Kheir R, et al. 2002. Relationship between biomarker activity and developmental endpoints in ChironomusripariusMeigen exposed to an organophosphate insecticide[J]. Ecotoxicology and Environmental Safety, 53(3) : 361–369. DOI:10.1016/S0147-6513(02)00038-6 |
| [${referVo.labelOrder}] | 梁恒,李星,韩宏大,等. 2004. 高锰酸盐复合剂(PPC)研究进展[C]. 海口:2004年水协净水专业委员会年会议文集. 1-4 |
| [${referVo.labelOrder}] | 罗凡, 董滨, 何群彪. 2010. 饮用水消毒技术的应用及其研究进展[J]. 环境科学与技术, 2010, 33(12F) : 393–396. |
| [${referVo.labelOrder}] | Munch J W, Hautman D P. 1995. Determination of chlorination disinfection by products, chlorinated solvents, and halogenated pesticides/herbicides in drinking water by liquid-liquid extraction and gas chromatography with electron-capture detection (Revision 1.0)[R]. Office of Research and Development, Washington, DC.1-45 |
| [${referVo.labelOrder}] | Osano O, Admiraal W, Klamer H J C, et al. 2002. Comparative toxic and genotoxic effects of chloroacetanilides, formamidines and their degradation products on Vibrio fischeri and Chironomusriparius[J]. Environmental Pollution, 119(2) : 195–202. DOI:10.1016/S0269-7491(01)00334-7 |
| [${referVo.labelOrder}] | Raveendran R, Chatelier B, Williams K. 2002. Oxidation of manganese in drinking water systems using potassium permanganate[J]. Water Supply, 2(5/6) : 173–178. |
| [${referVo.labelOrder}] | Rook J J. 1974. Formation of haloforms during chlorination of natural waters[J]. Water Treatment and Examination, 23 : 234–243. |
| [${referVo.labelOrder}] | 孙兴滨, 卢颖, 孙雷, 等. 2013. 摇蚊幼虫代谢产物生成氯化消毒副产物的特征[J]. 北京工业大学学报, 2013, 39(11) : 1713–1703. |
| [${referVo.labelOrder}] | Watts M M, Pascoe D. 1996. Use of the freshwater macroinvertebrate Chironomus riparius (Diptera:Chironomidae) in the assessment of sediment toxicity[J]. Water Science and Technology, 34(7) : 101–107. |
| [${referVo.labelOrder}] | 谢鹏超, 岳思阳, 邹景, 等. 2015. 四种预氧化方式对AOC及消毒副产物影响的对比[J]. 中国给水排水, 2015, 31(7) : 6–9. |
| [${referVo.labelOrder}] | 熊金林, 梅兴国, 胡传林. 2003. 不同污染程度湖泊底栖动物群落结构及多样性比较[J]. 湖泊科学, 2003, 15(2) : 160–168. |
| [${referVo.labelOrder}] | Yang X, Shang C, Westerhoff P. 2007. Factors affecting formation of haloacetonitriles, haloketones, chloropicrin and cyanogen halides during chloramination[J]. Water Research, 41(6) : 1193–1200. DOI:10.1016/j.watres.2006.12.004 |
| [${referVo.labelOrder}] | 叶少帆, 王志伟, 吴志超. 2010. 微污染水源水处理技术研究进展和对策分析[J]. 水处理技术, 2010, 36(6) : 22–28. |
| [${referVo.labelOrder}] | 张锦, 李圭白, 马军. 2003. 高锰酸钾复剂对给水处理中混凝的强化效应[J]. 工业用水与废水, 2003, 34(3) : 12–14. |
| [${referVo.labelOrder}] | 张永吉, 周玲玲, 李伟英, 等. 2009. 高锰酸盐复合剂强化混凝对水中天然有机物的去除机制研究[J]. 环境科学, 2009, 30(3) : 761–764. |
| [${referVo.labelOrder}] | 赵玉丽, 李杏放. 2011. 饮用水消毒副产物, 化学特征与毒性[J]. 环境化学, 2011, 30(1) : 20–33. |
| [${referVo.labelOrder}] | 周令, 张金松. 2003. 净水工艺中红虫污染治理的研究动态[J]. 给水排水, 2003, 29(1) : 25–28. |
 2017, Vol. 37
2017, Vol. 37


