2. 上海市青浦区环境保护局, 上海 201703;
3. 上海市浦东新区环境保护监测站, 上海 201200
2. Shanghai Qingpu District Environmental Protection Bureau, Shanghai 201703;
3. Shanghai Pudong New District Environmental Protection Monitoring Station, Shanghai 201200
合成麝香是生活污水排放的主要标志物之一.合成麝香具有亲脂憎水性,被作为香味成分普遍添加于个人护理用品中,由于连续使用和排放,合成麝香广泛存在于水体、沉积物、室内灰尘等各类环境介质中,被称为“类持久性”有机污染物(Rimkus,1999).比较常见的化合物包括佳乐麝香(1,3,4,6,7,8-六氢-4,6,6,7,8,8-六甲基环五-γ-2-苯并吡喃,HHCB)、吐纳麝香(7-乙酰基-1,1,3,4,4,6-六甲基-1,2,3,4-四氢化萘,AHTN)、二甲苯麝香(2,4,6-三硝基-1,3-二甲基-5-叔丁基苯,MX)、酮麝香(4-叔丁基-3,5-二硝基-2,6-二甲基苯乙酮,MK)和大环麝香中的麝香酮(3-甲基环十五烷酮,Muscone)等(Lu et al.,2011).这些物质通常被用于调配各种类型香气添加至个人护理用品中.
合成麝香在个人护理用品使用后可通过清洗过程随生活污水排入环境,引起水环境的污染(Buerger et al.,2003).研究报道,北京某污水处理厂的出水和污泥中合成麝香的污染浓度分别为30.4~686.0 ng·L-1和14.3~195.0 ng·g-1(Hu et al.,2011a);海河的HHCB检出浓度大约为3.5~32.0 ng·L-1,沉积物为1.5~32.3 ng·g-1干重(Hu et al.,2011b).流经城市的河流污染浓度偏高,接纳污水比例高的河流污染水平较重,湖泊的污染情况相对较轻(Quednow et al.,2008).Peck等(2006)对美国爱荷华州的五大湖水体研究发现,表层水中HHCB和AHTN浓度为100~500 ng·L-1.欧洲和北美地区的合成麝香污染水平与中国长三角相当,但国外使用香味个人护理用品频率高于中国大部分地区,某些结果会高于一些受纳生活污水较少的中国河流(Zhang et al.,2008).污染物组成和该地区个人护理用品的加香方式有关,大多以多环麝香中的HHCB为主.中国海河有硝基麝香MX和MK检出的报道(Hu et al.,2011b).Biselli等(2004)在水生生物鳗鱼、贻贝等体内检测到HHCB和它的环境转化物质,说明合成麝香这一类亲脂性物质(logKow为5.4~6.3)在生物体中存在也很普遍.它们在人体血液和脂肪组织中也有广泛发现(Kannan et al.,2005).少数地区水体中HHCB浓度有逐年升高的趋势.
淀山湖位于苏浙沪3地交界处,属于城市近郊的小型天然湖泊.湖面东西宽9 km,南北长18 km,面积62 km2,兼具调节径流、农田灌溉、养殖、风景旅游等多项功能,也曾作为水源地提供水源.淀山湖主要收纳太湖流域来水,沿湖流入的河流众多,出水则主要经黄浦江流入长江口至东海.随着城市的外扩和城市人口增加,淀山湖周边地区土地也由原来的农业用途逐渐转变为旅游和生活居住使用.有必要深入研究这类城市近郊湖泊在转型期的污染变化特点,探讨生活污染源对城市近郊湖泊的影响特性,为湖泊水环境研究积累更多基础数据.本文拟通过对淀山湖水体、沉积物和鱼体中合成麝香分析,研究它们的污染状况和时空分布特点,并进行人体暴露量的初步评估.
2 材料与方法(Materials and methods) 2.1 实验材料与仪器合成麝香标样包括5种多环麝香: HHCB、AHTN、粉檀麝香(1,1,2,3,3,6-六甲基-5-乙酰基茚满,AHMI)、萨利麝香(l,1-二甲基-4-乙酰基-6-叔丁基茚满,ADBI)和特拉斯(1,1,2,6-四甲基-3-异丙基-5-乙酰基-茚满,ATII); 2 种硝基麝香: MX和MK.HHCB、AHTN、ADBI、AHMI、ATII、MX、MK和回收率指示物d3-AHTN均购自德国Dr. Ehrenstorfer公司,HHCB 纯度为75%,其余标样纯度大于99%.内标六甲基苯购自德国Dr. Ehrenstorfer公司,纯度为99%;Bio-Beads S-X3 购自美国Bio-Rad公司;硅胶(80~200 目)购自青岛海洋化工有限公司.正己烷、二氯甲烷、丙酮和氧化铝均为分析纯,购于上海国药集团化学试剂有限公司,所有有机试剂均经全玻璃溶剂重蒸系统处理后使用.硅胶和中性氧化铝用二氯甲烷索氏抽提72 h,溶剂挥发后分别于180和250 ℃烘干12 h,以3%纯水去活化,平衡12 h后浸于正己烷中待用.无水硫酸钠于450 ℃灼烧6 h,冷却后待用.
2.2 采样在淀山湖共设置16个采样点,于2010-2011年间分3次(7月、11月和次年3月)采集表层水和沉积物样品各48个,采样点位置如图 1所示.采样时用采水器采集表层水5 L,同时用抓斗采泥器收集该采样点的表层沉积物,保存于密实袋中.在湖区采集野生鱼类,采集的品种为中国花鲈(Lateolabrax japonicus,n=5)、花鱼骨(Hemibarbus maculatus,n=5)、黄顙鱼(Pelteobagrus fulvidraco,n=5)、青梢红鲌(Erythroculter dabryi,n=5)、泥鳅(Oriental weather fish,n=5)、刀鲚(Coilia mystus,n=5)、团头鲂(Megalobrama amblycephala,n=2)、鳙鱼(Aristichys nobilis,n=3)、鲢鱼(Hypophthalmichthys molitrix,n=3)、鲤鱼(Cyprinus carpio,n=3)、青鱼(Mylopharyngo don piceus,n=1),共计42个鱼样.
 |
| 图 1 淀山湖采样位置分布示意图 注:S1#(31°11′13.6″N,120°58′53.3″E)、 S2#(31°08′35.4″N,120°55′13.2″E)、 S3#(31°07′05.1″N,120°54′28.8″E)、 S4#(31°06′46.3″N,120°55′12.3″E)、 S5#(31°05′17.8″N,120°54′29.1″E)、 S6#(31°05′02.2″N,120°54′12.0″E)、 S7#(31°06′02.9″N,120°59′09.4″E)、 S8#(31°05′33.4″N,120°58′30.9″E)、 S9#(31°05′24.7″N,120°58′38.2″E)、 S10#(31°09′52.6″N,120°58′20.9″E)、 S11#(31°08′01.6″N,120°58′00.6″E)、 S12#(31°07′26.8″N,121°00′05.3″E)、 S13#(31°06′14.6″N,120°56′08.8″E)、 S14#(31°05′10.0″N,120°55′27.9″E)、 S15#(31°06′26.7″N,120°59′51.4″E)、 S16#(31°04′55.6″N,120°56′27.6″E) Fig. 1 Sampling locations at the Dianshan Lake |
取5 L表层水样,用0.45 μm玻璃纤维滤膜分离水相和悬浮颗粒,分别进行分析,分析结果合并作为水样污染浓度.
水相中加入回收率指示物d3-AHTN,用二氯甲烷进行液液萃取,萃取液合并浓缩后用硅胶/氧化铝复合柱(2∶1)分离净化.分别收集80 mL正己烷/二氯甲烷淋洗液(V/V=7/3)和50 mL正己烷/二氯甲烷淋洗液(V/V=1/5),浓缩氮吹定容后,加入内标化合物六甲基苯,保存待GC-MS分析.
将分离后的悬浮物冷冻干燥后加入回收率指示物d3-AHTN,用二氯甲烷进行索氏抽提.抽提液浓缩后用硅胶/氧化铝复合柱(2∶1)分离净化.分离净化和定容过程同水相.
沉积物样品冷冻干燥后研细过筛.称取约5 g样品,加入回收率指示物d3-AHTN后进行索氏抽提,收集抽提液并浓缩,分离净化步骤同悬浮物.
新鲜鱼样采集后取可食用的肉质部分粉碎并冷冻干燥.中国花鲈、花鱼骨、黄顙鱼、青梢红鲌、泥鳅、刀鲚分析数条鱼肉的合并样;团头鲂、鳙鱼、鲢鱼、鲤鱼、青鱼分析单独样,取各单独样分析结果的数学平均值作为该鱼种的污染浓度.分析时称取4 g的干燥鱼肉,用正己烷/丙酮(V/V=1/1)进行索氏抽提.浓缩干燥后重量法测定脂肪含量.将脂肪溶解后经凝胶渗透色谱柱(30 g Bio-beads S-X3)去除脂肪.淋洗液浓缩后用硅胶-氧化铝复合柱进行净化.分离净化步骤同悬浮物.
2.4 仪器分析采用GC-MS分析合成麝香,色谱柱DB-5MS 毛细管柱(30 m × 0.25 mm × 0.25 μm);载气为高纯氦,流速为1.0 mL·min-1.无分流手动进样,进样量为1 μL;进样口温度为290 ℃;柱始温为80 ℃,8 ℃·min-1升至160 ℃并保持1 min,4 ℃·min-1升至175 ℃并保持2 min,3 ℃·min-1升至184 ℃,4 ℃·min-1升至240 ℃.采用EI轰击源,离子源温度200 ℃;选择性离子扫描模式检测;目标化合物通过特征离子和标样保留时间比较定性.定性特征离子(m/z)为:ADBI 229、173、187;AHMI 229、244;ATII 215、258、173;HHCB 243、258、213;AHTN 243、258、159;MK 279、294;MX 282、297;d3-AHTN 246、261;定量特征离子为ADBI 229;AHMI 229;ATII 215;HHCB 243;AHTN 243;MK 279;MX 282.
2.5 质量保证和质量控制在每批次检测中(12个样品)均加入空白、空白加标和基质加标实验以进行质量控制.空白实验时不加样本并重复全部处理过程,分析结果(试剂空白)作为该批次的背景空白;基质加标实验时用超净水、未检测出目标化合物的沉积物样本以及色拉油作为基质进行全流程处理.
仪器检出限(LOD)以低浓度标样响应值标准偏差的3.36倍计算,定量检出限LOQ是LOD的2倍.若化合物有空白值则样品检出浓度为空白值浓度3倍以上作为定量检出,样品最终浓度均相应减去该批次分析时的空白值.表层水和沉积物中合成麝香检测限分别为0.01×10-3 ng·L-1和0.01×10-3 ng·g-1(干重).HHCB存在背景空白,表层水中空白值为0.062 ng·L-1,沉积物中空白值为0.069 ng·g-1干重,鱼肉中空白值为0.086 ng·g-1脂重.表层水、沉积物和鱼肉样品测定的回收率指示物d3-AHTN回收率为63.4%~102.4%、68.5%~105.0%和51.4%~87.7%;空白加标中目标化合物回收率分别为89.2%~109.1%,102.2%~122.1%和104.5%~112.9%;基质加标样品中目标化合物回收率为71.5%~111.4%、84.0%~106.6%和84.7%~105.8%.
统计分析时浓度在LOD和LOQ之间的以1/2LOQ作为实际浓度,<LOD的样品,浓度为0.使用SPSS 19进行统计分析,统计学显著性为p<0.05.
2.6 暴露量评估计算方法人体暴露的计算方法如下:

|
(1) |
式中,DUfish为饮食摄入量(ng·d-1·kg-1体重);C为鱼肉中污染物的浓度(ng·g-1),等于污染物脂重浓度(ng·g-1)乘脂肪含量,鱼肉脂肪含量取本次测定的鱼肉脂肪平均值2%;W1为平均日摄入鱼虾量(g),成人摄取量以29.6 g计(环境保护部,2013);A为饮食暴露摄取率,以44%计(Yu et al.,2012);BW为单位体重(kg),成人以60.6 kg计(环境保护部,2013).
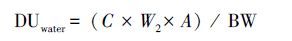
|
(2) |
式中,DUwater为饮水摄入量(ng·d-1·kg-1体重);C为水体的污染物浓度(ng·L-1);W2为日均直接饮水量(L),上海城乡地区成人饮水量以2.073 L计(环境保护部,2013);A为饮水暴露摄取率,以100%计(段小丽等,2011);BW为单位体重(kg),同上.
3 结果(Results) 3.1 合成麝香的浓度水平淀山湖表层水、沉积物和鱼肉样本中普遍存在合成麝香,如表 1所示,主要包括多环麝香HHCB和AHTN,以及硝基麝香MX和MK,这些污染物的检出率均为100%.多环麝香AHMI和ATII在表层水、沉积物和鱼肉样本中均有检出,但都低于定量检出限;ADBI在表层水和沉积物中也都低于定量检出限,12个鱼肉样本中仅1个存在低浓度的ADBI.
| 表 1 淀山湖各类介质中合成麝香的浓度 Table 1 The concentrations of synthetic musks in different samples from Dianshan Lake |
作为城市近郊的湖泊,淀山湖水环境也不可避免受到生活污染的影响.合成麝香的表层水年均浓度为12.7 ng·L-1.沉积物和鱼肉中也有一定量的合成麝香,平均浓度为1.11 ng·g-1干重和135 ng·g-1脂重.多环麝香总浓度(ΣPMs)在鱼肉、表层水和沉积物3类介质的浓度变化为14.0~264.0 ng·g-1脂重,2.80~26.00 ng·L-1和0.31~2.81 ng·g-1干重.
3.2 污染物的组成分布特征和时空分布特点合成麝香污染物浓度百分比组成如图 2所示,不同介质的污染物浓度百分比组成情况比较相似,3种介质中的主要污染物均为HHCB.在表层水和沉积物中,HHCB占总浓度的81%和94%;鱼肉样本中所占的浓度百分比也超过了80%.这说明国内目前个人护理用品的主要添香化合物为HHCB.3类介质中硝基麝香(MX+MK)的浓度百分比为3%~8%,沉积物和鱼肉中硝基麝香的浓度百分比略低.
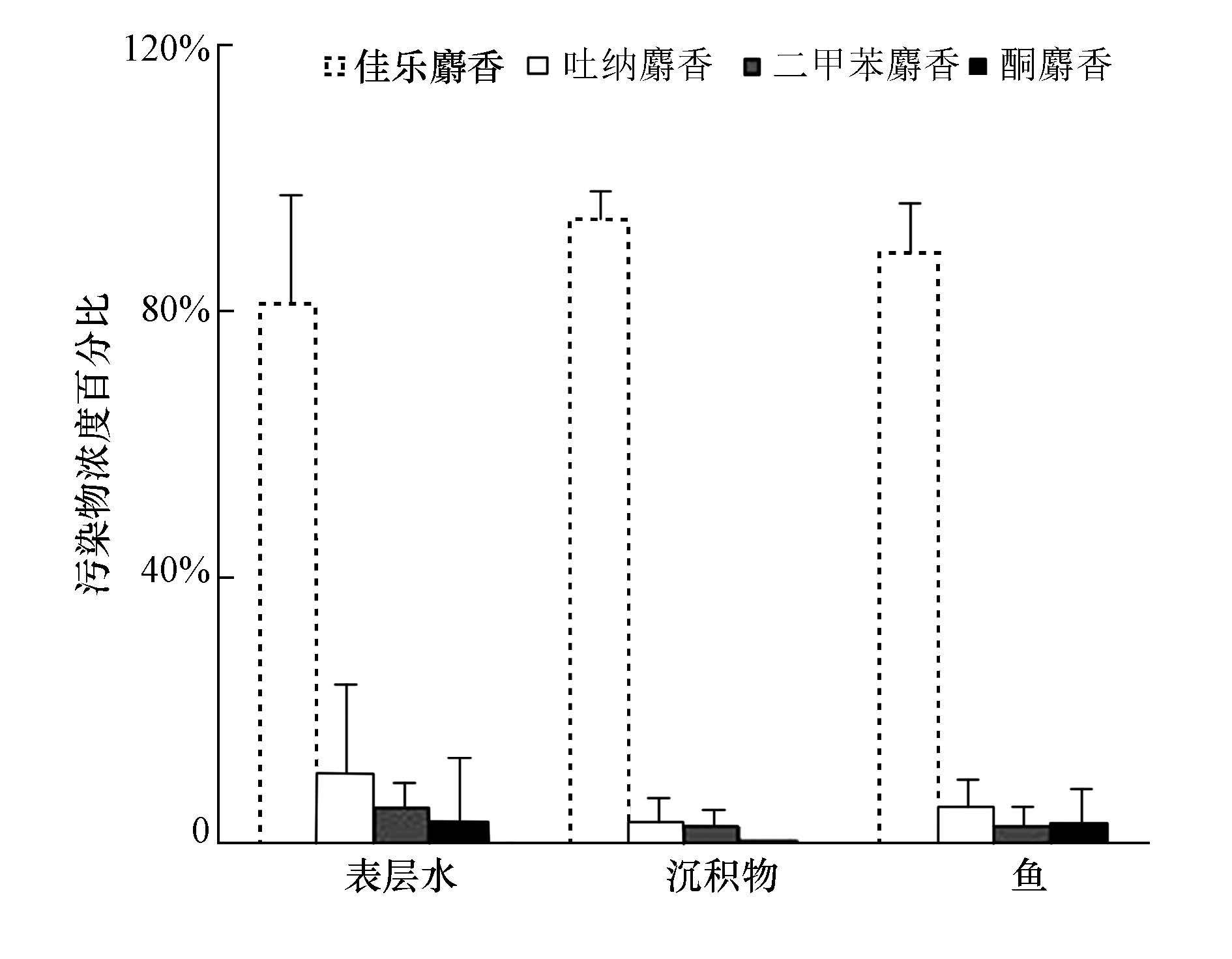 |
| 图 2 不同合成麝香的浓度分布特征 Fig. 2 The concentration distribution characteristics of synthetic musks |
比较不同采样时间的污染物浓度后发现(图 3),7月(丰水期)水体合成麝香浓度显著低于3月(平水期)和10月(枯水期)(Mann-Whitney U检验,p=0.000,p<0.05).平水期和枯水期的合成麝香浓度则没有明显的统计学差异(Mann-Whitney U检验,p=0.498,p>0.05).沉积物的污染水平随采样时间的变化不十分明显,平水期浓度和丰/枯水期浓度并没有统计学意义的差异(Mann-Whitney U检验,p=0.052~0.113,p>0.05);丰水期浓度略高于枯水期水平(Mann-Whitney U检验,p=0.000,p<0.05).
 |
| 图 3 合成麝香的时间分布特征 Fig. 3 The temporal distribution characteristics of synthetic musks |
将采样点分为进水区域(采样点S1#~S6#)和出水区域(采样点S7#~S9#),比较污染物的空间分布特点.结果表明,水体中合成麝香的浓度均为进水>出水,2组区域的浓度差比较明显(图 4).沉积物中合成麝香的污染水平也是进水>出水.进水区域的合成麝香平均浓度比出水区域高1~2倍.这说明淀山湖上游来水有相对较高的合成麝香,会对淀山湖湖区产生一定负面影响.
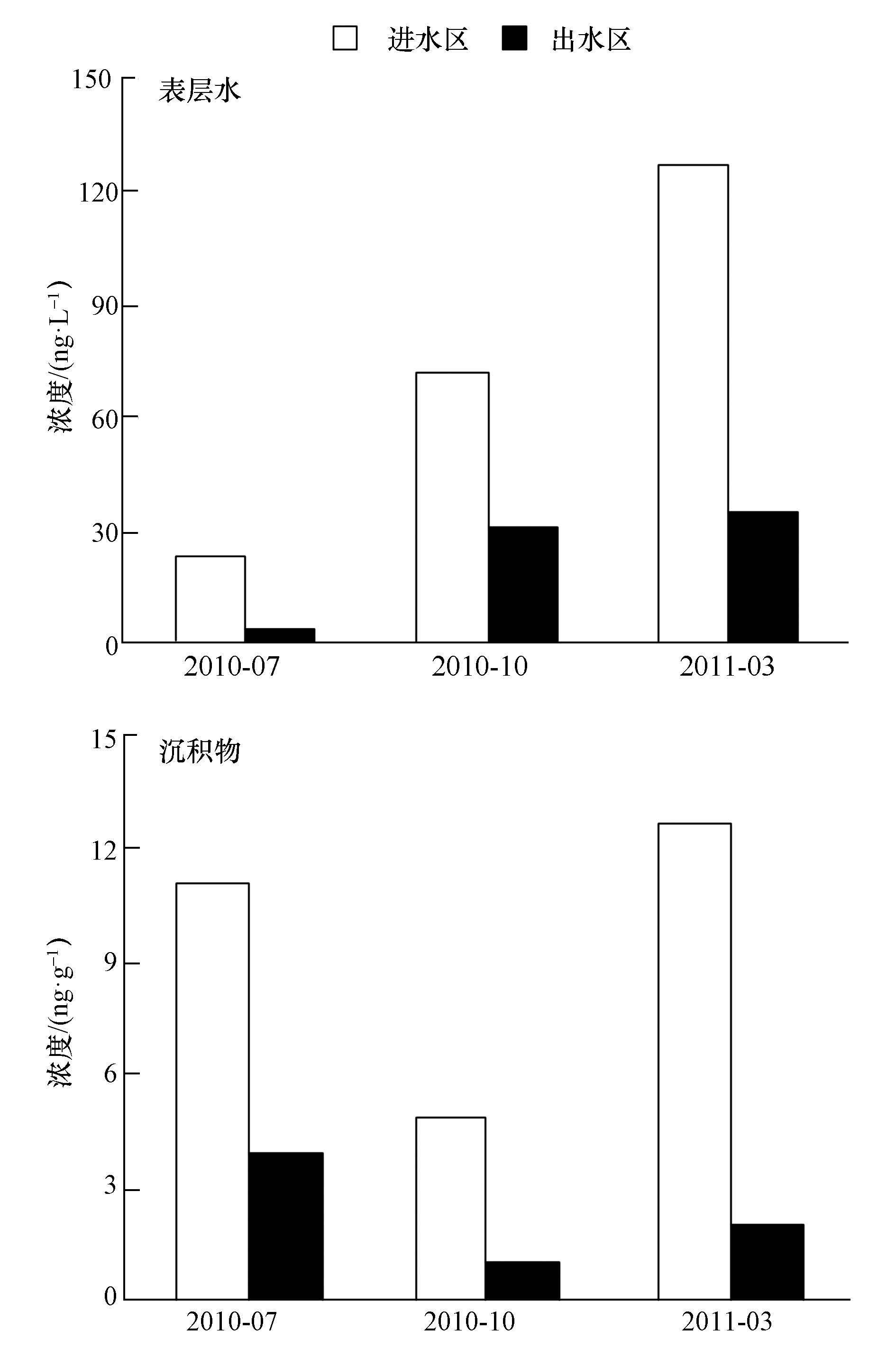 |
| 图 4 表层水和沉积物中合成麝香的空间分布特征 Fig. 4 The spatial distribution characteristics of synthetic musks in surface water and sediments |
水体环境中的合成麝香主要来源于生活污水的排放.直接排放的生活污水中常含有较高浓度的合成麝香(Hu et al.,2011a),经污水处理厂处置后的生活污水也仍有一定浓度的合成麝香存在,排放后影响接纳污水的河流湖泊.受纳水体的合成麝香污染水平与其接纳的生活污水总量以及污水处理方式等有关(马莉等,2014).相对来说,淀山湖水体的合成麝香污染水平并不高.表层水合成麝香浓度约为美国Michigan湖的5倍( et al,2004),和美国Hudson河的污染浓度在同一数量级(Zhi et al.,2007),但低于韩国河流的表层水污染浓度( et al,2013).沉积物中的浓度是德国Lippe河污染水平的1/10(Kronimus et al.,2004),也低于松花江的污染值(Lu et al.,2015).与流经上海市区的苏州河污染情况相比,淀山湖的合成麝香水体浓度是它的1/2(Wang et al.,2010).淀山湖作为上海曾经的水源地之一,水体生态环境得到较好的保护,生活污水的处理排放得到有效的控制.
多环麝香HHCB是水体、沉积物和鱼3类介质中主要的合成麝香类污染物,水体中也有相当浓度的硝基麝香MX和MK存在.说明淀山湖周边地区个人护理用品中麝香类物质的使用模式是以多环麝香HHCB为主,辅助添加少量硝基麝香(Zhang et al.,2008).Lu等(2011)曾分析了158种个人护理品中的合成麝香浓度,发现80%的样品都添加了一种以上的合成麝香,添加物质以HHCB为主,浓度约占合成麝香总浓度的52%.
受到合成麝香排放情况和迁移转化行为的直接影响,淀山湖表层水的合成麝香污染水平随采样时间而波动的特点较明显.夏季生活用水量增加,污水排放量及合成麝香排放总量相应增大.但夏季气温较高,增大了水环境中合成麝香的挥发量.Peck等(2004)通过通量计算提出大气挥发是Michigan湖水体合成麝香去除的一个主要机制.夏季处于丰水期,期间大量降水也对水体浓度起到稀释作用,可以降低表层水的污染水平.此外,夏季太阳辐射的加强也会提高光降解程度,降低表层水的污染浓度(Rubinfeld et al.,2008).上述原因可能导致淀山湖夏季表层水中合成麝香浓度的下降.合成麝香的半衰期较短,沉积物污染水平随时间累积增加的幅度不明显,平水期浓度和丰/枯水期的浓度相差不多.但短时污染水平也可能受到排放量等的直接影响,丰水期悬浮颗粒物可能吸附较高浓度的合成麝香污染物,迅速沉降后相应增大了该时间段沉积物的污染程度.
Pedersen等(2009)曾研究了HHCB对底栖生物新西兰泥螺(Potamopyrgus antipodarum)的慢性毒性效应,提出了1.0 mg·kg-1干重的无观察效应浓度(no observed effect concentration,NOEC).淀山湖沉积物的HHCB浓度远小于该NOEC值,不会对底栖生物产生明显的生态影响.利用检测数据和文献结果对非职业暴露人群的暴露量进行了评估,主要考虑的污染物为HHCB,考虑的暴露途径包括饮食摄入、呼吸吸入和皮肤渗透.饮食摄入分别考虑了水产品食用和饮水的影响;呼吸吸入主要考虑室内灰尘吸入的影响;皮肤渗透则包括个人护理用品使用所带来的影响,其中个人护理用品的使用以及呼吸吸入的暴露数据分别来自于文献(Liu et al.,2013;Nakata et al.,2015).结果表明,食物摄入(食鱼+饮水)的HHCB暴露量仅为0.90 ng·d-1·kg-1体重.考虑到饮用水处理过程也会对源水中的HHCB产生一定去除率,实际的食物摄入暴露量还会更小.个人护理用品使用后通过皮肤接触途径的HHCB暴露量为6.5 μg·d-1·kg-1体重(Nakata et al.,2015);呼吸吸入量为0.16 ng·d-1·kg-1体重(Liu et al.,2013).从以上数据比较可以看出,饮食途径产生的暴露量极小,皮肤接触是HHCB进入人体的最主要途径.这和许多文献的研究结果是一致的(Zhang et al.,2011).
5 结论(Conclusions)1) 淀山湖受到了合成麝香的污染,但总体污染水平较低.HHCB是主要的合成麝香类污染物.
2) 表层水浓度受采样时间的影响显著,丰水期的表层水合成麝香浓度偏低;沉积物的污染水平变化不十分明显,整体的时间积累性较弱.
3) 人体暴露评估表明,经食物摄入(饮食、饮水)途径产生的暴露量显著低于使用性皮肤接触途径的暴露量.
| [${referVo.labelOrder}] | Biselli S, Gatermann R, Kallenborn R, et al. 2004. Biotic and abiotic transformation pathways of synthetic musks in the aquatic Environment[M]. : 189–211. |
| [${referVo.labelOrder}] | Buerge I J, Buser H R, Müller M D, et al. 2003. Behavior of the polycyclic musks HHCB and AHTN in lakes, two potential anthropogenic markers for domestic wastewater in surface waters[J]. Environmental Science & Technology, 37(24) : 5636–5644. |
| [${referVo.labelOrder}] | Dirtu A C, Adrian C. 2010. Estimation of daily intake of organohalogenated contaminants from food consumption and indoor dust ingestion in Romania[J]. Environmental Science & Technology, 44(16) : 6297–6304. |
| [${referVo.labelOrder}] | 段小丽, 王宗爽, 李琴, 等. 2011. 基于参数实测的水中重金属暴露的健康风险研究[J]. 环境科学, 2011, 32(5) : 1329–1339. |
| [${referVo.labelOrder}] | Hu Z, Shi Y, Zhang S, et al. 2011a. Assessment of synthetic musk fragrances in seven wastewater treatment plants of Beijing, China[J]. Bulletin of Environmental Contamination & Toxicology, 86(3) : 302–306. |
| [${referVo.labelOrder}] | Hu Z, Shi Y, Cai Y. 2011b. Concentrations, distribution and bioaccumulation of synthetic musks in the Haihe River of China[J]. Chemosphere, 84(11) : 1630–1635. DOI:10.1016/j.chemosphere.2011.05.013 |
| [${referVo.labelOrder}] | 环境保护部编著. 2013. 中国人群暴露参数手册(成人版)[M]. 北京: 中国环境出版社 . |
| [${referVo.labelOrder}] | Kannan K, Reiner J L, Yun S H, et al. 2005. Polycyclic musk compounds in higher trophic level aquatic organisms and humans from the United States[J]. Chemosphere, 61(5) : 693–700. DOI:10.1016/j.chemosphere.2005.03.041 |
| [${referVo.labelOrder}] | Kronimus A, Schwarzbauer J, Dsikowitzky L, et al. 2004. Anthropogenic organic contaminants in sediments of the Lippe river, Germany[J]. Water Research, 38(16) : 3473–3484. DOI:10.1016/j.watres.2004.04.054 |
| [${referVo.labelOrder}] | Lee I S, Kim U J, Oh J E, et al. 2013. Comprehensive monitoring of synthetic musk compounds from freshwater to coastal environments in Korea:With consideration of ecological concerns and bioaccumulation[J]. Science of the Total Environment, 470-471(2) : 1502–1508. |
| [${referVo.labelOrder}] | Liu N, Shi Y, Xu L, et al. 2013. Occupational exposure to synthetic musks in barbershops, compared with the common exposure in the dormitories and households[J]. Chemosphere, 93(9) : 1804–1810. DOI:10.1016/j.chemosphere.2013.06.027 |
| [${referVo.labelOrder}] | Lu B, Feng Y, Gao P, et al. 2015. Distribution and fate of synthetic musks in the Songhua River, Northeastern China:influence of environmental variables[J]. Environmental Science & Pollution Research, 22(12) : 1–10. |
| [${referVo.labelOrder}] | Lu Y, Yuan T, Wang W, et al. 2011. Concentrations and assessment of exposure to siloxanes and synthetic musks in personal care products from China[J]. Environmental Pollution, 159(12) : 3522–3528. DOI:10.1016/j.envpol.2011.08.015 |
| [${referVo.labelOrder}] | 马莉, 敬烨, 周静, 等. 2014. 太湖梅梁湾水体合成麝香的分布特征[J]. 环境化学, 2014, 33(4) : 630–635. |
| [${referVo.labelOrder}] | Nakata H, Hinosaka M, Yanagimoto H. 2015. Macrocyclic-, polycyclic-, and nitro musks in cosmetics, household commodities and indoor dusts collected from Japan:Implications for their human exposure[J]. Ecotoxicology and Environmental Safety, 111 : 248–255. DOI:10.1016/j.ecoenv.2014.09.032 |
| [${referVo.labelOrder}] | Peck A M, Hornbuckle K C. 2004. Synthetic musk fragrances in Lake Michigan[J]. Environmental Science & Technology, 38(2) : 367–372. |
| [${referVo.labelOrder}] | Peck A M, Hornbuckle K C. 2006. Synthetic musk fragrances in urban and rural air of Iowa and the Great Lakes[J]. Atmospheric Environment, 40(32) : 6101–6111. DOI:10.1016/j.atmosenv.2006.05.058 |
| [${referVo.labelOrder}] | Pedersen S, Selck H, Salvito D, et al. 2009. Effects of the polycyclic musk HHCB on individual-and population-level endpoints in Potamopyrgus antipodarum[J]. Ecotoxicology and Environmental Safety, 72(4) : 1190–1199. DOI:10.1016/j.ecoenv.2008.10.012 |
| [${referVo.labelOrder}] | Quednow K, Püttmann W. 2008. Organophosphates and synthetic musk fragrances in freshwater streams in Hessen/Germany[J]. Clean-Soil Air Water, 36(1) : 70–77. DOI:10.1002/(ISSN)1863-0650 |
| [${referVo.labelOrder}] | Rimkus G G. 1999. Polycyclic musk fragrances in the aquatic environment[J]. Toxicology Letters, 111(3) : 37–56. |
| [${referVo.labelOrder}] | Rubinfeld S A, Luthy R G. 2008. Nitromusk compounds in San Francisco Bay sediments[J]. Chemosphere, 73(6) : 873–879. DOI:10.1016/j.chemosphere.2008.07.042 |
| [${referVo.labelOrder}] | Wang F L, Zhou Y, Guo Y W, et al. 2010. Spatial and temporal distribution characteristics of synthetic musk in Suzhou Creek[J]. Journal of Shanghai University, 14(4) : 306–311. DOI:10.1007/s11741-010-0649-3 |
| [${referVo.labelOrder}] | Yu Y X, Pang Y P, Li C, et al. 2012. Concentrations and seasonal variations of polybrominateddiphenyl ethers (PBDEs) in in-and out-house dust and human daily intake via dust ingestion corrected with bioaccessibility of PBDEs[J]. Environment International, 42(4) : 124–131. |
| [${referVo.labelOrder}] | Zhang X L, Yu Y, Zeng X Y, et al. 2008. Synthetic musks in the aquatic environment and personal care products in Shanghai, China[J]. Chemosphere, 72(10) : 1553–1558. DOI:10.1016/j.chemosphere.2008.04.039 |
| [${referVo.labelOrder}] | Zhang X, Liang G, Zeng X, et al. 2011. Levels of synthetic musk fragrances in human milk from three cities in the Yangtze River Delta in Eastern China[J]. Journal of Environmental Sciences (China), 23(6) : 983–990. DOI:10.1016/S1001-0742(10)60506-2 |
| [${referVo.labelOrder}] | Zhi X, Ralf E, Christian T, et al. 2007. Air-sea exchange fluxes of synthetic polycyclic musks in the North Sea and the Arctic[J]. Environmental Science & Technology, 41(16) : 5654–5659. |
 2017, Vol. 37
2017, Vol. 37


