含氮硫有机废水如味精发酵废水、炼油废水、酒精废水和畜禽废水等,通常采用厌氧消化预处理去除大部分有机物并回收沼气.由此产生的消化液中含有大量的氮(主要为氨氮)和硫化物,需进一步脱氮脱硫; 所产生的沼气中含大量硫化氢,需在利用前脱硫.厌氧消化液脱氮与沼气脱硫具有电子互补性,可应用反硝化脱硫实现厌氧消化液脱氮与沼气脱硫的耦联,在沼气脱硫的同时,弥补消化液脱氮的电子供体不足(魏本平等,2014).但常规反硝化脱硫不能回收氮、硫污染物蕴含的化学能.近年出现的MFC可在去除污染物的同时,回收这些污染物蕴含的化学能,其在废水脱氮脱硫方面具有良好的发展前景(Rabaey et al.,2006; 毛艳萍等,2010; Clauwaert et al.,2007).
以MFC分别进行阳极脱硫或阴极脱氮已有许多报道,Rabaey等首次在MFC阳极实现了可溶性硫向元素硫的转化(Rabaey et al.,2006),毛艳萍等(2010)采用MFC处理模拟含硫废水,硫化物大部分转化为单质硫.Clauwaert等(2007)首先报告了不依靠外加电源的反硝化生物阴极MFC,其他研究者通过优化反应条件,如采用涂布聚四氟乙烯的碳纸代替昂贵的质子膜作为MFC间隔材料,改善了反硝化MFC的产电与脱氮效果(谢倍珍等,2014).将同时含有S2-与NO3-的废水注入非生物阴极MFC的阳极室,可在回收电能的同时实现脱氮与除硫(Cai et al.,2013; Lee et al.,2012),但由于反硝化与硫化物氧化都在阳极室完成,反硝化与阳极电极共同竞争S2-氧化所释放的电子,降低了产电能力,且非生物阴极以高锰酸钾或者铁氰化钾作为电子受体,易产生二次污染等问题.如以MFC同步阳极脱硫和阴极脱氮则可化解上述问题,但尚未见此类报道.
本研究构建以S2-为阳极电子供体和以NO3-为阴极电子受体的反硝化脱硫MFC,探讨同步废水阳极除硫与阴极脱氮并回收电能的可行性,为厌氧消化液脱氮与沼气脱硫提供新思路.
2 材料与方法(Materials and methods) 2.1 实验装置如图 1所示双室型反硝化脱硫MFC采用有机玻璃制作.阴阳极室尺寸均为12 cm×3 cm×10 cm,净容积(Net Contents,NC)为Vnet=150 cm3.阴阳极室以nafion117型质子交换膜分隔开,质子交换膜在使用前参照于景荣等(2001)的方法进行预处理.以石墨纤维丝作为阴阳极的电极材料,固定石墨纤维丝的铂丝通过铜导线与变阻箱连接,形成电流通路.
 |
| 图 1 MFC装置示意图 Fig. 1 Schematic diagram of MFC |
阴阳两极分别通过蠕动泵(BT100-1L,保定兰格)连续进水,控制水力停留时间为2.8 h.阴阳极液分别以蠕动泵(BT100-1L,保定兰格)进行循环,循环流量为20 mL·min-1,使得阴阳极液分别混合均匀.控制环境温度为(30±0.5)℃,外阻为R=100Ω.
2.2 模拟废水与接种废泥模拟废水基本营养盐: NaHCO3(0.5 g·L-1),MgCl2·2H2O(0.017 g·L-1),CaCl2(0.01 g·L-1),NH4Cl(0.01 g·L-1),1 mL·L-1微量元素溶液(Clauwaert et al.,2007).缓冲溶液: KH2PO4(2.65 g·L-1),Na2HPO4·12H2O(10.91 g·L-1).控制阴极进水NO3--N为17mg·L-1,以Na2S·9H2O向阳极提供S2-.
接种污泥取自武汉市龙王嘴污水处理厂,阳极接种污泥取自其厌氧池,阴极接种污泥取自其缺氧池.
2.3 试验方案阳极进水S2-设为120.2 mg·L-1,阴阳极石墨纤维丝先不接种污泥,运行7 d以分析无微生物参与时的反硝化脱硫可行性.随后取出两极石墨纤维丝分别在各自的接种污泥中浸泡24 h,富集微生物后再转入阴阳极室,在相同进水条件下继续运行反硝化脱硫MFC,直至电压和污染物去除稳定,即可认为MFC启动完成.将阳极进水S2-分别设定为55.6 mg·L-1、125.7 mg·L-1、185.1 mg·L-1、250.8 mg·L-1.在每个S2-下产电稳定后,通过稳态放电法拟合MFC极化曲线(梁鹏等,2007).每次稳定后,取样测定至少3 d的污染物去除数据.
2.4 测试与分析方法常规水质分析采用国家标准方法(国家环境保护总局,2002),S2-:对氨基二甲基苯胺光度法,SO42--S:离子色谱法(ICS-900,DIONEX,美国),NO3--N:紫外分光光度法,NO2--N:N-(1-萘基)-乙二胺光度法.采用扫描电子显微镜(SEM: JSM-5610LV,JEOL,日本)观察石墨纤维丝表面形态.
电化学特性测定与计算:输出电压U由数字万用表每4 min记录1次,电流I由欧姆定律计算,I=U/R,功率密度的计算:P=U2/(RVnet).
库伦效率: 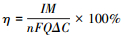
式中,F为法拉第常数(96485 C·mol-1); Q为阳极或阴极进水流量(L·s-1); M为硫的摩尔质量(32 g·mol-1)或氮的摩尔质量(14 g·mol-1); n为去除单位污染物所转移的电子数,计算阴极库伦效率时,n=5,计算阳极库伦效率时,假设S2-先全部转化为S0,然后S0再转化为SO42-,那么阳极实际氧化失电子量为上述两部分之和,公式中n·ΔC=n1·ΔC1+n2·ΔC2(n1=2,ΔC1为阳极进出水S2-浓度差(g·L-1),n2=6,ΔC2为阳极出进水SO42--S浓度差(g·L-1)).
3 结果与讨论(Results and discussion) 3.1 反硝化脱硫MFC的启动接种污泥前,MFC产生了较低的电压(约10 mV),阳极S2-大量被氧化,但阴极NO3-无去除,没有发生反硝化作用.微小的产电及S2-氧化是自发电化学作用的结果,但仅依靠自发电化学无法实现MFC的阴极脱氮.接种污泥后的前20 d,电压增长较为缓慢(图 2a),由最初的27.3 mV缓慢增长到78.9 mV,可能是由于大部分的电活性微生物还处于悬浮状态,并没有牢固地附着于石墨纤维丝上.随着电活性微生物的附着并富集,20 d后电压迅速爬升至176 mV左右趋于稳定.可见,MFC的产电是电化学作用与微生物作用共同作用的结果(Sun et al.,2009),但微生物作用对MFC产电起主导作用.本研究中以S2-为阳极唯一电子供体可稳定产电,说明电活性硫细菌可以依靠硫化物自养生存.
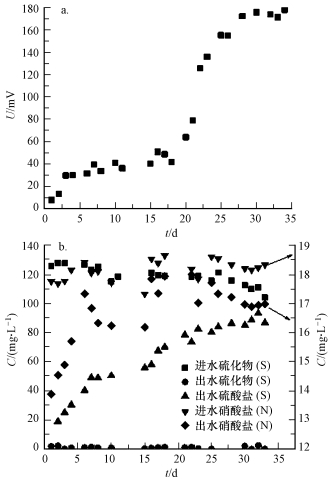 |
| 图 2 启动阶段(a)电压和(b)污染物浓度的变化 Fig. 2 Variations of (a) voltage and(b) pollutant concentrations during start-up stage |
如图 2b所示,尽管阳极中进水S2-浓度有所波动((118.9±14.7)mg·L-1),但出水S2-一开始均被氧化殆尽.接种污泥后,SO42-生成量在前7 d迅速上升到约50.0 mg·L-1,之后逐步上升至88.4 mg·L-1左右,SO42-(S)生成率达到82%.据报道,MFC阳极的S2-转化为S0可通过自发电化学作用和微生物作用共同实现,而S0进一步转化为SO42-则主要通过微生物作用完成(Sun et al.,2009).所以接种污泥后随着电活性微生物的富集,SO42-生成量逐步升高.
接种污泥后NO3-去除量先减小后增大,总体上波动不大.启动初期,阴极接种的污泥中含有部分异养反硝化菌及有机物,异养反硝化菌以有机物为电子供体去除NO3-,随着有机物消耗NO3-去除量减少.随着阳极提供的电子增多和阴极石墨纤维丝上电活性反硝化菌的富集,反硝化菌主要以阳极传递过来的电子进行反硝化,NO3-的去除量增大.实验发现出水NO2--N的浓度均低于0.01 mg·L-1,说明反硝化作用进行的较为完全.
接种污泥32 d后反硝化脱硫MFC的电压稳定在(176.0±6.9)mV,相应的S2-和NO3--N去除负荷分别为(0.94±0.04)kg·m-3NC·d-1和(11.1±0.6)g·m-3NC·d-1.阳极和阴极进水pH分别为7.0±0.03和6.9±0.04时,相应的出水pH分别为7.3±0.02和7.1±0.03.
3.2 进水S2-浓度对MFC性能的影响如图 3所示,进水S2-浓度分别为(55.6±0.6)mg·L-1、(125.7±0.7)mg·L-1、(185.1±0.7)mg·L-1、(250.8±1.3)mg·L-1时,最大体积功率密度分别为2.38 W·m-3NC、3.62 W·m-3NC、4.18 W·m-3NC、4.25 W·m-3 NC.反硝化脱硫MFC的产电能力随着阳极进水S2-浓度的增加逐渐增强,可能是因为随着阳极S2-浓度的增加,电活性微生物所能利用的S2-更加充足,电活性微生物的活性逐渐增强.但是S2-浓度从(185.1±0.7)上升到(250.8±1.3)mg·L-1时,最大功率密度仅增加了0.07 W·m-3NC,可能此时S2-浓度对阳极微生物的毒害作用的影响已经开始显现(Sun et al.,2009).Cai等(2013)以高锰酸钾为阴极电子受体,研究MFC阳极同时除硫与脱氮,在进水S2-浓度约60 mg·L-1时的最高电流密度为138.31 mA·m-2,如换算成体积功率密度约为0.45 W·m-3NC,低于本实验结果.导致不同产电能力的原因在于:Cai等(2013)采用的石墨棒电极的表面积低于
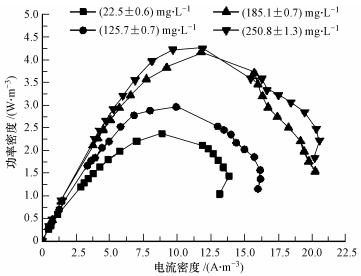 |
| 图 3 不同S2-浓度下的功率密度曲线 Fig. 3 Power density curves at different sulfide concentrations |
本实验所用的石墨纤维丝电极,会相应降低电子向阳极的传递速度; 另一主要原因是Cai等(2013)的研究中,NO3-和S2-同时存在于MFC阳极,相比于阳极电极而言NO3-是更好的电子受体,从而减少了S2-氧化所释放电子向阳极电极的传递量.其他研究者(Lee et al.,2012)也发现在MFC阳极脱硫时,如在阳极同时加入NO3-会降低其产电能力.
S2O32-、SO3-、S4O62-等是S不稳定的中间价态化合物,由于数次所测出水S2O32-的含量均在1 mg·L-1以下,故在计算S的生成率时忽略这些化合物.如表 1所示,在每个S2-浓度下,S2-的去除都比较彻底(去除率均高达97%),且大部分的S2-生成为SO42-(SO42-的生成率均超过65%),SO42-生成率随着S2-浓度升高而有小幅增加.与MFC阳极同时存在有机物和S2-时的情况相比(毛艳萍等,2010),本实验中S2-生成为S0,以及S0生成为SO42-的量都有大幅度增加.这是因为,当有机物和S2-共存于阳极时,两种电子供体的氧化存在竞争关系,抑制了S0和SO42-生成.实验发现阳极库伦效率偏低,其可能原因在于:阳极液中的S2-部分以H2S形式挥发去除或以硫化物沉淀形式去除; 未对进水采取严格的吹氮脱氧措施,阳极溶解氧也会部分消耗S2-氧化所释放的电子.
| 表 1 各S2-浓度下的MFC污染物去除性能 Table 1 Pollutant removal of MFC at different sulfide concentrations |
进水S2-浓度对NO3--N去除效果影响较小,NO3--N的去除负荷均在12 g·m-3NC·d-1左右.各S2-浓度下对应外阻为100Ω时的电流密度分别为11.9 A·m-3NC、13.0 A·m-3NC、15.7 A·m-3NC、15.5A·m-3NC,没有较大变化,与NO3--N去除负荷变化趋于一致.在以有机物为阳极电子供体的反硝化MFC的研究中(Li et al.,2013),外阻为100Ω时,电流密度为41.5A·m-3NC,相应的NO3--N去除负荷达57.0 g·m-3NC·d-1.相比之下,本研究的NO3--N去除负荷较低,但没有明显的NO2-积累,推测阴极反硝化作用较弱受制于较低的电流密度.阴极库伦效率均在200%以上,可能是由于阴极进水未采取严格除氧措施,阴极液中残存的溶解氧与NO3-共同作为电子受体消耗阳极传递来的电子,导致基于硝酸盐还原的阴极库伦效率计算值偏大.外阻较大(100Ω)时阴极液中溶解氧作为电子受体的作用较显著,而NO3--N去除量较小且变化不大; 因进水S2-浓度增加而引起的电流升高主要通过消耗更多的阴极溶解氧而实现,基于硝酸盐还原对MFC产电的贡献比变小,导致阴极库伦效率计算值随进水S2-浓度增加而增加(李金涛等,2012).
3.3 MFC阳极中的硫沉积MFC启动成功后,肉眼观察发现MFC阳极石墨纤维丝整体变白,推断是硫沉积在石墨纤维丝上的结果. SEM观察发现(图 4),MFC启动前,石墨纤维丝表面较为光滑,启动成功后阳极石墨纤维丝表面堆积有颗粒状物质,颗粒粒径约1~2μm,与其他研究者观察到的的生物硫粒形态相似(远野等,2014).
 |
| 图 4 MFC石墨纤维丝电镜照片;(a)空白石墨纤维丝, ×5000;(b)阳极石墨纤维丝, ×5000 Fig. 4 SEM images of graphite filament in the MFC; (a)control graphite filament, ×5000; (b) graphite filament in anode chamber, ×5000 |
通过拟合极化曲线欧姆损失段(图 5)的线性方程(梁鹏等,2007),可得各S2-浓度下MFC内阻分别为186.9Ω、189.19Ω、197.60Ω、191.52Ω.随着阳极进水S2-浓度的增加,溶液中离子浓度增加,导电能力增强,内阻理论上会有所降低,然而事实上内阻变化不大.可能是因为颗粒硫沉积导致电极表面有效面积变小,阻碍了电子向电极的传递过程(Liang et al.,2013),部分抵消了因离子浓度升高引起内阻减小的影响,因此阳极生成的颗粒硫沉积在石墨纤维丝上会影响MFC的内阻.
 |
| 图 5 各S2-浓度下的U-I曲线 Fig. 5 U-I curves at different sulfide concentrations |
1) 反硝化脱硫MFC同步阴极脱氮和阳极除硫是可行的,32 d成功启动了MFC,在外阻为100Ω时,电压稳定在(176.0±6.9)mV,S2-和NO3--N去除负荷分别为(0.94±0.04)kg·m-3NC·d-1和(11.1±0.6)g·m-3NC·d-1.
2) 反硝化脱硫MFC的产电能力随着阳极进水S2-浓度的增加逐渐增强,但是过高的S2-浓度可能产生抑制作用.在试验S2-浓度下,S2-去除较彻底,SO42-生成率随着S2-浓度升高而有小幅增加.S2-浓度变化对脱氮影响较小,NO3--N去除负荷均在12 kg·m-3NC·d-1左右.
3) 反硝化脱硫MFC阳极的石墨纤维丝上会沉积颗粒硫,进而降低电极的有效面积,使MFC的内阻升高,需定期清洗活化MFC阳极.
| [1] | Cai J, Zheng P, Zhang J, et al. 2013. Simultaneous anaerobic sulfide and nitrate removal in microbial fuel cell[J]. Bioresource Technology , 128 (1) : 760–764. |
| [2] | Clauwaert P, Rabaey K, Aelterman P, et al. 2007. Biological denitrification in microbial fuel cells[J]. Environmental Science & Technology , 41 (9) : 3354–3360. |
| [3] | 国家环境保护总局. 2002. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社 . |
| [4] | Lee C Y, Ho K L, Lee D J, et al. 2012. Electricity harvest from nitrate/sulfide-containing wastewaters using microbial fuel cell with autotrophic denitrifier, Pseudomonas sp. C27[[J]. International Journal of Hydrogen Energy , 37 (20) : 15827–15832. DOI:10.1016/j.ijhydene.2012.01.092 |
| [5] | Li J T, Zhang S H, Hua Y M. 2013. Performance of denitrifying microbial fuel cell subjected to variation in pH, COD concentration and external resistance[J]. Water Science & Technology , 68 (1) : 250–256. |
| [6] | 李金涛, 张少辉.2012. 反硝化微生物燃料电池的基础研究[J]. 中国环境科学 , 2012, 32 (4) : 617–622. |
| [7] | Liang F Y, Deng H, Zhao F. 2013. Sulfur Pollutants Treatment Using Microbial Fuel Cells from Perspectives of Electrochemistry and Microbiology[J]. Chinese Journal of Analytical Chemistry , 41 (8) : 1133–1139. DOI:10.1016/S1872-2040(13)60669-6 |
| [8] | 梁鹏, 范明志, 曹效鑫, 等.2007. 微生物燃料电池表观内阻的构成和测量[J]. 环境科学 , 2007, 28 (8) : 1894–1898. |
| [9] | 毛艳萍, 蔡兰坤, 张乐华, 等.2010. 微生物燃料电池处理模拟含硫废水的初步研究[J]. 水处理技术 , 2010, 36 (2) : 105–108. |
| [10] | Rabaey K, Van de Sompel K, Maignien L, et al. 2006. Microbial fuel cells for sulfide removal[J]. Environmental Science & Technology , 40 (17) : 5218–5224. |
| [11] | Sun M, Mu Z X, Chen Y P, et al. 2009. Microbe-Assisted Sulfide Oxidation in the Anode of a Microbial Fuel Cell[J]. Environmental Science & Technology , 43 (9) : 3372–3377. |
| [12] | 魏本平, 邓良伟, 陈子爱, 等.2014. 培养方式对废水脱氮与沼气脱硫污泥驯化影响[J]. 环境工程学报 , 2014, 8 (6) : 2237–2244. |
| [13] | 谢倍珍, 刘博杰, 杨少强, 等.2014. 生物阴极式碳纸隔膜微生物燃料电池的反硝化和产电性能[J]. 环境工程学报 , 2014, 8 (6) : 2163–2168. |
| [14] | 于景荣, 衣宝廉, 韩明, 等.2001. Nafion膜厚度对质子交换膜燃料电池性能的影响[J]. 电源技术 , 2001, 25 (6) : 384–386. |
| [15] | 远野, 王爱杰, 马素丽, 等.2014. 反硝化脱硫工艺中生物硫分布特征及分离方法[J]. 哈尔滨工业大学学报 , 2014, 46 (8) : 34–39. |
| [16] | Zhang B G, Zhou S G, Zhao H Z, et al. 2010. Factors affecting the performance of microbial fuel cells for sulfide and vanadium (V) treatment[J]. Bioprocess & Biosystems Engineering , 33 (2) : 187–194. |
 2016, Vol. 36
2016, Vol. 36


