苯酚(phenol)作为一种原生质毒物,对环境造成严重污染,长期饮用被苯酚污染的饮用水或食物,对人类的健康将造成极大的危害,苯酚对人体皮肤、粘膜有强烈的腐蚀作用,可抑制中枢神经或损害肝、肾功能,吸入高浓度蒸气可致头痛、头晕、乏力、视物模糊、肺水肿等(Ahmed et al.,2011;Jiang et al.,2013).因此,美国环保署把苯酚列入129种优先污染物和65种有毒污染物之列,中国也将苯酚列入环境优先处理的污染物“黑名单” 之中(Basha et al.,2010).
国内外苯酚主要的生产方式为氯苯水解法、苯磺酸钠碱熔法、异丙苯氧化法等,为了提高苯酚产量,常在生产过程中加入无机盐催化剂,并进行pH调节,此过程会使得体系中盐度增大,后期废水中不仅含有苯酚等有机污染物,也含有大量的盐分(Ca2+、Mg2+、Cl-、Na+)使废水难以处理(贺强礼等,2015a;Mollaei et al.,2010).目前含酚废水处理手段主要有两大类,即生物处理法和物理处理法(庞洁等,2010;Silva et al.,2013).由于生物处理法具有操作较简单、成本低廉、处理效果好、所需要的环境条件比较温和、对环境造成的二次污染很小等优点(贺强礼等,2014;Polymenakou and Stephanou,2005),已被广泛用于苯酚废水的处理之中.目前国内外学者在苯酚废水处理方面做了大量的研究,并筛选出多种具有良好苯酚降解效果的苯酚降解菌,但是这些菌耐盐能力弱,当酚类废水中盐度超过一定浓度,其生长以及降解苯酚的效果会受到严重影响.利用耐盐高效苯酚降解菌株对苯酚进行降解,不仅可以有效的降解废水中的苯酚,也解决了一般菌株在高盐条件下难以降解苯酚的难点.另外,对微生物苯酚降解效果产生影响的因素较多,传统的单因素实验难以区分各个因素之间的主次(Tsai and Li,2007;贺强礼等,2015b),所以寻求耐盐高效苯酚降解菌及其最佳降解条件具有重要意义.
本实验以海利(常德)有限公司废水处理池中提取的水样为菌源,通过筛选、分离、驯化得到在高盐条件下以苯酚为唯一碳源能源的苯酚降解菌,经耐盐和苯酚降解能力测定,得到耐盐高效苯酚降解菌zhtI.对耐盐高效苯酚降解菌zhtI菌落形态、菌体特征、生理生化反应、16S rRNA序列分析确定菌株的种属,利用响应面法(RSM)进行优化处理从而提高苯酚降解菌zhtI的降解效率,并对耐盐高效苯酚降解菌zhtI进行降酚动力学研究,研究结果将为生物法处理苯酚废水提供新的技术思路.
2 材料与方法(Materials and methods) 2.1 样品来源及耐盐高效苯酚降解菌的分离与纯化以海利(常德)有限公司苯酚废水处理池所取水样作为筛选苯酚降解菌株的菌源.通过逐渐提高苯酚浓度的驯化方法,将水样样品按2% 的接种量接种于以100 mg · L-1苯酚为唯一碳源,盐度2%的无机盐培养基中;温度30 ℃、摇床转速200 r· min-1,好氧培养2 d 后,以2%接种量转接至苯酚浓度为200 mg·L-1,盐度2%的无机盐培养基中,继续培养,直到苯酚浓度达到1000 mg·L-1;然后进行平板涂布,将培养皿放于30 ℃恒温培养箱中培养72 h,挑取单菌落,转接至苯酚浓度1000 mg·L-1,盐度2%的无机盐培养基中;经反复平板涂布,最后筛选出具有耐盐高效苯酚降解能力的菌株,保存在盐度2%,苯酚浓度为100 mg·L-1的LB固体培养基上.
2.2 培养基富集培养基(LB培养基):蛋白胨10 g·L-1,酵母膏5 g·L-1,盐度2%,pH值7.0,121 ℃下灭菌20 min,备用(LB固体培养基需加入18%琼脂粉).
无机盐培养基(MS培养基):KH2PO4 1 g·L-1,NaCl 0.1 g·L-1,(NH4)2SO4 0.04 g·L-1,MnSO4 .H2O 0.01 g·L-1,NaH2PO4 0.4 g·L-1,MgSO4.7H2O 0.1 g·L-1,Fe2(SO4)3.H2O 0.01 g·L-1,NaMo4.2H2O 0.01 g·L-1,加水定容至1000 mL,121 ℃下灭菌20 min,备用.
2.3 实验方法 2.3.1 菌体细胞浓度测定用分光光度计,测定光密度(OD值)设定为600 nm,进行菌体浓度测定.
2.3.2 苯酚浓度的测定运用4-氨基安替比林法测定苯酚的含量(潘杰等,2015).
2.3.3 形态特征鉴定用肉眼观察菌落的形状、大小、颜色、边缘特点、透明度、粘稠度、湿润度以及是否隆起.通过染色剂对降解菌进行染色(革兰氏染色、芽孢染色、鞭毛染色、荚膜染色等),在高倍显微镜下观察染色结果,并用扫描电镜观察菌体表面形态.
2.3.4 生理生化特性的测定按照《伯杰氏细菌鉴定手册》(Garrity,1974)进行甲基红实验、过氧化氢酶实验、吲哚实验、淀粉水解实验、硝酸盐还原实验、乳糖氧化发酵、明胶液化实验、VP实验、精氨酸双水解途径检测.
2.3.5 16S rDNA序列分析扩增通用引物: 27F 5′-AGACTTTGATCCTGGCTCAG -3′,1492R 5′-ACGGTT ACCTGTTACGACTT-3′
扩增体系设计:模板 DNA液10 μL、10×PCR Buffer 5 μL、dNTP 1 μL、Taq 酶 2 μL、两种引物各1 μL、ddH2O 31 μL.
PCR扩增反应条件:95 ℃(5 min)预变性→[95 ℃(30 s)→55 ℃(30 s)→72 ℃(90 s)](35cycles)→72 ℃(10 min)→4 ℃(holding)
PCR扩增产物电泳实验,获得目的条带,将PCR扩增产物交上海生工生物工程有限公司进行测序,将测序结果进行16S rRNA序列分析确定菌株的种属.
2.4 降解条件优化实验选取苯酚浓度、葡萄糖浓度、接种量、温度、pH值、盐度等6个对菌株zhtI降解苯酚影响最明显的因素,根据Placket-Burman实验设计原理,对11个考察因素进行N=12的组合实验,以苯酚降解率为响应值,从中筛选出对菌株降解苯酚影响最显著的3个因素;再通过中心组合实验设计原理,以Box-Benhnken设计进行实验,最后用Design Expert软件对实验数据进行处理,得到最佳降解条件组合(沈霞等,2010; 贺强礼等,2016).
2.5 耐盐苯酚降解菌的降酚动力学研究本文在降解菌的最佳培养条件下,以苯酚作为唯一碳源和能源,测定菌株对NaCl的最大耐受能力,根据每次实验测得的苯酚浓度和菌体生长量,求出不同苯酚浓度所对应降解速率,然后求出比降解速率值,最后运用origin7.5软件对实验数据进行非线性拟合,得出相应的动力学参数,鉴定菌株是否符合底物抑制模型(邹小玲等,2009;姜和等,2009).
3 结果与讨论(Results and discussion) 3.1 菌株的分离及鉴定 3.1.1 菌株的分离通过逐步提高苯酚浓度,从挑取的97个单菌落中分离纯化得到12株具有耐盐高效苯酚降解能力的菌株,分别命名为zhtA、zhtB、zhtC、zhtD、zhtE、zhtF、zhtG、zhtH、zhtI、zhtJ、zhtK、zhtL.对分离纯化得到的12株耐盐高效苯酚降解株进行降酚能力的测定,其中菌株zhtI的降解效果最佳,苯酚的降解率达到了80%以上.由此可知,在高盐条件下菌株zhtI对苯酚的降解能力最强.
3.1.2 菌株的鉴定对菌株进行形态特征鉴定,结果显示,菌株zhtI菌落呈圆形、白色、边缘整齐、中间隆起、湿润有光泽、较粘稠、不产色素,呈杆状,无端生鞭毛,无荚膜结构,无芽孢结构.菌株zhtI的革兰氏染色阳性、甲基红实验阴性、过氧化氢酶阳性、吲哚实验阴性、精氨酸双水解酶实验阳性、VP实验阴性、淀粉水解实验阴性、硝酸盐还原实验阳性、乳糖氧化发酵阴性、明胶液化实验阳性.根据《伯杰氏细菌鉴定手册》初步确定菌株zhtI为不动杆菌属(Acinetobacter sp.).
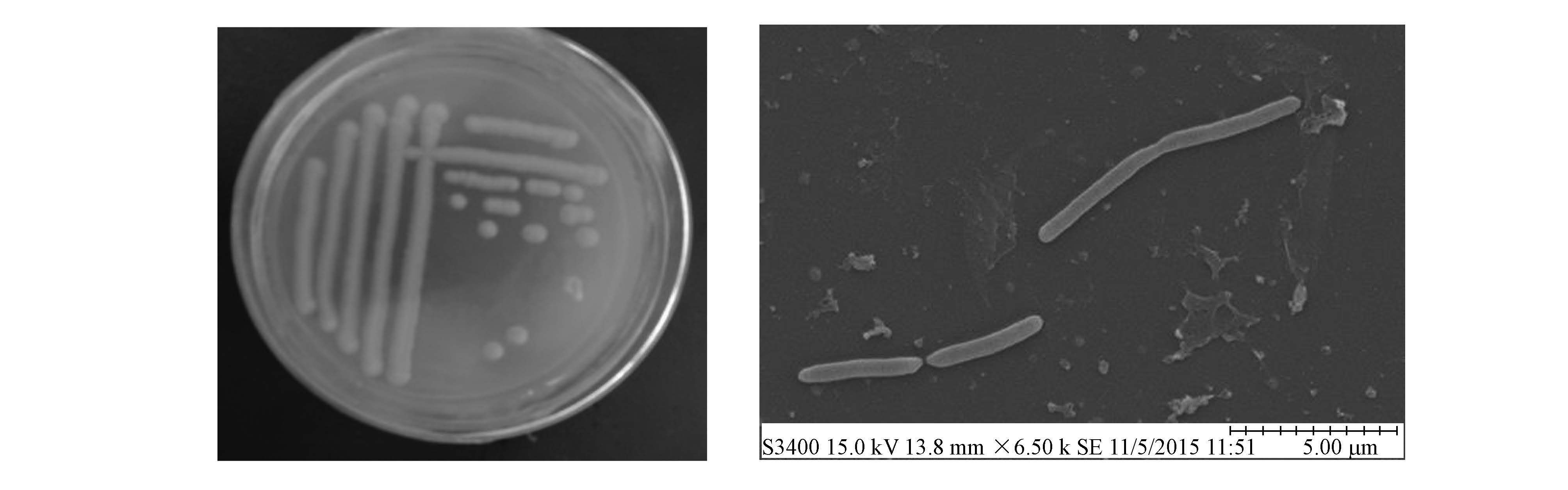 |
| 图 1 菌株zhtI的菌落形态及扫描电镜 Fig. 1 Colony morphology and scanning electron micrograph of strain zhtI |
菌株zhtI的16S rDNA经过PCR扩增得到一条大小在1400 bp左右的片段.测序得到菌株zhtI的16S rDNA核苷酸序列全长为1339 bp.经过BLAST同源性比对,菌株zhtI与Acinetobacter guillouiae(Genbank登录号为:KC904085)的同源性达到100%,按照16S rDNA序列的同源性在97%即为同一个种的标准(王延刚,2012),初步鉴定菌株zhtI为一株Acinetobacter guillouiae.菌株zhtI的系统发育树如图 2所示.
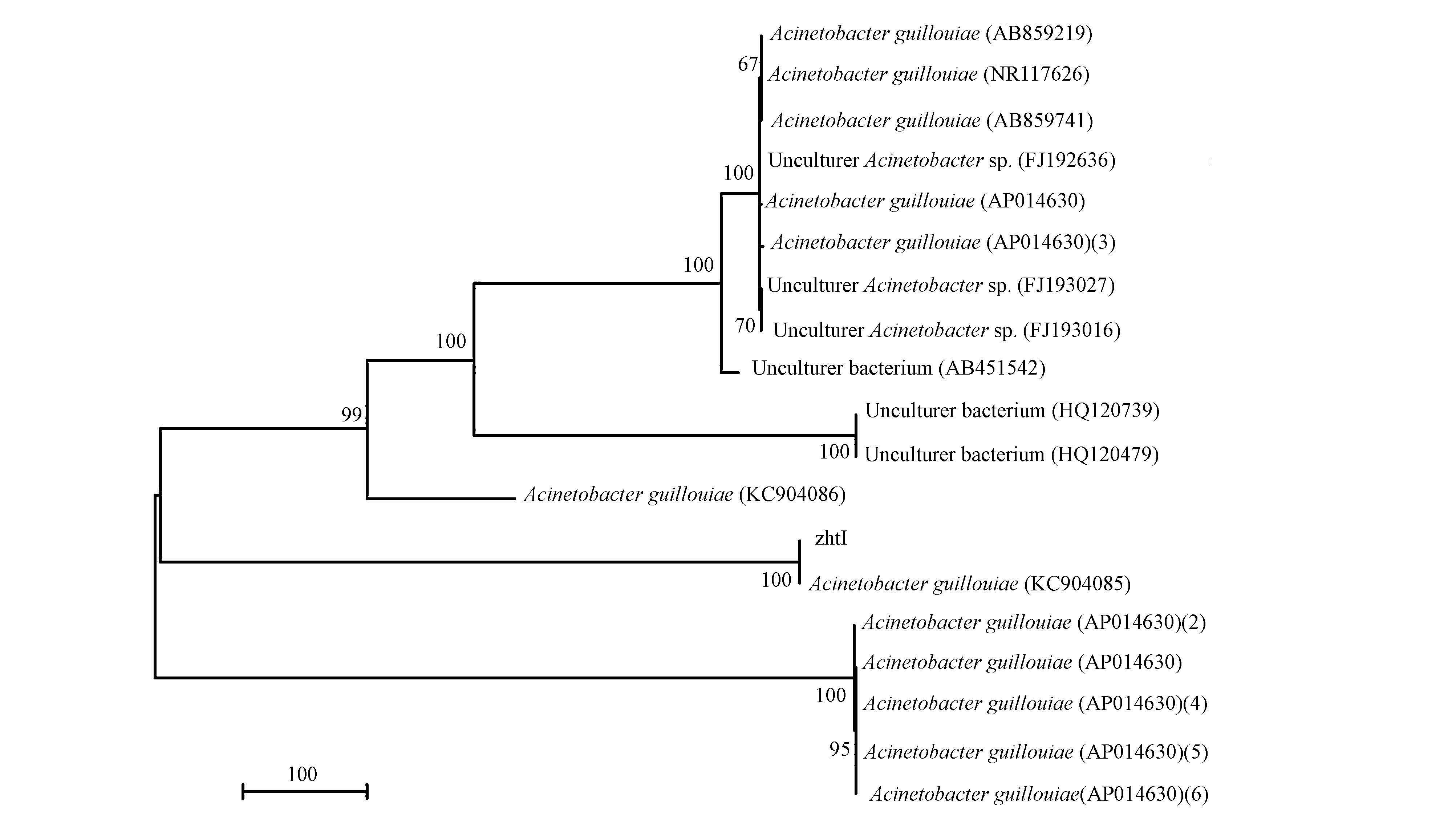 |
| 图 2 菌株zhtI的系统发育树 Fig. 2 Phylogenetic tree of zhtI |
通过单因素实验得出,NaCl浓度为3%时,菌株zhtI对苯酚的降解率达到最大值85.4%.在苯酚浓度为800 mg·L-1时,降解率达到最大值87.1%;当苯酚浓度高于800 mg · L-1时,菌株zhtI的生长量及其对苯酚的降解率均逐步下降;当pH值为7.5时,菌株zhtI对苯酚的降解率达到最大值;当接种量为6%时,菌株的生长量和苯酚降解率最高,而当接种量超过6%时,菌株的生长量和苯酚降解率变化均不明显;当温度为30 ℃时,菌株zhtI对苯酚的降解率达到最大值,当温度高于30 ℃时,菌株zhtI对苯酚的降解率和生长量均下降;外加碳源对菌株zhtI降解苯酚的效率影响较大,初始过程中菌株降解苯酚受到一定抑制,这是由于外加碳源被优先利用,但在后期苯酚的降解率上升明显,其中添加葡萄糖对菌株zhtI降解苯酚的促进作用最佳,能使苯酚的降解率达到91.6%;外加硝酸类氮源会使菌株zhtI降解苯酚的效率受到抑制,培养基中存在的NO-3是苯酚降解酶系的非竞争性抑制剂,使酶的活性降低,这与李凤敏(2010)以硝酸盐作为外加氮源会影响或抑制菌株对苯酚的降解研究结果一致.
3.4.2 菌株zhtI降酚条件的优化(1) Placket-Burman实验结果
根据Placket-Burman设计原理得出实验结果如表 1所示.
| 表 1 Placket-Burman实验设计结果 Table 1 Placket-Burman design of experiment results |
从表 1可知,实验组5的苯酚降解率最高,达到93.79%;实验组12的苯酚降解率最低为40.37%.运用SPPS 19.0软件进行拟合,得到方程:Y=69.93-8.71X1+43X2+9.85X3-0.62X4+4.71X5-1.14X6
X1表示苯酚浓度(mg · L-1);X2表示葡萄糖浓度(%);X3表示pH值;X4表示接种量(%);X5表示温度(℃);X6表示盐度(%).
通过Design Expert软件分析得到模型P=0.0355,说明该模型在研究区域拟合性良好;一般情况下变化系数越低说明实验的可信度和精确度越高,本实验变化系数为11.78%,表示Placket-Burman实验可信度和精确度比较高.线性回归分析结果如表 2所示.
| 表 2 Placket-Burman实验分析结果 Table 2 Placket-Burman experimental analysis results |
从表 2可知苯酚浓度、葡萄糖浓度及pH值对菌株zhtI降解苯酚的影响比较显著,其影响大小顺序为苯酚浓度(P=0.0134)>pH值(P=0.0193)>葡萄糖浓度(P=0.0211),其它因素对菌株zhtI降解苯酚的影响P值均大于0.05,所以影响效果不显著.由此可推断,酚浓度、葡萄糖浓度及pH为影响菌株zhtI降解苯酚的关键因素.
(2) 响应面法对菌株zhtI降酚条件的优化
由2.5.1 节筛选出3个对菌株zhtI苯酚降解效率产生影响的主要因素,即苯酚浓度、葡萄糖浓度、pH值,根据Box-Behnken的中心组合实验设计原理(Box and Hunter,1990),以苯酚降解率作为响应值,设计3因素3水平的响应面分析实验,组合方案见表 3.
| 表 3 中心组合实验方案 Table 3 Center combination experiment scheme |
苯酚浓度A、 葡萄糖浓度B、pH值C作如下变换Z1=(A - 800)/10、 Z2=(B-6)/1、Z3=(C-7.5)/10,以A、B和C为自变量,以苯酚降解率(Y)为响应值进行实验设计.结合响应面分析三维图(图 3),可更加直观地看出各个因素之间的相互作用,以及各个因素对苯酚的降解不是简单的线性关系,对响应值大小的影响存在一极值点.
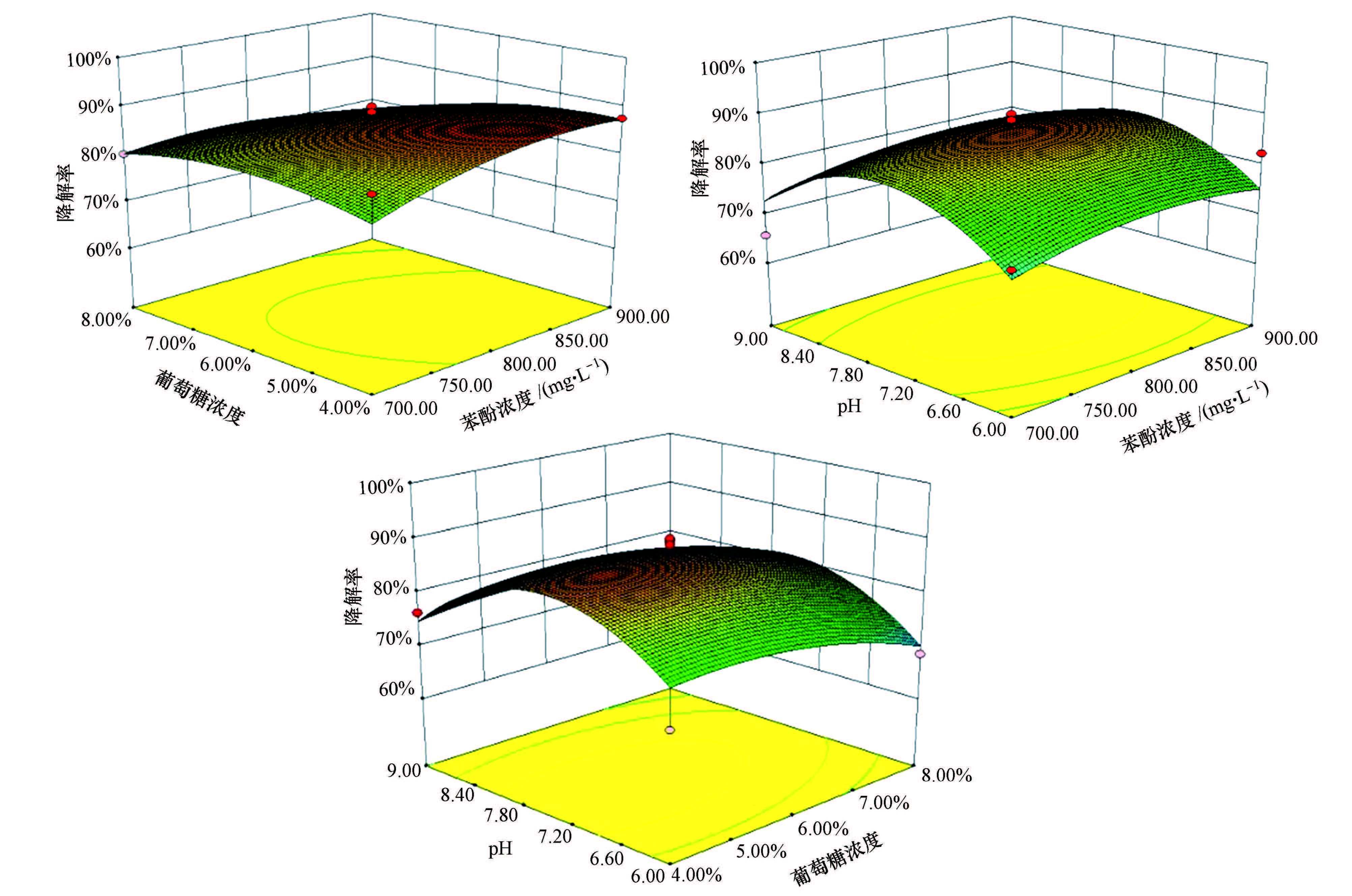 |
| 图 3 影响菌株zhtI降解苯酚的各因素交互作用响应曲面 Fig. 3 Response surface plotted on various influencing factors and phenol degradation of strain zhtI |
采用SAS RSREG程序对响应值与各因素进行处理,进行回归拟合后,得到回归方程:
Y=93.08+0.91Z1-2.66Z2-0.33Z3-2.72Z1Z2-0.40Z1Z3+1.00Z2Z3-2.90Z21-3.10Z22-10.582Z3,以及回归模型系数的显著性检验结果见表 5.
从表 4方差分析结果(F值)可得,对苯酚降解效率产生影响的3个因数大小依次为:葡萄糖浓度(Z2)>苯酚浓度(Z1)>pH值(Z3),其中失拟项数值大小为0.331 7,大于0.05,表示失拟不显著,因此该模型稳定,可作为各个因素水平对苯酚降解率影响的预测.根据回归方程,得到A=801.6,B=5.56,C=7.3,即苯酚浓度为801.6 mg·L-1,葡萄糖浓度为5.56%,pH值为7.3.将Z1、Z2、Z3代入回归方程可得Y=93.23,即菌株zhtI能使苯酚的降解率达到93.23%.
| 表 4 Box-Behnken实验回归分析结果 Table 4 Box-Behnken experimental regression analysis results |
(3) 验证实验
为了检验响应面分析方法的可靠性,按照优化后的条件(苯酚浓度801.6 mg·L-1、葡萄糖浓度5.56%、pH值7.3、接种量6%、温度30 ℃、盐度3%)进行苯酚降解实验(3次平行实验),培养72 h,结果检测到苯酚降解率分别为93.68%、92.47%、93.02%,取平均值为93.06%,预测值与实验结果之间偏差非常小,具有良好的拟合性,优化后菌株zhtI对苯酚的降解能力得到提升.说明响应面法能有效的对实验条件进行优化和预测,节约成本.
3.5 菌株zhtI的降酚动力学研究 3.5.1 菌株zhtI对苯酚耐受性检测结果菌株zhtI在pH值7.3、接种量6%、温度30 ℃、盐度3%、摇床转速200 r·min-1的不同苯酚浓度MS培养基中培养72 h.菌株zhtI的最高耐受苯酚浓度为1750 mg·L-1,当苯酚浓度过高时,菌株zhtI的生长会受到抑制甚至失活.对菌株zhtI进行降酚的动力学研究,降酚解动力学的相关数据如表 5所示.
| 表 5 菌株zhtI苯酚降解动力学实验数据 Table 5 Phenol degradation kinetics of Strains zhtI |
将表 5中的数据与Andrews抑制方程模型进行多元线性回归,如图 4所示,得到公式中的模型参数为:μmax=2.142 h-1,KS=126.952 mg·L-1,Ki=476.191 mg·L-1.模型方差为R2=0.9979.可知苯酚降解模型动力学方程曲线与实验值的拟合良好.对Andrews抑制方程求导可得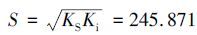
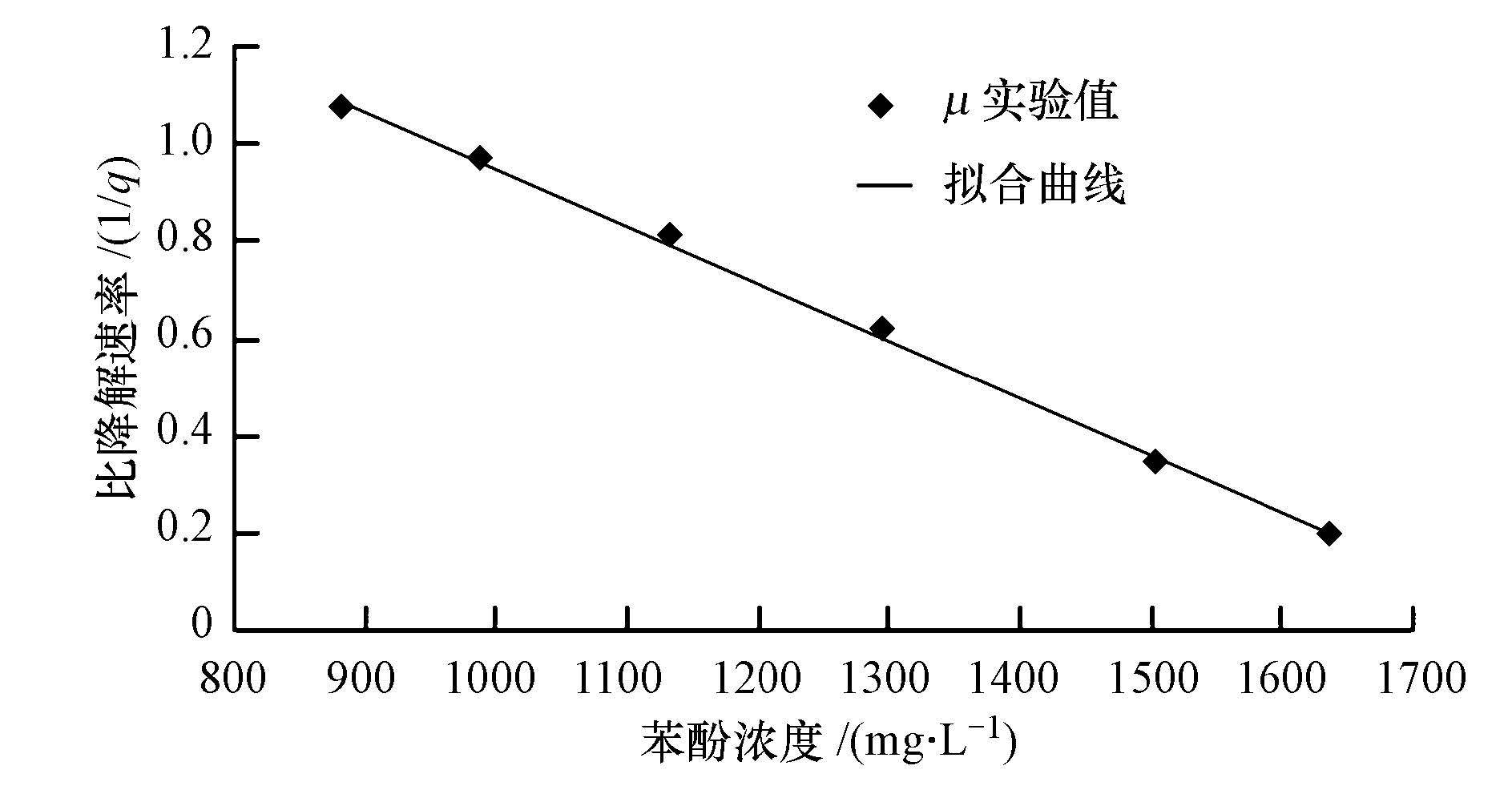 |
| 图 4 苯酚降解模型动力学方程拟合曲线与实验值 Fig. 4 Phenol degradation dynamics equations model fitting the experimental values |
1) 将筛选出的耐盐高效苯酚降解菌zhtI进行菌落形态、个体特征、生理生化鉴定,初步确定菌株zhtI为不动杆菌属(Acinetobacter sp.).对菌株菌株zhtI进行16S rDNA基因测序分析,通过BLAST与Genbank中相关序列比对以及MEGA4.1构建系统发育树,确定菌株zhtI为Acinetobacter guillouiae.
2) 通过单因素实验确定菌株最适盐度为3%,最适苯酚浓度为800 mg·L-1,最适pH值为7.5,最适接种量为6%,最适生长温度为30 ℃,最适外加碳源为葡萄糖,外加NO-3类氮源对菌株降解苯酚有抑制作用;利用Plackett-Burman实验确定葡萄糖浓度、苯酚浓度、pH值为菌株降解苯酚的3个主要因素,采用中心组合实验设计,结合Box-Behnken实验设计及响应面分析,确定最优降解条件为:苯酚浓度801.6 mg·L-1、葡萄糖浓度5.56%、pH值7.3、接种量6%、温度30 ℃、盐度3%,该条件下培养72 h,菌株zhtI对苯酚的降解率可达到93.23%
3) 菌株zhtI以苯酚为唯一碳源,接种于pH值7.3、接种量6%、盐度3%、温度30 ℃的液体MS培养基中,摇床转速200 r·min-1培养72 h,菌株zhtI对苯酚的最大耐受浓度为1750 mg·L-1.菌株zhtI降解苯酚的动力学模型符合典型的底物抑制模型,动力学参数为:μmax=2.142 h-1,KS=126.952 mg·L-1,Ki=476.191 mg·L-1.
| [1] | Ahmed S, Rasul M G, Brown R, et al. 2011. Influence of parameters on the heterogeneous photocatalytic degradation of pesticides and phenolic contaminants in wastewater: a short review[J]. Journal of Environmental Management , 92 (3) : 311–330. DOI:10.1016/j.jenvman.2010.08.028 |
| [2] | Basha K M, Rajendran A, Thangavelu V. 2010. Recent advances in the Biodegradation of phenol: a review[J]. Asian Journal of Experimental Biological Science , 1 (2) : 219–234. |
| [3] | Box G E P, Hunter W G. 1990. Statistics for experimerits: an introduction to design[A]//Data Analysis odel Building[M]. New York: Wiley |
| [4] | Garrity G M. 1974. Bergey's manual trust, department of microbiology and molecular genetics[M]. East Lansing: Michigan State University: MI48824 -1101. |
| [5] | 贺强礼, 关向杰, 黄水娥, 等.2014. 典型酚类废水的微生物处理研究现状及其进展[J]. 环境工程 , 2014, 32 (3) : 6–9. |
| [6] | 贺强礼. 2015a. 典型酚类高效降解菌的筛选、鉴定、降解条件优化及其降解成因研究[D]. 长沙: 湖南农业大学 http://cdmd.cnki.com.cn/Article/CDMD-10537-1016153130.htm |
| [7] | 贺强礼, 刘文斌, 杨海君, 等.2015b. 1株对叔丁基邻苯二酚降解菌的筛选鉴定及响应面法优化其降解[J]. 环境科学 , 2015b, 36 (7) : 2695–2706. |
| [8] | 贺强礼, 刘文斌, 杨海君, 等.2016. 一株苯酚降解菌的筛选鉴定及响应面法优化其降解[J]. 环境科学学报 , 2016, 36 (1) : 112–123. |
| [9] | 姜和, 曾虹燕, 夏葵, 等.2009. 高效复合菌群JHD降解苯酚的特性及其动力学研究[J]. 环境科学学报 , 2009, 29 (6) : 1184–1189. |
| [10] | Jiang L C, Ruan Q P, Li R L, et al. 2013. Biodegradation of phenol by using free and immobilized cells of Acinetobacter sp. BS8Y[J]. Journal of Basic Microbiology , 53 (3) : 224–230. DOI:10.1002/jobm.v53.3 |
| [11] | 李凤敏. 2010. 城市生活污水中低温高效苯酚降解菌的生理生化机制和降解特性的研究[D]. 哈尔滨: 哈尔滨师范大学 http://cdmd.cnki.com.cn/article/cdmd-10231-1010121272.htm |
| [12] | Mollaei M, Abdollahpour S, Atashgahi S, et al. 2010. Enhanced phenol degradation by Pseudomonas sp. SA01: gaining insight into the novel single and hybrid immobilizations[J]. Journal of Hazardous Materials , 175 (1/3) : 284–292. |
| [13] | 潘杰, 戴学文, 李晗, 等.2015. 4-氨基安替比林分光光度法测定苯酚滴耳液中苯酚含量[J]. 天津医科大学学报 , 2015, 21 (1) : 87–89. |
| [14] | 庞洁, 孟洪, 陆颖舟, 等.2010. 异相膜电渗析法处理苯酚废水[J]. 北京化工大学学报(自然科学版) , 2010, 37 (5) : 15–20. |
| [15] | Polymenakou P N, Stephanou E G. 2005. Effect of temperature and additional carbon sources on phenol degradation by an indigenous soil Pseudomonad[J]. Biodegradation , 16 (5) : 403–413. DOI:10.1007/s10532-004-3333-1 |
| [16] | 沈霞, 张艳红, 袁慧慧, 等.2010. 响应面分析法优化艾叶粗多糖提取工艺的研究[J]. 中成药 , 2010, 32 (1) : 48–51. |
| [17] | Silva C C, Hayden H, Sawbridge T, et al. 2013. Identification of genes and pathways related to phenol degradation in metagenomic libraries from petroleum refinery wastewater[J]. PLoS One , 8 (4) : e61811. DOI:10.1371/journal.pone.0061811 |
| [18] | Tsai S C, Li Y K. 2007. Purification and characterization of a catechol 1, 2-dioxygenase from a phenol degrading Candida albicans TL3[J]. Archives of Microbiology , 187 (3) : 199–206. DOI:10.1007/s00203-006-0187-4 |
| [19] | 王延刚. 2012. 耐盐硝基苯降解菌的筛选及降解特性研究[D]. 沈阳: 辽宁大学 http://cdmd.cnki.com.cn/Article/CDMD-10140-1013104093.htm |
| [20] | 邹小玲, 许柯, 丁丽丽, 等.2009. NaCl和KCl对厌氧污泥抑制的动力学研究[J]. 化工环保 , 2009, 29 (5) : 394–397. |
 2016, Vol. 36
2016, Vol. 36


