2. 福建农林大学林学院, 福州 350002
2. College of Forestry, Fujian Agriculture and Forestry University, Fuzhou 350002
伴随着采矿、冶炼、电镀等现代产业的快速发展,越来越多的重金属及其化合物被排放到环境中,致使重金属污染问题日趋严重.由于重金属无法降解,并且具有强烈的可移动性及复杂的化学存在形式,因此,如何从环境中去除及回收重金属一直是国内外的研究热点.传统的重金属污染治理技术主要包括化学沉淀、离子交换、膜分离、氧化还原等物理化学方法,但处理成本过高、易产生二次污染等问题一直制约着这些技术的发展(周东琴等, 2006; 张秀丽等, 2002).近年来,利用微生物吸附法对重金属进行回收处理引起人们的广泛关注,同其它传统手段相比,该技术具有成本低、能耗少、二次污染小等优点,具有明显的潜在应用价值,已成为重金属污染治理的重要研究方向之一(Hu et al., 1996; 周健等, 2008; 吴涓等, 2001).
胞外聚合物(Extracellular Polymeric Substances,EPS)是由微生物细胞分泌的一种粘性物质,由分布在内层且紧密结合在细胞表面的紧密粘附型EPS(TB-EPS)和松散分布在细胞表面外层的松散型EPS(LB-EPS)两部分组成(Adav et al., 2008).EPS的化学成分主要包括蛋白质、多糖、核酸和脂类等,其中存在着大量的阴离子基团(羟基、羰基、硫酸根),这些基团使胞外聚合物不但具有离子交换特性,也可以与金属离子发生相互作用.已有的研究表明,胞外聚合物对重金属有良好的吸附性能,在生物吸附过程中扮演着重要角色(Duan et al., 2013; Song et al., 2014).Sheng等(2013)采用热力学分析方法对活性污泥胞外聚合物的重金属吸附行为进行了分析,得出在EPS中蛋白质和腐殖酸均是Cu2+的强配位体,吸附主要受反应熵变的影响;Guibaud等(2005)研究了特定菌种提取的胞外聚合物与活性污泥中胞外聚合物对重金属吸附效果的对比,认为活性污泥胞外聚合物比特定菌种胞外聚合物吸附能力更强;Comte等(2008)研究了不同的pH对活性污泥胞外聚合物吸附Cd、Cu和Pb的影响,得出在pH=4时EPS对3种重金属的吸附量都是最少的,当pH=7时吸附量的顺序是Cu>Pb>Cd;Wei等(2011)研究了细菌胞外聚合物对Cd的吸附效应等,发现在细菌表面存在的胞外聚合物促进了对Cd的吸附作用,并且对革兰氏阳性枯草芽孢杆菌细胞比革兰氏阴性恶臭假单胞菌细胞的促进作用更显著.锌是环境中一种常见的重金属元素,摄入过量的锌元素会对人体皮肤组织及胃肠功能造成影响,严重时将导致贫血及免疫功能絮乱.截止目前,有关微生物胞外聚合物吸附重金属的研究仍大多停留在吸附量的理化条件等方面,且涉及的吸附离子也主要集中在Hg2+、Cd2+及Pb2+等少数几种,而有关重金属Zn2+的微生物吸附机制,特别是松散型(LB-EPS)和紧密结合型(TB-EPS)两类不同胞外聚合物在该过程中的功能作用,则少见报道.
因此,本文以一株具有Zn2+吸附功能的Aeromonas veronii N8菌为对象,对其松散型胞外聚合物(LB-EPS)和紧密型胞外聚合物(TB-EPS)的性质及吸附Zn2+过程进行研究,其结果对于深入揭示微生物Zn2+吸附机制,促进重金属生物吸附技术的实际推广应用具有重要的意义.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 菌株实验所用的Aeromonas veronii N8菌为本实验室保藏的具有Zn2+吸附功能的菌株,该菌株筛选自活性污泥,为革兰氏阴性杆菌(G-),菌落呈圆形,表面光滑,边缘无锯齿状且呈浅黄色,中央微微隆起.
2.1.2 实验试剂胰蛋白胨、酵母提取粉、NaCl、琼脂粉、NaOH、ZnSO4·7H2O、浓H2SO4、苯酚、考马斯、锌标液(硝酸为介质)、稀硝酸、碳酸氢钠、EDTA等购于国药集团.
2.1.3 培养基实验所需培养基为LB培养基.
2.2 EPS的制备EPS的提取采用热提取法(Ramesh et al., 2007; Wang et al., 2009),挑取在平板上培养的A.veronii单菌落,接种到液体培养基过夜培养作种子液.取种子液100 μL接种到100 mL液体培养基中培养至稳定期取出,4 ℃、4000 g下离心10 min,弃上清液,加70 ℃超纯水5 mL振荡摇匀,4 ℃、4000 g离心10 min,取上清液为松散型胞外聚合物(LB-EPS);再次用超纯水补至原始体积,60 ℃水浴30 min,然后在4 ℃、4000 g下离心15 min,取上清液为紧密型胞外聚合物(TB-EPS).将两次取得的EPS样品于4 ℃保存,待测.
2.3 EPS含量测定蛋白质含量测定采用考马斯亮蓝法(Bradford, 1976),多糖含量测定采用苯酚硫酸法(Dubois et al., 1956).
2.4 EPS性质分析 2.4.1 凝胶色谱(GFC)分析采用Waters1515凝胶渗透色谱仪(RI2410示差检测器)对所提取EPS的分子量特征进行分析,色谱柱为PL aquagel-OH MIXED-M,分子量标样为PEG(孔毅等, 2003).
2.4.2 核磁共振(NMR)分析1H NMR光谱采用AVANCEIII500型核磁共振波谱仪,在室温下以500 MHz操作,配备5 mm逆探针和z梯度线圈.化学位移相对于TMS以δ记录(Khan et al., 2014).
2.4.3 荧光光谱(EEM)分析EPS样品用Fluorolog-3型荧光光谱仪进行荧光特性分析,以氙弧灯为激发光源,激发波长λex=220~450 nm,间隔5 nm,发射波长λem=230~550 nm,间隔2 nm,荧光光谱在扫描完成后自动进行仪器校正(Pan et al., 2010).
2.4.4 X射线能谱(XPS)分析提取EPS样品,冷冻干燥后压片,采用美国Thermo Scientific ESCALAB 250型X射线能谱仪分析样品中的C、H、O高分辨能谱,分析样品的化学组成(Wang et al., 2014).
2.5 吸附试验. 2.5.1 时间对EPS吸附Zn2+的影响取50 mg·L-1的Zn2+溶液50 mL于150 mL聚乙烯瓶中,1400 0D的透析袋中放入10 mL 200 mg·L-1的EPS后,放入Zn2+溶液中,每组处理3个重复.25 ℃、150 r·min-1摇床中培养,分别于0、20、40、60、90、120 min时取样.用PinAAcle 900F型原子吸收光谱仪测定剩余Zn2+的浓度(Najera et al., 2005; Raungsomboon et al., 2006).
2.5.2 Zn2+浓度对EPS吸附Zn2+的影响EPS投加浓度为200 mg·L-1,分别添加10、30、50、70、90 mg·L-1的Zn2+初始溶液,吸附方法同2.5.1节,不同时间取样测定剩余Zn2+的浓度.
2.5.3 EPS浓度对EPS吸附Zn2+的影响分别将浓度为20、40、50、100、200 mg·L-1的EPS溶液放入50 mg·L-1的Zn2+溶液中,吸附方法同2.5.1节,不同时间取样测定剩余Zn2+的浓度.
2.6 EPS吸附Zn2+前后的傅里叶红外光谱(FTIR)分析将吸附Zn2+前后的EPS样品冷冻干燥后与溴化钾以1:100的比例混匀压片,采用傅里叶衰减全反射红外光谱法(ATR/FTIR)(美国尼高力360智能型红外光谱仪)检测,波数为4000~400 cm-1(d′Abzac et al., 2013).
2.7 吸附模型分别利用Langmuir模型(式(1))、Freundlich模型(式(2))、Redlich-peterson模型(式(3))、Temkin模型(式(4))、Sips模型(式(5))对LB-EPS和TB-EPS的Zn2+吸附过程进行研究.
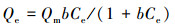
|
(1) |
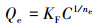
|
(2) |
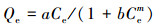
|
(3) |
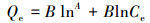
|
(4) |
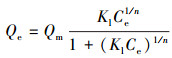
|
(5) |
式中, Qe为吸附剂的平衡吸附量(mg·L-1);Ce为平衡浓度(mg·L-1);Qm为吸附剂的最大吸附量(mg·L-1);Langmuir模型中的b表示其经验常数;Freundlich模型中的KF、n表示其常数;Redlich-peterson模型中a、b、m均表示常数;Temkin模型中的A和B为其常数;Sips模型中K和n为其常数(王远红等, 2010; Su et al., 2014).
3 结果与讨论(Results and discussion) 3.1 EPS的组成对A.veronii N8菌株所产LB-EPS与TB-EPS的蛋白质和多糖含量进行测定,其组成特征如图 1所示.由图 1可知,该菌株的LB-EPS含量要明显高于TB-EPS;在成分组成方面,两者也具有显著差别,其中,LB-EPS的蛋白质含量为84 mg·L-1,多糖含量为70.57 mg·L-1,蛋白质含量要高于多糖含量;而在TB-EPS中,多糖含量为83.99 mg·L-1,蛋白质含量为38.8 mg·L-1,多糖含量则大于蛋白质含量;另外,LB-EPS中的蛋白质含量要高于TB-EPS,但TB-EPS却含有更多的多糖.EPS是微生物向胞外分泌的一类高分子集合物,其产生受到营养条件、培养时间及环境因素等多方面的影响.如王亮等(2011)对白腐真菌胞外聚合物的含量进行了测定,得出在振荡培养113 h后,获得最大的EPS总量为125.5 mg·L-1,这少于A.veronii N8菌产生的LB-EPS和TB-EPS的量;而熊芬等(2009)则对烟曲霉胞外聚合物的含量进行测定,发现烟曲霉胞外聚合物的总量为220.1 mg·L-1,也小于A.veronii N8菌的EPS总量.
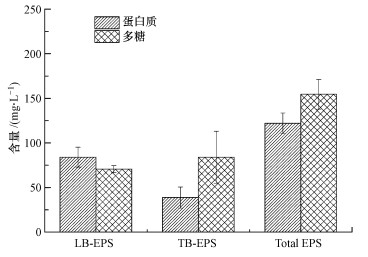 |
| 图 1 A.veronii N8产LB-EPS与TB-EPS的组成特征 Fig. 1 Composition of LB-EPS and TB-EPS produced by A.veronii N8 |
利用GFC对两种EPS的分子量特征进行分析,结果如图 2所示.两种EPS均具有较宽的分子量分布(10~10000 kDa),表明EPS是一类复杂多样的大分子有机物.进一步分析发现(表 1),LB-EPS和TB-EPS的分子量分散指数(Mw/Mn)分别为1.68和1.82,TB-EPS略大,说明该类型EPS具有更宽的分子量分布范围;而对比两者的平均分子量(Mw)则发现,LB-EPS的Mw(490752 Da)要高于TB-EPS的Mw(418824 Da).
| 表 1 EPS的分子量 Table 1 Molecular weight of EPS |
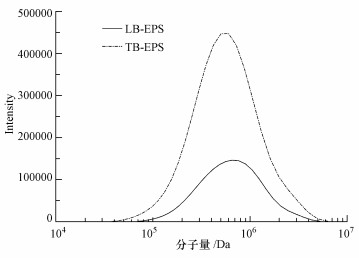 |
| 图 2 A.veronii N8产LB-EPS与TB-EPS的分子量分布 Fig. 2 Molecular weight distribution of LB-EPS and TB-EPS produced by A.veronii N8 |
对LB-EPS和TB-EPS进行1H NMR图谱分析.其中,LB-EPS由高场到低场存在的主要吸收峰化学位移分别4.75、3.85、3.2、2.4、2、1.4和0.9 ppm,而TB-EPS为8.5~7.5、6~5.5、4.75及4.3~0.8 ppm,其中,4.3~0.8 ppm区域信号重叠严重,在化学位移3.8、3.2、1.9、1.4和0.8 ppm处有5个强峰.进一步分析发现,TB-EPS在化学位移8.5~7.5 ppm之间的信号峰应来自芳环结构,而LB-EPS并不存在该信号峰;在5.0~3.0 ppm位置的信号峰表示羟基上的氢,主要是多糖的特征峰,TB-EPS在此区域的信号峰强度要大于LB-EPS;在3.0~0.5 ppm的1H化学位移范围内主要代表饱和的烷基伯氢、烷基仲氢和烷基叔氢,TB-EPS在该区域的信号峰也要强于LB-EPS;0.89~0.97 ppm则代表着甲基质子的特征吸收峰,此处TB-EPS的峰强度仍要强于LB-EPS;而1.2~1.23 ppm则为亚甲基质子的特征吸收峰,仅TB-EPS有此行征峰,LB-EPS并没有(图 3).
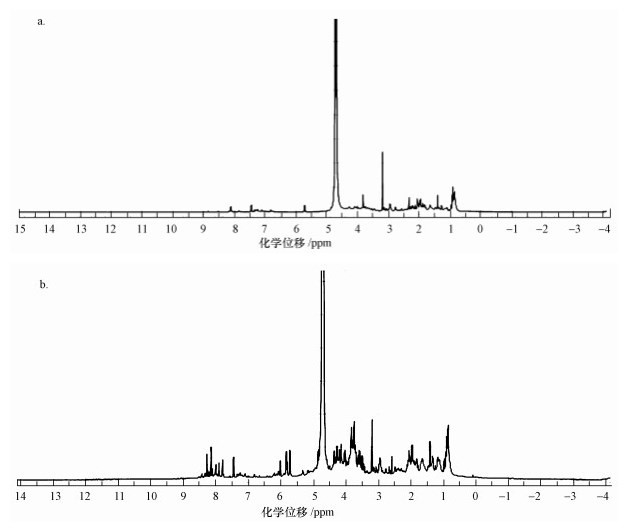 |
| 图 3 A.veronii N8产LB-EPS与TB-EPS的1H NMR图谱(a.LB-EPS, b.TB-EPS) Fig. 3 1H NMR spectrum of LB-EPS and TB-EPS produced by A.veronii N8(a.LB-EPS, b.TB-EPS) |
对A.veronii N8菌株所产LB-EPS与TB-EPS进行EEM检测,发现LB-EPS与TB-EPS各具有两个特征峰,分别是A、C和A、D(图 4).Chen等(2003)通过对不同有机物的荧光特征进行研究,将三维荧光光谱图分为5个区域(Ⅰ~Ⅴ),分别对应5类常见的有机物.本研究中Peak A属于区域Ⅳ,是溶解性的微生物副产物,如色氨酸类蛋白等;Peak C属于区域Ⅴ,是腐殖酸类物质;Peak D属于区域Ⅱ,是简单的芳香类蛋白质.另外,三维荧光光谱中荧光强度可以体现有机物的含量,通常有机物含量越高与其对应的荧光强度也越强,本文两种EPS在Peak A区域均具有较强的荧光,表明两者都含有较多的色氨酸类蛋白微生物副产物;由于具有Peak D区域,说明TB-EPS中含有一定数量的芳香类蛋白质;而LB-EPS中具有Peak C区域,则表明其成分中含有腐殖酸类物质.
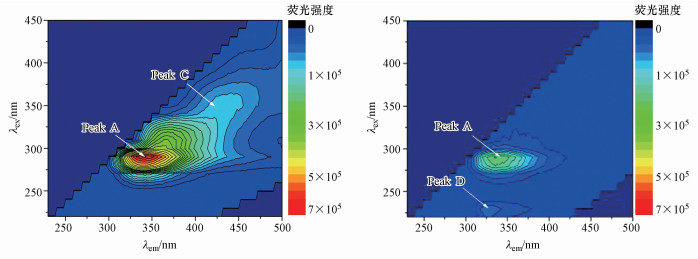 |
| 图 4 A.veronii N8产LB-EPS与TB-EPS的EEM图谱(a.LB-EPS, b.TB-EPS) Fig. 4 EEM spectrum of LB-EPS and TB-EPS produced by A.veronii N8(a.LB-EPS, b.TB-EPS) |
对A.veronii N8所产LB-EPS和TB-EPS的C、O和N 3种元素的XPS高分辨图谱进行分析.LB-EPS和TB-EPS中的C谱、O谱和N谱基团种类相似,但各个元素所占的比例却不同(图 5).LB-EPS和TB-EPS的C谱中284.59~284.65 eV处的峰是C—(C, H),为脂类或者氨基酸侧链,该峰值所占比例最高分别为41.1%和43.1%.对于O谱,LB-EPS和TB-EPS中532.18~532.57 eV处的CO和O—C—O来自醇,半缩醛或乙缩醛基在两个峰中比例也都为最高,分别为78.4%和60.6%,LB-EPS相对更高.对于N谱,非质子化的N所占比例都大于质子化的N,LB-EPS和TB-EPS中非质子化的N分别为65.5%和66.6%,这些都表明两种EPS的组成具有明显的差别.
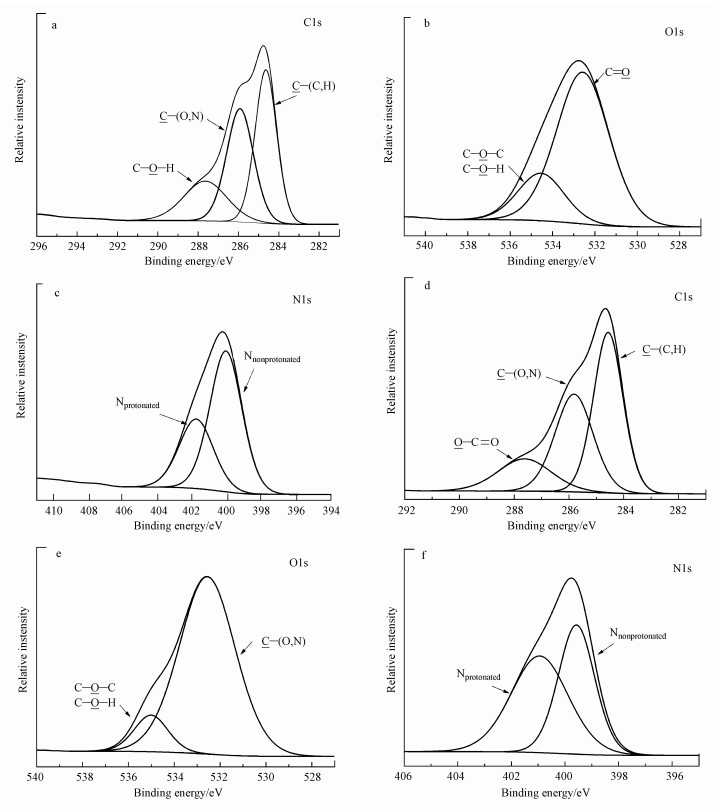 |
| 图 5 A.veronii N8产LB-EPS与TB-EPS的XPS图谱(a~c.LB-EPS, d~f. TB-EPS) Fig. 5 XPS spectrum of LB-EPS and TB-EPS produced by A.veronii N8 (a~c.LB-EPS, d~f.TB-EPS) |
通过研究LB-EPS和TB-EPS的Zn2+吸附率随时间的变化得出,两种类型EPS的Zn2+吸附过程具有类似的特征,都经历了3个阶段:快速吸附、慢速吸附和吸附平衡(图 6).其中,0~20 min为快速吸附阶段,在这段时间内,两类EPS的吸附率均迅速增加,在20 min时LB-EPS和TB-EPS对Zn2+的吸附率分别为46.2%和38.1%,LB-EPS的吸附要快于TB-EPS;20~90 min为慢速吸附阶段,此阶段两种EPS的Zn2+吸附率增速放慢,在90 min时两者的吸附率均达到最大,此时LB-EPS的吸附率为51.96%,吸附量为25.48 mg·L-1,而TB-EPS的吸附率为39%,吸附量为19.5 mg·L-1,同第一阶段相比,该阶段两种EPS的Zn2+吸附能力差距更为显著,LB-EPS具有明显的吸附优势;而经过90 min以后,两种EPS的Zn2+吸附率均变化缓慢,表明两者的吸附活动进入了吸附平衡阶段.EPS的重金属吸附是一个动态平衡过程,在反应初期两种EPS的吸附率都迅速增加,因为此时的吸附位点比较充足,而随着吸附时间的增加,吸附位点越来越少,吸附率的增加变得缓慢,最终吸附率随着吸附位点的饱和而达到平衡,这与郑蕾等(2005)的研究结果相一致.微生物EPS对重金属阳离子的吸附能力与其组成及化学性质密切相关.相关研究已表明,蛋白质与多糖比例及化学官能团种类的不同都会导致EPS重金属吸附特征的差异(郑蕾等,2008;熊芬等,2007).在本研究中,LB-EPS与TB-EPS具有不同的蛋白质和多糖组成比例,并且LB-EPS还含有少量的腐殖酸类物质,这些成分组成方面的不同使得两类EPS呈现出不同的化学性质,而上述GFC、NMR及XPS性质分析结果也直接证实了两类EPS在分子量分布及化学基团构成等方面具有显著差别.综上所述,正是由于LB-EPS和TB-EPS在成分组成及化学性质方面的差异,才导致两者呈现出不同的Zn2+吸附特征.
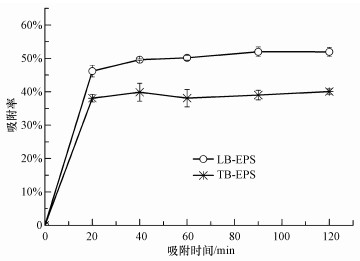 |
| 图 6 吸附时间对LB-EPS与TB-EPS吸附Zn2+的影响 Fig. 6 Effect of adsorption time on the Zn2+absorption ratios of LB-EPS and TB-EPS |
研究了不同Zn2+添加浓度对TB-EPS与LB-EPS对Zn2+吸附率的影响.结果(图 7)发现,两类EPS对Zn2+的吸附率都随着Zn2+浓度的增加而降低,当添加Zn2+浓度为10 mg·L-1时LB-EPS与TB-EPS的吸附率都达到了最大,分别为88%和63.4%,而当Zn2+浓度为90 mg·L-1时LB-EPS与TB-EPS的吸附率则最小,分别为43.47%和34.58%;另外,尽管两类EPS呈现出相似的Zn2+吸附特征,但从图 7可以看出,在相同Zn2+浓度条件下,LB-EPS的吸附率要明显高于TB-EPS.之所以出现上述结果,除了LB-EPS和TB-EPS在性质和组分方面存在差异之外,主要是因为在低Zn2+初始浓度下,EPS的吸附位点更充足,随着Zn2+浓度的增加吸附位点达到饱和,吸附量缓慢增加,而吸附量占总量的比例在不断减少(沈祥信, 2007).
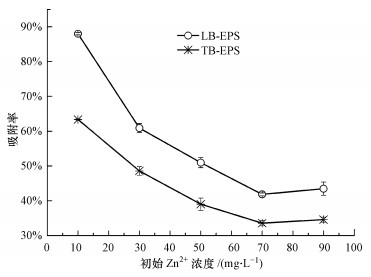 |
| 图 7 Zn2+浓度对LB-EPS与TB-EPS吸附Zn2+的影响 Fig. 7 Effect of Zn2+ concentration on the Zn2+ absorption ratios of LB-EPS and TB-EPS |
不同浓度EPS的Zn2+吸附特征如图 8所示.由实验结果可以得出,LB-EPS和TB-EPS对Zn2+的吸附率随EPS浓度的增加而上升,当EPS浓度小于50 mg·L-1时,两者的Zn2+吸附率随着浓度的增加增幅明显,LB-EPS的吸附效率从最初的40.3%增加到44.4%,TB-EPS的吸附率从30.4%增加到36.76%,由于吸附位点充足该阶段吸附效果受EPS浓度的影响明显;而当EPS的浓度高于50 mg·L-1时,两者的Zn2+吸附率则增幅较小,受EPS浓度的影响较小.在整个吸附过程中,EPS浓度的增加带来吸附位点的增多,因此,胞外聚合物对Zn2+的吸附率随之增加.而后增加变得缓慢,并且逐渐达到平衡,这可能是EPS量的增加降低了其比表面积的大小和参与反应的单位官能团数量,此外,还有静电相互作用及反应集团间的相互干扰等原因.而熊芬等(2009)研究胞外聚合物投加量对吸附Pb2+影响时也发现随着投加量的增加,吸附率增加变得缓慢,最终达到平衡(熊芬等, 2009).另外,尽管LB-EPS和TB-EPS呈现相似的吸附特征,但LB-EPS吸附率一直大于TB-EPS,而这也是两者在成分组成和化学性质上均存在差异所致.
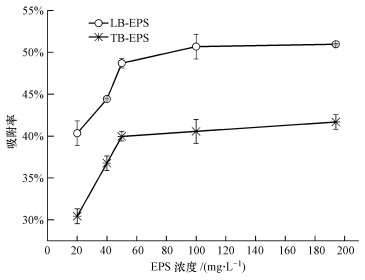 |
| 图 8 EPS浓度对LB-EPS与TB-EPS吸附Zn2+的影响 Fig. 8 Effect of EPS concentration on the Zn2+ absorption ratios of LB-EPS and TB-EPS |
图 9为A.veronii N8产生的LB-EPS和TB-EPS吸附Zn2+前后的红外对比图谱.LB-EPS吸附Zn2+后在531cm-1附近核酸的吸收峰强度明显减弱,且发生了移位现象,由531 cm-1移位到620 cm-1.而TB-EPS吸附重金属Zn2+后,在531 cm-1附近核酸的吸收峰强度几乎没发生变化,但也发生了由531 cm-1到607 cm-1的移位现象;LB-EPS和TB-EPS在1074 cm-1多糖特征峰区,吸附前后峰的位置变化不大,吸附Zn2+后峰的强度有略微增加;在1399 cm-1区为多糖的C—O的伸缩振动峰,当LB-EPS吸附Zn2+后,峰值明显减弱,而TB-EPS在此区并没出现C—O的伸缩振动峰.
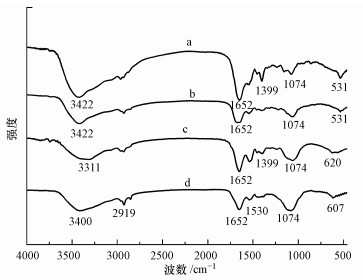 |
| 图 9 LB-EPS和TB-EPS吸附Zn2+前后的红外图谱(a、b分别为吸附前的LB-EPS和TB-EPS;c、d分别为吸附后的LB-EPS和TB-EPS) Fig. 9 FITRcomparison spectrum of LB-EPS and TB-EPS for Zn2+ absorption(a and b represent LB-EPS and TB-EPS before Zn2+adsorption, respectively; c and d represent LB-EPS and TB-EPS after Zn2+ adsorption, respectively) |
LB-EPS和TB-EPS在1652 cm-1蛋白质特征峰区,吸附Zn2+后峰的强度大大减弱,但位置并没有发生变化.而在3422 cm-1区的峰是—OH的伸缩振动峰,两类EPS吸附后特征峰的强度都明显变弱,并且发生了移位现象.本研究中EPS吸附Zn2+前后官能团特征峰变化的这一现象与Zhang等(2014)报道中所观察到的基团是相似的.
3.5 不同类型EPS的Zn2+吸附模型采用Langmuir、Freundlich、Redlich-peterson、Temkin和Sips 5种吸附等温模型对EPS吸附Zn2+的过程进行拟合分析,结果如表 2所示.对比5种模型的拟合结果发现,LB-EPS的Zn2+吸附数据采用Freundlich模型具有较高的拟合度,而TB-EPS的Zn2+吸附过程则更符合Temkin模型.重金属的EPS吸附是一个复杂的物理化学过程,与重金属类型和EPS的自身组成密切相关.从前面的研究结果可知,两类EPS在成份组成、分子量分布、化学基团等多个方面均具有区别,这直接导致了两类EPS吸附特征的不同.Freundlich模型通常能较好地描述水溶液中的吸附,LB-EPS用Freundlich拟合得到的n值(Freundlich经验常数)为2.67,可判断吸附是容易进行的.Temkin模型考虑到当吸附剂吸附溶质时,被吸附溶质间发生相互作用力,则必会对等温吸附行为产生影响,说明TB-EPS吸附Zn2+过程中,被吸附溶质之间有发生力的作用,说明随着吸附剂表面覆盖率增大,吸附热呈线性降低.
| 表 2 EPS对Zn2+吸附的热力学方程拟合参数 Table 2 Regressionparameter for the isotherm equations of Zn2+adsorbed by EPS |
1)A.veronii N8所产两种EPS的主要成份均为蛋白质和多糖,但两者的组成比例各不相同;TB-EPS的分子量分布范围较广,而LB-EPS则具有更大的平均分子量;而EEM图谱则发现,两种EPS均含有一定数量的色氨酸类蛋白微生物副产物,同时,TB-EPS含有简单的芳香型类蛋白质,LB-EPS则含有少量腐殖酸类物质;1H NMR与XPS图谱则表明,两种EPS的具有相似的结构组成,但在元素比例方面具有差异.
2)LB-EPS和TB-EPS均具有良好的Zn2+吸附特性,经过90 min吸附时间,两者均能达到吸附平衡,与TB-EPS相比,LB-EPS的吸附效果更好;两种EPS对Zn2+的吸附率均随着Zn2+浓度的增加而降低,而随着EPS投加量的增加而上升;对比吸附Zn2+前后红外图谱可以看出,参与Zn2+吸附反应的主要有C—O、—OH基团及蛋白质等.
3)采用5种热力学模型对两种EPS的Zn2+吸附过程进行描述,发现LB-EPS的Zn2+吸附过程符合Freundlich模型,而TB-EPS则采用Temkin模型更为合适,这表明两种EPS可能具有不同的Zn2+吸附机制.
| [${referVo.labelOrder}] | Adav S S, Lee D J. 2008. Extraction of extracellular polymeric substances from aerobic granule with compact interior structure[J]. Journal of Hazardous Materials , 154 (1/3) : 1120–1126. |
| [${referVo.labelOrder}] | Bradford M M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J]. Analytical Biochemistry , 72 (1/2) : 248–254. |
| [${referVo.labelOrder}] | Chen W, Westerhoff P, Leenheer J A, et al. 2003. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology , 37 (24) : 5701–5710. |
| [${referVo.labelOrder}] | Comte S, Guibaud G, Baudu M, et al. 2008. Biosorption properties of extracellular polymeric substances (EPS) towards Cd, Cu and Pb for different pH values[J]. Journal of Hazardous Materials , 151 (1) : 185–193. DOI:10.1016/j.jhazmat.2007.05.070 |
| [${referVo.labelOrder}] | d'Abzac P, Bordas F, Joussein E, et al. 2013. Metal binding properties of extracellular polymeric substances extracted from anaerobic granular sludges[J]. Environmental Science Pollution Research , 20 (7) : 4509–4519. DOI:10.1007/s11356-012-1401-3 |
| [${referVo.labelOrder}] | Duan L, Jiang W, Song Y H, et al. 2013. The characteristics of extracellular polymeric substances and soluble microbial products in moving bed biofilm reactor-membrane bioreactor[J]. Bioresource Technology , 148 : 436–442. DOI:10.1016/j.biortech.2013.08.147 |
| [${referVo.labelOrder}] | DuBois M, Gilles K A, Hamilton J K, et al. 1956. Colorimetric method for determination of sugars and related substances[J]. Analytical Chemistry , 28 (3) : 350–356. DOI:10.1021/ac60111a017 |
| [${referVo.labelOrder}] | Guibaud G, Comte S, Bordas F, et al. 2005. Comparison of the complexation potential of extracellular polymeric substances (EPS), extracted from activated sludges and produced by pure bacteria strains, for cadmium, lead and nickel[J]. Chemosphere , 59 (5) : 629–638. DOI:10.1016/j.chemosphere.2004.10.028 |
| [${referVo.labelOrder}] |
Hu X C, Boyer G L.
1996. Siderophore-mediated aluminum uptake by Bacillus megaterium ATCC |
| [${referVo.labelOrder}] | Khan M T, Busch M, Molina V G, et al. 2014. How different is the composition of the fouling layer of wastewater reuse and seawater desalination RO membranes?[J]. Water Research , 59 : 271–282. DOI:10.1016/j.watres.2014.04.020 |
| [${referVo.labelOrder}] | 孔毅, 吴梧桐, 吴如金.2003. 蛋白质分子量测定方法比较研究[J]. 分析仪器 , 2003 (2) : 44–47. |
| [${referVo.labelOrder}] | Najera I, Lin C C, Kohbodi G A, et al. 2005. Effect of chemical speciation on toxicity of mercury to Escherichia coli biofilms and planktonic cells[J]. Environmental Science & Technology , 39 (9) : 3116–3120. |
| [${referVo.labelOrder}] | Pan X L, Liu J, Zhang D Y. 2010. Binding of phenanthrene to extracellular polymeric substances (EPS) from aerobic activated sludge: a fluorescence study[J]. Colloids and Surfaces B: Biointerfaces , 80 (1) : 103–106. DOI:10.1016/j.colsurfb.2010.05.002 |
| [${referVo.labelOrder}] | Ramesh A, Lee D J, Lai J Y. 2007. Membrane biofouling by extracellular polymeric substances or soluble microbial products from membrane bioreactor sludge[J]. Applied Microbiology and Biotechnology , 74 (3) : 699–707. DOI:10.1007/s00253-006-0706-x |
| [${referVo.labelOrder}] | Raungsomboon S, Chidthaisong A, Bunnag B, et al. 2006. Production, composition and Pb2+ adsorption characteristics of capsular polysaccharides extracted from a cyanobacterium Gloeocapsa gelatinosa[J]. Water Research , 40 (20) : 3759–3766. DOI:10.1016/j.watres.2006.08.013 |
| [${referVo.labelOrder}] | 沈祥信. 2007.好氧颗粒污泥快速培养及其吸附重金属的研究[D].长沙:湖南大学 http://cdmd.cnki.com.cn/article/cdmd-10532-2007160393.htm |
| [${referVo.labelOrder}] | Sheng G P, Xu J, Luo H W, et al. 2013. Thermodynamic analysis on the binding of heavy metals onto extracellular polymeric substances (EPS) of activated sludge[J]. Water Research , 47 (2) : 607–614. DOI:10.1016/j.watres.2012.10.037 |
| [${referVo.labelOrder}] | Song C, Sun X F, Xing S F, et al. 2014. Characterization of the interactions between tetracycline antibiotics and microbial extracellular polymeric substances with spectroscopic approaches[J]. Environmental Science and Pollution Research , 21 (3) : 1786–1795. DOI:10.1007/s11356-013-2070-6 |
| [${referVo.labelOrder}] | Su X Y, Tian Y, Zuo W, et al. 2014. Static adsorptive fouling of extracellular polymeric substances with different membrane materials[J]. Water Research , 50 : 267–277. DOI:10.1016/j.watres.2013.12.012 |
| [${referVo.labelOrder}] | 王亮, 陈桂秋, 曾光明, 等.2011. 白腐真菌胞外聚合物及其对菌体吸附Pb2+的影响[J]. 环境科学 , 2011, 32 (3) : 773–778. |
| [${referVo.labelOrder}] | 王远红, 张红波, 罗世田, 等.2010. 胞外聚合物对水中Cd(Ⅱ)的吸附性能研究[J]. 环境工程学报 , 2010, 4 (10) : 2185–2189. |
| [${referVo.labelOrder}] | Wang Z C, Gao M C, Wang S, et al. 2014. Effect of hexavalent chromium on extracellular polymeric substances of granular sludge from an aerobic granular sequencing batch reactor[J]. Chemical Engineering Journal , 251 : 165–174. DOI:10.1016/j.cej.2014.04.078 |
| [${referVo.labelOrder}] | Wang Z W, Wu Z C, Tang S J. 2009. Extracellular polymeric substances (EPS) properties and their effects on membrane fouling in a submerged membrane bioreactor[J]. Water Research , 43 (9) : 2504–2512. DOI:10.1016/j.watres.2009.02.026 |
| [${referVo.labelOrder}] | Wei X, Fang L C, Cai P, et al. 2011. Influence of extracellular polymeric substances (EPS) on Cd adsorption by bacteria[J]. Environmental Pollution , 159 (5) : 1369–1374. DOI:10.1016/j.envpol.2011.01.006 |
| [${referVo.labelOrder}] | 吴涓, 李清彪.2001. 黄孢原毛平革菌吸附铅离子机理的研究[J]. 环境科学学报 , 2001, 21 (3) : 291–295. |
| [${referVo.labelOrder}] | 熊芬, 胡勇有, 银玉容.2009. 烟曲霉胞外聚合物对Pb2+的吸附特性[J]. 环境科学学报 , 2009, 29 (11) : 2289–2294. |
| [${referVo.labelOrder}] | Zhang P, Chen Y P, Guo J S, et al. 2014. Adsorption behavior of tightly bound extracellular polymeric substances on model organic surfaces under different pH and cations with surface plasmon resonance[J]. Water Research , 57 : 31–39. DOI:10.1016/j.watres.2014.03.018 |
| [${referVo.labelOrder}] | 郑蕾, 丁爱中, 王金生, 等.2008. 不同组成活性污泥胞外聚合物吸附Cd2+、Zn2+特征[J]. 环境科学 , 2008, 29 (10) : 2850–2855. |
| [${referVo.labelOrder}] | 张秀丽, 刘月英.2002. 贵、重金属的生物吸附[J]. 应用与环境生物学报 , 2002, 8 (6) : 668–671. |
| [${referVo.labelOrder}] | 周东琴, 魏德洲.2006. 沟戈登氏菌对重金属的生物吸附-浮选和解吸性能[J]. 环境科学 , 2006, 27 (5) : 960–964. |
| [${referVo.labelOrder}] | 周健, 栗静静, 龙腾锐, 等.2008. 胞外聚合物EPS在废水生物除磷中的作用[J]. 环境科学学报 , 2008, 28 (9) : 1758–1762. |
 2016, Vol. 36
2016, Vol. 36


