2. 辽宁省生物炭工程技术研究中心, 沈阳 110866
2. Liaoning Biochar Engineering and Technology Research Center, Shenyang 110866
耕地碳库是陆地碳库的重要组成部分,其微小的波动就可能对温室气体浓度乃至全球碳平衡产生重大影响(刘昱等,2015).因此,土壤有机碳作为耕地质量的重要指标,不仅是提高系统生产力的重要途径,更影响着陆地碳循环过程.研究土壤有机碳的保持与提升,对于保障食品安全和缓解气候变化具有深远意义.
生物炭是秸秆、粪便等有机物料在低氧环境下,经高温(300~700 ℃)热解而得到的一类比表面积大、孔隙多、吸附和稳定性强的高度芳香化富碳物质(Antal et al.,2003).近年来,生物炭在诸多研究领域上的应用引起广泛关注,其在改良土壤耕性、增加土壤碳汇、减排温室气体及修复污染等方面呈现出可观潜力(Lehmann ,2007).最近10年,国际上将生物炭作为土壤改良剂及固碳剂的研究日益增多,越来越多的证据表明生物炭施于土壤后可以显著提高土壤有机碳含量,利于土壤团聚体的形成并降低土壤容重(Krull et al.,2006;Novak et al.,2009;Zwieten et al.,2010).Kimetu等(2010)进一步研究发现,施用生物炭后土壤有机碳矿化量减少,使得已存在的有机碳稳定性上升.
以往的研究多注重总体碳库的评价,对微观碳组分和土壤固碳优势形成机理的研究较少.土壤有机碳库是由复杂的有机物组合而成,不同有机碳库由于团聚体和有机碳之间的相互联系而具有不同的活性和稳定性.团聚体的保护作用使有机碳的抗分解能力加强,增强其稳定性,同时有机碳的胶结作用也会促进团粒结构的形成.土壤团聚体按照颗粒大小分为大团聚体(粒径 > 0.25 mm)和微团聚体(粒径 < 0.25 mm),大团聚体丰富是土壤良好结构特征的表现,其与土壤肥力之间存在一定的正比例关系(Six et al.,2000).因此,研究生物炭对土壤团聚体组分特征及其有机碳库的变化的影响有利于明确生物炭土壤碳库的稳定性及其保护机制.基于土壤团聚体分组的土壤有机碳组分分析,是目前研究土壤有机碳物理保护机制的重要手段.一项针对砂姜黑土的盆栽试验表明,单施生物炭对土壤大团聚体含量和稳定性的影响不显著,而生物炭与秸秆配合效果明显,有效改善了土壤性状(侯晓娜等,2015).与此相左的是,吴鹏豹等在海南砖红壤上施用生物炭18个月后,土壤团聚体的几何平均直径(GMD)显著增加(吴鹏豹等,2012).
云南是我国最大的烤烟种植区,常年植烟面积稳定在35万hm2.该烟区的代表性土壤是红壤,通常较为黏重,发育欠完全,团聚体稳定性较差,加之长期集约化耕作,烟田土壤有机碳含量呈现逐渐降低态势(邱学礼等,2013),应用生物炭进行烟区土壤改良具有广阔的前景和积极的意义.然而,土壤有机碳的固定和保持是一个生物、物理、化学的综合过程,关于生物炭对云南典型酸性红壤团聚体组成及有机碳分布的影响还不清楚;多数研究均是盆栽试验或模拟试验,缺乏较长期的田间研究分析土壤团聚体保护与土壤有机碳稳定的相互作用机制.因此,针对云南烟区典型红壤,本研究通过3年期定位试验持续向植烟土壤添加不同用量的生物炭,研究生物炭对土壤团聚体组成和稳定性、有机碳含量以及有机碳分布等方面的影响及作用,旨在为生物炭在云南典型烟区土壤改良中的利用提供科学依据,保障当地农业生产健康可持续发展.
2 材料与方法(Materials and methods) 2.1 试验材料试验地位于玉溪市红塔区,地理坐标24°17′N,102°35′E,海拔1692 m,属亚热带季风气候,2012—2014年降雨量为819~883 mm,初始土壤理化性状等情况见表 1.在试验开始前为“烤烟-油菜-烤烟”栽培模式.本研究的烤烟栽培品种为K326.
| 表 1 试验地土壤背景情况 Table 1 Soil physical and chemical properties before experiment |
试验所用生物炭为烟秆炭,将烟秆粉碎至3~5 cm长,置于专用炭化设备(本单位与辽宁省生物炭工程技术研究中心合作研发),在450 ℃条件下进行缺氧干馏炭化,反应停留时间30 min,炭化完成后,自然冷却至室温后取出,混匀研磨,过80目筛,贮于干燥容器中,备用.所制备的烟秆生物炭含碳量为64.9%,灰分含量18.6%,全氮含量3.1%,比表面积6.2 m2·g-1.
2.2 试验设计试验设计3个处理,分别为B0:常规施肥不施用生物炭,B15:常规施肥并施用生物炭15 t·hm-2,B30:常规施肥并施用生物炭30 t·hm-2,生物炭按设计用量1年施用1次.每个处理均设3次重复,每次重复面积为1/15 hm2,各小区随机排列.试验为长期定位试验,自2011年烤烟收获后开始,至2014年烤烟收获后止,生物炭于2012—2014年每年的4月20—25日施用,试验区内统一采用“烤烟-冬闲-烤烟”的栽培模式.
常规施肥参照玉溪优质烤烟综合标准(云南省烟草公司玉溪市公司,2006),移栽时单株穴施50%烟草专用复合肥作为基肥,其余50%专用复合肥于移栽后25 d追施,施氮量统一为120 kg·hm-2,肥料类型为烤烟专用复合肥,N:P2O5:K2O = 12:6:24.移栽后40 d追施K2SO4(含K2O 50%),施用量120 kg·hm-2.株行距0.5 m × 1.2 m,种植密度为16500株·hm2,其他田间管理技术参照玉溪优质烤烟综合标准执行.烤烟移栽于每年的4月20—25日进行,每年9月1—5日采烤结束.生物炭施用方法为犁地前撒施,并翻耕,与耕层20 cm土壤充分混匀.
2.3 土壤样品采集自2011年至2014年,于每年12月中旬采集土样,采集深度0~20 cm,各小区五点采集原状土样,每份500 g,混匀后留取500 g备用.原状在风干过程中沿自然裂隙掰成直径为1 cm左右大小的团聚体,供土壤团聚体测定.同样按五点法采集各小区扰动土样,风干后过筛测定土壤总有机碳含量.
2.4 测定项目与方法 2.4.1 土壤团聚体特征及其有机碳含量分析土壤有机碳物理分组结合了Elliot等(Elliot,1986)方法的优点,采用改良湿筛法(Cambardella,1993),分离得到土壤水稳性团聚体.具体为:取10 g 过8 mm 筛的风干土,将土壤浸润20 min后,轻轻放入置于水桶中的套筛(孔径依次为2 mm、0.25 mm、0.053 mm)顶部,2 min后启动团聚体分析仪,转速为20 r·min-1,持续15 min.收集留在筛子上的各级团聚体,所有组分于50 ℃烘干称质量,并使用元素分析仪(Elementar Vario MAX 德国)测定有机碳含量.
2.4.2 土壤团聚体稳定性土壤团聚体稳定性指标采用平均重量直径(MWD)、几何平均直径(GMD)、以及大于0.25 mm的团聚体含量(R> 0.25)来描述(Vanavel,1949;Mazurak,1950),计算公式如下:
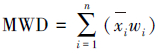
|
(1) |
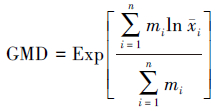
|
(2) |
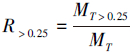
|
(3) |
式中,xi为i粒级团聚体平均直径,wi为i粒级团聚体质量比,mi为不同粒级团聚体的质量,MT为团聚体总质量.
2.5 数据分析采用SAS8.0和EXCEL2007分析软件进行数据的统计、分析与绘图制表.所有结果均为3次测定平均值,处理之间的多重比较采用Duncan新复极差法(p < 0.05).
3 结果与分析(Results and analysis) 3.1 不同施炭处理对耕层土壤有机碳含量的影响如图 1所示,整个试验期内施用生物炭显著提高了耕层土壤(0~20 cm)总有机碳含量.在试验的前2年,土壤总有机碳含量随着生物炭用量的增加快速上升,而到第3年总有机碳含量增幅放缓,施用生物炭的处理年际间差异显著.试验结束时,B15和B30处理土壤总有机碳含量较B0对照分别增加了38.7%和60.1%.
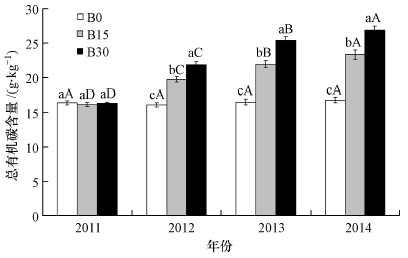 |
| 图 1 持续施用生物炭条件下土壤总有机碳含量 Total soil organic carbon content with persistent application of biochar Fig. 1 注:不同小写字母表示同一时期不同处理间差异达显著水平(P < 0.05),不同大写字母表示同一处理不同时期差异达显著水平(P < 0.05). Note:Different small letters indicate the significant difference between treatments with the same year (P < 0.05), and different capital letters indicate the significant difference between years with the same treatment (P < 0.05). |
施用生物炭对砂岩类红壤团聚体分布具有显著影响(表 2).与对照相比,施用生物炭在第一年就显著增加了 > 2 mm和0.25~2 mm粒级团聚体含量,而0.053~0.25 mm粒级团聚体含量无显著变化,< 0.053 mm粒级团聚体含量则显著降低.随着生物炭施用年限和累计施用量的增加, >2 mm和0.25~2 mm粒级团聚体含量也持续增加,与对照差异显著,年际间差异也显著,其中0.25~2 mm粒级团聚体增加量最大.到试验结束时,B15处理 > 2 mm和0.25~2 mm粒级团聚体含量较B0对照分别增加了57.8%和24.9%,B30处理则分别增加了77.8%和36.4%.与此同时,相较对照,B15和B30处理0.053~0.25 mm粒级团聚体含量仍无显著差异; < 0.053 mm粒级团聚体含量则分别降低了28.6%和39.5%.
| 表 2 持续施用生物炭条件下土壤团聚体分布情况 Table 2 Soil aggregate distribution with persistent application of biochar |
以MWD、GMD和R> 0.25为指标分析,结果如表 3所示.连续3年施用生物炭后,B15和B30处理MWD、GMD和R> 0.25值大幅提高,均显著高于对照,土壤团聚体稳定性增强.其中B15处理上述3指标分别提高了81.3%,54.5%和28.9%,B30处理则分别提高了106.3%,81.8%和42.1%.各处理间差异显著.
| 表 3 持续施用生物炭3年后土壤团聚体稳定性 Table 3 Soil aggregate stability with 3 years′ continued application of biochar |
施用生物炭显著提高了各粒级团聚体的碳浓度(表 4).与对照相比,施用生物炭在第一年就显著增加了各粒级团聚体碳浓度.随着生物炭施用年限和累计施用量的增加,各粒级团聚体碳浓度也持续增加,与对照差异显著.到试验结束时,B15处理 > 2 mm,0.25~2 mm,0.053~0.25 mm,< 0.053 mm粒级团聚体碳浓度较B0对照分别增加了10.3%,28.9%,31.4%和40.7%;B30处理则分别增加了15.8%,48.0%,50.5%和50.9%.同时,除 > 2 mm团聚体外,B15和B30处理之间其它各粒级团聚体碳浓度也呈显著差异.
| 表 4 持续施用生物炭条件下土壤团聚体的有机碳浓度 Table 4 Soil aggregate organic carbon concentrations with persistent application of biochar |
总体上,有机碳主要分布在0.053~2 mm粒级的团聚体上,> 2 mm的大团聚体分布较少(图 2).对于 > 0.25 mm粒级的团聚体,施用生物炭显著提高了其团聚体有机碳的贡献率;对于 < 0.25mm粒级的团聚体,则降低了其贡献率.其中0.25~2 mm粒级的团聚体随生物碳施用以及用量的增加,其有机碳贡献率增幅最大,试验结束时B15和B30处理该粒级有机碳贡献率相比对照分别增加7.3%和11.8%;而 < 0.053 mm粒级的团聚体,其有机碳贡献率降幅最大,B15和B30处理相比对照分别减少6.8%和10.6%.
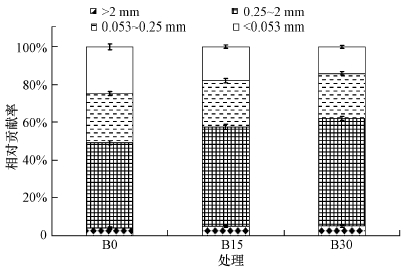 |
| 图 2 持续施用生物炭3年后土壤各粒级团聚体有机碳的相对贡献率 Fig. 2 Relative contributions of organic carbon in aggregates after 3 years′ biochar application |
生物炭富含有机碳且具有较强的生物化学稳定性,其本身不易被微生物利用(Lehmann,2007),还田后可作为一种相对稳定的碳源固定在土壤中.同时,生物炭与土壤团聚体结合,减少了其与外界的接触面积,降低了土壤有机质的矿化率,从而促进土壤固碳(Liang et al.,2010; 章明奎等,2012).有研究结果表明,生物炭添加到土壤后,会促进土壤腐殖质的形成,有助于碳水化合物、芳香烃等难以被微生物利用的有机大分子的形成(花莉等,2012),间接说明了生物炭对于提高土壤有机碳的截获和碳的固定潜力具有重要作用.本试验结果表明,随着试验年限的增加,B0处理耕层土壤有机碳含量无显著变化,而施炭处理(B15、B30)逐年增加,表现为B30 > B15.
土壤团粒结构是土壤肥力的物质基础,是作物优质高产所必须的土壤条件之一,土壤团聚体作为土壤团粒结构的基本单元,其组成及稳定性是反映土壤结构状况的重要指标(Lehmann,2007).Gaskin等(Gaskin et al .,2008)研究表明,生物炭还田有利于形成良好的土壤团聚体.土壤中生物炭一方面有利于团聚体的形成和稳定,另一方面受团聚体的保护而长期固持(尚杰等,2015).本研究发现,经过3年试验,不同用量生物炭处理对 > 0.25 mm土壤团聚体数量有显著影响,且表现为B30 > B15 > B0,对0.053~0.25 mm粒级的土壤团聚体数量没有显著影响,而对 < 0.053 mm粒级的土壤团聚体数量则表现为B0 > B15 > B30.
MWD 、GMD和R>0.25 是反映土壤团聚体大小分布状况的常用指标,其值越大,表示团聚体的平均粒径团聚度越高,稳定性越强.由表 3可知,连续施用生物炭可大幅提高耕层土壤团聚体稳定性,其中高炭量(B30)效果最好.Glaser等(2002)研究生物炭对土壤团聚体的作用时发现,生物炭刺激土壤生物活性增强,进而产生更多的分泌物,形成土壤团聚体的胶结物质,从而增强团聚体的稳定性.也有研究表明,施用生物炭虽然能增加土壤团聚体含量,却对土壤团聚体的形成和稳定性无显著影响,这与土壤质地及生物炭性质有关(Liu et al.,2012).施用粒径较大的生物炭可能限制土壤-微生物-生物炭之间的相互作用,从而减缓土壤团聚体的形成过程(Zhang et al.,2015).
分析本试验条件下各级土壤团聚体中有机碳浓度可知,连续多年施用生物炭可有效提高各级团聚体中的有机碳含量.与B0处理比较,B15处理在 > 2 mm、0.25~2 mm、0.053~0.25 mm、 < 0.053 mm 4个粒级团聚体中有机碳浓度分别提高10.3%、28.9%、31.4%、40.7%;B30处理则分别提高15.8%、48.0%、50.5%、50.9%.吴鹏豹等(2012)对花岗岩砖红壤施用生物炭,结果发现土壤大团聚体中总有机碳分配的比例显著提高,这与本研究结果相似.从图 2分析可发现,随施炭量的增加,> 0.25 mm粒级的土壤团聚体有机碳相对贡献率显著提高,而 < 0.25 mm粒级的土壤团聚体有机碳相对贡献率则呈现下降趋势,表明大团聚体富集外源有机碳的能力更强,生物炭主要通过增加大团聚体中碳含量的方式来增加土壤有机碳的稳定性.这可能由于生物炭通过稳定力作用与土壤矿物形成土壤团聚体,团聚体的物理保护作用降低了微生物对土壤有机碳的分解(Lu et al.,2014).还有研究认为原因可能在于生物炭对土壤酶的吸附降低了与有机碳周转相关酶的活性(Pravogo et al.,2002).
综合本试验结果可发现,连续施用生物炭能增加大团聚体比例,降低微团聚体比例,增加团聚体的平均重量直径和几何平均直径,提高土壤团聚体稳定性和各级团聚体有机碳含量,从而改善土壤结构及增加土壤碳汇能力.同时,土壤团聚体对施用生物炭的响应特征还与生物炭还田量及生物炭与土壤反应时间有关.随着施炭量的增加和试验时间的延长,生物炭对土壤团聚体组成及有机碳含量的影响愈发显著.
| [1] | Antal M J, Gronli M. 2003.The art, science and technology of charcoal production[J]. Industrial and Engineering Chemistry, 42 : 1619–1640. |
| [2] | Cambardella A C, Elliott T E. 1993.Carbon and nitrogen distribution in aggregates from cultivated and native grassland soils[J]. Soil Science Society of America Journal, 57 : 1071–1076. |
| [3] | Elliot E T. 1986.Aggregate structure and carbon, nitrogen, and phosphorus in native and cultivated soil[J]. Soil Science Society of America Journal, 50 : 627–633. |
| [4] | Gaskin J W, Steiner C, Harris K, et al. 2008.Effect of low temperature pyrolysis conditions on biochar for agricultural use[J]. Transations of the American Society of Agricultural and Biological Engineers, 51 : 2061–2069. |
| [5] | Glaser B, Lehmann J, Zech W. 2002.Ameliorating physical and chemical properties of highly weathered soils in the tropics with charcoal:A review[J]. Biology and Fertility of Soils, 35 : 219–230. |
| [6] | 侯晓娜, 李慧, 朱刘兵, 等.2015.生物炭与秸秆添加对砂姜黑土团聚体组成和有机碳分布的影响[J].中国农业科学, 48 (4):705–712. |
| [7] | 花莉, 金素素, 洛晶晶.2012.生物质炭输入对土壤微域特征及土壤腐殖质的作用效应研究[J].生态学报, 21 (11):1795–1799. |
| [8] | Kimetu J M, Lehmann J. 2010.Stability and stabilisation of biochar and green manure in soil with different organic carbon contents[J]. Soil Research, 48 (7): 577–585. |
| [9] | Krull E S, Swanston C W, Skjemstad J O, et al. 2006.Importance of charcoal in determining the age and chemistry of organic carbon in surface soils[J]. Journal of Geophysical Research, 111 : G04001. |
| [10] | Liang B Q, Lehmann J, Sohi S P, et al. 2010.Black carbon affects the cycling of non-back carbon in soil[J]. Organic Geochemistry, 41 (2): 206–213. |
| [11] | 刘昱, 陈敏鹏, 陈吉宁.2014.农田生态系统碳循环模型研究进展和展望[J].农业工程学报, 31 (3):1–9. |
| [12] | Lehmann J. 2007.A handful of carbon[J]. Nature, 447 : 143–144. |
| [13] | Liu X H, Han F P, Zhang X C. 2012.Effect of biochar on soil aggregates in the loess plateau:results from incubation experiments[J]. International Journal of Agriculture & Biology, 14 : 975–979. |
| [14] | Lu S G, Sun F F, Zong Y T. 2014.Effect of rice husk biochar and coal fly ash on some physical properties of expansive clayey soil(Vertisol)[J]. Catena, 114 : 37–44. |
| [15] | Mazurak A P. 1950.Effect of gaseous phase on water-stable synthetic aggregates[J]. Soil Science, 69 : 135–148. |
| [16] | Novak J M, Busscher W J, Laird D L, et al. 2009.Impact of biochar amendment on fertility of a southeastern coastal plain soil[J]. Soil Science, 174 (2): 105–112. |
| [17] | Prayogo C, Jones J E, Baeyens J, et al. 2014.Impact of biochar on mineralization of C and N from soil and willow litter and its relationship with microbial community biomass and structure[J]. Biology and Fertility of Soils, 50 : 695–702. |
| [18] | 邱学礼, 李军营, 李向阳, 等.2013.云南省植烟土壤有机碳分布特征及其影响因素[J].中国农学通报, 29 (04):51–56. |
| [19] | Six J, Elliot E T, Paus tian K. 2000. Soil structure and soil organic matter:Ⅱ. A normalized stability index and the effect of mineralogy[J]. Soil Science Society of America Journal, 64:1042-1049 |
| [20] | 尚杰, 耿增超, 赵军, 等.2015.生物炭对塿土水热特性及团聚体稳定性的影响[J].应用生态学报, 26 (7):1969–1976. |
| [21] | Vanavel C H M. 1949.Mean weight-diameter of soil aggregates as a statistical index of aggregation[J]. Soil Science Society of America Journal, 14 : 20–23. |
| [22] | 吴鹏豹, 解钰, 漆智平, 等.2012.生物炭对花岗岩砖红壤团聚体稳定性及其总有机碳分布特征的影响[J].草地学报, 20 (4):643–650. |
| [23] | 云南省烟草公司玉溪市公司. DB53/T 182.1-2006 玉溪优质烤烟综合标准体系[S]. 北京:中华人名共和国国家质量监督检验检疫总局 |
| [24] | Zwieten L Van, Kimber S, Morris S, et al. 2010.Effects of biochar from slow pyrolysis of papermill waste on agronomic performance and soil fertility[J]. Plant and Soil, 327 : 235–246. |
| [25] | 章明奎, 顾国平, 王阳.2012.生物质炭在土壤中的降解特征[J].浙江大学学报:农业与生命科学版, 38 (3):329–335. |
| [26] | Zhang Q Z, Du Z L, Lou Y L. 2015.A one-year short-term biochar application improved carbon accumulation in large macroaggregate fractions[J]. Catena, 127 : 26–31. |
 2016, Vol. 36
2016, Vol. 36


