2. 暨南大学环境学院, 广东省环境污染控制与修复材料工程中心, 广州 510632
2. Guangdong Provincial Research Center for Environment Pollution Control and Remediation Materials, School of Environment, Jinan University, Guangzhou 510632
抗生素被广泛用于人类医疗及动物养殖中,使用后大部分以药物原形随粪尿等形式进入土壤环境(Shi et al., 2012;Li et al., 2014) .目前,在土壤及蔬菜甚至所谓安全蔬菜(无公害蔬菜、绿色蔬菜和有机蔬菜)中均普遍检出抗生素,其中喹诺酮类抗生素检出较高(检出率 >95%),严重威胁农产品安全和人体健康(吴小莲等,2011;吴小莲等,2013a;吴小莲等,2013b).物化修复是解决土壤抗生素污染的直接方式,但成本较高,难以解决大面积农田土壤污染问题.通过筛选、研究和培育污染物低积累的作物品种,可实现有效利用污染土壤生产并对其修复的目的,已成为保障农产品质量安全的重要策略.为此,我们筛选获得了高、低吸收积累喹诺酮类抗生素环丙沙星(CIP)的菜心品种(高积累型-油青四九菜心,低积累型-油绿粗苔菜心).在不同浓度土培条件下,高、低积累菜心地上部CIP含量相差3~10倍(吕璇等,2014),但差异的机理尚未明确.
植物抗氧化系统可抵御污染物胁迫,是避免或降低污染物对植物损伤的重要屏障(Sun et al., 2007;Jin et al., 2008a).前人研究显示,重金属超积累作物抗氧化系统性能显著强于普通品种或低积累型品种(Jin et al., 2008b;Jin et al., 2009) .然而关于有机污染物高、低积累品种间抗氧化性能差异的研究鲜见报道.因此,本文以CIP高、低积累菜心为研究对象,研究二者抗氧化性能差异及其与菜心吸收积累CIP的联系,以期初步查明菜心高、低吸收积累CIP的机理
2 材料与方法(Materials and methods) 2.1 实验材料实验菜心:CIP高、低积累菜心种子均购自广东省农科院.
实验试剂:环丙沙星(CIP),购自德国Dr. Ehrenstorfer公司,纯度>98%.甲醇、乙腈为色谱纯,购自Sigma公司;超氧化歧化酶(SOD)试剂盒、过氧化物酶(POD)试剂盒、过氧化氢酶(CAT)试剂盒、蛋白质(TP)试剂盒以及丙二醛(MDA)试剂盒均购自南京建成有限公司;其他试剂均为分析纯,购自广州化学试剂有限公司,实验用水为去离子水
2.2 实验方法 2.2.1 水培实验选择籽粒饱满,大小均匀的高、低积累菜心种子,用1%(m/V)的氯化汞浸泡消毒5 min,之后用去离子水冲洗3遍,吸干水分,播种于育苗板.待菜心长到3片真叶时,采用叶菜类营养液配方(刘士哲,2011)分别配置含CIP浓度为0、0.2、1.0、5.0 mg·L-1的营养液,即空白、低、中、高CIP浓度处理组.再将两种菜心幼苗分别移植到盛放20 L含不同浓度CIP营养液的培养箱(长49 cm、宽42 cm、高47 cm)中,每箱种植12株菜心幼苗,水培实验于2013年3—5月在暨南大学环境工程系温室进行. 为保证植株氧气需求,采用通气泵24 h供气.各处理营养液pH值采用0.1 mol·L-1 NaOH或0.1 mol·L-1 HCl进行调节,使其在实验期间保持在6.2~6.5之间.每浓度抗生素处理设置3个重复.水培实验40 d后采集菜心样品,用去离子水多次冲洗以去除吸附于菜心根表的CIP,之后将其切分为根系及地上部分(切分过程在0 ℃冰水中进行),进行各项指标测定.
2.2.2 菜心中CIP含量的测定所采集菜心样品(根系或地上部分)经冷冻干燥、磨碎后,准确称取1.0 g样品于50 mL离心管,加入6 mL的1%酸化乙腈进行萃取,萃取3次后,以HLB固相萃取(3 mL/60 mg,Waters)柱富集、净化,之后氮吹浓缩,并以0.1%甲酸溶液(初始流动相)定容备测. CIP采用超高效液相色谱-串联质谱(HPLC-MS/MS)法测定(吴小莲等,2013c),色谱条件为高效液相色谱仪(Agilent 1100) ,Eclipse XDB-C18色谱柱(150 mm×2.1 mm,5 μm,Agilent),柱温35 ℃,进样量5 μL;质谱条件为电喷雾(ESI)串联质谱仪(AB4000QTRAP,Agilent),正离子扫描,多反应检测模式(MRM).为保证CIP测定的准确性,每间隔8个样品分别测定平行样、空白样以及样品基质加标样.结果显示,平行样间相对标准偏差均小于10%,空白样中未检出CIP,空白加标回收率在90%~95%之间;样品加标回收率在67%~88%之间;CIP的检测限为0.24 μg·kg-1,定量限为0.84 μg·kg-1.
2.2.3 菜心抗氧化系统酶、蛋白质及丙二醛测定方法菜心组织匀浆液制备:准确称取5.0 g菜心样品,加入25 mL pH值为7.4的磷酸盐缓冲液,冰浴条件下制备成20%(m/V,g·mL-1)的组织匀浆,离心10 min(3500 r·min-1)后,取上清液备测.
抗氧化系统酶活性、蛋白质及丙二醛测定:根据南京建成试剂盒标准方法(王震宇等,2010),以考马斯亮蓝法测定总蛋白含量(TP),以黄嘌呤氧化酶法测定过氧化歧化酶(SOD)活性,以愈创木酚法测定过氧化物酶(POD)活性,以硫代巴比妥酸法测定丙二醛(MDA)含量.TP的测定结果以每克植物样品(鲜重)的蛋白含量表示,记作mg·g-1;SOD酶及POD酶测定结果均以每毫克蛋白的酶活力表示,记作U·mg-1 ; MDA的测定结果以每毫克蛋白的MDA含量表示,记作nmol·mg-1
2.3 数据处理与分析采用Excel 2007进行数据处理和绘图.采用SPSS 17.0进行数据统计分析,计算平均值、标准差,并进行回归分析和方差分析.实验结果以平均值±标准偏差(Mean±SD)表示,p< 0.05指示处理组间或处理组与空白处理间差异显著.
3 结果(Results) 3.1 高、低积累菜心CIP含量特征不同CIP浓度条件下,高积累菜心根部及地上部分CIP含量均大于低积累菜心,且在高浓度CIP时,前者显著大于后者,二者差异可达2.1倍(表 1).需要说明的是,水培条件下高、低积累菜心CIP的含量差异(~2.1倍)小于二者在土培条件下的差异(3~10倍)(吕璇等,2014),这与CIP在水溶液中生物有效性较强,易于被菜心吸收积累有关(王朋等,2011;吴小莲等,2013b;尹倩等,2013).计算显示,高积累菜心根富集系数,即CIP根部含量与培养液含量之比(14.6~24.0) 高于低积累菜心(11.3~13.5) ,而其转运系数,即CIP地上部含量与根部含量之比(0.006~0.014) 与低积累菜心(0.006~0.011) 相当,指示高积累菜心根部对CIP的高富集作用是其高积累CIP的重要原因.
| 表 1 不同浓度CIP胁迫下高、低积累菜心各部位CIP含量 Table 1 CIP concentration in low- and high-CI |
空白处理条件下,高、低积累菜心地上部生物量相当,但前者根部生物量显著大于后者(图 1).在低浓度下,CIP即可抑制两种菜心生物量,且随其浓度增加,抑制作用显著增强.相关性分析显示,两种菜心地上部和根部生物量均与其CIP含量呈显著负相关关系,指示吸收积累CIP是造成两种菜心生物量降低的主要原因.值得注意的是,在各CIP浓度处理下,高积累CIP菜心地上部和根部生物量均与低积累CIP菜心相当,但其CIP含量高于后者,指示高积累菜心对CIP的解毒和耐受能力强于后者
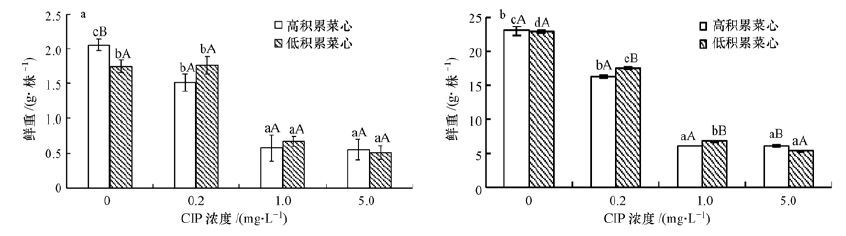 |
| 图 1 CIP胁迫下高、低积累菜心生物量差异(a.根部;b.地上部)(注:同一CIP浓度不同菜心品种含相同大写字母者差异不显著,同一菜心品种不同CIP浓度含相同小写字母者差异不显著) Fig. 1 Biomass differences in low- and high-CIP accumulation cultivars of Chinese flowering cabbages under CIP stress(a. root; b. shoot) |
蛋白质是生物体细胞代谢(物质吸收积累等)及抗逆性(氧化损伤等)的物质基础(林仁漳等,2008;Liu et al., 2010) .空白处理条件下,高积累菜心根部(1.1 mg·g-1)及地上部分蛋白质含量(3.4 mg·g-1)分别与低积累菜心相当(根部 1.1 mg·g-1,地上部 4.4 mg·g-1).CIP胁迫下,两种菜心根部蛋白质含量均较空白处理有所提高,且提高率随CIP浓度升高而提高,在16%~105%之间(图 2a).值得注意的是,不同浓度CIP胁迫下,高积累菜心根部蛋白质含量均高于低积累菜心,且在高浓度CIP胁迫下二者差异显著.对于地上部而言(图 2b),低浓度CIP(0.2 mg·L-1)胁迫下高积累菜心蛋白质含量显著高于空白处理,随着CIP浓度提高(1~5 mg·L-1),高积累菜心蛋白质含量有所下降,但均与空白含量相当.与此不同,CIP胁迫下低积累菜心地上部蛋白质含量显著低于空白处理,且随CIP浓度提高其含量显著降低.可见,CIP胁迫下高积累菜心根部及地上部蛋白质含量总体大于低积累菜心
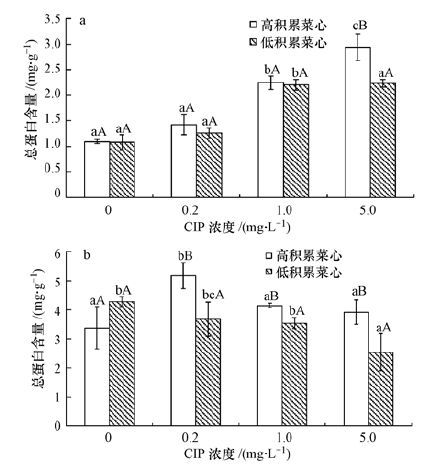 |
| 图 2 CIP胁迫下高、低积累菜心蛋白质含量差异(a. 根部; b.地上部)(注:同一CIP浓度不同菜心品种含相同大写字母者差异不显著,同一菜心品种不同CIP浓度含相同小写字母者差异不显著) Fig. 2 Protein content differences in low- and high-CIP accumulation cultivars of Chinese flowering cabbages under CIP stress(a. root; b. shoot) |
SOD酶可清除污染物诱导产生的过氧自由基(O2-·),是植物抗氧化系统发挥功能的首要酶(张琼等,2010;雷静静等,2013;徐湘博等,2014). 空白处理条件下,高、低积累菜心根部(64.4~64.5 U·mg-1)及地上部分SOD酶活性(19.5~21.1 U·mg-1)均分别相当. 低浓度CIP胁迫时,高、低积累菜心根部SOD酶活性均与空白相当;随着CIP浓度升高,在中浓度时,高、低积累菜心根部SOD酶活性均显著降低,但二者差异不显著;在高浓度时,高积累菜心根部SOD酶活性有所提高,而低积累菜心根部SOD酶活性有所下降,因此前者根部SOD酶活性显著大于后者.对于地上部而言,低浓度CIP胁迫下,高、低积累菜心SOD酶活性均与空白相当,但随CIP浓度升高,二者SOD酶活性均显著高于空白处理,且高积累菜心SOD酶活性显著大于低积累菜心.
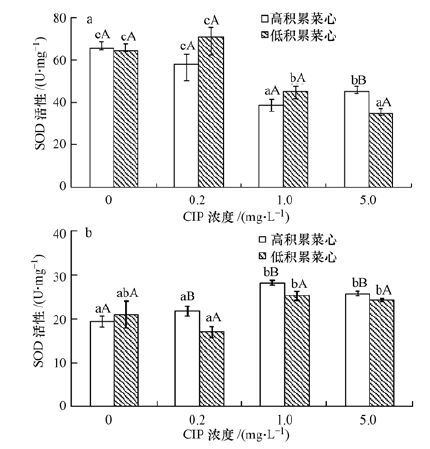 |
| 图 3 CIP胁迫下高、低积累菜心SOD酶差异(a. 根部; b.地上部)(注:同一CIP浓度不同菜心品种含相同大写字母者差异不显著,同一菜心品种不同CIP浓度含相同小写字母者差异不显著.) Fig. 3 SOD activity differences in low- and high-CIP accumulation cultivars of Chinese flowering cabbages under CIP stress(a. root; b. shoot) |
POD酶可清除植物体内的过氧化氢(H2O2),是组成植物抗氧化系统的重要酶(华涛和周启星,2009;周坤等,2014).空白处理条件下,两种菜心根部(52.40~59.70 U·mg-1)及地上部分POD酶活性(230.8~223.5 U·mg-1)均无显著差异(图 4).CIP胁迫下,两种菜心根部POD酶活性均随CIP浓度升高而显著降低,当CIP为中、低浓度时,两种菜心根部POD酶活性相当,当CIP为高浓度时,高积累菜心根部POD酶活性显著高于低积累菜心.对于地上部分而言,高积累菜心POD酶活性呈现随CIP浓度上升而上升的特征,而低积累菜心POD酶活性随CIP浓度变化不大,即CIP胁迫下,高积累菜心地上部POD酶活性总体大于低积累菜心.
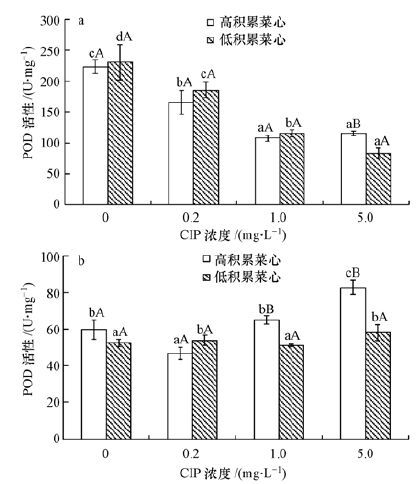 |
| 图 4 CIP胁迫下高、低积累菜心POD酶的差异(a. 根部; b.地上部)(注:同一CIP浓度不同菜心品种含相同大写字母者差异不显著,同一菜心品种不同CIP浓度含相同小写字母者差异不显著.) Fig. 4 POD activity differences in low- and high-CIP accumulation cultivars of Chinese flowering cabbages under CIP stress(a. root; b. shoot) |
MDA是污染物胁迫产生的主要膜脂过氧化产物之一,其含量高、低是衡量植物膜脂损伤程度的重要指标(Wang et al., 2008;田文静等,2010;Wang et al., 2011) .空白处理条件下,高积累菜心根部MDA含量(5.3 nmol·mg-1)显著高于低积累菜心(3.4 nmol·mg-1).CIP胁迫下(低至高浓度),低积累菜心根部MDA含量均显著高于高积累菜心,但随CIP浓度增加二者MDA含量均显著下降,这与CIP激活菜心抗氧化酶有关.对于地上部而言,空白处理下,低积累菜心MDA含量(0.65 nmol·mg-1)显著高于高积累菜心(0.37 nmol·mg-1).CIP胁迫下(低至高浓度),低积累菜心MDA含量较其空白处理增高迅速,达到0.87~0.97 nmol·mg-1,显著高于高积累菜心MDA含量(0.29~0.49 nmol·mg-1).
4 讨论(Discussion)抗氧化系统是植物防御污染物胁迫与耐性机制的重要组成部分,其对减少或避免细胞氧化损伤有重要意义(An et al.,2009 .前人研究显示,CIP胁迫下(0~50 mg·L-1),玉米幼苗抗氧化酶(过氧化氢酶CAT、超氧化物歧化酶SOD及过氧化物酶POD等)呈现低浓度被激活,而高浓度被抑制的特征(王朋等,2011).与此不同,本文研究显示,CIP(0~5 mg·L-1)对高、低积累菜心根部及地上部可溶性蛋白质、SOD酶活性和POD酶活性的影响呈现出多种特征,包括随CIP浓度增加而增加,随CIP浓度升高而降低,或随CIP浓度变化不大等(图 2、图 3、图 4).不同研究间结果的差异与实验设置浓度及作物品种差异等因素有关.
植物品种间抗氧化系统性能的差异由其基因型差异决定(Jin et al., 2008) .抗氧化能力强的作物品种,清除污染物产生活性氧化物质(如O-·2、H2O2、OH·等)的能力较强,因此污染物胁迫下其细胞氧化损伤程度较低,对污染物耐受性高,有利于其吸收累积污染物.反之,抗氧化能力弱的作物品种,为减少污染物造成的氧化损伤,尽量低吸收积累污染物(Andrade et al., 2010) .前人研究发现,重金属超积累植物抗氧化能力显著强于普通品种(Sun et al., 2007;Jin et al., 2008) .与此类似,有机污染物CIP胁迫下,高积累菜心根部及地上部诱导出更多的功能蛋白质(如载体蛋白、识别蛋白、抗氧化蛋白等(苏恩平等,2014),且其SOD酶活性和POD酶活性总体强于低积累菜心(图 2、图 3、图 4),因此,高积累菜心膜脂损伤程度(MDA含量)低于后者(图 5),对CIP的耐性和解毒能力更强,有利于其吸收积累CIP.可见,菜心品种间抗氧化性能是决定其高、低积累CIP的重要生理生化机制. 需要指出的是,除抗氧化性能外,决定作物高、低积累污染物的因素还包括植物根际微生物、根系分泌物、根脂成分与含量以及污染物辛醇水分配系数等(Dettenmaier et al., 2008) ,这些因素对作物高、低积累污染物的影响还有待深入研究
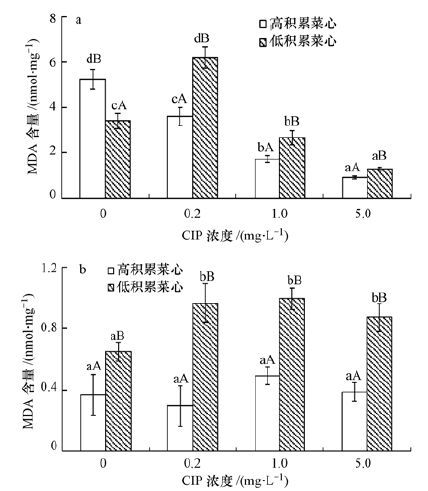 |
| 图 5 CIP胁迫下高、低积累菜心MDA含量的差异(a. 根部; b.地上部)(注:同一CIP浓度不同菜心品种含相同大写字母者差异不显著,同一菜心品种不同CIP浓度含相同小写字母者差异不显著.) Fig. 5 MDA concentration differences in low- and high-CIP accumulation cultivars of Chinese flowering cabbages under CIP stress(a. root; b. shoot) |
1) CIP胁迫下,高积累菜心根部及地上部蛋白含量及抗氧化系统酶(POD和SOD)活性总体高于低累积型菜心,而膜脂损伤程度低于后者
2) 高积累菜心对CIP的解毒和耐受能力高于低积累菜心,从而利于其吸收积累CIP.
3) 菜心品种间抗氧化性能的差异是其吸收累积CIP差异的重要生理生化机制.
| [1] | An J, Zhou Q X, Sun Y B, et al. 2009. Ecotoxicological effects of typical personal care products on seed germination and seedling development of wheat (Triticum aestivum L.) [J]. Chemosphere, 76(10): 1428-1434 |
| [2] | Andrade L R, Leal R N, Noseda M, et al. 2010. Brown algae overproduce cell wall polysaccharides as a protection mechanism against the heavy metal toxicity. Marine Pollutution Bulletin, 60(9): 1482-1488 |
| [3] | Dettenmaier E M, Doucette W J, Bugbee B. 2008.Chemical hydrophobicity and uptake by plant roots[J]. Environmental Science and Technology, 43 (2): 324–329. |
| [4] | 华涛, 周启星.2009.Cd-Zn 对草鱼(Ctenopharyngodon idellus) 的联合毒性及对肝脏超氧化物歧化酶(SOD) 活性的影响[J].环境科学学报, 29 (3):600–606. |
| [5] | Liu F, Pang S J. 2010.Stress tolerance and antioxidant enzymatic activities in the metabolisms of the reactive oxygen species in two intertidal red algae Grateloupia turuturu and Palmaria palmate[J]. Journal of Experimental Marine Biology and Ecology, 382 (2): 82–87. |
| [6] | Li X Y, Xie Y F, Li C L, et al. 2014.Investigation of residual fluoroquinolones in a soil-vegetable system in an intensive vegetable cultivation area in Northern China[J]. Science of the Total Environment, : 468–264. |
| [7] | 雷静静, 冯佳, 谢树莲.2013.纳米氧化镍对3 种绿藻的毒性效应[J].中国环境科学, 33 (10):1842–1849. |
| [8] | 林仁漳, 杜文超, 王晓蓉, 等.2008.土壤外源Cd胁迫对小麦幼苗生长自由基代谢及抗氧化酶活性的影响[J].农业环境科学学报, 27 (1):23–29. |
| [9] | 刘士哲. 2011. 现代实用无土栽培技术[M]. 北京: 中国农业出版社: 132 -135. |
| [10] | 吕旋, 向垒, 李彦文, 等.2014.环丙沙星-镉复合污染对高低累积型菜心种子发芽的影响[J].农业环境科学学报, 33 (4):819–820. |
| [11] | Jin X F, Yang X E, Islam E, et al. 2008a.Ultrastructural changes, zinc hyperaccumulation and its relation with antioxidants in two ecotypes of Sedum alfredii Hance[J]. Plant Physiology and Biochemistry, 46 (11): 997–1006. |
| [12] | Jin X F, Yang X E, Mahmood Q, et al. 2008b.Responses of Glutathione Metabolism and Antioxidant Enzymes towards Cadmium in Hyperaccumulator and Non-hyperaccumulator Ecotypes of Sedum alfredii H[J]. Envrionmental Toxicity, 23 (4): 517–529. |
| [13] | Jin X F, Liu D, Islam E, et al. 2009. Effects of zinc on root morphology and antioxidant adaptations of cadmium-treated Sedum alfredii H. J [J]. Plant Nutrtion, 32(10): 1642-1652 |
| [14] | Sun R L, Zhou Q Y, Sun F H, et al. 2007.Antioxidative defense and praline/phytochelatin accumulation in a newly-discovered Cd-hyperaccumulator, Solanum nigrum L[J]. Environmental and Experimental Botany, 60 (3): 468–476. |
| [15] | Shi Y, Gao L, Li W, et al. 2012.Investigation of fluoroquinolones, sulfonamides and macrolides in long-term wastewater irrigation soil in Tianjin, China[J]. Bull Environ Contam Toxicol, 89 (4): 857–861. |
| [16] | 苏恩萍, 孟范平, 孙婷, 等.2014.短期暴露于城市污水处理厂尾水的文蛤抗氧化酶响应[J].中国环境科学, 34 (2):511–517. |
| [17] | 田文静, 白伟, 赵春禄, 等.2010.纳米 ZnO 对斑马鱼胚胎抗氧化酶系统的影响[J].中国环境科学, 30 (5):705–709. |
| [18] | Wang J, Zhu J Y, Liu S P, et al. 2011.Generation of reactive oxygen species in cyanobacteria and green algae induced by allelochemicals of submerged macrophytes[J]. Chemosphere, 85 (10): 977–982. |
| [19] | Wang J X, Zhang X Z, Chen Y S, et al. 2008.Toxicity assessment of manufactured nanomaterials using the unicellular green alga Chlamydomonas reinhardtii[J]. Chemosphere, 73 (7): 1121–1128. |
| [20] | 王朋, 温蓓, 张淑贞.2011.环丙沙星对玉米芽期抗氧化酶活性及自由基代谢的影响[J].环境化学, 30 (4):754–757. |
| [21] | 吴小莲, 莫测辉, 李彦文, 等.2011.蔬菜中喹诺酮类抗生素污染探查与风险评价:以广州市超市蔬菜为例[J].环境科学, 32 (6):1703–1709. |
| [22] | 吴小莲, 向垒, 莫测辉, 等.2013a.长期施用粪肥蔬菜基地蔬菜中典型抗生素的污染特征[J].环境科学, 34 (6):2442–2447. |
| [23] | 吴小莲, 莫测辉, 严青云, 等.2013b.东莞市蔬菜基地蔬菜中喹诺酮类抗生素污染特征及健康风险[J].中国环境科学, 33 (5):910–916. |
| [24] | 吴小莲, 向垒, 莫测辉, 等.2013c.超高效液相色谱-电喷雾串联质谱测定蔬菜中喹诺酮类抗生素[J].分析化学, 41 (6):876–881. |
| [25] | 王震宇, 于晓莉, 高冬梅.2010.人工合成纳米TiO2和MWCNTs对玉米生长及其抗氧化系统的影响[J].环境科学, 31 (2):480–487. |
| [26] | 徐湘博, 史雅娟, 吕永龙, 等.2014.2,2',4,4'-四溴联苯醚对赤子爱胜蚓的抗氧化酶、代谢酶及其基因表达的影响[J].环境科学学报, 34 (11):2948–2955. |
| [27] | 尹倩, 黄献培, 李彦文, 等.2013.不同基因型空心菜对环丙沙星及恩诺沙星的吸收累积特征[J].农业环境科学学报, 32 (2):407–408. |
| [28] | 周坤, 刘俊, 徐卫红, 等.2014.外源锌对不同番茄品种抗氧化酶活性镉积累及化学形态的影响[J].环境科学学报, 34 (6):1592–1599. |
| [29] | 张琼, 伍琴, 高香玉, 等.2010.二溴联苯醚对纤细裸藻的生态遗传毒性效应[J].中国环境科学, 30 (6):833–838. |
 2016, Vol. 36
2016, Vol. 36


