2. 莆田出入境检验检疫局, 莆田 351100;
3. 福建师范大学环境科学与工程学院, 福州 350007
2. Putian Entry-Exit Inspection and Quarantine Bureau, Putian 351100;
3. School of Environmental Science and Engineering, Fujian Normal University, Fuzhou 350007
随着铅和镉及其化合物在印染、皮革、蓄电池、压延产品、合金等行业应用的不断扩大,其残留污染日益增加(Karthik et al., 2015). 由于铅和镉具有高毒性、难降解和易被生物富集等特性,因此,它们对环境所造成的污染具有持续性,已经成为当今世界严重的环境问题之一(Coelho et al., 2014). 目前,去除水体中Pb(Ⅱ)和Cd(Ⅱ)的方法有离子交换法、吸附法、化学处理法、膜分离法、微生物法等(Karthik et al., 2015; Coelho et al., 2014;Xiong et al., 2011;Vasudevan et al., 2012;Mortaheb et al., 2010). 虽然以上方法在去除水体中Pb(Ⅱ)和Cd(Ⅱ)的研究中起着重要作用,但这些方法不同程度地存在去除效率低、设备投资大、能源消耗高、二次污染等缺陷.因此,如何发展高效、经济的去除水体中Pb(Ⅱ)和Cd(Ⅱ)的新方法,已经成为当今从事环境修复研究人员需要继续解决的科学问题之一.
在水污染治理领域中,纳米铁修复技术是一种颇具潜力的新技术.纳米铁具有较强的还原性,比表面积大,并且在水中能以胶体粒子的形态保持较长时间,因此,已被广泛应用于去除水体中的Pb(Ⅱ)、Cd(Ⅱ)、Cu(Ⅱ)、Co(Ⅱ)、As(Ⅲ)和Cr(VI)等重金属污染物(Boparai et al., 2011; Kanel et al., 2005; Cai et al., 2014; Shahwan et al., 2010; Liu et al., 2013). 但大部分纳米铁材料是通过液相还原制备纳米铁,即在含有Fe2+或Fe3+液相体系中采用强还原剂(如硼氢化钠、硼氢化钾等)对Fe2+或Fe3+进行还原制得(Boparai et al., 2011; Kanel et al., 2005; Cai et al., 2014; Shahwan et al., 2010; Liu et al., 2013). 化学合成法在促进纳米技术发展中起着积极作用,但所合成的纳米铁存在易团聚、易被氧化等缺陷,并且在应用过程中成本居高不下,无法大规模实施原位修复.
利用植物提取液绿色合成纳米铁材料具有环境友好、成本低和资源再利用等优点.其原理是利用植物提取液中的生物活性还原剂,如多酚、黄酮、酶、蛋白质等将铁盐或亚铁盐还原为纳米铁,而这些有机成分同时作为合成过程中的分散剂和掩蔽剂,大大提高了纳米铁材料的稳定性(Mittal et al., 2013). 近年,各种植物提取液已用于制备纳米铁粒子:如利用茶叶提取液绿色合成纳米铁(Kuang et al., 2013;Nadagouda et al., 2012;Weng et al., 2013),榄仁树绿色合成钯和铁(Kumar et al., 2013),高粱麸皮提取物制备纳米银和纳米铁(Njagi et al., 2011),桉树叶提取液制备纳米铁粒子(Wang et al., 2013)等.由于苦丁茶种植适应能力强、成长速度快,是取之不尽、用之不竭的可再生能源,且富含多酚、黄酮、酶、蛋白质等(赵天湖等,2011;姜启双,2011),是安全无毒、可生物降解的环境友好材料.
因此,本实验以苦丁茶叶提取液作为还原剂和稳定剂,绿色合成纳米铁(Fe NPs),并通过扫描电子显微镜(SEM)、X射线能量色散谱分析(EDS)、X 射线光电子能谱仪(XPS)、傅立叶红外光谱(FT-IR)等表征手段对Fe NPs反应前后的形貌进行表征.同时,以Pb(Ⅱ)和Cd(Ⅱ)为目标去除物,比较Fe NPs单独去除Pb(Ⅱ)和Cd(Ⅱ)与同时去除Pb(Ⅱ)和Cd(Ⅱ)的去除率,并考察不同反应温度对Fe NPs同时去除水中Pb(Ⅱ)和Cd(Ⅱ)的影响,探讨反应动力学和可能的去除机理.
2 材料与方法(Materials and methods) 2.1 试剂和材料硫酸亚铁、硝酸铅、氯化镉和无水乙醇购于国药集团化学试剂有限公司,所有试剂均为分析纯.苦丁茶叶购于福建省安溪县如意茶厂.
2.2 仪器JJ-4 六联电动搅拌器(国华电器有限公司),DZF-6020 型真空干燥箱(上海精宏实验设备有限公司),BS-224S 电子天平(北京赛多利斯仪器系统有限公司),GZX-9070MBE 数显鼓风干燥箱(上海博迅实业有限公司医疗设备厂).
2.3 Fe PNs的制备称取60 g苦丁茶叶,加入到1 L去离子水中,在353 K下加热1 h,过滤,滤液即为苦丁茶叶提取液.在氮气保护下,将200 mL 0.1 mol·L-1 FeSO4·7H2O溶液逐滴滴入上述400 mL提取液中,边滴边搅拌,滴加完成后继续搅拌20 min,将反应液过滤,固体用乙醇洗涤,并在333 K真空干燥箱中干燥过夜,取出,研磨,即制得Fe NPs.
2.4 去除Pb(Ⅱ)和Cd(Ⅱ)的反应去除水中单独的Pb(Ⅱ)和Cd(Ⅱ)的反应是在50 mL棕色摇瓶中进行,摇床的振荡速度为220 r·min-1,在一定温度下,将一定质量的Fe NPs与15 mL浓度均为10 mg·L-1的Pb(Ⅱ)或Cd(Ⅱ)溶液加入到摇瓶中,反应温度为303 K,在摇床中振动0、3、5、10、20、30、40、60 min后,用0.45 μm滤膜快速过滤,用AAS测定溶液中残余Pb(Ⅱ)和Cd(Ⅱ)的浓度,用去除率来评价绿色合成纳米铁的活性.同时去除Pb(Ⅱ)和Cd(Ⅱ)的反应是在同时加入15 mL浓度均为10 mg·L-1的Pb(Ⅱ)和Cd(Ⅱ)混合液中加入Fe NPs,其初始溶液的 pH 值为3.5,考察反应温度分别为293、303、313 K时对Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)的影响.所有实验平行测定3次.
2.5 表征采用日本JEOL公司的JSM-7500型扫描电子显微镜(SEM)观察样品的表面形貌及元素组成,附件能量色散谱仪(EDS); 采用英国Thermo Scientific公司的ESCALAB 250型X 射线光电子能谱仪(XPS)分析样品表面的元素价态和成分;采用美国THERMO NICOLET公司的Thermo Nicolet 5700红外光谱仪,获取试样的FTIR谱图,溴化钾压片,扫描范围4000~400 cm-1;采用AA240FS/Z火焰原子吸收分光光度计测定溶液中Pb(Ⅱ)和Cd(Ⅱ)的浓度.
3 结果与讨论(Results and discussion) 3.1 Fe NPs单独去除Pb(Ⅱ)、Cd(Ⅱ)及同时去除Pb(Ⅱ)和Cd(Ⅱ)的比较Fe NPs去除水溶液中Pb(Ⅱ)和Cd(Ⅱ)的变化研究如图 1所示,实验条件为:15 mL Pb(Ⅱ)、Cd(Ⅱ)、Pb(Ⅱ)-Cd(Ⅱ)混合液的初始浓度均为10 mg·L-1,Fe NPs投加量为2.0 g·L-1,初始pH为3.5,振荡速度为220 r·min-1,温度为303 K,反应时间为60 min. 从图 1a可以看出,Fe NPs单独去除Pb(Ⅱ)时的去除率在10 min和60 min时分别达到85.2%和93.8%,Fe NPs对Pb(Ⅱ)-Cd(Ⅱ)中Pb(Ⅱ)的去除率在10 min和60 min时仅达到75.9%和91.0%. 从图 1b可以看出,Fe NPs单独去除Cd(Ⅱ)时的去除率在10 min和60 min时分别达到35.2%和41.7%,Fe NPs对Pb(Ⅱ)-Cd(Ⅱ)中Cd(Ⅱ)的去除率在10 min和60 min时仅达到23.2%和31.4%. Pb(Ⅱ)和Cd(Ⅱ)在单独体系中其去除率比Pb(Ⅱ)-Cd(Ⅱ)复合体系中高,这是因为Fe NPs在同时去除Pb(Ⅱ)和Cd(Ⅱ)反应体系中Pb(Ⅱ)和Cd(Ⅱ)存在着竞争反应的关系,Cd(Ⅱ)会占据Fe NPs的表面反应活性位,阻碍Pb(Ⅱ)的去除;同时,Pb(Ⅱ)与Fe NPs中的纳米铁反应形成钝化层,阻碍Cd(Ⅱ)的去除(牛少凤等,2009).
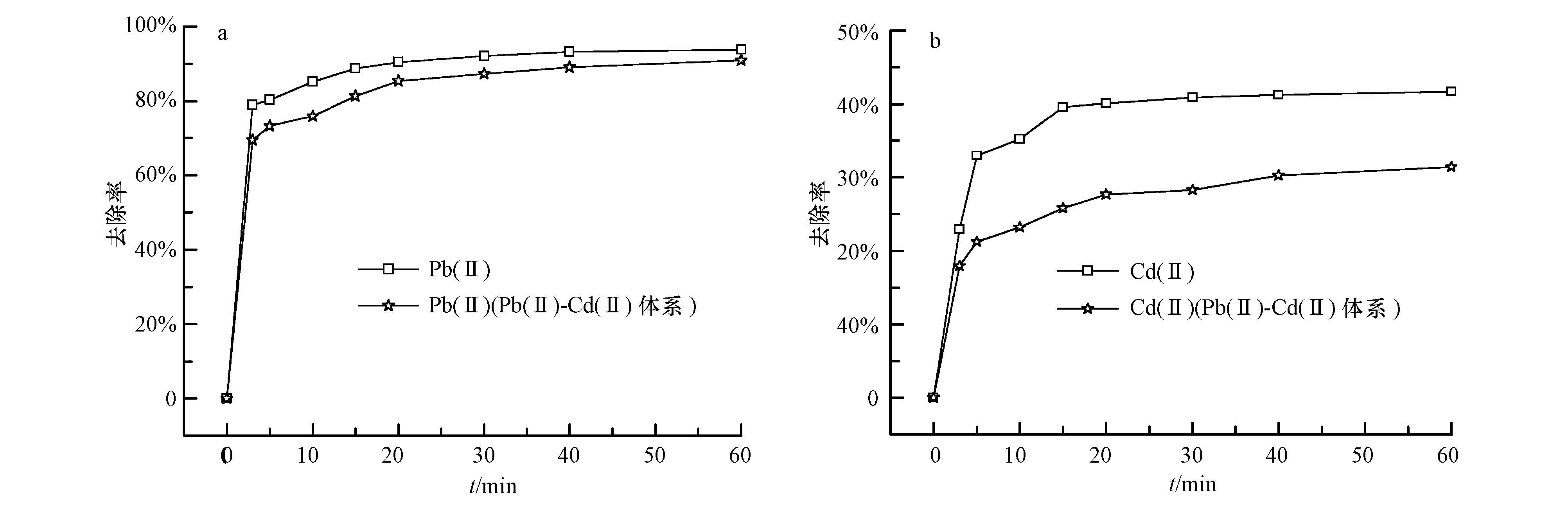 |
| 图 1 Fe NPs 单独去除Pb(Ⅱ)、Cd(Ⅱ)及同时去除Pb(Ⅱ)和Cd(Ⅱ)的比较 (a. Fe NPs 对Pb(Ⅱ)的去除; b. Fe NPs 对Cd(Ⅱ)的去除) Fig.1 Individual and simultaneous removal of Pb(Ⅱ)(a) and Cd(Ⅱ)(b) by Fe NPs |
为观察Fe NPs反应前后形貌结构上的变化,采用SEM对其进行表征.图 2为Fe NPs同时去除 Pb(Ⅱ)和Cd(Ⅱ)反应前后的SEM图.由图 2a可知,反应前的Fe NPs呈较规整的球状结构,但部分纳米铁也存在团聚的现象,通过对颗粒大小的粒径统计发现其平均粒径在75~90 nm之间,说明通过绿色合成的方法制得的是纳米铁颗粒(Wang et al., 2013).反应后,Fe NPs表面的纳米铁粒子减少,大部分颗粒不再呈球状,颗粒之间主要以团聚态的形式紧密相连(图 2b),这说明Fe NPs与Pb(Ⅱ)和Cd(Ⅱ)反应是通过Fe NPs中的纳米铁的腐蚀作用,纳米铁在反应过程中被氧化并与Pb(Ⅱ)离子形成共沉淀及Cd(Ⅱ)吸附在Fe NPs的表面(Zhang et al., 2013; Boparai et al., 2011).
 |
| 图 2 Fe NPs反应前(a)和反应后(b)的扫描电镜图 Fig.2 SEM images of Fe-NPs before (a) and after reaction(b) |
图 3是Fe NPs反应前后的EDS谱图.由图 3a可知,Fe NPs样品中主要含有元素C(63.8%)、O(33.3%)和Fe(3.1%);而在图 3b中,除了含有C(55.9%)、O(41.7%)和Fe(1.2%)以外,还含有Pb(0.8%)和Cd(0.4%)两种元素.从Fe NPs反应后的EDS数据发现,氧元素的含量上升了8.5%,铁元素的含量降低了1.9%,并且出现了Pb和Cd两种元素.这是因为Fe NPs中的纳米铁在反应过程发生腐蚀形成铁氧化物,使得反应后的材料中铁的相对含量降低.而在反应后Fe NPs的EDS数据中有Pb和Cd两种元素,说明反应后Pb与纳米铁腐蚀后的产物形成共沉淀在Fe NPs的表面上,Cd吸附在Fe NPs的表面上(Zhang et al., 2013; Boparai et al., 2011). Fe NPs中的C元素主要来源于苦丁茶提取液中的有机活性成分,说明纳米铁表面覆盖有黄酮、生物碱、萜类物质,作为稳定剂将合成的Fe NPs 包裹,从而减少 Fe NPs 被氧化.
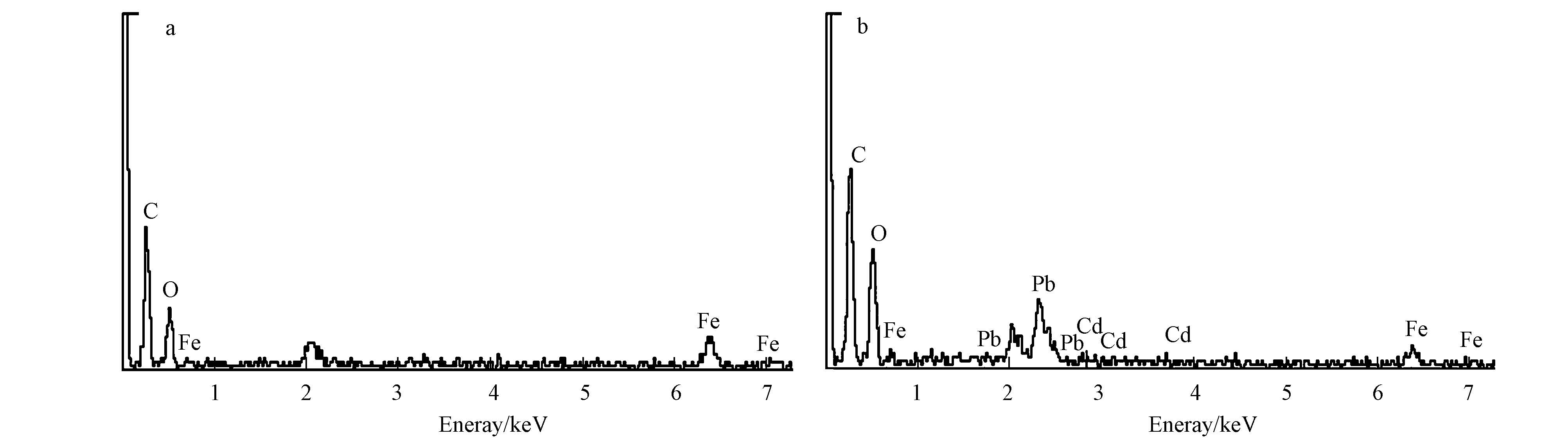 |
| 图 3 Fe NPs反应前(a) 和反应后(b)的EDS图 Fig.3 EDS patterns of Fe NPs before (a) and after reaction (b) |
图 4为Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)后的XPS图.由图 4a 可知,结合能为141.7 eV处的峰对应的是Pb0,结合能为138.3 eV处的峰对应的是PbO中的Pb(Ⅱ)(Chada et al., 2005). 从图 4b可知,结合能为412.0 eV和405.3 eV处的峰对应的是Cd2+(Chada et al., 2005).从图 4可知,反应后的铅 主要以Pb0和PbO存在,而镉主要以Cd2+存在,说明Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)的过程中,铅离子主要是被Fe NPs中的纳米铁还原成Pb0或形成PbO,而镉离子主要是通过Fe NPs对其吸附.
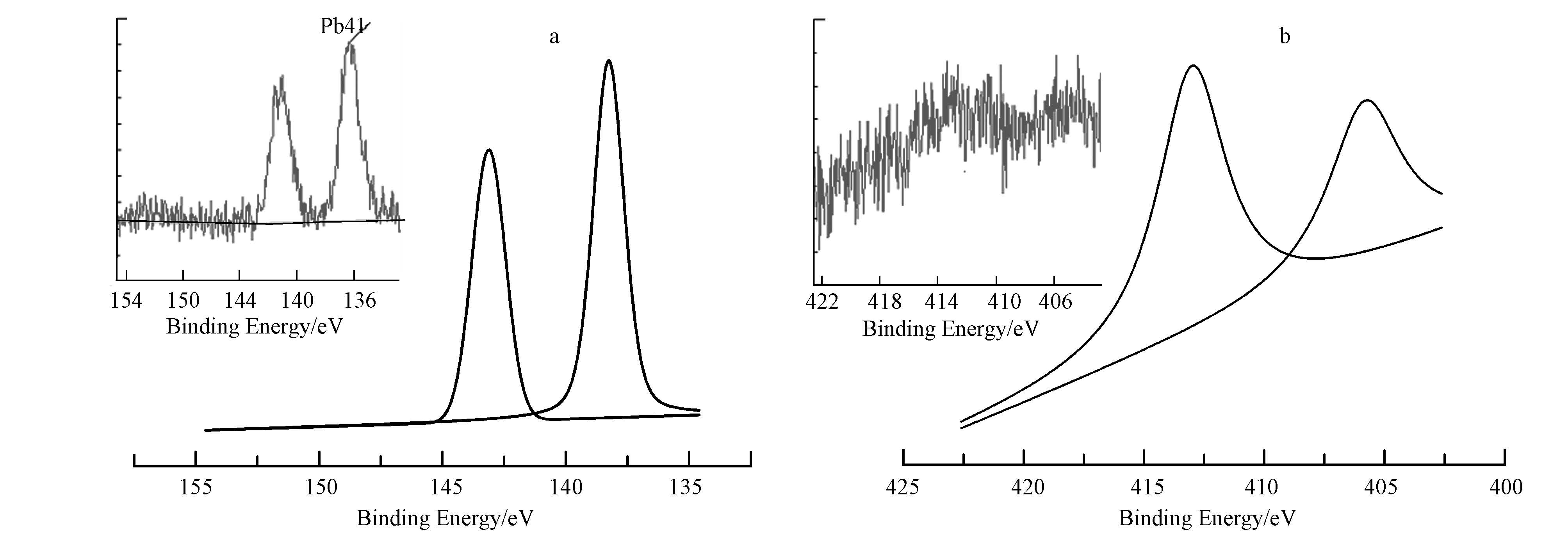 |
| 图 4 Fe NPs上Pb(a)和Cd(b)对应的XPS图 Fig.4 XPS patterns of Fe NPs with Pb(a) and Cd(b) |
图 5是苦丁茶提取液、Fe NPs 反应前后的的红外谱图.从图 5a可知,3351 cm-1附近的吸收峰为羟基自由基的振动吸收峰,1693 cm-1处的强吸收峰为C O伸缩振动峰,1603、1515和1446 cm-1处的吸收峰为苦丁茶中苯环或杂芳环的骨架振动峰,在1377 cm-1处的吸收峰为苦丁茶提取液的特征峰,1058 cm-1处的吸收峰为C—O—C的对称伸缩吸收峰,615 cm-1处的吸收峰为苦丁茶提取液在指纹区的特征吸收峰(庞涛涛等,2007). 比较图 5a和图 5b可知,Fe NPs的红外谱图与苦丁茶提取液的各个官能团的特征吸收峰的变化不大,这可能是因为Fe NPs的表面被苦丁茶提取液中的有机物包裹,这些有机物如多酚及黄酮是纳米铁的掩蔽剂和稳定剂. 图 5c是反应后的Fe NPs红外谱图,与图 5b比较,在435 cm-1附近出现一个新的特征吸收峰,这是Fe2O3和Fe3O4中的Fe—O伸缩振动峰,说明Fe NPs在同时去除Pb(Ⅱ)和Cd(Ⅱ)的过程中纳米铁被氧化生成Fe2O3和Fe3O4.
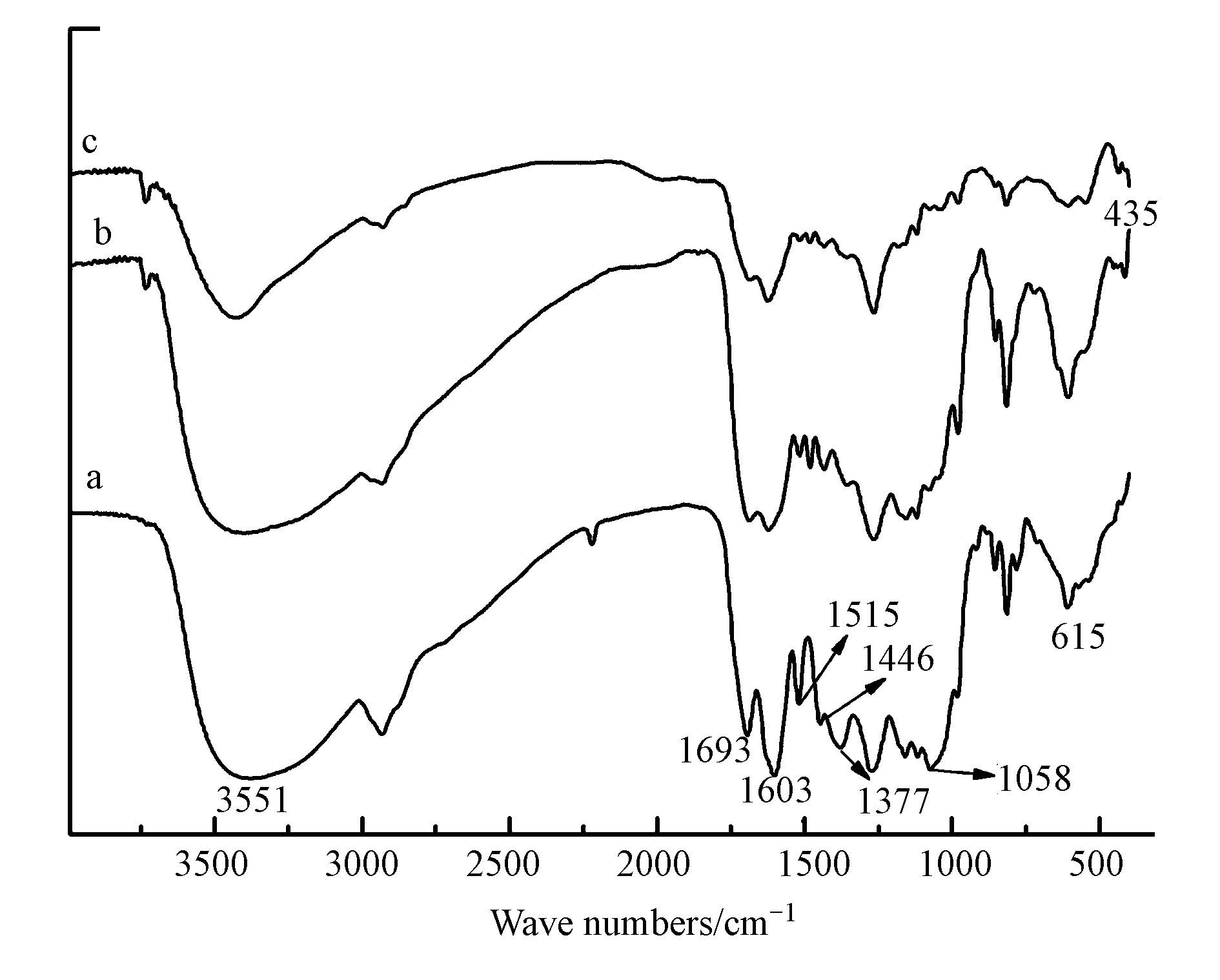 |
| 图 5 Fe NPs的红外光谱图 (a.苦丁茶提取液; b. Fe NPs反应前; c. Fe NPs反应后) Fig.5 FTIR spectrum of Fe NPs with HE (a), before reaction (b) and after reaction (c) |
采用Pb(Ⅱ)和Cd(Ⅱ)作为研究对象,分别向每个离心管中移入15 mL浓度均为10 mg·L-1的Pb(Ⅱ)和Cd(Ⅱ)混合液,Fe NPs投加量为2.0 g·L-1,摇床振荡速率为220 r·min-1,在温度分别为293、303、313 K条件下,考察Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)的情况,结果如图 6所示.由图 6可知,温度为293 K,反应时间为60 min时,Fe NPs对Pb(Ⅱ)和Cd(Ⅱ)的去除率分别为86.0%和23.0%;温度为303 K,反应时间为60 min时,Fe NPs对Pb(Ⅱ)和Cd(Ⅱ)的去除率分别为91.0%和31.4%;温度为313 K,反应时间为60 min时,Fe NPs对Pb(Ⅱ)和Cd(Ⅱ)的去除率分别为93.2%和38.2%. 在293~313 K之间,Pb(Ⅱ)和Cd(Ⅱ)的去除率和去除速率均随温度的增加而增大.温度越高,越有利于溶液中Pb(Ⅱ)和Cd(Ⅱ)在水溶液中的迁移,增加了Pb(Ⅱ)和Cd(Ⅱ)与Fe NPs的接触几率,从而加快了Fe NPs对其去除.
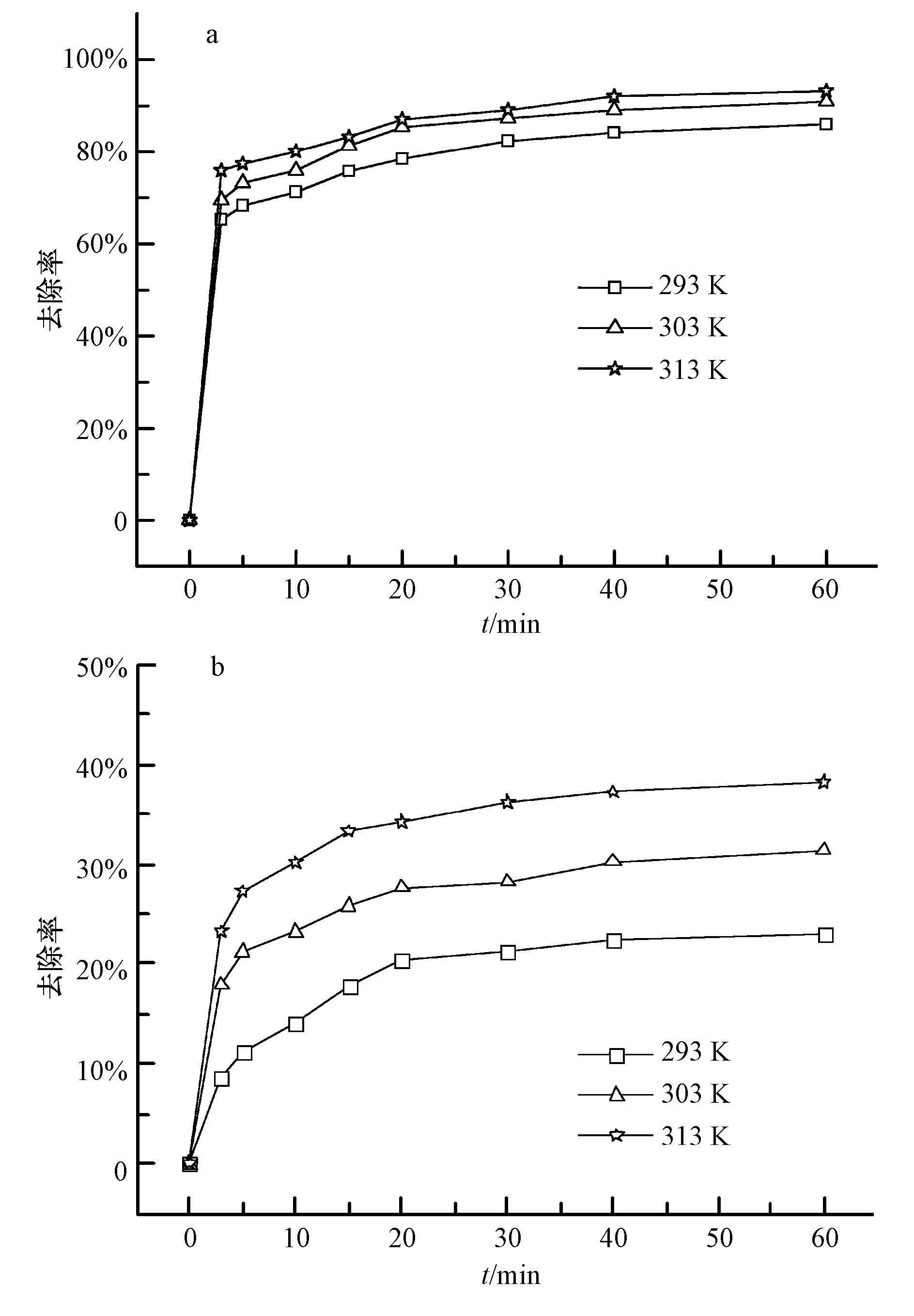 |
| 图 6 不同温度对Fe NPs同时去除水溶液中的Pb(Ⅱ)和Cd(Ⅱ)的影响(a. Pb(Ⅱ); b. Cd(Ⅱ)) Fig.6 The effect of temperature on the removal of Pb(Ⅱ) and Cd(Ⅱ) by Fe NPs(a. Pb(Ⅱ); b. Cd(Ⅱ)) |
通常认为Fe NPs去除Pb(Ⅱ)是由于Fe NPs表面的控制过程,分别用伪一级动力学方程(1)、伪二级对动力学方程(2)结果进行拟合(Cai et al., 2014).
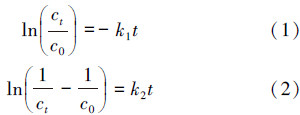
根据图 6a的数据,通过线性回归直线拟合的数据如表 1所示.从表 1可知,随着温度的升高,表观速率常数均随着温度的升高而增大,并且在不同反应温度下,伪一级可决系数R12高于伪二级可决系数R22,且R12均大于0.94,表明Fe NPs与Pb(Ⅱ)反应更符合表观一级反应动力学方程.
| 表 1 不同温度条件下Pb(Ⅱ)的动力学常数 Table 1 Pseudo-first-order kinetic parameters of Pb(Ⅱ) removal under different temperatures |
为了理解Cd(Ⅱ)在Fe NPs上的吸附行为,利用温度条件实验数据对其进行吸附动力学拟合,可以用如下的伪二级动力学方程表示(Boparai, et al., 2011):


从表 2可以看出,k2、qe和h均随着温度的升高而增大.根据公式计算出来的qe与实验数据的相吻合(如图 6b),且R22>0.99,表明Cd(Ⅱ)吸附在Fe NPs的表面符合伪二级动力学.
| 表 2 不同温度条件下Cd(Ⅱ)的伪二级动力学常数 Table 2 Pseudo-second-order kinetic parameters of Cd(Ⅱ) removal under different temperatures |
根据对Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)反应前后的表征和分析结果,以及Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)的去除率的分析结果和φ°Fe2+/Fe0的标准还原电位(-0.41 V)、φ°Pb2+/Pb0的标准还原电位(-0.13 V)、φ°Cd2+/Cd0的标准还原电位(-0.40 V)之间的标准还原电位的大小(Zhang et al., 2013; Boparai et al., 2011),可以推断Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)中的Pb(Ⅱ)可能机理是Fe NPs对Pb(Ⅱ)吸附和还原两个同时进行的过程(Sherman et al.,2000),而Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)中的Cd(Ⅱ)可能机理是Fe NPs对Cd(Ⅱ)进行吸附的过程具体如方程(5)~(10)所示.混合液中的Pb(Ⅱ)吸附在Fe NPs颗粒表面上的同时,纳米铁在水的侵蚀作用下产生自由电子,与Pb(Ⅱ)发生还原作用,达到去除Pb(Ⅱ)的作用.并且由于Fe NPs中的纳米铁被氧化成为氧化铁,而氧化铁对Pb(Ⅱ)也具有吸附作用(张晓蕾等,2013).另外,混合液中的Cd(Ⅱ)吸附在Fe NPs的表面,也由于Fe NPs中的纳米铁被氧化成为氧化铁,而氧化铁对Cd(Ⅱ)也具有吸附作用.从中可以说明Fe NPs对同时去除Pb(Ⅱ)和Cd(Ⅱ)起着主要作用的是纳米铁粒子及其相应产物,其对混合液中的Pb(Ⅱ)起到还原、吸附作用,而对混合液中的Cd(Ⅱ)起到吸附的作用.
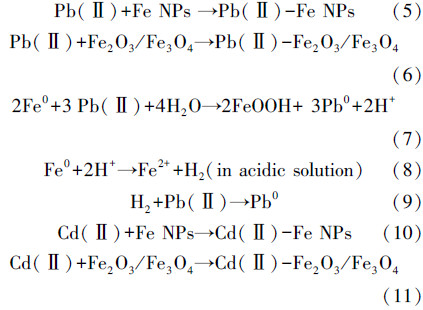
1)利用苦丁茶叶提取液既作还原剂又作稳定剂成功合成了纳米铁颗粒.通过SEM、EDS、XPS、FT-IR等表征手段对绿色合成的纳米铁颗粒进行表征,发现所合成的纳米铁颗粒是球状的颗粒,粒径大约在75~90 nm,对反应后的绿色合成的纳米铁进行表征,表明绿色合成的纳米铁部分被氧化.
2)以水中Pb(Ⅱ)和Cd(Ⅱ)单独和复合污染为目标去除物,发现Pb(Ⅱ)和Cd(Ⅱ)共同存在时,存在竞争反应的关系. Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)时,随着反应温度的升高,Pb(Ⅱ)和Cd(Ⅱ)的去除率和去除速率都增大.动力学研究表明,Pb(Ⅱ)的去除过程符合伪一级反应和Cd(Ⅱ)的去除过程符合伪二级动力学反应.
3)Fe NPs同时去除Pb(Ⅱ)和Cd(Ⅱ)的可能机理是Fe NPs中的纳米铁粒子及其相应产物,对混合液中的Pb(Ⅱ)起到还原、吸附作用,而对混合液中的Cd(Ⅱ)起到吸附的作用,从而达到去除Pb(Ⅱ)和Cd(Ⅱ)的目的.
| [1] | Boparai H K,Joseph M,O'Carroll D M.2011.Kinetics and thermodynamics of cadmium ion removal by adsorption onto nano zerovalent iron particles[J].Journal of Hazardous Materials,186(1): 458-465 |
| [2] | Cai X,Gao Y,Sun Q,et al.2014.Removal of co-contaminants Cu (Ⅱ) and nitrate from aqueous solution using kaolin-Fe/Ni nanoparticles[J].Chemical Engineering Journal,244: 19-26 |
| [3] | Chada V G R,Hausner D B,Strongin D R,et al.2005.Divalent Cd and Pb uptake on calcite {10ī4} cleavage faces: An XPS and AFM study[J].Journal of Colloid and Interface Science,288(2): 350-360 |
| [4] | Coelho G F,Gonçalves A C,Jr,Tarley C R T,et al.2014.Removal of metal ions Cd (Ⅱ),Pb (Ⅱ),and Cr (Ⅲ) from water by the cashew nut shell Anacardium occidentale L[J].Ecological Engineering,73: 514-525 |
| [5] | 姜启双.2011.苦丁茶北方保护地密植矮化栽培技术[J].中国园艺文摘,(6): 189-190 |
| [6] | Kanel S R,Manning B,Charlet L,et al.2005.Removal of arsenic(Ⅲ) from groundwater by nanoscale zero-valent iron[J].Environmental Science & Technology,39(5): 1291-1298 |
| [7] | Karthik R,Meenakshi S.2015.Removal of Pb(Ⅱ) and Cd(Ⅱ) ions from aqueous solution using polyaniline grafted chitosan[J].Chemical Engineering Journal,263: 168-177 |
| [8] | Kuang Y,Wang Q P,Chen Z L,et al.2013.Heterogeneous Fenton-like oxidation of monochlorobenzene using green synthesis of iron nanoparticles[J].Journal of Colloid and Interface Science,410: 66-73 |
| [9] | Kumar K M,Mandal B K,Kumar K S,et al.2013.Biobased green method to synthesise palladium and iron nanoparticles using Terminalia chebula aqueous extract[J].Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy,102: 128-133 |
| [10] | Liu T Y,Yang X,Wang Z L,et al.2013.Enhanced chitosan beads-supported Fe0-nanoparticles for removal of heavy metals from electroplating wastewater in permeable reactive barriers[J].Water Research,47(17): 6691-6700 |
| [11] | Mittal A K,Chisti Y,Banerjee U C.2013.Synthesis of metallic nanoparticles using plant extracts[J].Biotechnology Advances,31(2): 346-356 |
| [12] | Mortaheb H R,Zolfaghari A,Mokhtarani B,et al.2010.Study on removal of cadmium by hybrid liquid membrane process[J].Journal of Hazardous Materials,177(1): 660-667 |
| [13] | Nadagouda M N,Castle A B,Murdock R C,et al.2012.In vitro biocompatibility of nanoscale zerovalent iron particles (NZVI) synthesized using tea polyphenols[J].Green Chemistry,12(1): 114-122 |
| [14] | 牛少凤,李春晖,楼章华,等.2009.纳米铁对水中Cr (VI)和p-NCB的同时修复机制[J].环境化学,30(1): 146-150 |
| [15] | Njagi E C,Huang H,Stafford L,et al.2011.Biosynthesis of iron and silver nanoparticles at room temperature using aqueous sorghum bran extracts[J].Langmuir,27(1): 264-271 |
| [16] | 庞涛涛,杜黎明,苑戎.2007.红外光谱法直接鉴别苦丁茶的研究[J].分析科学学报,23(2): 213-215 |
| [17] | Shahwan T,Üzüm Ç,Eroğlu A E,et al.2010.Synthesis and characterization of bentonite/iron nanoparticles and their application as adsorbent of cobalt ions[J].Applied Clay Science,47(3/4): 257-262 |
| [18] | Sherman M P,John G D,Thoman E M.2000.Remediation of Cr(VI) and Pb(Ⅱ) aqueous solutions using supported,nanoscale zero-valent iron[J].Environmental Science & Technology,34(12): 2564-2569 |
| [19] | Vasudevan S,Lakshmi J,Sozhan G.2012.Simultaneous removal of Co,Cu,and Cr from water by electrocoagulation[J].Toxicological and Environmental Chemistry,94(10): 1930-1940 |
| [20] | Wang T,Jin X Y,Chen Z L,et al.2013.Green synthesis of Fe nanoparticles using eucalyptus leaf extracts for treatment of eutrophic wastewater[J].Science of the Total Environment,466-467: 210-213 |
| [21] | Weng X L,Huang L L,Chen Z L,et al.2013.Synthesis of iron-based nanoparticles by green tea extract and their degradation of malachite[J].Industrial Crops and Products,51: 342-347 |
| [22] | Xiong L,Chen C,Chen Q,et al.2011.Adsorption of Pb(Ⅱ) and Cd(Ⅱ) from aqueous solutions using titanate nanotubes prepared via hydrothermal method[J].Journal of Hazardous Materials,189(3): 741-748 |
| [23] | 张晓蕾,陈静,韩京龙,等.2013.壳-核结构 Fe3O4/MnO2磁性吸附剂的制备、表征及铅吸附去除研究[J].环境科学学报,33(10): 2730-2736 |
| [24] | Zhang Y L,Su Y M,Zhou X F,et al.2013.A new insight on the core-shell structure of zerovalent iron nanoparticles and its application for Pb(Ⅱ) sequestration[J].Journal of Hazardous Materials,263: 685-693 |
| [25] | 赵天湖,范嘉龙,闫冬,等.2011.大叶冬青苦丁茶多糖提取、纯化与抗氧化活性研究[J].作物研究,25(1): 56-60 |
 2015, Vol. 35
2015, Vol. 35


